2. 四川大学水力学与山区河流开发保护国家重点实验室, 成都 610065;
3. 四川蜀禹水利水电工程设计有限公司, 成都 610065
2. State Key Laboratory of Hydraulics and Mountain River Engineering, Sichuan University, Chengdu 610065, China;
3. Sichuan Shuyu Water Conservancy and Hydropower Engineering Design Co., Ltd., Chengdu 610065, China
目前, 城镇饮水安全已成为我国全社会关注的热点之一.自“十一五”规划实施农村饮水安全工程建设以来, 到“十二五”末, 我国农村饮水安全问题已基本解决[1], 农民健康水平得到了提高, 农村生产生活条件得到了改善.我国村镇供水分为集中式供水和分散式供水, 水厂大多以临近江河、中小型水库、山溪水为水源.四川丘陵区因其水库具有水量稳定的特点, 多为城镇饮用水源和应急备用水源.而这些中小型水库则由于农业面源污染的影响, 由此造成富营养化问题, 水中污染物种类多、量超标、低浓度难去除, 长期以来饮水不安全问题十分突出[2].水厂现行的常规处理工艺即絮凝+沉淀+过滤+消毒虽然对总磷去除效果明显, 去除率可达60%~90%[3, 4], 但对有机物的去除效果却不理想[3, 5~8], 而有机物与消毒副产物的生成有重要关联[9~11].对水质安全性的检测、评价与分析, 判断水源水质指标是否符合《生活饮用水卫生标准》[12]的相关规定, 是目前急需解决的问题.而我国村镇人口规模较小, 一般为2 000~30 000人, 水利公共基础服务设施主要集中在城市, 对村镇供水水源水质安全关注度不够[13], 本文针对我国西南丘陵区村镇供水的典型水源进行了详细的分析以探究其水质特征, 并对上述水源经常规净水工艺处理后的出水水质也进行了相应地分析, 以期为提高该区域村镇居民饮水安全提供依据.
1 材料与方法 1.1 取水水源本实验选取四川省遂宁市内中小型水库:狮子湾水库、麻子滩水库、跑马滩水库、白安河及板凳垭村河塘为饮水水源水质分析取样点.其中狮子湾水库为小(二)型水库, 正常水位库容为57.6万m3, 地处浅丘区域, 周边为农田; 麻子滩水库为中型水库, 正常水位库容为5 729万m3, 地处浅丘和深丘区域, 周边多为农田和林地; 跑马滩水库为中型水库, 正常水位库容1 360万m3; 白安河干流长80 km, 流域面积456.4 km2, 上游建有中型水库3座, 小型水库24座; 板凳垭村河塘容积为8万m3.所选取水点地形为浅丘或深丘地域, 水源周边多为农田, 其中跑马滩水库横跨乐至和安居两县市, 城镇供水厂规模大小不一, 规模从600~30 000m3·d-1不等, 是该区域县城或村镇的供水水源, 具有典型的西南丘陵地区村镇供水水源的特点.因此选取上述水源点对其水源水及净化出厂水进行水质分析研究, 对于了解西南丘陵区域村镇供水水源水质状况和饮水安全具有重要意义.
在实验室内以聚合氯化铝(PAC)为絮凝剂, 进行混凝、沉淀和过滤处理后(由于本实验的立足点在于消毒之前能去除更多的有机物, 以期减少消毒副产物的产生, 所以不进行消毒实验), 对原水及处理水进行水质常规指标和有机物指标分析.
1.2 常规指标检测常规检测项目包括pH、浊度、总有机碳(TOC)、总磷(TP)、氨氮(NH4+-N)、硝酸盐氮(NO3--N)、亚硝酸盐氮(NO2--N).检测方法按照《生活饮用水标准检验方法》(GB/T 5750-2006)进行.同时还测量了水中有机物在254 nm波长紫外光下的吸光度(UV254)和溶解氧(DO)两个指标, UV254采用紫外分光光度计(UV765, 上海佑科仪器仪表有限公司提供)测量, 用以表征水中天然存在的腐殖质类大分子有机物以及含C=C双键和C=O双键芳香族化合物的含量. DO采用便携式DO溶解氧测定仪(JPBJ-608, 上海仪电科学仪器股份有限公司)测定.
1.3 有机物检测 1.3.1 有机物分子量分布检测采用超滤膜法检测原水和处理水的有机物分子量分布.首先水样经0.45 μm微滤膜真空抽滤以去除水中非溶解性物质, 然后依次通过截留相对分子质量为100×103、50×103、30×103、10×103、5×103、3×103、1×103、0.5×103的超滤膜, 分别测定其TOC值, 从而确定有机物分子量分布.超滤仪器为氮气加压搅拌型超滤杯(型号:SMC-300, 上海摩速科学器材有限公司提供), 有效容积300 mL, 最大耐压为0.22 kPa; 超滤膜为美国sepro系列的PS超滤膜; TOC测定采用日本岛津公司总有机碳分析仪(型号:TOC-VE).
1.3.2 有机物基团及结构检测原水及处理水经浓缩蒸干后, 与干燥的KCl(光谱纯)磨细混匀, 以10 t的压力压制1 min, 制成空白KCl压片, 采用Nicolet 6700傅里叶变换红外光谱仪(美国Thermo Fisher生产)测定得出其红外光谱图, 分析水中有机物基团、结构.
1.3.3 有机物定性定量检测有机物定性定量检测采用日本岛津GCMS-QP2010 Plus气质联用仪, 定量方法采用内标法, 内标物为乙酸乙酯.水样经固相微萃取前处理之后进行测定.气相色谱条件:柱箱温度40℃; 进样温度250℃; 载气:99.99%氦气; 分流进样, 分流比为2.0;柱流量(恒流模式):1.0 mL·min-1; 升温程序:40℃保持8 min, 以10℃·min-1的速率升温至280℃保持5 min; 总流量为6.0 mL·min-1, 平衡时间0.5 min.质谱条件:电子轰击(EI)离子源; 离子源温度5℃·min-1的速率升温至80℃保持2 min, 以200℃, 接口温度220℃, 溶剂延迟时间0.20 min, 扫描速度1 000 u·s-1, 质量范围33.00~1 090 m/z.
2 结果与讨论 2.1 常规指标各取水样点原水水质及处理水水质情况表 1.
|
|
表 1 原水及出厂水水质指标1) Table 1 Water quality indexes of raw and treated water |
由表 1可知, 各水源水的pH值在7~8之间, 属于中性偏弱碱性水.浊度指标不同, 浊度最高的是板凳垭村河塘, 达到了93.487NUT, 浊度最低的是跑马滩水库, 为28.370NUT.各水源水总磷含量较高, 在0.348~0.656 mg·L-1之间, 最高的是麻子滩水库, 为0.656 mg·L-1, 最低的是白安河, 为0.348 mg·L-1, 但依据《地表水环境质量标准》(GB 3838-2002), 各水源点总磷均超过了0.3 mg·L-1, 为Ⅳ类以下水质水体.对于氨氮指标而言, 则狮子湾水库和板凳垭村河塘较高, 分别为0.860 mg·L-1和0.789 mg·L-1, 其他水源水氨氮浓度较低, 并且狮子湾水库和板凳垭村河塘的亚硝酸盐氮、硝酸盐氮浓度也远高于其他类型的水源, 其DIN(三氮之和)分别达到1.177 mg·L-1和0.990 mg·L-1, 超过Ⅲ类地表水标准. TOC在3~9 mg·L-1之间, 为Ⅱ~Ⅳ类水质水体, 其中板凳垭村河塘TOC超标严重, 水质为低于Ⅴ类水质.由上述不同水源水质状况可知, 水源类型, 水库大小以及周边环境是影响其水质的重要原因, 对于较大水源, 如麻子滩水库和跑马滩水库, 其水质相对较好, 但总磷和TOC污染严重, 是影响其水源水质的主要指标.而对于小型水源, 如狮子湾水库及板凳垭村河塘, 则受周边面源污染影响严重, TOC、总氮和总磷均不符合作为水源水的水质标准.
经混凝+沉淀+过滤的常规工艺处理后, 浊度指标去除效果较好, 去除率在95.42%~96.63%之间, 处理水浊度可基本达到饮用水标准[12]的要求.总磷的去除率在50%~ 80%之间, 但对TOC、UV254、氨氮、硝酸盐氮及亚硝酸盐氮指标去除效果较差, TOC去除率在20%~40%之间, UV254去除率在10%~50%之间, 这与其他相关研究结论相一致[3~5, 14].对溶解性的氮, 如氨氮、硝酸盐氮和亚硝酸盐氮去除率则很低, 氨氮、硝酸盐氮的平均去除率为7.5%、11.40%, 亚硝酸盐氮去除基本没效果, 甚至出现亚硝酸盐氮的增加.从以上分析可知, 对于西南丘陵地区村镇水源而言, TOC、氮和磷是其主要超标污染物, 现有常规处理对其无法有效去除, 是该区域饮水安全的主要矛盾.
2.2 有机物分析 2.2.1 有机物相对分子质量分布不同水源原水及处理水的溶解性有机物分子量分布见图 1, 相应相对分子量区间有机物浓度及其去除率见表 2.

|
图 1 水中有机物相对分子质量分布 Fig. 1 Organic matter molecular weight distribution of raw and treated water |
|
|
表 2 不同相对分子量区间有机物处理前后TOC值及去除率1) Table 2 TOC and removal rate for different molecular weight ranges for raw and treated water |
水中大分子有机物与小分子有机物的相对分子质量没有明显界限, 一般以相对分子质量>1×103的有机物为大分子有机物, <1×103的有机物为小分子有机物[7, 15, 16].从图 1(a)可知, 原水中有机物以溶解性中小分子有机物为主, 相对分子质量<1×103的有机物占总TOC的50%~80%, 其中, 中小分子有机物中<0.5×103的小分子有机物占比最大, 占中小分子有机物的15%~30%, 可能为腐殖质中的富里酸(FA)[16]; 其次, 占比依次降低的有机物相对分子质量区间是(5~10)×103(10%~20%)、(0.5~1)×103(10%~20%)、(3~5)×103(10%~15%)、(1~3)×103(5%~10%).大分子量有机物含量较小, 相对分子质量>10×103的有机物占总TOC的20%~40%, 大分子量有机物中以(10~30)×103区间的有机物为主, 占大分子量有机物的40%~60%, 可能为胡敏酸(HA)[16]; 其次, 占比依次降低的有机物相对分子质量区间是(30~50)×103(15%~25%)、>100×103(10%~15%)、(50~100)×103(5%~15%).
处理水中有机物则大部分为中小分子有机物, 相对分子质量<10×103的有机物占总TOC的70%~90%, 其中, 以相对分子质量<1×103的小分子有机物为主, 占中小相对分子质量有机物的40%~80%.而相对分子质量>10×103的有机物则大幅度减小, 只占总TOC的5%~20%.
结合表 1和表 2可知, 水质净化常规工艺对原水中溶解性有机物去除率不高, 在20%~40%之间, 并且主要去除的是相对分子质量>10×103的大分子有机物, 其去除率随着有机物相对分子质量的增加而增大.分子量>10×103的有机物, 其去除率在60%~80%之间, 其中, 相对分子质量>100×103的有机物去除率在60%~90%之间; 对小分子质量有机物去除效果极差, 相对分子质量<1×103的有机物去除率小于10%.不同相对分子质量有机物去除率的不同可由不同相对分子质量区间有机物极性差异解释[14], 大分子有机物憎水性强, 易被混凝沉淀去除, 而小分子有机物亲水性强, 难被混凝沉淀去除.相对分子质量<0.5×103的有机物则不能有效去除, 甚至有所增加(如表 2中狮子湾原水中<0.5×103的有机物TOC为1.66 mg·L-1, 处理水相应的TOC为1.67 mg·L-1), 这可能是因为大分子有机物或无机胶体吸附的部分小分子有机物在混凝沉淀过程中由于大分子有机物或胶体与金属离子络合作用而释放出来所至[17].
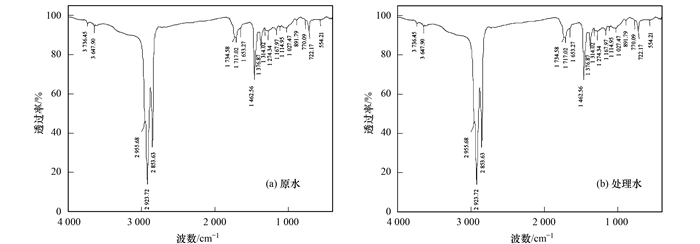
2.2.2 有机物基团及结构实验室采用红外光谱仪对不同水源的原水和处理水中有机物进行分子基团结构分析, 其红外光谱图基本一致.文中为方便后文分析, 列出跑马滩水库原水及处理水的红外光谱图, 见图 2.
|
图 2 跑马滩水库原水及处理水红外光谱图 Fig. 2 FTIR spectra of raw and treated water from the Paomatan Reservoir |
由红外光谱分析可知, 波峰主要集中在3个区域, 即3 400 cm-1左右、3 000~2 800 cm-1和1 800~430 cm-1.根据相关研究[18, 19], O—H键和C—O键特征吸收峰值在3 500~3 200 cm-1范围内, 对应醇类物质或酸类物质; 若O—H键特征吸收峰值在3 500~3 200 cm-1范围内, 同时C—O键特征吸收峰在1 300~1 200 cm-1范围内, 则为酚类物质; C—H键特征吸收峰位置在1 380 cm-1和1 470 cm-1附近及(2 960±10)cm-1和(2 570±10)cm-1, 对应烷类化合物; 羰基化合物主要有醛、酮、酯、酰胺, 醛和饱和酯的吸收峰值都在1 740 cm-1左右; 酸酐和酸卤的羰基键伸缩振动吸收在1 870~1 650 cm-1之间; 酮的羰基吸收峰在1725~1700 cm-1之间; 苯环特征吸收峰在1 600 cm-1、1 580 cm-1附近; C—O键和C—C键吸收在1 275~1 020 cm-1之间, C—O—C键不对称伸缩振动的吸收峰在1 150~1 060 cm-1之间, 对应醚类物质; C=C键伸缩振动在1 690~1 560 cm-1, 对应烯烃化合物, 根据指纹区可判断结构特征.
分析不同水源原水和处理水红外光谱图, 在3 200~3 500 cm-1之间存在吸收峰(如跑马滩原水3 343.93 cm-1、狮子湾原水3 429.43 cm-1、狮子湾处理水3 434.45 cm-1等), 判断存在醇类或酸类; 同时, 在1 300~1 200 cm-1范围内存在吸收峰, (如跑马滩原水1 280.37 cm-1、狮子湾原水1 259.27 cm-1、狮子湾处理水1 272.05 cm-1), 判断存在酚类物质; 在1 380 cm-1和1 470 cm-1附近及(2 960±10)cm-1和(2 570±10)cm-1处均有强烈吸收, 判断烷烃类化合物的确存在; 在1740 cm-1左右(如跑马滩原水1 735.88 cm-1、狮子湾原水3 429.43 cm-1、狮子湾处理水3 434.45 cm-1等), 判断存在醇类、醛类或酸类物质; 同时, 在1 300~1 200 cm-1范围内存在吸收峰, (如跑马滩原水1 280.37 cm-1、狮子湾原水1 259.27 cm-1、狮子湾处理水1 272.05 cm-1), 判断存在酚类物质; 在1 380 cm-1和1 470 cm-1附近及(2 960±10)cm-1和(2 570±10)cm-1处均有强烈吸收, 判断烷烃类化合物的确存在; 在1 870~1 650 cm-1之间有吸收峰(如跑马滩1 735.88、1 714.95、1 653.27 cm-1等), 判断存在酸酐类物质或酸卤物质; 在1 725~1 700 cm-1之间有吸收峰(如跑马滩1 714.95 cm-1、跑马滩处理后1 717.02 cm-1等), 判断存在酮类物质; 在1 600、1 580 cm-1附近存在吸收峰(如跑马滩原水1 602.80 cm-1), 判断存在苯类物质; 在1 275~1 020 cm-1和1 150~1 060 cm-1之间存在吸收峰(如狮子湾1 166.40 cm-1、1 076.57 cm-1), 判断存在醚类物质; 在1 690~1 560 cm-1之间有吸收峰(如跑马滩原水1 602.80 cm-1、1 630.80 cm-1等), 判断存在烯烃化合物, 且指纹区在730~650 cm-1范围内有吸收峰(如722.64 cm-1、767.29 cm-1等), 判断C=C为对称二取代顺式结构.
跑马滩处理水中3 500~3 200 cm-1之间的特征吸收峰消失, 可知水质净化常规工艺去除了原水中的醇类物质或酸类物质; 狮子湾处理水中1 725~1 700 cm-1之间的特征吸收峰消失, 可知水质净化常规工艺去除了原水中的酮类物质; 板凳垭村河塘新增了1 275~1 020 cm-1和1 150~1 060 cm-1之间的特征吸收峰, 可知处理水中新增了醚类物质.
2.2.3 有机物定性定量采用气相色谱-质谱联用分析不同水源原水及处理水中的有机物, 主要有机物及其质量浓度见表 3.将检测到的有机物分为烷、烯、酚、醇、醛、酯、苯、有机酸等8类主要物质, 根据以上各类物质质量浓度算得其占有机物总量的质量分数见表 4.
|
|
表 3 不同水源水处理前后主要有机物及质量浓度1)/mg·L-1 Table 3 Main organics and their concentrations in the raw and treated water from different water sources/mg·L-1 |
|
|
表 4 不同水源水处理前后有机物种类及质量分数1)/% Table 4 Main organic components and their contents in the raw and treated water from different water sources/% |
经检测, 狮子湾水库、麻子滩水库、跑马滩水库、白安河、板凳垭村河塘源水中分别检测出有机物30种、24种、30种、28种、27种, 包括烷类、烯类、醇类、醛类、酮类、酚类、苯类、酯类、酸类、酰胺类、酸酐类、农药、抗生素、内分泌干扰物等14类物质.其中, 属于集中式生活饮用水地表水源地特定项目[12]的有二氯甲烷、三氯甲烷、甲苯、乙苯、二甲苯、邻苯二甲酸二丁酯、丙烯腈、甲醛、乙醛等; 特定项目之外的其他物质如特丁津(terbuthylazine)[20, 21]、双酚A(bisphenol A, BPA), 食品添加剂2, 6-二叔丁基对甲酚(butylhydroxytoluene, BHT)、抗生素萘啶酸(NDA)等.特丁津常为除草剂, 具有“三致”作用, 且其结构稳定而被微生物矿化过程十分缓慢.双酚A是苯酚、丙酮的衍生物, 常用于生产高分子材料, 如塑料瓶、眼镜镜片、食品容器等, 其在工业中的广泛应用使其易进入水体, 进而危害水生生物和人体健康[22~24]. 2, 6-二叔丁基对甲酚为常用食品抗氧化剂[25], 有致癌、致畸性[26], 有实验研究表明, 它能引起老鼠后代脑部产生化学变化, 导致非正常行为[27], 人体饮入过量, 会对肾脏造成严重伤害.在狮子湾水库中检测到的萘啶酸, 属第一代喹诺酮类抗生素, 能有效治疗肾盂肾炎等由细菌感染引起的炎症, 但近年来, 该类药物在牛奶中残留进而危害人类健康的现象普遍发生, 各国已发布相关法规[28], 对牛奶中的喹诺酮类物质作了限量规定.显然, 水源水中出现这类物质, 是应当引起重视的.
从表 3可知, 二氯甲烷、苯酚、邻苯二甲酸二丁酯浓度较高, 二氯甲烷浓度在0.09~1 mg·L-1之间, 苯酚浓度在0.1~2.5 mg·L-1之间, 邻苯二甲酸二丁酯浓度在0.5~1.5 mg·L-1之间, 其浓度远超出饮用水标准限值[29].跑马滩水库中苯酚浓度极高, 为2.004 mg·L-1, 因其横跨乐至和安居两县市, 受工业污染严重而致.从表 4可知, 原水中酚、烷、酯、苯类含量较高, 酚类占总体有机物的20%~60%, 烷类占总体有机物的15%~30%, 酯类占总体有机物的10%~40%左右, 苯类占总体有机物的10%~20%左右.醛、烯、醇、有机酸类物质(比如萘啶酸)则含量较小, 所占比例大多不超过5%.
处理水中酯类、有机酸类在总的有机物中占比比原水有所减少, 有机酸几乎完全去除, 红外光谱中有机酸的吸收峰消失, 能得到同样的结论.而主要有机物如醛类、烷类、烯类、苯类、酚类物质所占比例增减不一, 去除效果不理想, 这与红外光谱图中处理前后基团的出现结果表现一致.其中, 出水中的致癌物二氯甲烷的去除率虽然在30%以上, 但处理水中其浓度仍超标[29](标准限值:0.02 mg·L-1, 除白安河外, 其他水源点处理水中二氯甲烷浓度均大于0.02 mg·L-1, 在0.1~0.5 mg·L-1之间).三氯甲烷、苯类、酚类等有毒物质去除不稳定, 甚至有所增加, 可见, 水质净化常规工艺对致癌性有机物不能有效去除, 尤其应引起饮水处理的关注.
3 结论(1) 西南丘陵区村镇典型供水水源受到不同程度污染, 为微污染水源水.水中有机物以中小分子有机物为主, 不同水源原水中, <10×103的有机物占总TOC的50%~80%, 相应处理水中占总TOC的70%~90%.由于大分子有机物去除效果好, 则处理水中小分子有机物占比增大.
(2) 通过红外光谱对有机物基团结构分析, 水中存在烷烃、烯烃、酚、苯、醇、醛、酯、醚、酮、酸类等物质.
(3) 通过气质联用对有机物定性定量分析, 不同水源水中共检测到53种共14类有机物, 包括烷烃、烯烃、酚、苯、醇、醛、酯、酮、酸、酰胺类、酸酐类、农药、抗生素、内分泌干扰物, 验证了红外光谱分析结果.其中, 以烷烃、酚、酯和苯类物质为主, 占总有机物的80%~90%左右, 有机酸、烯烃、醇和醛类物质质量浓度较小, 占总有机物的5%~20%左右.二氯甲烷、苯酚、邻苯二甲酸二丁酯等物质质量浓度较高, 并检测到除草剂、食品添加剂、抗生素等污染物, 如特丁津、2, 6-二叔丁基对甲酚、萘啶酸等, 以上物质应引起饮水处理的重视.
| [1] | 马葳, 盛卉. 汩汩清流润心田——"十二五"时期我国解决农村饮水安全问题纪实[N]. 经济日报, 2016-01-11(3). |
| [2] |
杨林章, 冯彦房, 施卫明, 等. 我国农业面源污染治理技术研究进展[J]. 中国生态农业学报, 2013, 21(1): 96-101. Yang L Z, Feng Y F, Shi W M, et al. Review of the advances and development trends in agricultural non-point source pollution control in China[J]. Chinese Journal of Eco-Agriculture, 2013, 21(1): 96-101. |
| [3] |
韩晓刚, 黄廷林. 水厂常规工艺去除有机物和总磷[J]. 环境工程学报, 2013, 7(5): 1616-1620. Han X G, Huang T L. Removal efficiency of organics and total phosphorus in conventional process of water plants[J]. Chinese Journal of Environmental Engineering, 2013, 7(5): 1616-1620. |
| [4] |
宋澄杰, 杜尔登, 王利平, 等. 饮用水预处理和深度处理工艺对有机物去除的特征研究[J]. 中国农村水利水电, 2014(10): 13-18. Song C J, Du E D, Wang L P, et al. The removal characteristics of organic matter by pre-treatment process and advanced treatment process in water treatment works[J]. China Rural Water and Hydropower, 2014(10): 13-18. DOI:10.3969/j.issn.1007-2284.2014.10.004 |
| [5] |
刘武平, 吕锡武, 朱光灿, 等. 常规处理与深度处理工艺对南京长江原水中有机物去除效能比较[J]. 净水技术, 2012, 31(2): 24-29. Liu W P, Lv X W, Zhu G C, et al. Comparison of organic matters removal efficiency between conventional and advanced treatment processes for Yangtze River raw water in Nanjing[J]. Water Purification Technology, 2012, 31(2): 24-29. |
| [6] |
高梦鸿, 高乃云, 周金金, 等. 由混凝或气浮构成的组合工艺处理太湖原水比较[J]. 哈尔滨工业大学学报, 2014, 46(8): 90-95. Gao M H, Gao N Y, Zhou J J, et al. Comparison of pilot effect between sedimentation and dissolved air flocculation for the treatment of Taihu Lake water[J]. Journal of Harbin Institute of Technology, 2014, 46(8): 90-95. |
| [7] |
韩瑾, 李星, 杨艳玲, 等. 东江水源水有机物分子量分布及其处理工艺选择[J]. 北京工业大学学报, 2013, 39(1): 87-91. Han J, Li X, Yang Y L, et al. Organic matter molecular weight distribution and process selection for the raw water of East River[J]. Journal of Beijing University of Technology, 2013, 39(1): 87-91. |
| [8] |
刘增军, 童祯恭, 侯煜堃, 等. 原水有机物分子量分布及去除特性研究——基于北方某水厂实测数据[J]. 华东交通大学学报, 2014, 31(4): 123-129. Liu Z J, Tong Z G, Hou Y K, et al. Molecular weight distribution and removal of raw water organics based on measured data of North China's water plant[J]. Journal of East China Jiaotong University, 2014, 31(4): 123-129. |
| [9] | Im ai, Fukushima T, Matsushige K, et al. Fractionation and characterization of dissolved organic matter in a shallow eutrophic lake, its inflowing rivers, and other organic matter sources[J]. Water Research, 2001, 35(17): 4019-4028. DOI:10.1016/S0043-1354(01)00139-7 |
| [10] |
龙小庆, 王占生. 活性炭-纳滤膜工艺去除饮用水中总有机碳和Ames致突变物[J]. 环境科学, 2001, 22(1): 75-77. Long X Q, Wang Z S. Removal of TOC and Ames mutagens from drinking water using AC-NF process[J]. Environmental Science, 2001, 22(1): 75-77. |
| [11] | Chang C N, Chao A, Lee F S, et al. Influence of molecular weight distribution of organic substances on the removal efficiency of DBPs in a conventional water treatment plant[J]. Water Science and Technology, 2000, 41(10-11): 43-49. |
| [12] | GB 5749-2006, 生活饮用水卫生标准[S]. |
| [13] | 胡锦涛. 胡锦涛总书记、温家宝总理、回良玉副总理关于农村饮水解困的重要批示和论述[J]. 中国水利, 2004(21): 5. |
| [14] | 王占生, 刘文君. 微污染水源饮用水处理[M]. 北京: 中国建筑工业出版社, 1999: 57-60. |
| [15] |
李公伟, 张奇, 卞荣星, 等. 纳滤浓缩液腐殖质组成及分子量分布特性[J]. 环境工程, 2016, 34(10): 31-34. Li G W, Zhang Q, Bian R X, et al. Composition and molecular weight distribution of humic substances in nanofiltration concentrate[J]. Environmental Engineering, 2016, 34(10): 31-34. |
| [16] |
朱文倩, 徐斌, 林琳, 等. 微污染水源中溶解性有机氮组成规律及其水处理特性[J]. 中国环境科学, 2014, 34(1): 130-135. Zhu W Q, Xu B, Lin L, et al. Studies on dissolved organic nitrogen compositions and water-treatment behavior in micro-polluted water[J]. China Environmental Science, 2014, 34(1): 130-135. |
| [17] |
施锦岳, 张玉先, 包卫彬. 姚江水源水有机物分子量分布[J]. 云南环境科学, 2005, 24(S1): 125-126. Shi J Y, Zhang Y X, Bao W B. Distribution of molecular weight of organic material of water source in Yaojiang River[J]. Yunnan Environmental Science, 2005, 24(S1): 125-126. |
| [18] | Silverstein R M, Webster F X, Kiemle D J. Spectrometric identification of organic compounds[M]. Shanghai: East China University of Science and Technology Press, 2007. |
| [19] |
姜小萍. 红外光谱定性解析原则[J]. 张家口师范专科学校学报, 2001, 17(6): 56-58. Jiang X P. About the Principl of IR in the characteristics of analyses[J]. Journal of Zhangjiakou Teachers College, 2001, 17(6): 56-58. |
| [20] | 王贵启, 张秀仿. 农药与环境安全国际会议论文集[M]. 北京: 中国农业大学出版社, 2005: 510-514. |
| [21] |
连玉朱, 王金信, 李龙森, 等. 特丁津与扑草净、莠去津活性比较[J]. 农药科学与管理, 2005, 26(11): 23-25. Lian Y Z, Wang J X, Li L S, et al. Biological activity comparation of terbuthylazine with prometryn and atrazine[J]. Pesticide Science and Administration, 2005, 26(11): 23-25. DOI:10.3969/j.issn.1002-5480.2005.11.011 |
| [22] | Mountfort K A, Kelly J, Jickells S M, et al. Investigations into the potential degradation of polycarbonate baby bottles during sterilization with consequent release of bisphenol A[J]. Food Additives & Contaminants, 1997, 14(1-7): 737-740. |
| [23] |
徐红梅, 江云, 谢庆效, 等. 双酚A对昆明小鼠免疫毒性的研究[J]. 环境科学学报, 2015, 35(9): 3013-3019. Xu H M, Jiang Y, Xie Q X, et al. Immunotoxicity of bisphenol A on Kunming mice[J]. Acta Scientiae Circumstantiae, 2015, 35(9): 3013-3019. |
| [24] | Staples C A, Dome P B, Klecka G M, et al. A review of the environmental fate, effects, and exposures of bisphenol A[J]. Chemosphere, 1998, 36(10): 2149-2173. DOI:10.1016/S0045-6535(97)10133-3 |
| [25] |
段文仲, 马育松, 庞津霞. 新欧盟指令对塑料食品接触材料产业影响及对策研究[J]. 塑料包装, 2011, 21(6): 23-28. Duan W Z, Ma Y S, Pang J X. New EU directives lead to influence and countermeasures research for the food plastic packaging and related industrieslevels[J]. Plastics Packaging, 2011, 21(6): 23-28. |
| [26] | Umemura T, Kodama Y, Hioki K, et al. Butylhydroxytoluene (BHT) increases susceptibility of transgenic rasH2 mice to lung carcinogenesis[J]. Journal of Cancer Research and Clinical Oncology, 2001, 127(10): 583-590. DOI:10.1007/s004320100268 |
| [27] |
刘志刚, 王志伟. 塑料包装材料化学物向食品迁移的模型研究进展[J]. 高分子材料科学与工程, 2007, 23(5): 19-23. Liu Z G, Wang Z W. Study on mathematical model for predicting migration of chemical substances from plastic packaging materials[J]. Polymer Materials Science & Engineering, 2007, 23(5): 19-23. |
| [28] | European Union. Commission Regulation (EC) No 508/1999 of 4 March1999[Z]. Official Journal of the European Communities, 1999. |
| [29] | GB 3838-2002, 地表水环境质量标准[S]. |
 2018, Vol. 39
2018, Vol. 39


