2. 江苏省水处理技术与材料协同创新中心, 苏州 215009;
3. 江苏省环境科学与工程重点实验室, 苏州 215009
2. Jiangsu Collaborative Innovation Center of Water Treatment Technology and Material, Suzhou 215009, China;
3. Key Laboratory of Environmental Science and Engineering of Jiangsu Province, Suzhou 215009, China
传统生物脱氮除磷工艺(如A2/O)存在氮和磷去除对碳源的竞争.生活污水的生物脱氮除磷常因碳源不足影响处理效果[1].自Kuba等[2]观察到一类能够以O2或者NO3--N作为电子受体吸磷的兼具反硝化和除磷作用的兼性厌氧菌, 以及Satio等[3]报道NO2--N也可以作为电子受体进行吸磷反应, 并将此类微生物统称为反硝化除磷菌(denitrifying phosphorus removal bacteria, DPBs), 为这一问题的解决提供了有效途径.与聚磷菌(PAOs)的不同之处在于, DPBs可在缺氧环境下利用NO3-/NO2-而非O2作为电子受体进行吸磷[4, 5].因此, 可在碳源有限的条件下实现“一碳两用”之效[6~8].
有研究表明, 厌氧折流板反应器(ABR)可与其它好氧反应器协同组合, 获得上述问题的解决[9]. ABR反应器不仅可实现微生物相的有效分离, 亦可实现对底物不同阶段和不同程度的转化[10], 产生VFA等优质碳源, 为除磷以及反硝化除磷提供优质碳源.近年来, 膜生物反应器(MBR)凭借其高效的生物截留作用及泥龄(SRT)与水力停留时间(HRT)完全分离的优势, 并随着制膜成本和运转费用的下降而被日趋广泛地得到应用[11].
实现短程硝化(亚硝化)的主要控制因素有:HRT[12]、DO浓度[13]、温度[14]、SRT[15]、pH值[16]、游离氨(FA)和游离亚硝酸(FNA)[17, 18]等.本研究以生活污水为研究对象, 采用前期研究构建、旨在节能低碳消耗并取得满意效果[19~21]的ABR-MBR协同组合工艺, 考察其实现短程硝化的调控措施, 以期为实现基于短程硝化的反硝化除磷提供优化运行条件.
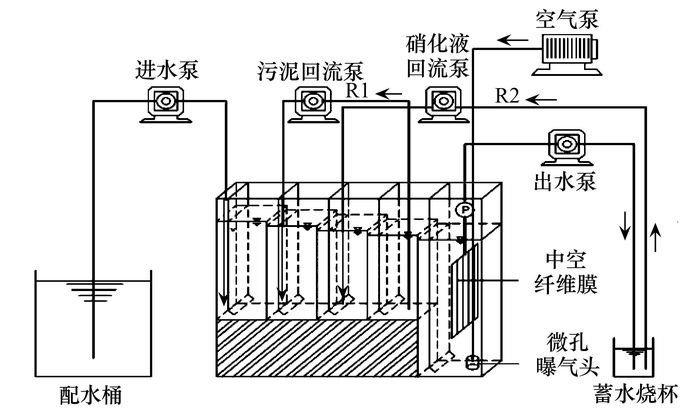
1 材料与方法 1.1 试验装置本研究采用的ABR-MBR一体化反应器工艺如图 1所示.其中, ABR由4个隔室组成, 有效容积为7.2 L; MBR有效容积为3.6 L.运行过程中, 控制ABR第1、2隔室为厌氧, 第3、4隔室为缺氧, MBR为好氧运行. MBR反应器采用间歇抽吸出水, 抽吸周期为10 min(8 min出水/2 min反冲洗), 底部采用微孔曝气供氧.膜组件采用PVDF柱状式中空纤维膜, 膜孔径为0.2 μm, 采用真空压力表测定跨膜压差(TMP)以反映膜的污染情况, 一旦TMP≥30 kPa, 则对膜组件进行化学清洗.
|
图 1 ABR-MBR工艺试验装置 Fig. 1 Schematic diagram of the ABR-MBR setup |
为实现短程反硝化除磷, 设置两个回流.一是污泥回流R1:将ABR第4隔室污泥回流至ABR第2隔室, 旨在利用优质碳源释磷; 二是硝化液回流R2:将MBR硝化液回流至ABR第3隔室, 使其处于缺氧环境而实现反硝化除磷.采用蠕动泵控制进、出水和R1、R2, 并采用可编程逻辑控制器(PLC)控制水位的恒定并实现出水、冲洗等运行过程的自动控制.
1.2 试验用水和污泥试验用水为生活污水与人工配水为1:1的低C/N模拟污水, 各项水质指标见表 1所列.采用葡萄糖、淀粉和蛋白胨及氯化铵、磷酸二氢钾适当补充、调节碳源和氮、磷.试验用生活污水取自苏州市某高校生活污水, 接种污泥取自苏州某城市污水处理厂贮泥池及A2/O好氧池, 后者属全程硝化污泥. ABR反应器各隔室接种污泥MLSS约为28 000 mg·L-1, MBR反应器内接种污泥MLSS约为4 000 mg·L-1.
|
|
表 1 原水水质 Table 1 Characteristics of the raw wastewater |
1.3 分析测定方法
水样经0.45 μm中性滤纸过滤后按照标准方法[22]分别测定COD、NH4+-N、NO2--N、NO3--N、PO43--P.试验中检测项目及其分析方法详见表 2.数据分析中, 分别按式(1)和式(2)计算亚硝酸盐积累率(NAR)和MBR的实际水力停留时间(AHRT).
|
|
表 2 检测项目分析方法 Table 2 Test items and analytical methods for water quality |
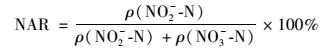
|
(1) |
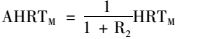
|
(2) |
式中, ρ(NO2--N)和ρ(NO3--N)为MBR反应器出水NO2--N和NO3--N的质量浓度(mg·L-1); AHRTM为MBR的实际水力停留时间(h); HRTM为MBR的名义水力停留时间(h).
1.4 试验过程本研究运行分为5个阶段(Ⅰ~Ⅴ), 各个阶段的运行参数如表 3所列.每个运行工况均在系统稳定运行后进行取样分析.试验过程中, 以水浴加热控制温度.冬季反应器内水温维持在25℃±2℃, 夏季则维持在30℃±2℃. MBR采用低氧曝气方式运行, 其DO浓度为0.3~1.0 mg·L-1.
|
|
表 3 试验过程及参数和条件控制 Table 3 Experimental processes and parameter/condition control |
2 结果与讨论 2.1 ABR-MBR工艺短程硝化的实现
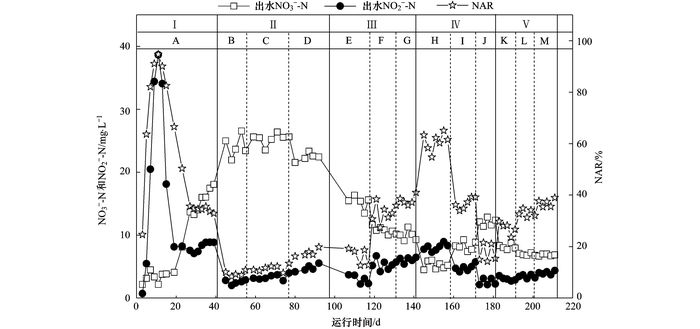
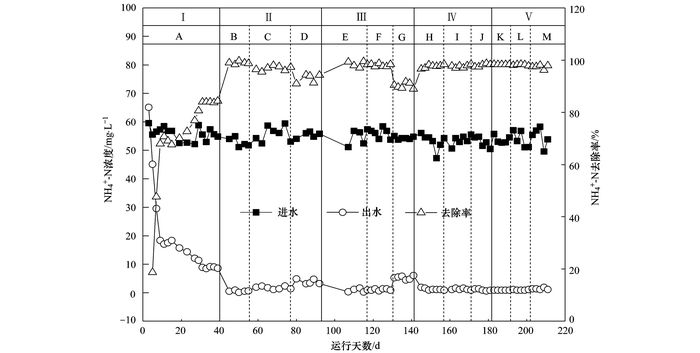
图 2所示为5个阶段的试验期间13个工况下MBR出水NO3--N、NO2--N和亚硝酸盐积累率(NAR)的变化情况. 图 3所示为进出水氨氮浓度及氨氮去除率的变化.
|
图 2 ABR-MBR工艺中NO3--N和NO2--N浓度及NAR的变化 Fig. 2 Variations of NO3--N, NO2--N and NAR in the ABR-MBR process |
|
图 3 ABR-MBR工艺中氨氮去除情况 Fig. 3 Removal of NH4+-N in the ABR-MBR process |
运行的1~39 d为第Ⅰ阶段.此阶段为污泥适应期, 未进行污泥和硝化液的回流.因研究中所接种的污泥为全程硝化污泥, 因而本身无NO2--N的积累.采取低DO运行, 利用低氧条件下AOB和NOB增值速率上的差异, 逐步实现AOB的富集.由图 2可见, 在运行的较短时间内出现了亚硝酸盐的积累, 其亚硝酸盐积累率(NAR)高于90%.其原因有3个:一是较短的HRT有利于AOB将氨氮氧化过程控制在亚硝化阶段.二是由图 3可见, 进水氨氮平均浓度为55 mg·L-1, 最高达60 mg·L-1.高的氨氮负荷利于AOB的增殖.三是游离氨(FA)的增多有利于亚硝酸盐的积累.试验阶段Ⅰ初期氨氮去除率较低, 导致MBR反应器中存在大量FA.
第Ⅱ阶段进行污泥回流和硝化液回流, 并控制ABR的HRT为12h, 污泥回流比和硝化液回流比均为100%, 其中通过调节MBR的HRT以实现短程硝化.由图 2可见, 在第Ⅱ阶段初期, MBR的HRT为6h时, MBR出水NO2--N浓度较第Ⅰ阶段有所降低, 随着MBR的HRT继续缩短, MBR出水NO2--N浓度略有增加, 而出水NO3--N浓度基本维持在25 mg·L-1左右, NAR平均仅有12.7%.由此可见, 由于第Ⅰ阶段的适应期较长且系统HRT较长, 导致污泥的硝化性能良好, 本阶段属于稳定的全程硝化阶段.
第Ⅲ阶段将ABR的HRT缩短至9h, 硝化液回流比增大至200%.如图 2所示, 随着MBR的HRT逐渐从6h缩短至4h, MBR出水NO2--N浓度逐步上升, NAR逐渐升高, 由第Ⅱ阶段最低的8%提高至40%左右, 相较于第Ⅱ阶段有显著的提高.由此可见, 系统HRT的缩短以及由增大硝化液回流比引起的在HRTM逐步缩短基础上AHRTM更进一步的降低导致了NAR逐渐升高, 本阶段为亚硝酸盐积累率上升期.
第Ⅳ阶段将ABR的HRT缩短至6 h, 硝化液回流比增大至300%, 本阶段将HRTM从第Ⅲ阶段末期的3 h逐步延长至5 h.由图 2可见, 在HRTM=3h工况下实现了短程硝化, 并稳定维持至下一工况, 时间长达15 d, NAR平均为61%, 最高达到65%, 而随着HRTM的增大, 短程硝化被破坏, NAR呈下降趋势.由此可见, 低HRT对短程硝化的影响很大, 当R2=300%, HRTM=3 h时, AHRTM达到一个最优值, 使短程硝化得以实现并稳定维持.
第Ⅴ阶段将ABR的HRT继续缩短至4 h, 硝化液回流比增大至400%, 由图 2可见, 虽然系统的HRT和AHRTM较第Ⅳ阶段更短, 且NAR也随着HRTM的缩短而升高, 但仍然未获得理想的短程硝化效果, MBR出水NO2--N浓度有所降低, 从而本阶段的NAR在整体上低于第Ⅳ阶段.
2.2 ABR-MBR系统中亚硝酸盐积累的影响因素Hellinga等认为[23], 实现与维持短程硝化的最佳温度是30~35℃, 此时AOB的生长速率高于NOB. Balmelle等认为[24], AOB最佳生长pH值约为8.5.本研究试验期间, MBR中pH值平均为8.27, 变化范围为8.03~8.54, 在此范围内AOB与NOB活性相当, 故pH值不能作为实现短程硝化的主要影响因素. Anthonisen等报道[25], FA对AOB和NOB抑制范围分别是10~150 mg·L-1和0.1~1.0 mg·L-1.本研究根据式(3)计算得出短程硝化期间FA浓度仅为0.22 mg·L-1, 处于较低水平, 无法作为实现短程硝化的控制因素. Vadivelu等发现[26], 当FNA>0.1mg·L-1时, AOB受到抑制; 当FNA>0.011 mg·L-1时, NOB受到抑制.根据式(4)计算得出本研究短程硝化期间FNA平均值为0.00027mg·L-1, 对AOB和NOB均未起到抑制作用, 因此FNA亦不是本系统实现短程硝化的控制因素.
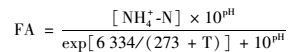
|
(3) |
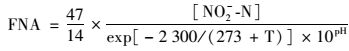
|
(4) |
本研究中成功实现并维持短程硝化的原因有以下4点:①低DO. Guisasola等报道[27], AOB和NOB的氧饱和常数分别为0.3~0.5 mg·L-1和0.7~1.8 mg·L-1, 另外有研究得出AOB和NOB的氧饱和常数分别为0.25~0.6 mg·L-1和0.72~2.2 mg·L-1, 均证实AOB的氧饱和常数低于NOB, 说明低DO浓度下AOB具有比NOB更强的竞争优势.本试验全程维持DO浓度在较低水平, 导致NOB的活性长期受到抑制并通过排泥而被淘汰出系统, AOB成为优势菌种. ②短HRTM.有研究表明, 好氧HRT过长不利于短程硝化的实现并维持[28, 29].延长好氧HRT意味着降低了氨氮负荷, 限制了AOB的增殖, 不利于促进系统系统对NOB的淘洗和AOB的富集.本研究在既定HRT时逐步缩短HRTM, NAR也逐渐升高并稳定维持. ③短AHRTM.第Ⅳ阶段, HRTM=3 h, R2=300%时, 成功实现了短程硝化, 这是因为随着硝化液回流比的增大, AHRTM进一步缩短, 将氨氮的氧化过程控制在了亚硝化阶段, 加速了NO2--N在好氧区和缺氧区的交替, 在MBR中生成的NO2--N立即随回流液进入到了缺氧区, 以充当缺氧吸磷的电子受体而被去除. ④合适的固体停留时间(SRT). Van等[15]认为AOB世代周期较NOB略短, 温度在14℃以上时, AOB和NOB的世代周期分别为8~36 h和12~59 h.控制SRT介于AOB和NOB的泥龄之间便可一定程度实现AOB的积累, 通过排泥将NOB逐渐淘洗掉, 进一步提高AOB在硝化菌群中的比例[12].本试验控制SRT为15~20 d, 与前述控制因素共同作用, 最终实现短程硝化.
2.3 ABR-MBR工艺对氮素的去除图 3所示为ABR-MBR工艺中氨氮去除情况.从中可见, 试验第Ⅰ阶段为污泥适应期, MBR硝化性能不好, NH4+-N去除率不高.试验第Ⅱ阶段好氧MBR的DO维持在0.5~1.0 mg·L-1, 系统对NH4+-N的去除率在95%以上(见图 4), 但由于该阶段硝化液回流比为100%, 导致系统对TN去除率仅为45.8%, 出水NO3--N浓度在24 mg·L-1左右.从图 3中第Ⅱ阶段的B、C、D工况可以看出, 随着HRTM的逐渐缩短, NH4+-N的去除率也随之下降, 可见, HRTM的长短对MBR的硝化性能影响较大.如图 3所示, 在试验第Ⅲ阶段, MBR的DO维持在0.3~0.7 mg·L-1, ABR水力停留时间缩短至9 h, 回流比提高至200%, 系统TN去除率平均达到65%, 出水NO3--N浓度在12 mg·L-1左右, 随着HRTM的缩短依旧与上一阶段一样出现NH4+-N去除率下降的趋势, 且由于DO浓度进一步降低的缘故下降幅度较上一阶段有所增大.试验第Ⅳ阶段, ABR水力停留时间缩短至6 h, 回流比提高至300%, 系统TN去除率平均达到72%, 在此阶段的工况H下, MBR实现了短程硝化, 出水NAR达到60%以上, MBR对NH4+-N的去除率稳定在97.8%(见图 3和图 4).试验第Ⅴ阶段, ABR的HRT缩短至4 h, 回流比提高至400%, TN去除率可达78%, 且随着HRTM的变化, NH4+-N去除率维持在98%左右.
|
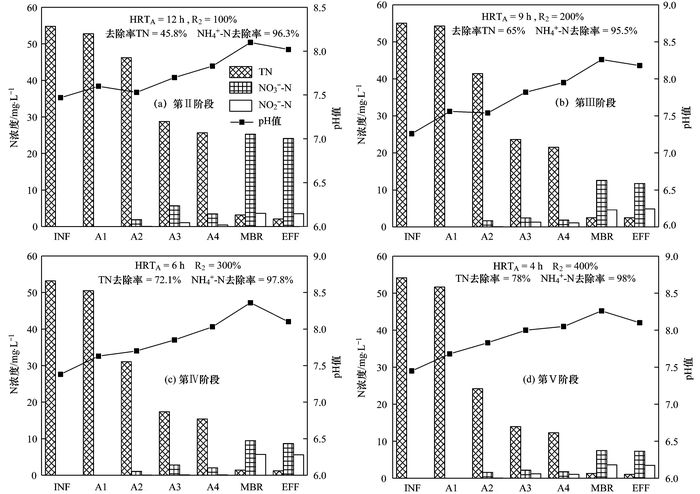
图 4 ABR-MBR工艺各阶段氮素和pH值变化 Fig. 4 Variation of nutrients and pH along the reactor in the ABR-MBR process during different stages |
图 4是系统在不同阶段下, 稳定运行后具有代表性的各项水质指标的沿程变化情况. 图 4(a)是试验第Ⅱ阶段反应器各隔室氮素和pH值的变化规律.由图 4(b)可见, 第Ⅲ阶段缩短ABR水力停留时间和增大回流比后反硝化脱氮和除磷性能均有提升, 相比于第Ⅱ阶段, 缺氧区的pH值上升幅度更大, 第2隔室pH值下降幅度减小, 降幅由第Ⅱ阶段的0.08变为第Ⅲ阶段的0.04, 但整体仍表现为低于第1隔室的pH值. 图 4(c)反映的是由于ABR的HRT缩短和回流比的增大, 反硝化脱氮和除磷性能进一步提升, 但反硝化脱氮作用强于释磷作用, 导致整体表现为第2隔室pH值上升. 图 4(d)为第Ⅴ阶段时氮素和pH值的变化情况, 总体趋势与上一阶段相同, 第2隔室pH值上升幅度较第Ⅳ阶段更大, 升幅由0.08提高至0.12, 由此可见, 此阶段反硝化脱氮作用产生了较第Ⅳ阶段更多的碱度, 也说明了反硝化脱氮作用与释磷作用之间的差距更为明显.
|
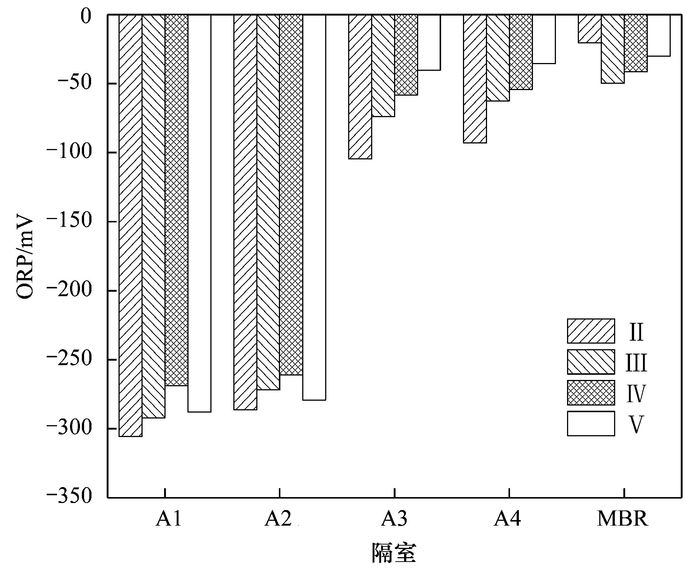
图 5 不同阶段下各隔室ORP变化规律 Fig. 5 Variation of ORP along the reactor in the ABR-MBR process during different stages |
不同阶段下, 系统ORP各隔室变化情况见图 5. 4个阶段ORP的变化规律相同.由于首段厌氧区DO浓度最低且无NOx--N, 因此ORP也最低.由于后续好氧区的硝化液回流, 缺氧区存在少量的DO和NOx--N, 其浓度介于厌氧区和好氧区之间, 因此缺氧区ORP自然也介于两者之间.好氧区由于曝气的作用DO浓度较高, 且含有大量的NOx--N, 因此ORP最高.另外, 从图 5中也可以看出, 随着硝化液回流比的逐渐增大, ABR第3、4隔室的ORP也随之依次增大.
3 结论(1) 采用ABR-MBR耦合工艺处理实际生活污水, 在ABR的HRT为6 h, MBR的HRT为3 h, DO浓度为0.3~0.7mg·L-1, 污泥回流比为100%, 硝化液回流比为300%, 温度为30℃±2℃的条件下, MBR中成功实现了短程硝化, 且平均亚硝酸盐积累率为60%, 最高达65%.
(2) 短程硝化期间, 系统获得了高效且稳定的COD和NH4+-N去除效果, 平均出水浓度分别低于50mg·L-1和2mg·L-1, 去除率均在90%以上, TN平均去除率高达72%.
(3) 短程硝化影响因素的分析表明:pH值、游离氨(FA)和游离亚硝酸(FNA)对本试验实现短程硝化无显著影响, 维持低DO浓度(0.3~0.7mg·L-1)并逐步缩短HRT是本试验实现短程硝化的关键控制因素, 温度和污泥停留时间(SRT)可作为辅助因素与之共同调控.
| [1] | Baeza J A, Gabriel D, Lafuente J. Improving the nitrogen removal efficiency of an A2/O based WWTP by using an on-line knowledge based expert system[J]. Water Research, 2002, 36(8): 2109-2123. DOI:10.1016/S0043-1354(01)00402-X |
| [2] | Kuba T, Smolders G, Van Loosdrecht M C M, et al. Biological phosphorus removal from wastewater by anaerobic-anoxic sequencing batch reactor[J]. Water Science and Technology, 1993, 27(5-6): 241-252. |
| [3] | Saito T, Brdjanovic D, Van Loosdrecht M C M. Effect of nitrite on phosphate uptake by phosphate accumulating organisms[J]. Water Research, 2004, 38(17): 3760-3768. DOI:10.1016/j.watres.2004.05.023 |
| [4] | Carvalho G, Lemos P C, Oehmen A, et al. Denitrifying phosphorus removal:linking the process performance with the microbial community structure[J]. Water Research, 2007, 41(19): 4383-4396. DOI:10.1016/j.watres.2007.06.065 |
| [5] | Hu Z R, Wentzel M C, Ekama G A. Anoxic growth of phosphate-accumulating organisms(PAOs) in biological nutrient removal activated sludge systems[J]. Water Research, 2002, 36(19): 4927-4937. DOI:10.1016/S0043-1354(02)00186-0 |
| [6] | Lee D S, Jeon C O, Park J M. Biological nitrogen removal with enhanced phosphate uptake in a sequencing batch reactor using single sludge system[J]. Water Research, 2001, 35(16): 3968-3976. DOI:10.1016/S0043-1354(01)00132-4 |
| [7] | Merzouki M, Bernet N, Delgenès J P, et al. Effect of prefermentation on denitrifying phosphorus removal in slaughterhouse wastewater[J]. Bioresource Technology, 2005, 96(12): 1317-1322. DOI:10.1016/j.biortech.2004.11.017 |
| [8] | Tsuneda S, Ohno T, Soejima K, et al. Simultaneous nitrogen and phosphorus removal using denitrifying phosphate-accumulating organisms in a sequencing batch reactor[J]. Biochemical Engineering Journal, 2006, 27(3): 191-196. DOI:10.1016/j.bej.2005.07.004 |
| [9] |
沈耀良, 王宝贞. 废水生物处理新技术:理论与应用[M]. 第二版. 北京: 中国环境科学出版社, 2006. Shen Y L, Wang B Z. New thchnologies for biological wastewater treatment theory and application[M]. 2nd ed. Beijing: China Environmental Science Press, 2006. |
| [10] | Shen Y L, Wu P, Wang J F, et al. State-of-the-art of anaerobic baffled reactor treating low-strength sewage[J]. Journal of Suzhou University of Science and Technology(Engineering and Technology), 2015, 28(2): 1-10. |
| [11] | Brown P, Ong S K, Lee Y W. Influence of anoxic and anaerobic hydraulic retention time on biological nitrogen and phosphorus removal in a membrane bioreactor[J]. Desalination, 2011, 270(1-3): 227-232. DOI:10.1016/j.desal.2010.12.001 |
| [12] |
曾薇, 李磊, 杨莹莹, 等. A2O工艺处理生活污水短程硝化反硝化的研究[J]. 中国环境科学, 2010, 30(5): 625-632. Zeng W, Li L, Yang Y Y, et al. Short-cut nitrification and denitrification in A2O process treating domestic wastewater[J]. China Environmental Science, 2010, 30(5): 625-632. |
| [13] |
张小玲, 王志盈. 低溶解氧下SBR内短程硝化影响因素试验研究[J]. 环境科学与技术, 2011, 34(1): 163-166. Zhang X L, Wang Z Y. Experimental study on influencing factors of short-cut nitrification at low DO concentration[J]. Environmental Science & Technology, 2011, 34(1): 163-166. |
| [14] | Blackburne R, Yuan Z, Keller J. Partial nitrification to nitrite using low dissolved oxygen concentration as the main selection factor[J]. Biodegradation, 2008, 19(2): 303-312. DOI:10.1007/s10532-007-9136-4 |
| [15] | Van Kempen R, Mulder J W, Uijterlinde C A, et al. Overview:full scale experience of the SHARON® process for treatment of rejection water of digested sludge dewatering[J]. Water Science andTechnology, 2001, 44(1): 145-152. |
| [16] |
孙洪伟, 王淑莹, 魏东洋, 等. pH对高氨氮渗滤液短程生物脱氮反硝化过程动力学的影响[J]. 环境科学学报, 2010, 30(4): 742-748. Sun H W, Wang S Y, Wei D Y, et al. The effect of pH on the kinetics of denitritation in nitrogen removal via nitrite from landfill leachate with high ammonia concentration[J]. Acta Scientiae Circumstantiae, 2010, 30(4): 742-748. |
| [17] | Park S, Bae W. Modeling kinetics of ammonium oxidation and nitrite oxidation under simultaneous inhibition by free ammonia and free nitrous acid[J]. Process Biochemistry, 2009, 44(6): 631-640. DOI:10.1016/j.procbio.2009.02.002 |
| [18] | Vadivelu V M, Keller J, Yuan Z. Free ammonia and free nitrous acid inhibition on the anabolic and catabolic processes of Nitrosomonas and Nitrobacter[J]. Water Science and Technology, 2007, 56(7): 89-97. DOI:10.2166/wst.2007.612 |
| [19] | Wu P, Ji X M, Song X K, et al. Nutrient removal from municipal wastewater and microbial community analysis of a combined ABR-MBR(CAMBR) process[J]. CLEAN-Soil, Air, Water, 2014, 42(6): 753-759. DOI:10.1002/clen.v42.6 |
| [20] |
刘捷, 吴鹏, 沈耀良. CAB-MBR复合反应器实现亚硝化-脱氮除磷的启动研究[J]. 环境工程学报, 2014, 8(8): 3247-3252. Liu J, Wu P, Shen Y L. Start-up of CAB-MBR nitrosation-nitrogen and phosphorus removal[J]. Chinese Journal of Environmental Engineering, 2014, 8(8): 3247-3252. |
| [21] |
程继辉, 吴鹏, 程朝阳, 等. 基于优质碳源提供的CAMBR复合工艺短程硝化-反硝化除磷研究[J]. 环境科学, 2015, 36(12): 4539-4545. Cheng J H, Wu P, Cheng C Y, et al. Shortcut nitrosation-denitrifying phosphorus removal based on high-quality carbon source in combined process of CAMBR[J]. Environmental Science, 2015, 36(12): 4539-4545. |
| [22] | AP HA. Standard methods for the examination of water and wastewater[M]. 17th ed. Washington, DC: American Public Health Association, 1989. |
| [23] | Hellinga C, Schellen A A J C, Mulder J W, et al. The sharon process:an innovative method for nitrogen removal from ammonium-rich waste water[J]. Water Science and Technology, 1998, 37(9): 135-142. |
| [24] | Balmelle B, Nguyen K M, Capdeville B, et al. Study of factors controlling nitrite build-up in biological processes for water nitrification[J]. Water Science and Technology, 1992, 26(5-6): 1017-1025. |
| [25] | Anthonisen A C, Loehr R C, Prakasam T B, et al. Inhibition of nitrification by ammonia and nitrous acid[J]. Journal-Water Pollution Control Federation, 1976, 48(5): 835-852. |
| [26] | Vadivelu V M, Keller J, Yuan Z G. Effect of free ammonia and free nitrous acid concentration on the anabolic and catabolic processes of an enriched Nitrosomonas culture[J]. Biotechnology and Bioengineering, 2006, 95(5): 830-839. DOI:10.1002/(ISSN)1097-0290 |
| [27] | Guisasola A, Jubany I, Baeza J A, et al. Respirometric estimation of the oxygen affinity constants for biological ammonium and nitrite oxidation[J]. Journal of Chemical Technology and Biotechnology, 2005, 80(4): 388-396. DOI:10.1002/(ISSN)1097-4660 |
| [28] | Ma Y, Peng Y Z, Wang S Y, et al. Achieving nitrogen removal via nitrite in a pilot-scale continuous pre-denitrification plant[J]. Water research, 2009, 43(3): 563-572. DOI:10.1016/j.watres.2008.08.025 |
| [29] | Zeng W, Li L, Yang Y, et al. Nitritation and denitritation of domestic wastewater using a continuous anaerobic-anoxic-aerobic(A2O) process at ambient temperatures[J]. Bioresource Technology, 2010, 101(21): 8074-8082. DOI:10.1016/j.biortech.2010.05.098 |
 2017, Vol. 38
2017, Vol. 38


