2. 北京市环境保护监测中心, 北京 100048
2. Beijing Municipal Environmental Monitoring Centre, Beijing 100048, China
酸性矿山废水(acid mine drainage, AMD)是硫化矿物暴露于地表, 与水、大气、微生物相互作用, 发生氧化性溶解形成的, pH通常小于3, 且含有高浓度重金属如Fe、Al、Cu等和SO42-, 危害十分严重[1].在自然界, 酸性矿山废水主要由黄铁矿(FeS2)氧化形成[2].黄铁矿的氧化过程为:
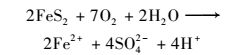
|
(1) |
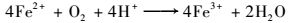
|
(2) |
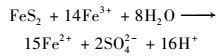
|
(3) |
可以看出, 在黄铁矿的氧化过程中, Fe3+是主要的氧化剂[2]. Fe3+氧化FeS2产生H2SO4和Fe2+, Fe2+可以被氧化产生Fe3+, Fe3+又可以氧化FeS2, 从而形成了一个循环.但在酸性条件下Fe2+的氧化速度非常缓慢, 是黄铁矿氧化的限速步骤.而化能自养的嗜酸微生物可以氧化Fe2+而获得能量, 促进Fe2+向Fe3+转化, 在反应中起到高效催化剂的作用[3].由此可见, 研究酸性环境中嗜酸菌的群落组成和分布规律对理解酸性矿山废水的形成机制、修复矿山环境污染有重要意义.
酸性矿山废水在世界上广泛分布.在我国, 酸性矿山废水问题也相当严重, 我国绝大部分金属矿山为原生硫化物矿床.采矿过程中遗弃的大量硫化物废石, 经过风化、淋溶, 极易形成酸性矿山废水[4].安徽某铁矿排土场是一个典型的酸性矿山废水污染环境, 排土场是该铁矿的主要废矿石堆放地, 每年都要接纳700~800万t废矿石, 现已堆放废矿石约1亿t.这些废矿石在嗜酸菌催化下发生氧化分解, 含硫酸根和重金属的酸性废水汇集到排土场中央, 并于20世纪70年代形成一个酸水库.目前, 该酸水库东西宽约300 m, 南北长约700 m, 库容量约300万m3, pH常年在3.5以下.此外, 在该酸水库周边还存在一些形成于近年的小范围酸性矿山废水, 其酸性更强, 金属离子含量更高, 危害十分严重.
为研究该区域废矿石的产酸潜力及产酸微生物群落, 采集了该酸水库周边长期堆放的废矿石以及附近另外两处新形成的酸性矿山废水周边的废矿石, 利用分子生物学方法研究样品中嗜酸微生物群落组成和变化规律.本研究结果有助于人们更好地了解极端酸性环境中产酸微生物群落组成, 真正认识微生物在废矿石不同产酸阶段所扮演的角色, 以期为修复和控制重金属污染的矿山排土场环境提供一定技术支持.
1 材料与方法 1.1 样品采集为研究该区域废矿石的产酸潜力及产酸微生物群落, 于2014年5月在安徽某铁矿排土场采集废矿石样品6个, 分别为大型酸水库边1号位裸露1LL, 新形成的小型酸水坑AMD 5号位旁5号位近5J、5号位远5Y, 围绕6号位酸水坑边周围距离酸水0.5 m采集6-1、6-2和6-3.所有样品均为0~20 cm表层废矿石.样品采集后装于无菌封口袋中尽快返回实验室操作.
1.2 物化参数测定用烘干法测定含水率[5].用KCl溶液测定pH值.按1:5水土比测定土壤浸提液的电导率[6].使用M3浸提液浸提阳离子和金属元素[7], Ca(H2PO4)2浸提剂浸提硫酸根.阴离子浓度用美国Thermo公司ICS-600离子色谱仪测定, 金属元素用ICP(iCAP 6000, Thermo)测定. Fe2+参照文献[8]的方法测定. M3浸提液离心后, 用钼锑抗分光光度法测定有效磷.总有机碳(total organic carbon, TOC)用总有机碳分析仪(Multi N/C 2100) 测定.硫元素用元素分析仪(EA3000意大利, EuroVector公司)测定.
1.3 基因组DNA提取取0.5g样品, 用基因组DNA提取试剂盒提取样品中的基因组DNA, 参照MPbio试剂盒生产商建议的步骤.提取的DNA用Nanodrop 2000 Spectrophotometer(Thermo Scientific, 美国)测定DNA浓度后置于-80℃超低温冰箱保存.
1.4 16S rRNA基因片段的扩增以基因组DNA为模板, 使用高通量测序引物F515 (5′-GTGCCAGCMGCCGCGGTAA-3′)和R806 (5′-GGACTACVSGGGTATCTAAT-3′)对16S rRNA基因V4区进行扩增[9].在反向引物806R的5′端添加一段12bp的碱基序列作为barcode, 用于区分不同的样品. PCR反应条件为:预变性94℃ 3 min; 94℃ 30 s, 50℃ 60 s, 72℃ 90 s, 共35个循环, 最后在72℃下延伸10 min.
将各样品PCR产物等摩尔比混匀, 用Life Technologies公司的PGM测序系统进行高通量测序.测序工作在中国农业科学院作物研究所完成.
1.5 微生物组成与统计学分析用Mothur软件将反向序列反转, 去除低质序列和嵌合体, 统一测序深度至1万条序列.将目的片段与Sliva. bacteria-archaea数据库对齐, 构建距离矩阵.以97%的序列相似性进行OTU划分.用R语言做PCoA分析, 加载gplots程序包用heatmap.2函数绘制热图, 选用Bray-Curtis距离聚类, 采用Canoco for Windows 4.5软件对微生物群落和环境因子做典范对应分析(CCA).
2 结果与分析 2.1 物理化学参数样品物理化学参数见表 1.可以看出6个样品酸性均很强, 样品pH均在3.0以下, 其中新堆放样品的pH均在2.60以下, 5J最低仅为2.37. 1LL最高, 也仅为2.77. 5号和6号位样品的电导率高达2.25~7.08 mS·cm-1, 1LL样品电导率明显低于其他样品仅为0.32mS·cm-1.新堆放样品Fe2+含量明显高于1LL, 新堆放样品Fe2+含量达2.91~33.40 mg·kg-1 1LL中Fe2+含量仅为0.80mg·kg-1. TFe含量也呈同样规律, 新堆放样品高于1LL. 6个样品SO42-含量均很高, 5J样品最高为20.16 g·kg-1, 其中1LL样品最低也达到1.07 g·kg-1.所有样品有机碳含量明显低于我国平均水平的17.8 g·kg-1[10].
|
|
表 1 样品物理化学参数 Table 1 Physicochemical parameters of the samples |
2.2 微生物群落分析 2.2.1 嗜酸菌群落聚类分析
将6个样品统一以0.03差异分型后得到3 812个OTU.用R软件, 取丰度最高的50个OTU以Bray-Curtis距离做微生物群落聚类分析. 图 1为PCoA分析主坐标分析结果, 1LL与5、6号位样品完全分开, 证明其微生物组成较为特殊, 与5、6号位样品存在较大差异.

|
图 1 微生物组成主坐标分析 Fig. 1 Principal co-ordinate analysis of the samples based on the OTU abundance |
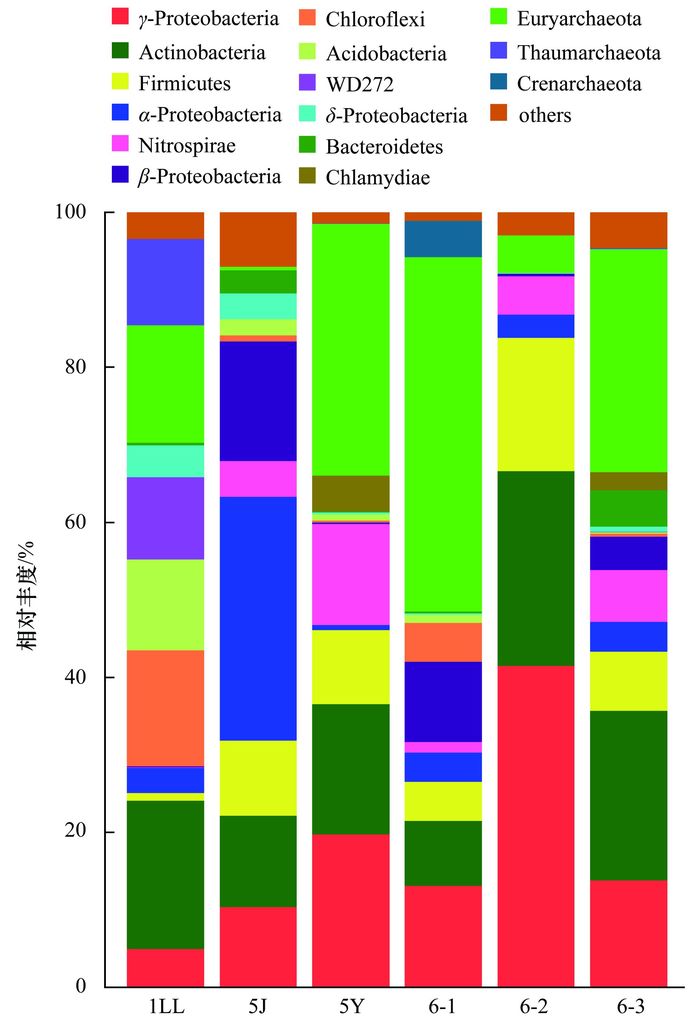
用Mothur软件将6个样品序列与Silva数据库中标准序列比对, 得到各分类单元的分类学信息.将在6个样品中所占比例之和低于4%的门类统一归为其他门, 得到门水平的微生物类群比例如图 2所示, γ变形菌门(γ-Proteobacteria)在6个样品中均有分布, 其中在5、6号位样品中均占10%以上, 在6-2中分布最多达41.48%.在1LL中分布最少仅占5%.放线菌门(Actinobacteria)在6个样品均有分布, 该类群在6-3中是第一大细菌类群占到21.90%, 在5Y占16.78%、6-2中占到25.11%, 是这两个样品中第二大细菌类群, 它在1LL占19.10%, 是该样品中的优势类群. 5Y、6-1和6-3中占主导地位的是广古菌门(Euryarchaeota)古菌, 分别占32.51 %、45.65%和28.78%, 同时它也是1LL样品中第二大类群.值得注意的是酸杆菌门(Acidobacteria), 该类群在5、6号位样品中的5J中分布最多, 也仅为2.1%, 然而它在1LL中占11.73%, 是该样品第三大细菌类群.奇古菌门(Thaumarchaeota)在5、6号位样品中分布极少, 在6-3中占0.1%, 5Y中仅占0.03%, 其余5、6号位样品中则没有检出, 但在1LL中有较多分布, 达到11.12%.可以看出5、6号位新废矿石样品与1号位裸露1LL微生物组成存在较大差异. 1LL样品没有明显占优势地位的类群, 其微生物类群组成相对复杂, 分布比较均匀.
|
图 2 样品中细菌和古菌在门水平所占比例 Fig. 2 Relative abundance of bacteria and archaea phyla in the samples |
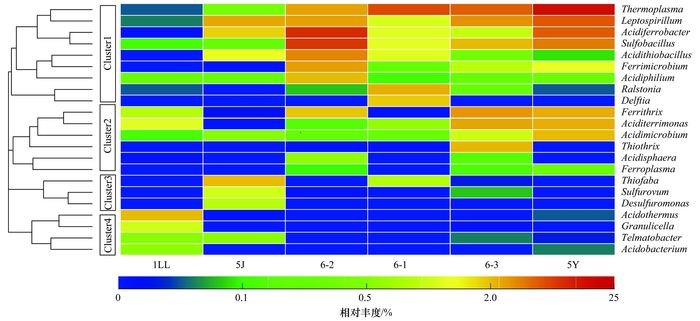
以属作为分类单元考察微生物群落的组成, 可以得到如图 3所示的结果.将6个样品序列与Silva.nr_v119.align数据库中标准序列比对, 选取丰度最高的前22个属来观察微生物类群分布.左侧聚类基于样品属水平的分布, 使用Bray-Curtis距离. 5、6号样品主要属包括Thermoplasma、钩端螺菌属(Leptospirillum)、Acidiferrobacter、硫化杆菌属(Sulfobacillus)、铁微菌属(Ferrimicrobium)、Ferrithrix、Aciditerrimonas、Acidimicrobium、Acidiphilium. 1LL主要的属有Telmatobacter、Acidobacterium、Granulicella和Acidothermus.从图 3中可以观察到大多数5、6号位样品与1LL微生物组成存在明显差异.在5、6号位丰度较高的属, 在1LL中分布较少, 而在1LL中分布较多的属, 在多数5、6号位样品中分布较少.上图左侧属水平的聚类也显示, 与氧化铁硫相关的属聚在一个分支上.长期堆放样品中占较高比例的属聚在一个分支上.下面分四类讨论样品属水平的微生物组成.
|
图 3 样品中细菌和古菌主要属相对丰度 Fig. 3 Relative abundance of bacteria and archaea genus in the samples |
(1) Cluster 1氧化铁硫产酸的嗜酸菌
氧化铁硫产酸的化能自养微生物归为Cluster1, 它们主要分布在5、6号位样品中, 主要是铁氧化化能自养菌.热原体属(Thermoplasma)在5Y和6-3中丰度较高, 在1LL中分布极少.热原体属(Thermoplasma)为广古菌门古菌, 专性嗜热嗜酸.生长pH范围为0.5~4.0, 最适pH=2.0.专性异养, 可以生长在酵母提取物中.兼性好氧.厌氧条件下可将单质硫还原为H2S. Thermoplasma的菌种分离自煤矸石堆和酸性硫质喷气孔.模式种是Thermoplasma acidophilum[11].
钩端螺菌属(Leptospirillum)可氧化亚铁自养生长, 在5、6号位样品中丰度较高(1.34%~12.99%), 在1LL中极少, 仅占0.06%. Leptospirillum嗜酸, 可在pH=1.3~4.0范围内氧化亚铁自养生长, 不能利用硫磺和硫代硫酸盐, 能利用黄铁矿和硫铁矿生长, 模式种是Leptospirillum ferrooxidans[12].
酸微菌属(Acidiferrobacter)在5、6号位样品中有较多分布, 均多于1%, 在5Y和6-2中占12.22%和18.57%.然而它在1LL中仅有0.01%.该属嗜酸最适pH值约为2, 氧化Fe2+自养生长.分离自酸性, 铁硫矿物或硫化物大量存在的环境[13].
硫化杆菌属(Sulfobacillus)除在5J中占0.27%外, 在大多数5、6号位样品中硫化杆菌属(Sulfobacillus)均有较高丰度(2.1%~16.97%), 在1LL中最低, 仅占0.13%.该属模式种Sulfobacillus thermotolerans sp.嗜酸, 混合营养型, 可以氧化单质硫、亚铁、硫化矿.生长pH范围为1.2~2.4, 最适pH=2.0[13].
嗜酸硫杆菌属(Acidithiobacillus)在其5、6号位样品中均有一定分布, 在6-2中占7.67%, 在1LL中未检出. Acidithiobacillus专性嗜酸, 最适pH小于4.可以利用还原态硫化物自养生长.某些种可氧化亚铁, 利用金属硫化物产生能量.模式种是Acidithiobacillus thiooxidans[14].
(2) Cluster 2可氧化铁的化能异养嗜酸菌
Cluster2中包括具有氧化铁性质的嗜酸菌, 也含有一些分离自极端酸性环境的嗜酸菌. Ferrithrix属在6个样品中均有分布, 在5Y中占3.59%、在6-3中占6.23%, 在1LL样品中占1.04%.该属细菌嗜酸专性异养, 能氧化和还原铁.模式种是Ferrithrix thermotolerans, 该菌株Y005T分离自温泉[15].
Aciditerrimonas属在5Y中占3.45%、6-3中占4.54%, 1LL样品中占1.41%.该属细菌嗜酸, 最适pH=3.0.自养兼性厌氧, 模式种是Aciditerrimonas ferrireducens, 可以在含有Fe3+的条件下厌氧生长.可以利用酵母提取物, 葡萄糖, 乳糖, 甘露糖和木糖作为碳源和能源异养生长, 也可以在厌氧存在条件下利用氢还原Fe3+生长.不能氧化Fe2+.该菌种IC-180T分离自日本箱根涌泉火山喷气孔土壤[16].
Thiothrix仅在6号位样品中有少量分布, 在6-3中占2.33%.该细菌是硫氧化菌, 通常存在于含硫的自然水体中, 生长在pH中性环境, 生长需要的硫化物浓度至少0.1 mg·kg-1[17].
(3) Cluster 3硫氧化还原嗜酸菌
Cluster 3中的嗜酸菌和硫的氧化还原有关. Thiofaba在5J、6-1中分布大于1%, 在1LL中没有分布.该属是需氧专性化能自养硫氧化细菌.通过固定CO2和氧化还原态硫化物生长.属于γ-Proteobacteria, 模式种是Thiofaba tepidiphila[18].
Sulfurovum同样仅在5、6号位样品5J和6-2、6-3中有一定分布, 在1LL中未检出.它属于ε-Proteobacteria, 具有氧化硫的能力.属于化能自养兼性厌氧菌, 生长需要元素硫或硫代硫酸盐作为电子供体, 氧和硝酸盐作为电子受体, 利用CO2作为碳源, 模式种Sulfurovum lithotrophicum[19].
Desulfuromonas仅在5J中有一定分布.该属的某些种具有还原铁硫的性质.如Desulfuromonas svalbardensis、Desulfuromusa ferrireducens. Desulfuromusa ferrireducens可以还原Fe3+为Fe2+, 严格厌氧, 化能异养, 氧化多种有机酸或氢来还原Fe3+, 单质硫、锰的氧化物作为电子受体.生长pH范围6.9~7.9, 最适pH值是7.0~7.3.分离自海湾沉积物[20].
(4) Cluster 4不能氧化铁的化能异养嗜酸菌
Cluster 4中嗜酸菌全部属于酸杆菌门(Acidobacteria)的GP1类, 主要分布在1LL中, 属于化能异养型微嗜酸菌, 分离自酸性湿地、泥炭沼泽等较温和的环境.
Acidothermus在1LL中占2.15%, 在5、6号位样品中分布极少或未检出.专性需氧菌, 原养型.嗜酸, 生长pH值范围3.5~7.0.分离自黄石国家公园的酸性温泉.模式种是A. cellulolyticus[21].
Granulicella属于酸杆菌门, 同样仅在1LL中有一定分布1.28%, 在5、6号样品中几乎没有分布.该属细菌严格好氧化能异养, 嗜酸.不能利用硫代硫酸盐产生硫化氢.模式种是Granulicella paludicola,其能利用多种碳源, 生长pH范围3.0~7.5, 最适pH=4.2.菌株分离自酸性湿地、泥炭藓、泥炭沼泽[22].
2.3 环境因子对微生物群落结构的影响根据表 1所示环境因子, 将其与微生物操作分类单元(OTU)做典范对应分析(CCA),
以求得所选环境因子对细菌类群变化的解释程度以及影响细菌群落结构的主要环境因子, 所得典范对应分析结果如图 4所示, CCA1轴和CCA2轴分别可以解释群落变化的31.6%和24.8%. pH与第一排序轴的相关系数最高为0.7851, 是影响群落结构最主要的因素.

|
图 4 样品物种和物化参数的CCA分析 Fig. 4 Canonical correspondence analysis between acidophiles and the environmental variables |
虽然本研究采集的6个样品都是酸性矿山废水旁的裸露废矿石样品, 但因为堆放时间不同, 氧化程度各异, 所以物理化学参数有着明显的区别. 5、6号位样品堆放时间较短, 还在进行着旺盛的产酸作用, 所以pH较低、Fe2+含量较高、电导率较高; 而排土场中央的酸水库因为形成于20世纪70年代, 所以采集于其旁边的1号位样品1LL氧化也较为彻底, pH比其它样品要高, Fe2+含量和电导率则较低.
相应地, 两类样品的微生物群落组成也有着明显的差异.在5号位和6号位样品中, 存在着大量氧化铁硫的嗜酸菌, 如硫化杆菌属(Sulfobacillus)、钩端螺菌属(Leptospirillum)、Ferroplasma、Sulfurovum、Desulfuromonas 、Thiofaba、Thiothrix、罗尔斯通菌属(Ralstonia)、Delftia、Ferrithrix、Aciditerrimonas、嗜酸硫杆菌属(Acidithiobacillus)、铁微菌属(Ferrimicrobium)、热原体属(Thermoplasma)、Ferroplasma, 它们主要属于γ变形菌门(γ-Proteobacteria)、厚壁菌门(Firmicutes)、硝化螺旋菌门(Nitrospirae)、广古菌门(Euryarchaeota).这些微生物在硫化矿物的氧化过程中发挥着至关重要的作用[23].这些属都在1LL样品中占很低比例或未检出.这些菌属多为化能自养菌, 生活在寡营养环境, 分离自与本研究相似的重金属浓度较高的极端酸性环境.这证明5号位和6号位样品处于旺盛产酸阶段.
1LL中主要有Telmatobacter、Acidobacterium、Granulicella、Acidothermus, 其中前三者均属于酸杆菌门(Acidobacteria)的GP1类, 他们在5、6号位样品中分布极少或者未检出.这些菌属多为化能异养菌, 并且多数不能氧化铁硫, 能利用多种有机物, 生长在微酸性环境, 分离自泥炭沼泽等环境.该样品中化能异养菌占较高比例也可以证明样品中还原态铁硫不足以维持化能自养菌大量生长.可以推断1LL样品中的还原态铁硫大部分已经氧化完全.值得注意的是, 奇古菌门(Thaumarchaeota)在1号位样品中占相当高比例.奇古菌门是2008年从温泉古菌划分出来的一个新类群[24].本课题组前期研究发现, 该矿区有植被覆盖的废矿石古菌文库中归类于奇古菌门的古细菌均与氨氧化作用相关[25].本研究在长期堆放的裸露废矿石样品中检出大量奇古菌门(Thaumarchaeota)微生物, 表明裸露的废矿石样品中可能同样存在氨氧化古菌驱动的氨氧化作用.
根据微生物的群落组成可以推断1号位裸露样品已经处于产酸末期, 经过长期的堆放, 几乎已经不再产酸.本课题组前期研究结果也证明了这一点, 废水库已形成多年, 废水库和周边废矿石、土壤样品中并未大量检测到铁硫氧化菌的存在[26], 而5号位和6号位样品是新形成的AMD周边的废矿石, 其中含有大量的铁硫氧化菌, 说明样品正处于旺盛产酸阶段.聚类分析结果也证明了1号位裸露样品微生物组成不同于其他5个样品. 1号位样品和5、6号位样品虽然都是极端酸性环境, 但是其微生物群落结构不同.造成这一差别的原因是样品处于不同的产酸阶段, 物理化学性质存在一定差异.嗜酸微生物不仅在适应着环境, 同时它们也在改变着环境.
4 结论(1) 新堆放废矿石和长期堆放的废矿石物理化学条件有较大差异, 新堆放的废矿石更为极端.
(2) 新堆放的5、6号位废矿石样品处于旺盛产酸阶段, 其中含有大量的氧化铁硫相关的微生物.长期堆放的1号位废矿石样品环境条件比新鲜废矿石相对温和, 几乎不存在氧化铁硫产酸的微生物, 其微生物群落结构也相对复杂, 主要的嗜酸菌为化能异养菌.
(3) 处于旺盛产酸阶段5、6号位样品与处于产酸末期的1号位裸露1LL微生物组成存在明显差异, 表明不同的物化条件对微生物群落结构有决定性影响.
| [1] | Johnson D B, Hallberg K B. Acid mine drainage remediation options:a review[J]. Science of the Total Environment, 2005, 338(1-2): 3-14. DOI:10.1016/j.scitotenv.2004.09.002 |
| [2] | Baker B J, Banfield J F. Microbial communities in acid mine drainage[J]. FEMS Microbiology Ecology, 2003, 44(2): 139-152. DOI:10.1016/S0168-6496(03)00028-X |
| [3] | Edwards K J, Gihring T M, Banfield J F. Seasonal variations in microbial populations and environmental conditions in an extreme acid mine drainage environment[J]. Applied and Environmental Microbiology, 1999, 65(8): 3627-3632. |
| [4] |
丛志远, 赵峰华. 酸性矿山废水研究的现状及展望[J]. 中国矿业, 2003, 12(3): 15-18. Cong Z Y, Zhao F H. Current situation and prospect of the research on acid mine drainage[J]. China Mining Magazine, 2003, 12(3): 15-18. |
| [5] |
HJ 613-2011, 土壤干物质和水分的测定重量法[S]. HJ 613-2011, Soil-determination of dry matter and water content-gravimetric method[S]. |
| [6] |
刘广明, 杨劲松, 姚荣江. 影响土壤浸提液电导率的盐分化学性质要素及其强度研究[J]. 土壤学报, 2005, 42(2): 247-252. Liu G M, Yang J S, Yao R J. Chemical factors to electrical conductivity of soil extract and their intensity[J]. Acta Pedologica Sinica, 2005, 42(2): 247-252. |
| [7] | Mehlich A. Mehlich 3 soil test extractant:a modification of mehlich 2 extractant[J]. Communications in Soil Science and Plant Analysis, 1984, 15(12): 1409-1416. DOI:10.1080/00103628409367568 |
| [8] |
鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000: 82. Lu R K. Soil argrochemistry analysis protocoes[M]. Beijing: China Agriculture Science Press, 2000: 82. |
| [9] | Caporaso J G, Lauber C L, Walters W A, et al. Ultra-high-throughput microbial community analysis on the Illumina HiSeq and MiSeq platforms[J]. The ISME Journal, 2012, 6(8): 1621-1624. DOI:10.1038/ismej.2012.8 |
| [10] |
王绍强, 周成虎, 李克让, 等. 中国土壤有机碳库及空间分布特征分析[J]. 地理学报, 2000, 55(5): 533-544. Wang S Q, Zhou C H, Li K R, et al. Analysis on spatial distribution character istics of soil organic carbon reservoir in China[J]. Acta Geographica Sinica, 2000, 55(5): 533-544. DOI:10.11821/xb200005003 |
| [11] | Segerer A, Langworthy T A, Stetter K O. Thermoplasma acidophilum and Thermoplasma volcanium sp. nov. from Solfatara fields[J]. Systematic and Applied Microbiology, 1988, 10(2): 161-171. DOI:10.1016/S0723-2020(88)80031-6 |
| [12] | Hippe H. Leptospirillum gen. nov. (ex Markosyan 1972), nom. rev., including Leptospirillum ferrooxidans sp. nov. (ex Markosyan 1972), nom. rev. and Leptospirillum thermoferrooxidans sp. nov. (Golovacheva et al. 1992)[J]. International Journal of Systematic and Evolutionary Microbiology, 2000, 50: 501-503. DOI:10.1099/00207713-50-2-501 |
| [13] | Bogdanova T L, Tsaplina I A, Kondrat'eva T F, et al. Sulfobacillus thermotolerans sp. nov., a thermotolerant, chemolithotrophic bacterium[J]. International Journal of Systematic and Evolutionary Microbiology, 2006, 56(5): 1039-1042. DOI:10.1099/ijs.0.64106-0 |
| [14] | Kelly D P, Wood A P. Reclassification of some species of Thiobacillus to the newly designated genera Acidithiobacillus gen. nov., Halothiobacillus gen. nov. and Thermithiobacillus gen. nov[J]. International Journal of Systematic and Evolutionary Microbiology, 2000, 50(2): 511-516. DOI:10.1099/00207713-50-2-511 |
| [15] | Johnson D B, Bacelar-Nicolau P, Okibe N, et al. Ferrimicrobium acidiphilum gen. nov., sp. nov. and Ferrithrix thermotolerans gen. nov., sp. nov.:heterotrophic, iron-oxidizing, extremely acidophilic actinobacteria[J]. International Journal of Systematic and Evolutionary Microbiology, 2009, 59(5): 1082-1089. DOI:10.1099/ijs.0.65409-0 |
| [16] | Itoh T, Yamanoi K, Kudo T, et al. Aciditerrimonas ferrireducens gen. nov., sp. nov., an iron-reducing thermoacidophilic actinobacterium isolated from a solfataric field[J]. International Journal of Systematic and Evolutionary Microbiology, 2011, 61(6): 1281-1285. DOI:10.1099/ijs.0.023044-0 |
| [17] | Brigmon R L, Furlong M, Whitman W B. Identification of Thiothrix unzii in two distinct ecosystems[J]. Letters in Applied Microbiology, 2003, 36(2): 88-91. DOI:10.1046/j.1472-765X.2003.01256.x |
| [18] | Mori K, Suzuki K I. Thiofaba tepidiphila gen. nov., sp. nov., a novel obligately chemolithoautotrophic, sulfur-oxidizing bacterium of the Gammaproteobacteria isolated from a hot spring[J]. International Journal of Systematic and Evolutionary Microbiology, 2008, 58(8): 1885-1891. DOI:10.1099/ijs.0.65754-0 |
| [19] | Inagaki F, Takai K, Nealson K H, et al. Sulfurovum lithotrophicum gen. nov., sp. nov., a novel sulfur-oxidizing chemolithoautotroph within the ε-Proteobacteria isolated from Okinawa Trough hydrothermal sediments[J]. International Journal of Systematic and Evolutionary Microbiology, 2004, 54(5): 1477-1482. DOI:10.1099/ijs.0.03042-0 |
| [20] | Vandieken V, Muẞmann M, Niemann H, et al. Desulfuromonas svalbardensis sp. nov. and Desulfuromusa ferrireducens sp. nov., psychrophilic, Fe(Ⅲ) -reducing bacteria isolated from Arctic sediments, Svalbard[J]. International Journal of Systematic and Evolutionary Microbiology, 2006, 56(5): 1133-1139. DOI:10.1099/ijs.0.63639-0 |
| [21] | Mohagheghi A, Grohmann K, Himmel M, et al. Isolation and characterization of Acidothermus cellulolyticus gen. nov., sp. nov., a new genus of thermophilic, acidophilic, cellulolytic bacteria[J]. International Journal of Systematic and Evolutionary Microbiology, 1986, 36(3): 435-443. |
| [22] | Pankratov T A, Dedysh S N. Granulicella paludicola gen. nov., sp. nov., Granulicella pectinivorans sp. nov., Granulicella aggregans sp. nov. and Granulicella rosea sp. nov., acidophilic, polymer-degrading acidobacteria from Sphagnum peat bogs[J]. International Journal of Systematic and Evolutionary Microbiology, 2010, 60(12): 2951-2959. DOI:10.1099/ijs.0.021824-0 |
| [23] | Johnson D B, Hallberg K B. The microbiology of acidic mine waters[J]. Research in Microbiology, 2003, 154(7): 466-473. DOI:10.1016/S0923-2508(03)00114-1 |
| [24] | Brochier-Armanet C, Boussau B, Gribaldo S, et al. Mesophilic crenarchaeota:proposal for a third archaeal phylum, the thaumarchaeota[J]. Nature Reviews Microbiology, 2008, 6(3): 245-252. DOI:10.1038/nrmicro1852 |
| [25] |
刘莹, 王丽华, 郝春博, 等. 酸性矿山废水库周边土壤微生物多样性及氨氧化菌群落研究[J]. 环境科学, 2014, 35(6): 2305-2313. Liu Y, Wang L H, Hao C B, et al. Microbial diversity and ammonia-oxidizing microorganism of a soil sample near an acid mine drainage lake[J]. Environmental Science, 2014, 35(6): 2305-2313. |
| [26] |
王丽华, 郝春博, 李思远, 等. 安徽某铁矿排土场废矿石中细菌群落分子生态学研究[J]. 地学前缘, 2014, 21(4): 199-209. Wang L H, Hao C B, Li S Y, et al. Molecular research of acidophilic bacteria in abandoned ores in waste dump of an iron mine in Anhui Province[J]. Earth Science Frontiers, 2014, 21(4): 199-209. |
 2017, Vol. 38
2017, Vol. 38


