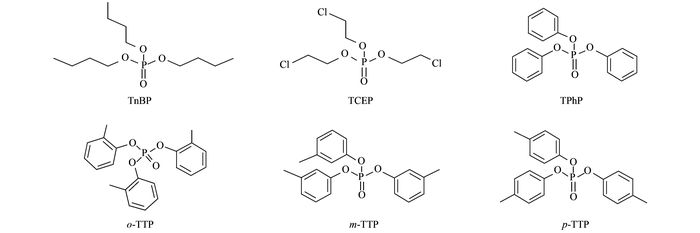
有机磷酸酯(organophosphate esters, OPEs)是由烷烃、芳香烃、卤代烷烃等烃类取代基取代磷酸分子上的氢所形成的一类磷酸酯类化合物, 一般烷烃和芳香烃取代的OPEs常被用作增塑剂, 而含卤OPEs则被广泛用作阻燃剂[1].随着多溴二苯醚(polybrominated diphenyl ethers, PBDEs)等溴代阻燃剂的逐步禁用, OPEs由于具有阻燃效果好、生产成本低以及生产工艺简单等优点, 其用量逐年上升. 2011年全球OPEs的消费量达到约500 000 t[2], 2006年欧洲OPEs的消费量达93 000 t, 约占阻燃剂市场的20%[3].我国已成为OPEs生产、使用、出口大国, 2011年我国OPEs产量达到约10万t, 年产量增长率达15%以上[4].
有研究表明, 多种OPEs具有神经毒性、生殖毒性、基因毒性和致癌性, 其环境危害逐渐被发现.毒理学实验发现, 长期暴露TCEP和磷酸三(1, 3-二氯异丙基)酯[tris(2-chloro-1-(chloromethyl)ethyl)phosphate, TDCPP]可以引起啮齿类动物的不同器官发生癌变[5], 而磷酸三苯酯(triphenyl phosphate, TPhP)则被发现具有神经毒性和生殖毒性[6].欧盟在2008年将TCEP列为“潜在人类致癌物”(第三类致癌物)[7].美国加州致癌定义委员会在2011年决定将TDCPP加入到《加州65提案》中, 该列表中的化学物质被归类为会引发癌症、生殖缺陷或其他生殖危害[8].最新的研究已经开始关注环境中OPEs对人体的影响, 已有报道表明TDCPP和TPhP可抑制人体荷尔蒙水平, 并严重降低男性精液质量[9].作为新型有害污染物, OPEs对环境和人体产生的风险仍需进一步研究.
OPEs多以物理方式添加到材料中, 因此在材料的生产、使用和废弃处理过程中很容易释放到周围环境中, 而大多数OPEs的水溶性较高, 其在各种水体, 特别是饮用水中的污染状况正逐渐引起环境学者的广泛关注.目前, 美国[10]、德国[11]、韩国[12]和西班牙[13]等多个国家的饮用水中均检测出了OPEs.另外其它研究[10, 14]也显示, 现有的饮用水处理工艺(包括煮沸)对OPEs的去除效果并不明显.因此, 摄取饮用水可能是人类暴露于OPEs的重要途径之一.
目前, 国内关于饮用水中OPEs的污染水平及健康风险评估还鲜见报道, 但我国饮用水净化工艺比较落后, 而且水源污染较为严重, 因此我国饮用水中OPEs污染可能更为严重[15].考虑到自来水、地下水是居民主要的饮用水类型, 本研究采集了山东省潍坊滨海经济技术开发区的自来水和地下水, 使用固相萃取-气相色谱-三重四极杆质谱联用法(SPE-GC-MS/MS)分析了已有报道较为集中的6种OPEs的水平与分布(理化性质和分子结构见表 1和图 1)[10~15], 并研究了潍坊滨海经济技术开发区饮用水与居民血清中OPEs的相关性, 初步评估了当地居民的暴露风险.
1 材料与方法 1.1 样品的采集
2016年5月, 在山东省潍坊滨海经济技术开发区滨海人民医院周边的村庄, 随机选取不同的住户, 入户采集自来水样品(n=8).采样前, 用自来水润洗玻璃样品瓶, 然后采集约500 mL水样.地下水(n=4) 采自潍坊滨海经济技术开发区农村的浅水井.采样前, 用地下水润洗玻璃样品瓶, 然后采集约500 mL水样.样品采集后置于-18℃冰箱冷冻保存.
1.2 实验仪器与试剂主要仪器:TSQ 8000 Evo三重四极杆气相色谱-质谱联用仪(Thermo Fisher Scientific), BF2000氮气吹干仪(北京八方世纪科技有限公司), SPE小柱处理系统(美国ALLTECH公司), Sep-pak Vac 6cc C18固相萃取柱(500 mg·3 mL-1, 美国Waters公司).
主要试剂:乙酸乙酯(农残级, 美国J.T.Baker公司), 甲醇(农残级, 美国J.T.Baker公司), 甲苯(农残级, 美国J.T.Baker公司), 超纯水(自制, 美国Millipore公司超纯水处理系统).
标准样品:2H1-labeled TCEP、2H1-labeled TPhP均购自美国AccuStandard公司.
1.3 实验方法 1.3.1 样品前处理取200 mL水样, 加入100 ng 2H1-labeled TCEP、2H1-labeled TPhP作为同位素内标, 充分混匀. SPE小柱使用前依次用5 mL乙酸乙酯、5 mL甲醇和5 mL超纯水活化.然后通过SPE小柱处理系统将水样加载到SPE小柱上, 控制水样过柱流速为10 mL·min-1.上样结束后, 用10 mL乙酸乙酯分2次洗脱目标物.将洗脱液氮吹浓缩, 并用甲苯定容至100 μL, 待仪器分析测定.
1.3.2 色谱-质谱条件色谱条件:TG-5HT色谱柱(15 m×0.25 mm i.d., 膜厚0.10 μm, Thermo Fisher Scientific), 进样口温度为280℃.升温程序:初始温度100℃保持2 min, 以20℃·min-1升至300℃保持5 min.载气为高纯氦气, 柱流速为1.0 mL·min-1, 采用不分流进样, 进样量为1 μL.
质谱条件:电子轰击离子源(EI), 选择离子监测模式(SRM), 离子源温度为280℃, 四极杆温度为280℃. SRM监测离子对(母离子-子离子, m/z)分别为:TnBP 211-99; TCEP 249-63; TPhP 326-170; TTP 368-165; 2H1-labeled TCEP 261-67; 2H1-labeled TPhP 341-180. TCEP、TnBP、TPhP、2H1-labeled TCEP、2H1-labeled TPhP二级碰撞电压为20 eV, o-TPP、m-TPP、p-TPP二级碰撞电压为38 eV.
1.3.3 质量保证和质量控制(QA/QC)为保证样品分析流程的可靠性, 尽量避免样品分析过程中可能造成的污染和损失, 本研究设置过程空白实验, 并加入2H1-labeled TCEP、2H1-labeled TPhP作为内标来检测回收率.两种内标回收率为2H1-labeled TCEP:105%±19%、2H1-labeled TPhP:69%±12%, 过程空白实验中均未发现目标化合物.仪器检出限(S/N=3) 为:0.12~4.11 pg, 仪器定量限(S/N=10) 为:0.39~13.7 pg.
1.4 健康风险评价方法采用美国环保署(US EPA)推荐的健康风险评价模型, 评价潍坊滨海经济技术开发区饮用水中OPEs的健康风险.根据OPEs有无致癌性将健康风险分为致癌(TCEP)和非致癌(TnBP、TPhP、o-TTP、m-TTP、p-TTP)两类.
1.4.1 暴露量人群通过饮用水摄入OPEs的日均暴露剂量(DI)按下式计算:
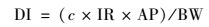
|
(1) |
式中, c为饮用水中OPEs的浓度(ng·L-1), IR为日饮水量(L·d-1), AP为饮水的吸收率, 本研究取AP为100%[14], BW为平均体重(kg).饮用水中OPEs的成人暴露风险计算参数引自中国人群暴露参数手册(成人卷)[16], 儿童暴露风险计算参数(表 2)引自文献[17]. OPEs的中值浓度和95%分值浓度分别作为平均暴露水平和高暴露水平计算暴露量.
|
|
表 2 饮用水中OPEs暴露风险计算参数[16, 17] Table 2 Parameters for the calculation of the risk of exposure to OPEs in drinking water |
1.4.2 健康风险表征
(1) 非致癌性风险表征
RfD为美国环保署(US EPA)等权威机构对OPEs建议的参考剂量[ng·(kg·d)-1][15, 18], 表示在单位时间、单位体重摄取的不会引起人体不良反应的污染物最大量, 用无明显损害作用水平(NOVEL)除以安全因子(10 000) 得到, 计算公式如下:
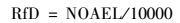
|
(2) |
人群通过饮用水摄入OPEs的非致癌性风险用危害商(HQ)表征, 计算公式如下:
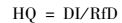
|
(3) |
一般认为, 当HQ>1时人群暴露OPEs存在非致癌性风险.
(2) 致癌性风险表征
TCEP的致癌性风险用Risk表征, 计算公式如下:
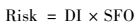
|
(4) |
式中, SFO为斜率系数, 表示人体暴露于一定剂量某种污染物下产生致癌效应的最大概率[(ng·(kg·d)-1)-1], TCEP的SFO值为2×10-8 (ng·(kg·d)-1)-1[15]. Risk为致癌性风险, 表示癌症发生的概率, 通常以单位数量人口出现癌症患者的比例表示, 当Risk>10-6.00时, (即每100万人增加1个癌症患者), 认为人群暴露TCEP具有潜在致癌风险.
2 结果与讨论 2.1 饮用水中OPEs的水平潍坊滨海经济技术开发区所采集的饮用水样品中均检测出了OPEs, 但自来水和地下水中各种OPEs的浓度水平差异较大(表 3). TnBP、TCEP和TPhP在两种类型的饮用水中的检出率均为100%. o-TTP, m-TTP, p-TTP这3种同分异构体在饮用水中的浓度相差不大, 且污染水平很低.
|
|
表 3 饮用水中OPEs的含量及检出率1) Table 3 Concentrations and detection rates of OPEs in drinking water |
2.1.1 自来水中OPEs的水平
表 3是潍坊滨海经济技术开发区自来水中6种OPEs的含量及检出率.自来水中OPEs的总浓度在162~253 ng·L-1范围内, 中值浓度为218 ng·L-1.已有研究报道的国内外饮用水中OPEs的浓度在0.30~510 ng·L-1的水平[11, 13, 14, 19, 20, 21].与国外研究相比, 本研究所检测自来水中OPEs的水平较高, 远远高于德国(0.3~3 ng·L-1)[11]和意大利(4~15 ng·L-1)[19]自来水中的浓度, 是西班牙(11~148 ng·L-1)[13]浓度的2倍左右, 但低于美国(210~510 ng·L-1)[20].而对比于国内的其他研究, 如杭州、衢州(123~338 ng·L-1)[21], 南京、哈尔滨(85.1~325 ng·L-1)[14]等地区, 其自来水中OPEs的浓度与本研究相接近.
相较于国内外的报道, 本研究所检测的自来水中TCEP水平最高, 是美国[20]报道浓度的2倍左右, 是杭州、衢州[21]报道浓度的4倍左右, 超过贵阳[14]报道浓度的3倍, 且远远高于西班牙[13]所报道的浓度.
2.1.2 地下水中OPEs的水平潍坊滨海经济技术开发区地下水中6种OPEs的含量及检出率如表 3所示.地下水中OPEs的总浓度在3.52~13.9 ng·L-1范围内, 中值浓度为8.97 ng·L-1, 比自来水低约两个数量级.相较于已有报道, 本研究所检测地下水中OPEs的水平与杭州、衢州(2.5~8.4 ng·L-1)[21]、德国深层地下水监测井(3~9 ng·L-1)[22]浓度相近.有研究表明, 地下水更新过程中土壤等介质对地下水中的OPEs具有天然的过滤和净化作用[23], 土壤优越的吸附作用以及土壤微生物的吸附、转化作用可能是地下水中OPEs浓度水平低的原因.
与已有研究相比较, 潍坊滨海经济技术开发区地下水中TPhP的浓度水平较高, 比自来水中的浓度高出一个数量级, 是杭州、衢州[21]报道浓度的25倍左右, 这说明当地地下水可能有TPhP的输入.
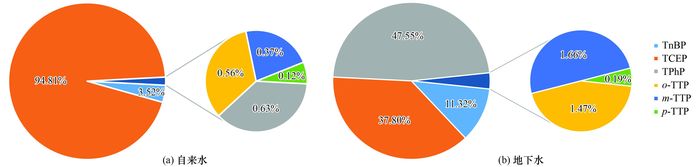
2.2 饮用水中OPEs的组成潍坊滨海经济技术开发区采集的所有饮用水样品中均检测出了TCEP、TnBP和TPhP, 而TTP的3种同分异构体的检出率则较低.根据图 2可以看出自来水与地下水中OPEs的组成相差较大. TCEP是自来水中浓度水平最高的OPEs, 占Σ6OPEs总浓度的94.81%, 其次为TnBP和TPhP.而地下水中TPhP为主要的OPEs, 占Σ6OPEs总浓度的47.55%, 其次为TCEP和TnBP.
|
图 2 饮用水中OPEs的组成 Fig. 2 Composition of OPEs in drinking water |
作为自来水中主要的OPEs污染物, TCEP是优良的阻燃剂和增塑剂, 广泛应用于聚氯乙烯、聚乙烯的阻燃处理, 建筑夹层板的难燃处理以及聚醋酸乙烯、醋酸纤维素的增塑剂[24, 25, 26].潍坊滨海经济技术开发区工厂对TCEP的大量生产、使用会造成地表水等环境介质中污染水平的升高, 因此水源污染可能是自来水中TCEP水平高的重要原因, 且当地自来水厂的絮凝、沉淀、过滤、消毒等处理工艺也较难去除水体中的TCEP[27].另外, 供水管网系统广泛使用了PVC塑料管、UPVC塑料管等, 其中都大量添加了以TCEP为代表的阻燃剂[22, 23], 望秀丽等检测出PVC塑料中TCEP的含量为11.3 mg·kg-1[26], 超过了欧盟限定的5 mg·kg-1, 因此由PVC和其它塑料制成的供水管系统也可能是自来水中TCEP的污染源.
TPhP是地下水中占比最高的OPEs, 而作为芳香基取代的OPEs, TPhP主要作为增塑剂应用于PVC材料、热塑性塑料以及合成橡胶中[28].而研究区的农田普遍使用塑料薄膜[29], 由于塑料薄膜的稳定性相对较差, TPhP易从塑料膜中渗出, 另外老化、腐烂的塑料膜残留在土壤中, 也易使得TPhP以淋滤的方式进入地下水中. TPhP的辛醇水分配系数为104.59, 易被可溶的有机碳或腐殖质胶体吸附, 从而随可溶性有机物一起发生迁移, 大大提高了TPhP向地下水中迁移的能力.因此, 地下水中TPhP的含量较高.
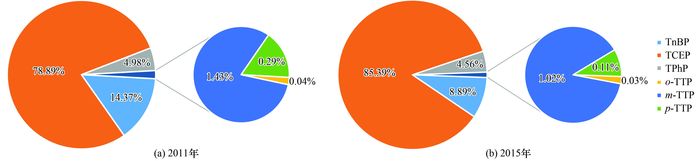
2.3 饮用水中OPEs的健康风险评价结合本研究组2011年、2015年对潍坊滨海经济技术开发区居民血清中6种OPEs的研究[30], 用SPSS 16.0分析了当地自来水和居民混合血清中OPEs的分布间的相关性.居民混合血清中OPEs的组成见图 3. SPSS分析结果显示, 2011年采集的居民混合血清中OPEs的分布与自来水中OPEs的分布间显著正相关(r=0.990, P<0.01), 2015年采集的居民混合血清中OPEs的分布与自来水中OPEs的分布间也显著正相关(r=0.997, P<0.01), 表明饮用水中的OPEs可能对人体血清中OPEs的污染水平有重要的贡献.
|
图 3 居民混合血清中OPEs的组成 Fig. 3 Composition of OPEs in human mixed serum |
潍坊滨海经济技术开发区不同人群通过饮用水摄入OPEs的日均暴露剂量(DI)如表 4所示.其中, 以自来水为主要饮用水类型的人群的OPEs日均暴露剂量为6.42~7.48 ng·(kg·d)-1.以地下水为主要饮用水类型的人群的OPEs日均暴露剂量为0.26~0.31 ng·(kg·d)-1, 比自来水低一个数量级.考虑到饮用水中的OPEs可能对人体血清中OPEs的污染水平有重要的贡献, 以自来水为主要饮用水类型的人群相对处于较高的暴露水平.
|
|
表 4 不同人群通过饮用水摄入OPEs的日均暴露剂量/ng·(kg·d)-1 Table 4 Human daily intake of OPEs through drinking water/ng·(kg·d)-1 |
对于不同年龄、性别的人群通过自来水摄入OPEs的日均暴露剂量, 成人男性略高于女性, 女性儿童略高于成人, 这可能是单位体重饮水量的不同所引起的.
2.3.2 饮用水中OPEs的健康风险表征鉴于OPEs在潍坊滨海经济技术开发区饮用水中的浓度较高, 且饮用水中的OPEs可能对人体血清中OPEs的污染水平有重要的贡献, 评价饮用水中OPEs的健康风险至关重要.
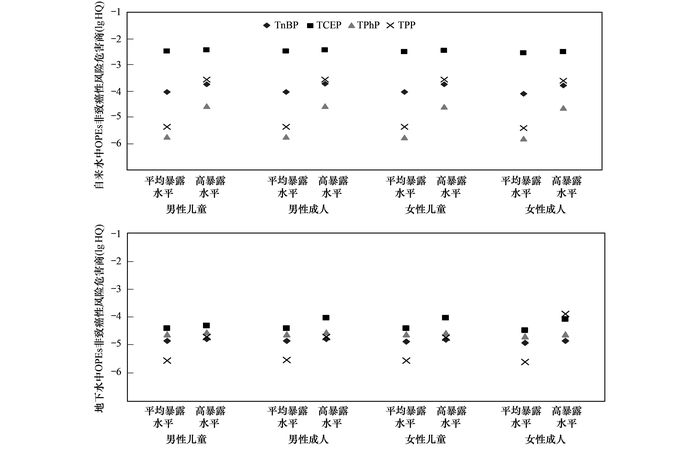
饮用水中OPEs非致癌性风险危害商(HQ)如图 4所示.其中, 自来水中各OPEs的HQ在10-5.76~10-2.43之间, 地下水中各OPEs的HQ在10-5.81~10-3.88之间.不论是平均暴露还是高暴露水平, 各OPEs的非致癌性风险较理论风险阈值都低2~6个数量级, 即人们通过饮用水摄入的OPEs非致癌性风险处于较低的水平.但考虑到人体可以通过呼吸、皮肤接触等其他方式摄入OPEs, 同时考虑到人体对于其他OPEs的暴露以及各污染物之间可能存在的毒性加和效应[31], 仍需持续关注人体对OPEs的暴露情况.
|
图 4 饮用水中OPEs非致癌性风险危害商 Fig. 4 Non-cancer risks of OPEs in drinking water |
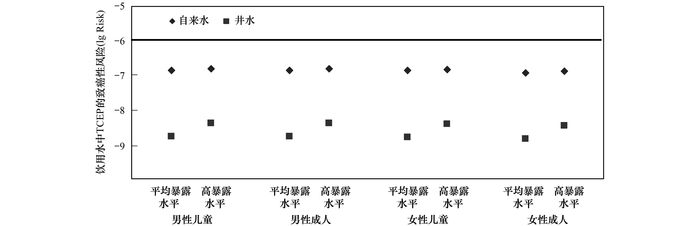
饮用水中TCEP的致癌性风险如图 5所示.其中, 自来水中TCEP的致癌性风险在10-6.90~10-6.79之间, 地下水中TCEP的致癌性风险在10-8.82~10-8.37之间.两种饮用水中TCEP的致癌性风险均低于理论风险阈值(Risk=10-6.00, 图 5中实线), 但自来水中TCEP的致癌性风险相对高于地下水, 接近理论风险阈值, 因此TCEP在自来水中的污染应当引起足够关注, 建议当地自来水厂改进净水工艺与供水管系统, 以避免TCEP浓度进一步升高所带来的致癌性风险.
|
图 5 饮用水中TCEP的致癌性风险 Fig. 5 Carcinogenic risks posed by TCEP in drinking water |
不确定性分析:完整的健康风险评价应包括对大气、土壤、水和食物链这4种介质携带的污染物通过食入、吸入和皮肤接触3种暴露途径进入人体对人体健康产生危害的评价.本研究只评价了居民通过饮用水摄入OPEs对健康产生危害的风险, 实际则可能低估了OPEs的暴露风险.另外, 风险评价本身涉及到很多参数, 有些参数因难以确切测定而需要估算, 且本研究的样本量有限, 增加了评价结果的不确定性.由于客观原因, 本研究的暴露风险评估具有一定的不确定性, 但基本上能反映研究区的实际情况.
3 结论(1) 相较于国内外报道的水平, 潍坊滨海经济技术开发区自来水中OPEs的浓度水平较高, 而地下水中的污染水平则很低, 且自来水与地下水中OPEs的组成差异较大.自来水中TCEP的水平高于国内外已有的报道, 供水系统所使用的塑料管可能是TCEP浓度水平高的重要来源.地下水中TPhP的浓度水平较高, 其污染源可能是农田普遍使用的塑料薄膜.
(2)2011年采集的潍坊滨海经济技术开发区居民混合血清中OPEs的分布与自来水中OPEs的分布间显著正相关(r=0.990, P<0.01), 2015年采集的居民混合血清中OPEs的分布与自来水中OPEs的分布间也显著正相关(r=0.997, P<0.01), 表明饮用水中的OPEs可能对人体血清中OPEs的污染水平有重要的贡献.
(3) 潍坊滨海经济技术开发区不同人群通过饮用水摄入OPEs的日均暴露剂量为0.26~7.48 ng·(kg·d)-1, 通过饮用水摄入OPEs的非致癌性风险和致癌性风险均低于理论风险阈值, 但是自来水中TCEP的致癌性风险相对高于地下水, 应当引起足够重视.
| [1] |
鹿建霞, 季雯, 马盛韬, 等. 气相色谱/质谱法检测灰尘、土壤和沉积物中有机磷酸酯[J]. 分析化学, 2014(6): 859-865. Lu J X, Ji W, Ma S T, et al. Analysis of organophosphate esters in dust, soil and sediment samples using gas chromatography coupled with mass spectrometry[J]. Chinese Journal of Analytical Chemistry, 2014(6): 859-865. |
| [2] | 王润梅. 环渤海主要入海河流有机磷酸酯阻燃剂的初步研究[D]. 烟台: 中国科学院烟台海岸带研究所, 2015. 2-6. http://cdmd.cnki.com.cn/Article/CDMD-80180-1015957043.htm |
| [3] | van der Veen I, de Boer J. Phosphorus flame retardants: properties, production, environmental occurrence, toxicity and analysis[J]. Chemosphere, 2012, 88(10): 1119-1153. DOI:10.1016/j.chemosphere.2012.03.067 |
| [4] | Wang R M, Tang J H, Xie Z Y, et al. Occurrence and spatial distribution of organophosphate ester flame retardants and plasticizers in 40 rivers draining into the Bohai Sea, north China[J]. Environmental Pollution, 2015, 198: 172-178. DOI:10.1016/j.envpol.2014.12.037 |
| [5] | WHO. Environmental Health Criteria 209. Flame retardants: Tris(chloropropyl) phosphate and Tris (2-chloroethyl) phosphate[Z]. Geneva, Switzerland: World Health Organization, 1998. |
| [6] | 谭晓欣. 珠江三角洲沉积物和水生生物中有机磷系阻燃剂的分布特征[D]. 北京: 中国科学院大学, 2016. 4-5. http://cdmd.cnki.com.cn/Article/CDMD-80165-1016188275.htm |
| [7] | EU. (European Union). Risk assessment report of Tri(2-chloroethyl) phosphate, 2008. CAS No: 115-96-8 EINECS No: 204-118-5[Z]. Luxembourg: Office for Official Publications of the European Communities, 2008. |
| [8] | Stapleton H M, Sharma S, Getzinger G, et al. Novel and high volume use flame retardants in US couches reflective of the 2005 PentaBDE phase out[J]. Environmental Science & Technology, 2016, 46(24): 13432-13439. |
| [9] | Meeker J D, Stapleton H M. House dust concentrations of organophosphate flame retardants in relation to hormone levels and semen quality parameters[J]. Environmental Health Perspectives, 2010, 118(3): 318-323. |
| [10] | Stackelberg P E, Furlong E T, Meyer M T, et al. Persistence of pharmaceutical compounds and other organic wastewater contaminants in a conventional drinking-water-treatment plant[J]. Science of the Total Environment, 2004, 329(1-3): 99-113. DOI:10.1016/j.scitotenv.2004.03.015 |
| [11] | Andresen J, Bester K. Elimination of organophosphate ester flame retardants and plasticizers in drinking water purification[J]. Water Research, 2006, 40(3): 621-629. DOI:10.1016/j.watres.2005.11.022 |
| [12] | Sang D K, Cho J, Kim I S, et al. Occurrence and removal of pharmaceuticals and endocrine disruptors in South Korean surface, drinking, and waste waters[J]. Water Research, 2007, 41(5): 1013-1021. DOI:10.1016/j.watres.2006.06.034 |
| [13] | Rodil R, Quintana J B, Concha-Graña E, et al. Emerging pollutants in sewage, surface and drinking water in Galicia (NW Spain)[J]. Chemosphere, 2012, 86(10): 1040-1049. DOI:10.1016/j.chemosphere.2011.11.053 |
| [14] | Li J, Yu N Y, Zhang B B, et al. Occurrence of organophosphate flame retardants in drinking water from China[J]. Water Research, 2014, 54(4): 53-61. |
| [15] | 丁锦建. 典型有机磷阻燃剂人体暴露途径与蓄积特征研究[D]. 杭州: 浙江大学, 2016. 49-66. http://cdmd.cnki.com.cn/Article/CDMD-10335-1016118136.htm |
| [16] |
赵秀阁, 段小丽. 中国人群暴露参数手册(成人卷):概要[M]. 北京: 中国环境科学出版社, 2014: 88. Zhao X G, Duan X L. Highlights of the Chinese exposure factors handbook (adults)[M]. Beijing: China Environmental Science Press, 2014: 88. |
| [17] | Shi W, Zhang F X, Zhang X W, et al. Identification of trace organic pollutants in freshwater sources in Eastern China and estimation of their associated human health risks[J]. Ecotoxicology, 2011, 20(5): 1099-1106. DOI:10.1007/s10646-011-0671-8 |
| [18] | Ali N, Ali L, Mehdi T, et al. Levels and profiles of organochlorines and flame retardants in car and house dust from Kuwait and Pakistan: Implication for human exposure via dust ingestion[J]. Environment International, 2013, 55: 62-70. DOI:10.1016/j.envint.2013.02.001 |
| [19] | Bacaloni A, Cavaliere C, Foglia P, et al. Liquid chromatography/tandem mass spectrometry determination of organophosphorus flame retardants and plasticizers in drinking and surface waters[J]. Rapid Communications in Mass Spectrometry, 2007, 21(7): 1123-1130. DOI:10.1002/(ISSN)1097-0231 |
| [20] | Benotti M J, Trenholm R A, Vanderford B J, et al. Pharmaceuticals and endocrine disrupting compounds in U.S. drinking water[J]. Environmental Science & Technology, 2009, 43(3): 597-603. |
| [21] | Ding J J, Shen X L, Liu W P, et al. Occurrence and risk assessment of organophosphate esters in drinking water from Eastern China[J]. Science of the Total Environment, 2015, 538: 959-965. DOI:10.1016/j.scitotenv.2015.08.101 |
| [22] | Regnery J, Püttmann W, Merz C, et al. Occurrence and distribution of organophosphorus flame retardants and plasticizers in anthropogenically affected groundwater[J]. Journal of Environmental Monitoring, 2011, 13(2): 347-354. DOI:10.1039/C0EM00419G |
| [23] | Stepien D K, Regnery J, Merz C, et al. Behavior of organophosphates and hydrophilic ethers during bank filtration and their potential application as organic tracers. A field study from the Oderbruch, Germany[J]. Science of the Total Environment, 2013, 458 -460: 150-159. DOI:10.1016/j.scitotenv.2013.04.020 |
| [24] | Stapleton H M, Klosterhaus S, Eagle S, et al. Detection of organophosphate flame retardants in furniture foam and U.S. house dust[J]. Environmental Science & Technology, 2009, 43(19): 7490-7495. |
| [25] | 刘同保, 张文秋. 阻燃剂TCEP的合成[J]. 化学世界, 1990(12): 539-543. |
| [26] |
望秀丽, 于文佳, 卫碧文, 等. 加速溶剂萃取-气相色谱-质谱法测定塑料中7种有机磷酸酯阻燃剂和增塑剂[J]. 分析试验室, 2017, 36(1): 109-113. Wang X L, Yu W J, Wei B W, et al. Determination of 7 organophosphate ester flame retardants and plasticizers in plastic products by accelerated solvent extraction-gas chromatography-mass spectrometry[J]. Chinese Journal of Analysis Laboratory, 2017, 36(1): 109-113. |
| [27] | Marklund A, Andersson B, Haglund P. Organophosphorus flame retardants and plasticizers in Swedish sewage treatment plants[J]. Environmental Science & Technology, 2005, 39(19): 7423-7429. |
| [28] | Van den Eede N, Dirtu A C, Neels H, et al. Analytical developments and preliminary assessment of human exposure to organophosphate flame retardants from indoor dust[J]. Environment International, 2011, 37(2): 454-461. DOI:10.1016/j.envint.2010.11.010 |
| [29] | 孙增平. 提高潍坊市蔬菜质量安全水平的对策研究[D]. 北京: 中国农业科学院, 2008. 28-29. |
| [30] | Ma Y, Jin J, Li P, et al. Organophosphate ester flame retardant concentrations and distributions in serum from inhabitants of Shandong, China, and changes between 2011 and 2015[J]. Environmental Toxicology & Chemistry, 2017, 36(2): 414-421. |
| [31] | Cristale J, Vázquez A C, Barata C, et al. Priority and emerging flame retardants in rivers: occurrence in water and sediment, Daphnia magna toxicity and risk assessment[J]. Environment International, 2013, 59(3): 232-243. |
 2017, Vol. 38
2017, Vol. 38