2. 暨南大学化学系, 广州 510632
2. Department of Chemistry, Jinan University, Guangzhou 510632, China
全氟辛烷磺酸(perfluorooctane sulfonate, PFOS)是水体中广泛存在的典型全氟化合物(perfluorochemicals, PFCs)之一.因其具有环境持久性、生物蓄积性、内分泌干扰性和其它生物毒性而备受关注[1, 2]. PFOS具有高能量C—F键, 是最难降解的持久性有机污染物之一, 虽在PFOS的物化降解[3]、光化学降解[4]和生物降解[1]方面有不少尝试, 但均需在苛刻的条件下反应, 不利于规模化去除PFOS.比较而言, 吸附是一种去除水中PFOS的简单有效的方法, 已研究的吸附剂有碳纳米管、氧化铝、树脂、活性炭、天然沉积物等[5~10].目前普遍认为污水处理厂的出水是水生生态系统中PFCs的主要污染源.在世界范围内的污水处理厂的进水和出水中, 浓度不等的PFOS被检出[11~14].在污水厂二级处理中, 因部分PFOS会吸附到活性污泥上, 因此在剩余污泥中也检测到了不同水平的PFOS[12, 15]. Guo等[16]分析了国内16个污水处理厂的污泥, 发现广州的污泥含PFOS最多, 达到5.383 mg ·kg-1(以污泥干重计,下同), 而香港污水厂剩余污泥中PFOS浓度达到7.305 mg ·kg-1[17], 瑞士的污水处理厂剩余污泥中检测到PFOS浓度更高达600 mg ·kg-1[18].
已有研究发现沉积物上有机碳的含量影响沉积物对PFOS的吸附富集[10, 19, 20].而活性污泥主要是由活的和死亡的微生物以及EPS组成[21], EPS的主要成分是多糖和蛋白质.相对于沉积物, 污泥EPS中有机碳的比例更高, 结合PFOS易于在蛋白质中富集理论[22], 可以推断活性污泥吸附PFOS受到蛋白质含量的影响, 但具体的作用机制有待进一步探究. Zhou等[21]通过污泥吸附PFOS实验, 发现静电相互作用和疏水作用是主要吸附机制并推测金属离子的存在有助于PFOS吸附. PFOS的功能基团硫酸根虽不能直接结合金属离子形成复杂的化合物[23], 但金属离子可与污泥表面EPS中的羧基、氨基化合物以及酚基反应[24], 改变了活性污泥表面的活性基团, 进而影响PFOS的吸附, 但是目前针对金属离子对污泥吸附PFOS影响的研究还较少.
本文采用城市污水处理厂活性污泥和去除了EPS的污泥对PFOS进行吸附研究, 从吸附动力学、等温线、金属离子等方面考察了影响PFOS吸附的因素, 探究了污泥吸附PFOS过程中EPS的作用机制, 以期为污水处理厂去除PFCs类物质提供参考.
1 材料与方法 1.1 药品全氟辛烷磺酸钾盐(Perfluorooctane sulfonic acid potassium salt, PFOS-K, 98%)购自百灵威(J&K Scientific Ltd), 色谱纯乙酸铵(98%)和色谱纯乙腈购自安谱公司(CNW Technologies). 732强酸苯乙烯阳离子交换树脂购自阿拉丁(Aladdin Industrial Corpo-ration), 其它试剂均为分析纯, 购自广州化学试剂厂.
1.2 污泥来源和去除EPS污泥的制备活性污泥取自广州某城市污水处理厂二沉池, 用蒸馏水洗涤3次, 浓缩后放入4℃冰箱保存, 混合液悬浮固体浓度(mixed liquid suspended solids, MLSS)为17.73 g ·L-1.去除污泥EPS采用经过调整的阳离子交换树脂法[25], 用0.85%的生理盐水清洗活性污泥3次, 加入阳离子交换树脂, 4℃搅拌24 h, 静置15 min后收集上层液体, 离心后重悬, 制成去除EPS的浓缩污泥, MLSS为22.73 g ·L-1.
1.3 吸附实验本实验采用序批式方法, 准确加入去离子水和PFOS标液, 根据预实验结果调节pH为6, 再加入污泥浓缩液, 使体系总体积为30 mL, 体系中污泥MLSS为800 mg ·L-1, PFOS浓度为0.5 mg ·L-1, 在25℃下, 以160 r ·min-1的速度振荡, 直至达到吸附平衡.吸附动力学实验于48 h内的不同时间点取样, 过0.22 μm水系滤膜.吸附等温线实验, PFOS初始浓度控制在0.07~0.7 mg ·L-1范围内, 体系中污泥MLSS为800 mg ·L-1, 吸附率在30%~70%之间, 25℃恒温振荡36 h取样.研究金属离子对PFOS吸附的影响, 分别设定Ca2+浓度为0.1~100 mmol ·L-1, Cu2+浓度为0.01~0.5 mmol ·L-1, 25℃恒温振荡36 h取样.
1.4 分析方法PFOS浓度采用Agilent 1200 Series高效液相色谱和6410质谱联用仪(Agilent Technologies, 美国)检测.色谱柱:C18(2.1 mm×150 mm, 5 μm); 柱温:40℃; 进样量:10 μL; 流速:0.30 mL ·min-1; 流动相:乙腈(A)/5 mmol ·L-1乙酸铵溶液(B)(体积比25 :75);梯度洗脱程序:0~1 min, 25%~95% A; 1~6 min, 95% A; 6~6.5 min, 95%~25%A; 6.5~7 min, 25% A; 7~12 min, 25% A.离子源:电喷雾电离(ESI); 负离子模式扫描; 多重反应监测(MRM)模式.
冷冻干燥后的污泥样品, 与溴化钾粉末充分混合后压片, 采用傅里叶红外光谱仪(Thermo Nicolet CCR-1, 美国)对其进行分析.污泥样品压片后采用X射线光电发射光谱分析(Thermo Fisher Scientific-K-Alpla 1063, 美国).
1.5 质量控制与保证实验所用容器均为聚丙烯(PP)材质.吸附实验中每个处理均设置3个平行.在每批样品进行仪器分析前, 用空白溶剂和已知浓度标样检查仪器的灵敏度和稳定性, 同一标样测定的误差小于20%方可进行样品测定.实验所获数据利用Microsoft Excel 2013和Origin Pro 8进行统计、分析及绘图.
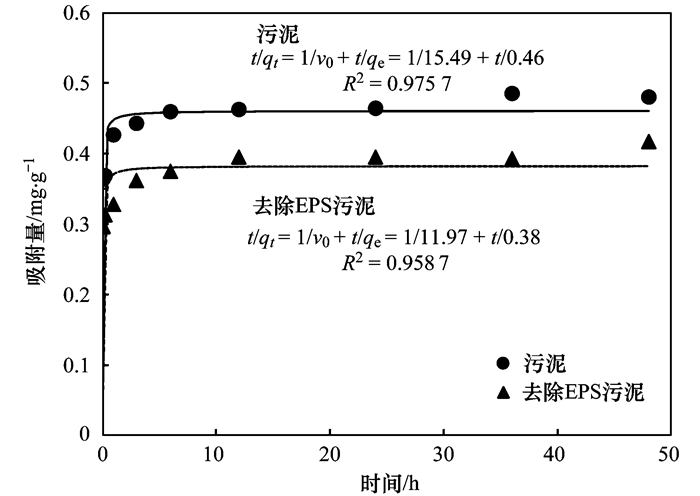
2 结果与讨论 2.1 PFOS的吸附动力学由图 1看出, 正常活性污泥吸附PFOS在6 h基本达到平衡, 符合一般污水处理厂的水力停留时间, 而去除了EPS的污泥吸附PFOS需要12 h才能达到平衡.准二级吸附动力学模型被应用于描述污染物在水溶液中的化学吸附过程, 方程如下:

|
|
图 1 PFOS的准二级吸附动力学模型拟合结果 Fig. 1 Sorption kinetics of PFOS using the pseudo-second-order model |
式中, t为吸附时间(h), qt为t时刻活性污泥对PFOS的吸附量(mg ·g-1), k2为吸附速率常数(g ·mg-1 ·g-1), qe是吸附平衡时的饱和吸附量(mg ·g-1), v0=k2qe2可以反映初始吸附速率(mg ·h-1).本实验结果显示采用准二级动力学模型拟合动力学数据, 拟合程度非常高, R2均在0.958以上, 这说明污泥和去除EPS污泥吸附PFOS过程以化学吸附占主导.正常活性污泥的平衡吸附量qe和初始吸附速率v0(0.46 mg ·g-1和15.49 mg ·h-1)大于去除EPS后污泥(0.38 mg ·g-1和11.97 mg ·h-1), 说明EPS对PFOS吸附起到重要作用.有研究指出PFOS易于在蛋白质中富集[22], 而活性污泥主要成分EPS中含有大量蛋白质, 这为PFOS的吸附富集提供了可能.污泥EPS中蛋白质与PFOS之间易于结合, 可能与蛋白质中的活性基团(羟基、氨基等)有关.
2.2 PFOS的吸附等温线Freundlich、Langmuir及Temkin模型被用来描述PFOS的吸附过程[26], 实验结果(表 1) 显示3种模型均能较好地拟合活性污泥吸附PFOS的过程, 而对去除EPS后污泥的拟合效果均变差. Langmuir模型描述的是均匀表面的单层吸附, Freundlich模型描述的是不均匀表面的多层吸附.拟合结果说明活性污泥对PFOS的吸附以相似表面的单层吸附为主, 同时具有一定的多层吸附的位点和能力[27].由于Temkin模型主要用于描述发生正负离子强烈静电作用的化学吸附过程, 从Temkin模型拟合结果可以推断活性污泥在吸附PFOS过程中有静电相互作用现象, 而去除污泥的EPS后, 拟合效果变差, 说明污泥与PFOS之间的静电作用减弱.
|
|
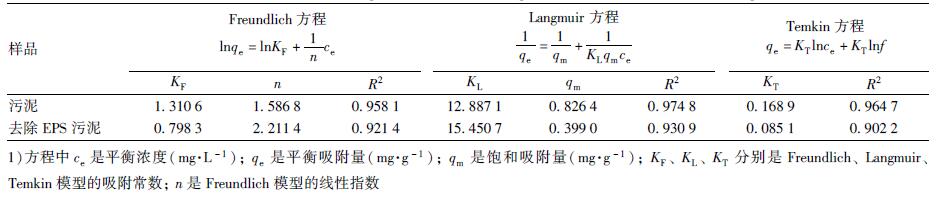
表 1 Freundlich、Langmuir、Temkin吸附等温方程拟合参数 Table 1 Parameters from the fitting of the Freundlich, Langmuir and Temkin model for PFOS sorption |
2.3 Ca2+、Cu2+对PFOS吸附的影响
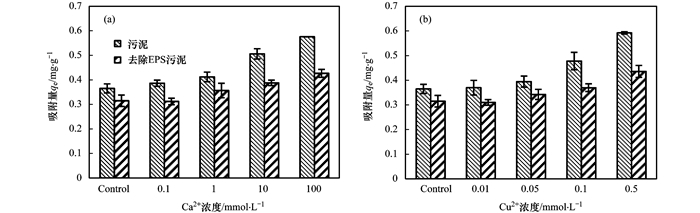
有研究发现, 金属离子通过离子架桥作用可以促进PFOS在天然沉积物和活性污泥上的吸附[10, 21].如图 2所示, PFOS在活性污泥和去除EPS污泥上的吸附量随着Ca2+和Cu2+浓度的增大而增加.在100 mmol ·L-1Ca2+存在下吸附量较对照组分别提高了36.6%和26.2%, 0.5 mmol ·L-1Cu2+存在下吸附量分别提高了38.4%和27.2%, 说明Ca2+和Cu2+存在促进了污泥对PFOS的吸附.主要原因可能是:① 阳离子Ca2+和Cu2+浓度增加中和了污泥表面的负电荷, 降低了污泥与PFOS之间的静电斥力, 有助于PFOS通过静电引力作用吸附在活性污泥表面[21]; ② PFOS钾盐在纯水中的溶解度为608 mg ·L-1, 但在0.005 mol ·L-1CaCl2溶液中的溶解度为307 mg·L-1 [28], 盐度的升高使PFOS在水中的溶解度减小, 在活性污泥上的吸附量增大; ③ 有研究指出在Ca2+离子架桥作用下, 天然沉积物对PFOS的吸附量提高[10], Cu2+也可与活性污泥(主要指氨基化合物)通过内配位作用形成复合物, 进而与有机物结合[24]. Ca2+和Cu2+在活性污泥吸附PFOS过程中存在离子架桥作用, 促进PFOS吸附.
|
图 2 Ca2+和Cu2+对PFOS吸附的影响 Fig. 2 Influence of Ca2+ and Cu2+ on the adsorption of PFOS |
随着Ca2+和Cu2+浓度增加, 去除EPS后污泥对PFOS的吸附增加量明显小于正常污泥, 推断污泥EPS中有能与Ca2+和Cu2+结合的活性基团, 去除EPS后污泥活性基团减少, 影响离子架桥作用.
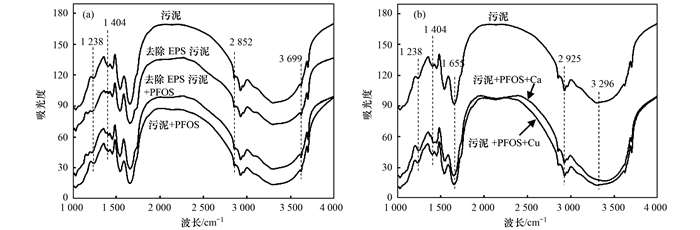
2.4 吸附PFOS前后污泥表面基团变化 2.4.1 FTIR分析从图 3(a)和表 2红外光谱分析结果表明, 污泥在去除EPS后, 1238 cm-1处峰值大幅降至1217 cm-1, 对应的是羧基的C=O键和氨基中的C—N键的伸缩振动[5]; 1404 cm-1处峰值降低至1379 cm-1, 对应的是C—H键, 可能是蛋白质分子中甲基的对称和反对称弯曲振动峰. 2852 cm-1和3699 cm-1处对应—OH的伸缩振动.由此看出, 污泥去除EPS后, 引起羧基、氨基和羟基官能团变化, 活性基团减少, 验证了2.1中的推断.污泥吸附PFOS后, 1238 cm-1处峰值红移至1240 cm-1, 3699 cm-1处峰值降低至3697 cm-1, 对应氨基和羟基变化, 而氨基是蛋白质的主要成分, 表明PFOS在活性污泥上的吸附过程中主要是与蛋白质发生反应, 而去除EPS后污泥中蛋白质减少, 这也进一步说明了去除EPS后污泥对PFOS吸附量下降的原因.
|
图 3 不同处理下活性污泥的红外图谱 Fig. 3 FTIR spectra of the activated sludge under different treatments |
|
|
表 2 活性污泥和去除EPS污泥吸附PFOS前后波长变化1)/cm-1 Table 2 Functional group changes before and after adsorption by activated sludge and EPS-removed sludge/cm-1 |
如图 3(b)和表 2所示, 在Ca2+存在下, 污泥吸附PFOS后, 2925 cm-1处峰值下降至2923 cm-1, 对应C—H、—OH伸缩振动[21];代表官能团—COOH的峰值从1655 cm-1下降至1653 cm-1[5, 29];代表羟基和氨基的峰值从3296 cm-1红移至3392 cm-1[21].在Cu2+存在的溶液中, 污泥吸附PFOS后, 1655 cm-1处峰值下降至1653 cm-1; 3296 cm-1处峰值红移至3300 cm-1.这些变化说明, 活性污泥上的羧基和氨基与Ca2+、Cu2+之间存在相互作用, 而在Ca2+和Cu2+存在下, PFOS在活性污泥上的吸附量明显增大. Ca2+和Cu2+在PFOS吸附过程中起架桥作用, 促进了PFOS在活性污泥上的吸附, 而产生架桥机制的主要基团还是蛋白质中的羧基和氨基.
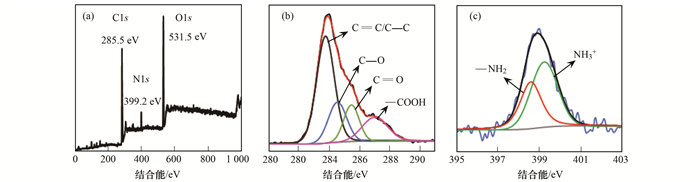
2.4.2 XPS分析采用XPS进一步分析污泥吸附PFOS后表面基团变化情况, 从图 4(a)看出污泥中含量最高的是C(285.5 eV)、N(399.2 eV)和O(531.5 eV)这3种元素, C1s高辨析能谱图[图 4(b)]由4个不同峰组成, 代表不同的含碳基团(C—C/C=C、C—O、C=O和—COOH), N1s高辨析能谱图[图 4(c)]由两个不同峰组成, 代表不同的含氮基团(—NH2和NH3+)[30].活性污泥碳和氮元素频谱数据分析结果如表 3所示.活性污泥去除EPS后, 含碳基团(C—O、C=O、—COOH)和含氮基团(—NH2和NH3+)的峰面积均减小, 说明污泥去除EPS过程中蛋白质和多糖等成分被部分去除, 羧基、氨基等基团随之减少, 这与FTIR结果一致.污泥吸附PFOS后, C=O和—COOH处峰面积均减小. —NH2峰面积减小, 并且在399.2 eV处氮元素半峰宽(FWHM)由1.51 eV增大到2.15 eV, 说明氮元素的化学存在形态发生变化, 羧基和氨基参与了吸附反应.
|
(a)活性污泥XPS图谱; (b)活性污泥C1s分峰拟合; (c)活性污泥N1s分峰拟合 图 4 活性污泥的XPS能谱分析 Fig. 4 XPS survey spectra of the activated sludge |
|
|
表 3 污泥样品XPS C1s和N1s频谱分析 Table 3 Analysis of the XPS spectra of C1s and N1s of different activated sludge samples |
Ca2+存在下C=O和—COOH峰面积减小, Cu2+存在下C—O基团峰面积增大, C=O和—COOH峰面积减小, 同时—NH2和NH3+峰面积也明显减小, 这些说明羟基、羧基和氨基均参与了吸附反应, 这与FTIR结果一致.与活性污泥单独吸附PFOS相比, 金属离子存在下, 羟基、羧基和氨基基团变化更大, 这与金属离子浓度增大, PFOS吸附量变大情况一致, 说明金属离子吸附在活性污泥上, 可以通过架桥机制促进PFOS的吸附.在24.5 eV处出现Ca2+峰, FWHM为2.44 eV, 说明活性污泥对Ca2+有吸附作用.
3 结论(1) 活性污泥吸附PFOS过程主要是化学机制主导, 吸附过程以相似表面的单层吸附为主, 同时具有一定的多层吸附, 并存在静电引力作用.金属离子添加有助于PFOS在污泥上的吸附.
(2) 在25℃下活性污泥吸附效果优于去除EPS后污泥, 平衡吸附量分别为0.46 mg ·g-1和0.38 mg ·g-1.去除污泥EPS对PFOS吸附有明显负面影响.
(3) PFOS在吸附过程中主要是与活性污泥上的羧基和氨基反应.污泥去除EPS后, 主要成分蛋白质含量减少, 活性基团(羧基、羟基和氨基)数量随之减少, 导致PFOS吸附量下降.通过离子架桥机制促进PFOS吸附过程中, 蛋白质(羧基和氨基)也起到重要作用.
| [1] | Kwon B G, Lim H J, Na S H, et al. Biodegradation of perfluorooctanesulfonate (PFOS) as an emerging contaminant[J]. Chemosphere, 2014, 109: 221-225. DOI:10.1016/j.chemosphere.2014.01.072 |
| [2] | Shan G Q, Ye M Q, Zhu B Z, et al. Enhanced cytotoxicity of pentachlorophenol by perfluorooctane sulfonate or perfluorooctanoic acid in HepG2 cells[J]. Chemosphere, 2013, 93(9): 2101-2107. DOI:10.1016/j.chemosphere.2013.07.054 |
| [3] | Zhang K L, Huang J, Yu G, et al. Destruction of perfluorooctane sulfonate (PFOS) and perfluorooctanoic acid (PFOA) by ball milling[J]. Environmental Science & Technology, 2013, 47(12): 6471-6477. |
| [4] | Jin L, Zhang P Y, Shao T, et al. Ferric ion mediated photodecomposition of aqueous perfluorooctane sulfonate (PFOS) under UV irradiation and its mechanism[J]. Journal of Hazardous Materials, 2014, 271: 9-15. DOI:10.1016/j.jhazmat.2014.01.061 |
| [5] | Kwadijk C J A F, Velzeboer I, Koelmans A A. Sorption of perfluorooctane sulfonate to carbon nanotubes in aquatic sediments[J]. Chemosphere, 2013, 90(5): 1631-1636. DOI:10.1016/j.chemosphere.2012.08.041 |
| [6] | Wang F, Shih K. Adsorption of perfluorooctanesulfonate (PFOS) and perfluorooctanoate (PFOA) on alumina: influence of solution pH and cations[J]. Water Research, 2011, 45(9): 2925-2930. DOI:10.1016/j.watres.2011.03.007 |
| [7] | Yu Q, Zhang R Q, Deng S B, et al. Sorption of perfluorooctane sulfonate and perfluorooctanoate on activated carbons and resin: kinetic and isotherm study[J]. Water Research, 2009, 43(4): 1150-1158. DOI:10.1016/j.watres.2008.12.001 |
| [8] |
童锡臻, 石宝友, 解岳, 等. 改性活性炭对水中PFOS的吸附去除研究[J]. 环境科学, 2012, 33(9): 3132-3138. Tong X Z, Shi B Y, Xie Y, et al. Adsorption of perfluorooctanesulfonate (PFOS) onto modified activated carbons[J]. Environmental Science, 2012, 33(9): 3132-3138. |
| [9] | Deng S B, Nie Y, Du Z W, et al. Enhanced adsorption of perfluorooctane sulfonate and perfluorooctanoate by bamboo-derived granular activated carbon[J]. Journal of Hazardous Materials, 2015, 282: 150-157. DOI:10.1016/j.jhazmat.2014.03.045 |
| [10] | You C, Jia C X, Pan G. Effect of salinity and sediment characteristics on the sorption and desorption of perfluorooctane sulfonate at sediment-water interface[J]. Environmental Pollution, 2010, 158(5): 1343-1347. DOI:10.1016/j.envpol.2010.01.009 |
| [11] | Flores C, Ventura F, Martin-Alonso J, et al. Occurrence of perfluorooctane sulfonate (PFOS) and perfluorooctanoate (PFOA) in N. E. Spanish surface waters and their removal in a drinking water treatment plant that combines conventional and advanced treatments in parallel lines[J]. Science of the Total Environment, 2013, 461-462: 618-626. DOI:10.1016/j.scitotenv.2013.05.026 |
| [12] | Thompson J, Eaglesham G, Reungoat J, et al. Removal of PFOS, PFOA and other perfluoroalkyl acids at water reclamation plants in South East Queensland Australia[J]. Chemosphere, 2011, 82(1): 9-17. DOI:10.1016/j.chemosphere.2010.10.040 |
| [13] | Kim S K, Im J K, Kang Y M, et al. Wastewater treatment plants (WWTPs)-derived national discharge loads of perfluorinated compounds (PFCs)[J]. Journal of Hazardous Materials, 2012, 201-202: 82-91. DOI:10.1016/j.jhazmat.2011.11.036 |
| [14] | Arvaniti O S, Ventouri E I, Stasinakis A S, et al. Occurrence of different classes of perfluorinated compounds in Greek wastewater treatment plants and determination of their solid-water distribution coefficients[J]. Journal of Hazardous Materials, 2012, 239-240: 24-31. DOI:10.1016/j.jhazmat.2012.02.015 |
| [15] | Llorca M, Farré M, Picó Y, et al. Analysis of perfluorinated compounds in sewage sludge by pressurized solvent extraction followed by liquid chromatography-mass spectrometry[J]. Journal of Chromatography A, 2011, 1218(30): 4840-4846. DOI:10.1016/j.chroma.2011.01.085 |
| [16] | Guo R, Zhou Q F, Cai Y Q, et al. Determination of perfluorooctane sulfonate and perfluorooctanoic acid in sewage sludge samples using liquid chromatography/quadrupole time-of-flight mass spectrometry[J]. Talanta, 2008, 75(5): 1394-1399. DOI:10.1016/j.talanta.2008.01.052 |
| [17] | Ma R W, Shih K. Perfluorochemicals in wastewater treatment plants and sediments in Hong Kong[J]. Environmental Pollution, 2010, 158(5): 1354-1362. DOI:10.1016/j.envpol.2010.01.013 |
| [18] | Sun H W, Gerecke A C, Giger W, et al. Long-chain perfluorinated chemicals in digested sewage sludges in Switzerland[J]. Environmental Pollution, 2011, 159(2): 654-662. DOI:10.1016/j.envpol.2010.09.020 |
| [19] | Higgins C P, Luthy R G. Sorption of perfluorinated surfactants on sediments[J]. Environmental Science & Technology, 2006, 40(23): 7251-7256. |
| [20] | Becker A M, Gerstmann S, Frank H. Perfluorooctanoic acid and perfluorooctane sulfonate in the sediment of the Roter Main river, Bayreuth, Germany[J]. Environmental Pollution, 2008, 156(3): 818-820. DOI:10.1016/j.envpol.2008.05.024 |
| [21] | Zhou Q, Deng S B, Zhang Q Y, et al. Sorption of perfluorooctane sulfonate and perfluorooctanoate on activated sludge[J]. Chemosphere, 2010, 81(4): 453-458. DOI:10.1016/j.chemosphere.2010.08.009 |
| [22] | Liao C Y, Li X Y, Wu B, et al. Acute Enhancement of synaptic transmission and chronic inhibition of synaptogenesis induced by perfluorooctane sulfonate through mediation of voltage-dependent calcium channel[J]. Environmental Science & Technology, 2008, 42(14): 5335-5341. |
| [23] | Higgins C P, Luthy R G. Modeling sorption of anionic surfactants onto sediment materials: an a priori approach for perfluoroalkyl surfactants and linear alkylbenzene sulfonates[J]. Environmental Science & Technology, 2007, 41(9): 3254-3261. |
| [24] | Song X C, Liu D F, Zhang G W, et al. Adsorption mechanisms and the effect of oxytetracycline on activated sludge[J]. Bioresource Technology, 2014, 151: 428-431. DOI:10.1016/j.biortech.2013.10.055 |
| [25] | 中华人民共和国环境保护部. 水和废水监测分析方法[M]. (第四版). 北京: 中国环境科学出版社, 2002: 200-281. |
| [26] |
陈瑞萍, 张丽, 于洁, 等. 活性污泥对四环素的吸附性能研究[J]. 环境科学, 2012, 33(1): 156-162. Chen R P, Zhang L, Yu J, et al. Study on the sorption behavior of tetracycline onto activated sludge[J]. Environmental Science, 2012, 33(1): 156-162. |
| [27] | Duong H A, Pham N H, Nguyen H T, et al. Occurrence, fate and antibiotic resistance of fluoroquinolone antibacterials in hospital wastewaters in Hanoi, Vietnam[J]. Chemosphere, 2008, 72(6): 968-973. DOI:10.1016/j.chemosphere.2008.03.009 |
| [28] | Pan G, Jia C X, Zhao D Y, et al. Effect of cationic and anionic surfactants on the sorption and desorption of perfluorooctane sulfonate (PFOS) on natural sediments[J]. Environmental Pollution, 2009, 157(1): 325-330. DOI:10.1016/j.envpol.2008.06.035 |
| [29] |
张涵瑜, 王兆炜, 高俊红, 等. 芦苇基和污泥基生物炭对水体中诺氟沙星的吸附性能[J]. 环境科学, 2016, 37(2): 689-696. Zhang H Y, Wang Z W, Gao J H, et al. Adsorption characteristics of norfloxacin by biochars derived from reed straw and municipal sludge[J]. Environmental Science, 2016, 37(2): 689-696. |
| [30] |
郑蕾. 活性污泥胞外聚合物吸附重金属效能与机制研究[D]. 哈尔滨: 哈尔滨工业大学, 2006. 78-80. Zheng L. Research on efficiency and mechanisms of heavy metal adsorption by EPS from activated sludge[D]. Harbin: Harbin Institute of Technology, 2006. 78-80. |
 2017, Vol. 38
2017, Vol. 38