2. 工业聚集区污染控制与生态修复教育部重点实验室, 广州 510006;
3. 固体废物处理与资源化广东省环境保护重点实验室, 广州 510006;
4. 广东省环境纳米材料工程技术研究中心, 广州 510006
2. Key Laboratory of Pollution Control and Ecosystem Restoration in Industry Clusters, Ministry of Education, Guangzhou 510006, China;
3. Guangdong Environmental Protection Key Laboratory of Solid Waste Treatment and Recycling, Guangzhou 510006, China;
4. Guangdong Engineering and Technology Research Center for Environmental Nanomaterials, Guangzhou 510006, China
贵金属钯因具备多种优良性能而广泛应用于电子产品、航空航天、信息传感、工业催化等现代工业.贵金属钯的需求量不断增加[1], 然而近半个世纪的开采已经将储存量有限的钯矿产资源由地下转为地上, 且存在于废弃物中, 所以从二次资源中如电子废弃物、废汽车催化剂、甚至军事装备的废物中回收钯已成为日益关注的问题[2~4].传统方法如离子交换、溶剂萃取、膜过滤和化学沉淀法从废物中回收钯普遍存在成本高、效率低、污染环境等局限性[5~7].因此, 亟需寻求成本低、效率高、环境友好的方法回收钯.
近年来, 微生物因其资源丰富、廉价易得、污染小等优点, 被尝试通过生物吸附、还原作用将贵金属由离子态还原为单质态[8~11], 从而实现贵金属的回收.然而, 现有的对于钯生物回收研究集中在纯钯溶液的微生物吸附和还原, 但实际的含钯废物中会存在其它金属离子[12].有研究表明, 其它金属离子可能在生物回收过程中出现目标金属离子竞争[13], 而对其它金属离子存在条件下钯的生物回收研究显得明显不足.
本研究的目的是探讨从3种模拟废水包括工业废液(IW)、废旧电路板(PCBS)和废汽车催化剂(SAC)[12, 14~16]中生物回收钯, 评估废水中各金属离子如Pt(Ⅳ)、Ag(Ⅰ)、Cu(Ⅱ)、Au(Ⅲ)和Fe(Ⅱ)对钯回收过程的影响, 并将回收所得的纳米钯掺杂四氧化三铁, 应用于非均相芬顿反应中催化降解亚甲基蓝.
1 材料与方法 1.1 菌种及实验药品实验所用四氯钯酸钠、氯铂酸、氯金酸、硫酸亚铁、酵母提取粉、蛋白胨、氯化钠、硫酸、氢氧化钠、氨水(30%)、双氧水(30%)、亚甲基蓝等药品均为分析纯(阿拉丁), 实验用水为去离子水.采用氯钯酸钠配成钯浓度为2 864.6 mg·L-1的水溶液作为储备液.所用菌种为由本实验室自行分离获得的粪肠球菌Z5(CCTCC M2012445), 菌株所用培养基为luria broth(LB)培养基(蛋白胨10 g·L-1, 酵母提取粉5 g·L-1, NaCl 10 g·L-1), pH值调节至7. 0左右, 培养条件为30℃[17].在厌氧培养箱中培养2~3 d至稳定期, 经10 000 r·min-1离心3 min得到菌体(Sigma 3X-KL, USA), 经去离子水清洗3次后配成细菌干重为1.2 g·L-1(biomass dry weight, BDW)菌悬储备液备用.
1.2 实验过程 1.2.1 模拟废水中钯的回收所有实验均在以下条件进行:50 mL离心管作为反应容器, 1.2 g·L-1的菌悬液10 mL, 温度为30℃, pH为3.5, 振荡30 min充分混合和吸附后, 视情况加入电子供体进行还原.
生物法从模拟废水中还原钯设置菌悬液+钯溶液(0.21g·L-1)+甲酸钠(25 mmol·L-1)实验组, 以及菌悬液+钯溶液(0.21 g·L-1)对照组.还原所得的含钯粪肠球菌超声破碎30 min后用去离子水离心清洗3遍, 60℃下烘干6 h得到钯纳米颗粒产物[18].
钯的吸附实验采用配制的工业废液[12]、废旧线路板[14]和废旧汽车催化剂[16]这3种模拟废水(表 1), 分别加菌悬液反应.还原实验在吸附实验基础上分别加入25 mmol·L-1甲酸钠电子供体.
|
|
表 1 模拟废水中不同金属离子的浓度/mg·L-1 Table 1 Composition of samples containing various metal ions for biorecovery experiments/mg·L-1 |
单一金属离子对钯吸附实验设定钯的浓度为0.21 g·L-1, 设置Pd(Ⅱ)+Au(Ⅲ)、Pd(Ⅱ)+Pt(Ⅳ)、Pd(Ⅱ)+Ag(Ⅰ)、Pd(Ⅱ)+Cu(Ⅱ)和Pd(Ⅱ)+Fe(Ⅱ)这5个实验组, 钯与上述5组金属浓度比设置为2:1、1:1和1:2.还原实验在吸附实验条件基础上加入25 mmol·L-1甲酸钠.
1.2.2 Pd/Fe3O4制备将上述钯溶液(0.21g·L-1)+甲酸钠(25 mmol·L-1)实验中回收的生物钯经超声后释放出纳米颗粒, 用于Pd/Fe3O4的合成[19].简言之, 将一定量的三氯化铁、硫酸亚铁和钯纳米颗粒溶于水中, 与氨水溶液中超声辅助共沉淀得到Pd/Fe3O4纳米颗粒.超声过程中溶液温度保持在60℃, 向氨水中逐滴加入三氯化铁、硫酸亚铁和钯纳米颗粒混合溶液, 后继续超声30 min, 放置在60℃热水浴中静置2 h, 使纳米颗粒陈化, 然后用磁铁将Pd/Fe3O4纳米颗粒从溶液中分离出来, 用超纯水清洗4~5次至上清液的pH值为7左右.
1.2.3 Pd/Fe3O4催化亚甲基蓝降解选用100 mL的离心管作为反应容器, 称取0.100 0 g的催化剂投加到50 mL的2.5 mg·L-1的亚甲基蓝溶液中, 调节pH为3.5左右放入超声洗涤器中溶解2 min.最后加入双氧水(30%)0.5 mL放入超声洗涤器中反应.在该实验的基础上, 分别做:Pd/Fe3O4+亚甲基蓝+双氧水+超声、双氧水+亚甲基蓝+超声、Pd/Fe3O4+亚甲基蓝、Fe3O4+亚甲基蓝+双氧水+超声共4组实验, 每组实验3个平行.间隔20 min取样, 总取样时间为2 h.取样时以0.5 μm的针管滤头过滤后迅速用紫外可见分光光度计(Shimazu-UV2450, Japan)在663 nm处进行测定.
1.3 分析及表征方法反应体系中溶液摇匀后取少量滴在铜网上, 室温风干后进行透射电镜(HITACHIH-7650, Japan)观察.金属浓度采用火焰原子吸收法(Shimadzu-AA6880, Japan)测定, 样品测定前溶液经离心并用0.22 μm的微孔滤膜过滤并经过适当倍数稀释.实验每组重复3次.样品中钯纳米颗粒和Pd/Fe3O4的晶体状态利用X射线衍射(Bruker Corp Billerica, USA)进行分析; 钯和Pd/Fe3O4形态采用X射线光电子能谱(Kratos-Axis UltraDLD, England)分析, 结合能以C 1s的自然碳的结合能进行校准, 采用XPSPEAK Version 4. 1分峰软件对数据进行分峰拟合.
2 结果与分析 2.1 生物法回收模拟废水中钯如图 1(a)所示, 二价钯离子溶液在紫外可见分光光谱(200~800 nm)425 nm处有吸收峰, 而钯生物回收体系中无吸收峰, 溶液颜色由乳白色变为黑色, 由此说明Pd(Ⅱ)生物回收体系中的状态有变化.将钯生物回收体系中获得的产物和化学方法制备的产物XRD图谱进行比较[图 1(b)], 发现粪肠球菌从模拟废水中回收的钯和化学制备的钯的出峰位置相同, 2θ角位于40.1°、46.7°、68.1°和82.1°分别对应钯单质的(111)、(200)、(220) 和(311) 的衍射晶面[8, 19], 由此可以证实粪肠球菌在电子供体存在下可以从模拟废液中还原钯并形成零价钯纳米颗粒.从透射电镜图图 1(c)和图 1(d)对比可以看出,在钯生物回收体系中细胞的表面以及细胞周质中存在大量的纳米颗粒, 通过超声破碎将颗粒释放出来, 会观察到形态各异的纳米颗粒[图 1(e)].

|
图 1 生物回收钯的表征 Fig. 1 Characterization of biogenic palladium |
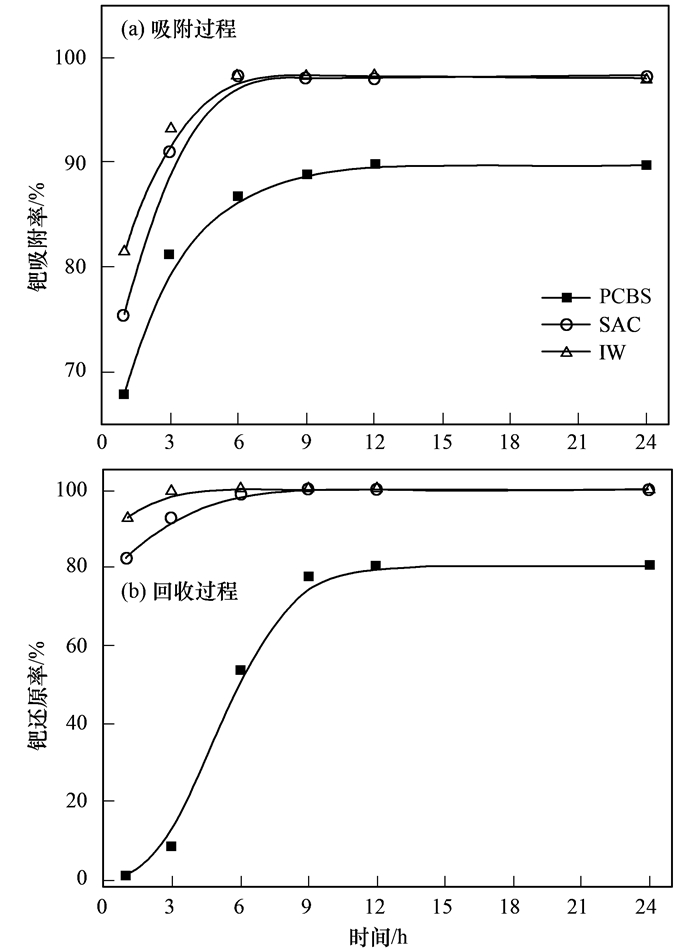
3种模拟废水钯的吸附率和还原率如图 2所示.在吸附过程中, IW废水最先达到吸附平衡, 在6 h时达到最大钯吸附率99.8%, SAC废水吸附速率其次, 在8 h后达到吸附平衡, 吸附率为99.7%.而PCBS废水12 h时钯的吸附率却只有90.3%.钯的还原率结果与吸附效率类似, IW废水在4 h时还原平衡, SAC废水6 h达到还原平衡.而PCBS废水在36 h达到最大还原率80.4%低于IW, SAC两种废水的还原率99.9%. 3种模拟废水中钯的吸附和还原效率的差异, 可能由于3种模拟废水中金属离子的量不同会影响粪肠球菌的吸附和还原速度.粪肠球菌的浓度一定导致其表面的活性位点有限, Pd(Ⅱ)浓度增加会形成活性位点竞争, 并且其它金属离子的存在也可能会竞争吸附, 从而导致吸附率和还原率下降.在钯的吸附和还原体系中, PCBS的Pd(Ⅱ)浓度最高, 其次SAC、IW, 所以吸附与还原率表现为IW>SAC>PCBS.
|
图 2 模拟废水中钯的生物回收率 Fig. 2 Biorecovery efficiency of Pd(Ⅱ) from simulation of wastewater resources |
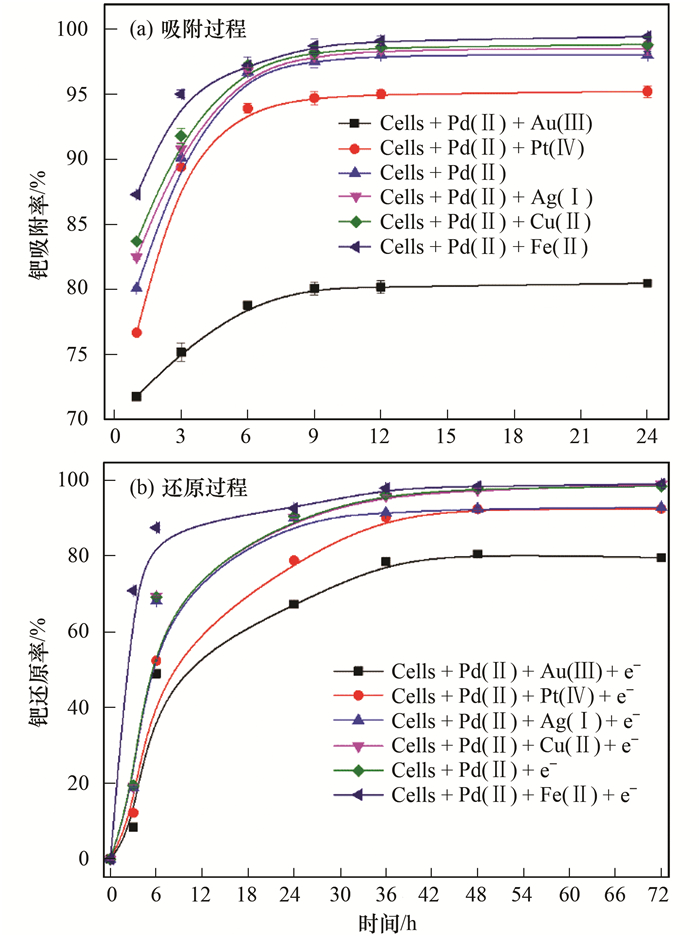
不同模拟废水中的其它金属离子对钯的吸附还原过程的影响如图 3所示.在吸附过程中[图 3(a)], 随着时间增加, 钯吸附率均逐渐上升, 而吸附速率和达到平衡的时间有所不同.所有组的吸附率依次为细菌+Pd(Ⅱ)+Fe(Ⅱ) (99.8%)、细菌+Pd(Ⅱ) (99.4%)、细菌+Pd(Ⅱ)+Cu(Ⅱ) (98.6%)、细菌+Pd(Ⅱ)+Ag(Ⅰ) (98.5%)、细菌+Pd(Ⅱ)+Pt(Ⅳ) (95.8%)和细菌+Pd(Ⅱ)+Au(Ⅲ) (81.3%).可以看出, Fe(Ⅱ)的存在会提升钯的吸附效率, 而Cu、Ag、Pt、Au则会降低钯的吸附效率.
|
图 3 单一金属离子对钯生物回收过程的影响 Fig. 3 Pd(Ⅱ) biosorption efficiency in the presence of other single metal ions at intervals |
在还原过程中[图 3(b)], 从溶液中完全去除钯, Cells+Pd(Ⅱ)体系需要36 h, 而当添加Fe(Ⅱ)后, Pd(Ⅱ)从溶液中完全去除只要24 h.其他离子的存在使钯的还原效率在72 h后为84.2%~99.7%, 这说明其它金属离子的存在会影响钯的生物回收.原因可能是钯离子和金、银、铜、铂离子竞争吸附粪肠球菌表面的活性位点, 从而导致钯的吸附和还原效率降低, 而Fe(Ⅱ)却和钯不形成竞争关系, 反而会促进粪肠球菌对钯离子的吸附与还原.
钯与其它金属离子不同浓度比条件下的钯吸附率和回收率如图 4所示.在吸附过程中[图 4(a)], [Cells+Pd(Ⅱ)]和添加铁时[Pd(Ⅱ):Fe(Ⅱ)为2:1、1:1和3:1]钯的吸附率最高为99.5%~99.9%.而Au(Ⅲ)、Pt(Ⅳ)、Ag(Ⅰ)、Cu(Ⅱ)与钯按比例的添加会使得吸附率逐渐降低, 依次为Au(Ⅲ) (99.2%~93.9%)、Ag(Ⅰ) (99.1%~93.4%)、Pt(Ⅳ) (98.8%~91.9%)和Cu(Ⅱ) (95.1%~75.2%).与生物吸附相似, 钯的生物还原率随着Pt(Ⅳ)、Ag(Ⅰ)、Cu(Ⅱ)和Au(Ⅲ)的添加会降低[图 4(b)], 依次为Ag(Ⅰ)(99.6%~98.7%)、Cu(Ⅱ)(98.5%~95.4%)、Pt(Ⅳ) (99.8%~93.8%)和Au(Ⅲ) (97.3%~76.8%), 而Fe(Ⅱ)的添加则使钯的还原率达100%.

|
图 4 不同的金属离子浓度比下钯的回收率 Fig. 4 Pd(Ⅱ) biorecovery efficiencies in the presence of other single metal ions at various concentration ratios |
综合以上结果, 可以进一步证实其它金属离子的存在会影响钯的生物回收率, 影响程度为Au(Ⅲ)>Pt(Ⅳ)>Cu(Ⅱ)>Ag(Ⅰ)>Fe(Ⅱ), 其中Fe(Ⅱ)的存在会促进钯的生物回收.
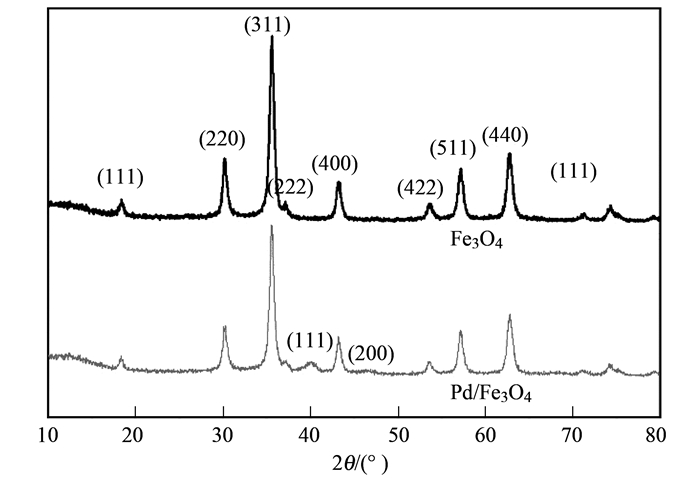
2.4 Pd/Fe3O4纳米颗粒及其催化性能 2.4.1 Pd/Fe3O4纳米颗粒的表征为了确定合成产物的晶型, 将制备的Fe3O4和Pd/Fe3O4进行X射线衍射分析, 结果如图 5所示, 在18.32°、30.12°、35.44°、37.12°、40.1°、43.12°、46.7°、53.4°、57.0°、62.56°等处出现衍射强峰. 2θ角位于分别对应四氧化三铁的(111)、(200)、(220)、(311)、(222)、(422)、(511)、(440)[20]以及钯单质的(111)、(200)[19]的衍射晶面.说明采用超声法制备的Fe3O4和Pd/Fe3O4具备晶体结构, 并且钯单质掺杂进入四氧化三铁中.
|
图 5 四氧化三铁和掺杂纳米钯的四氧化三铁XRD图谱 Fig. 5 XRD diffraction spectra of Fe3O4 and Pd/Fe3O4 |
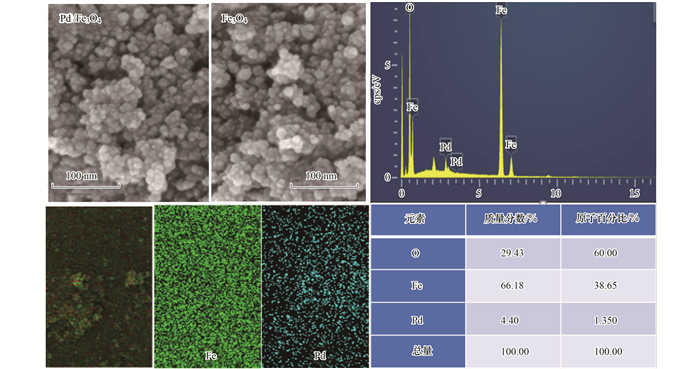
扫描电镜和能谱分析可以进一步确定掺杂纳米钯的四氧化三铁的形态、粒径及元素分布.从图 6可以看出, 超声法制备的Fe3O4和Pd/Fe3O4为球形, 粒径大小在10 nm左右, 且大小均一.由能谱可发现, 钯在四氧化三铁中分布均匀.
|
图 6 扫描电镜和能谱分析 Fig. 6 SEM images and EDS analysis |
为了研究Pd/Fe3O4催化剂的元素组成和原子价态, 对Pd/Fe3O4颗粒进行XPS表征.如图 7(a)所示, 全谱扫描图检测到了较强的C、Fe、O、Pd的特征峰, 说明颗粒表面有着4种元素组成.为了进一步分析颗粒表面的组成和原子价态, 分别对Fe2p和Pd2p进行了窄谱扫描, 其中Fe2p的窄谱谱图见图 7(b), Pd/Fe3O4纳米颗粒在710.8 eV和724.5 eV处出现两个峰, 分别对应Fe2p3/2和Fe2p1/2结合能, 与文献[21]中的值吻合, 而且无伴峰的存在, 表明得到的样品是Fe3O4.钯在335.5 eV和341.4 eV处出现两个峰, 分别对应Pd3d5/2和Pd3d3/2的结合能[22, 23], 说明钯为单质形态.

|
图 7 Pd/Fe3O4的XPS能谱 Fig. 7 XPS of Pd/Fe3O4 |
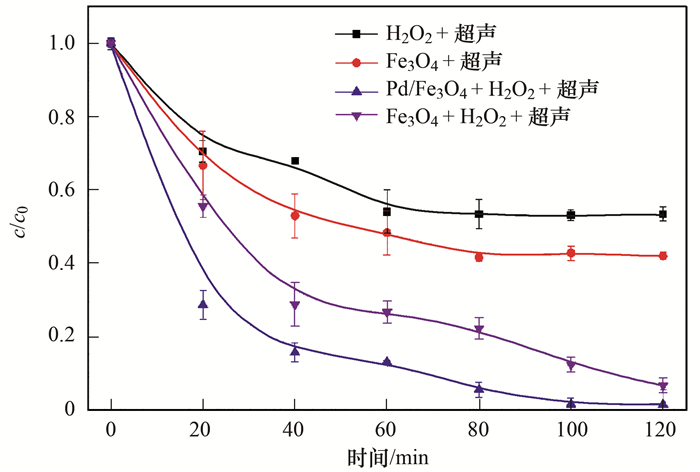
Pd/Fe3O4作为芬顿反应的催化剂, 对催化过氧化氢氧化降解染料的反应有明显的效果. 图 8所示为不同体系中的去除效果随时间的变化.当只把双氧水加入到溶液中时, 染料的去除率较低(47%), 这表明直接氧化的能力是很有限的.当只加入催化剂到溶液中时, 亚甲基蓝的120 min去除率为58.1%, 这主要是由于纳米复合物对污染物的吸附引起的.而所制备的催化剂和双氧水同时加入到溶液中时, 亚甲基蓝的去除率得到明显提高, Fe3O4+H2O2+超声体系对亚甲基蓝在120 min时去除率为93.4%.主要原因可能是四氧化三铁具有类似过氧化氢模拟酶的性质, 能够有效地加速分解且产生羟基自由基或者超氧自由基等活性中间体, 从而加快氧化反应速率和污染物降解或者彻底矿化[24, 25].当Pd/Fe3O4替代Fe3O4, Pd/Fe3O4+H2O2+超声体系在80 min时对亚甲基蓝的去除率达到96.7%.其原因可能是掺杂钯进一步加快了电子转移速度, 加速羟基自由基的产生, 从而获得了更高的染料降解速率[18, 26, 27].
|
图 8 不同体系下亚甲基蓝的去除 Fig. 8 Removal of methylene blue in the different systems |
近年来, 采用生物技术手段从废弃物中回收贵金属是研究热点.尽管从含有复杂金属离子的废水中回收钯的研究很少, 但是单一金属离子对微生物回收钯的影响却备受关注.例如, 使用D. desulfuricans NCIMB 8307在以氢气作为电子供体时钯的还原效率可以达到58%, 而当添加铂时微生物对钯的还原效率降为29.3%[8].当添加不同浓度的铜离子时(2%、5%、7%和10%), D. desulfuricans ATCC 29577回收钯的效率会随着铜离子的浓度升高呈现更为明显的抑制作用[28].本研究中, 粪肠球菌对钯的最大回收率出现在钯铂比为1时, 钯的吸附率和还原率分别达到95.8%和96.5%.而Au(Ⅲ)、Pt(Ⅳ)、Ag(Ⅰ)、Cu(Ⅱ)都会抑制Pd(Ⅱ)的吸附和还原, 抑制作用的影响程度为Au(Ⅲ)>Pt(Ⅳ)>Ag(Ⅰ)>Cu(Ⅱ).相反, Fe(Ⅱ)的存在会促进粪肠球菌对Pd(Ⅱ)的回收.
实际废水一般均含有多种金属离子, 所以采用模拟废水研究生物回收钯对于实际废水处理具有重要的现实意义.本研究结果表明, 生物法不仅可以有效回收含钯废水中的钯, 还可以同时将废水中的金属离子Au(Ⅲ)、Pt(Ⅳ)、Ag(Ⅰ)、Cu(Ⅱ)去除.然而, 实际废水中往往含有更多的金属离子如Zn、Al、Mg和Mn等阳离子和Cl-、SO4-、CO3-、NO3-等阴离子[29], 甚至有机物也可能对钯生物回收造成影响[30].因此, 可以进一步采用实际废水, 研究废水中其它物质的存在对钯微生物回收过程的影响.
众所周知, 钯能高效催化难降解污染物的降解, 生物钯可用于催化卤代污染物的脱卤反应[31]、硝基芳香烃污染物还原为芳香胺的反应[32]、偶氮化合物偶氮键加氢断裂反应[33]等.本研究尝试采用微生物回收纳米钯掺杂四氧化三铁应用于亚甲基蓝染料的非均相芬顿反应中并辅以超声, 发现染料在钯掺杂后的纳米四氧化三铁使得脱色速度明显提高, 在80 min时基本完全脱色.这不仅实现了生物法回收的钯产物高效催化污染物降解, 而且与四氧化三铁掺杂后有利于催化剂的回收和循环利用.今后可开展含钯废水中铁钯的同步回收和钯掺杂四氧化三铁纳米颗粒制备方法研究, 同时进一步研究钯掺杂后的纳米四氧化三铁在非均相芬顿反应中的机制.
4 结论(1) 利用粪肠球菌Z5可以从3种模拟废水中回收贵金属钯, 3种废水中钯的回收效率依次为IW>SAC>PCBS.
(2) 废水中其它金属离子的存在会影响钯的回收, 影响程度依次为Au(Ⅲ)>Pt(Ⅳ)>Cu(Ⅱ)>Ag(Ⅰ)>Fe(Ⅱ).
(3) 将生物回收所得的零价纳米钯颗粒掺杂到四氧化三铁中所得的Pd/Fe3O4作为非均相芬顿反应的催化剂催化降解亚甲基蓝具有明显效果, 80 min内亚甲基蓝的降解率为96.7%.
| [1] | Hagelüken C. Recycling the platinum group metals: a European perspective[J]. Platinum Metals Review, 2012, 56(1): 29-35. DOI:10.1595/147106712X611733 |
| [2] | Lu C Y, Zhang L, Zhong Y G, et al. An overview of e-wastes management in China[J]. Journal of Material Cycles and Waste Management, 2015, 17(1): 1-12. DOI:10.1007/s10163-014-0256-8 |
| [3] | Zhou C, Ontiveros-Valencia A, Wang Z C, et al. Palladium recovery in a H2-based membrane biofilm reactor: formation of Pd(0) nanoparticles through enzymatic and autocatalytic reductions[J]. Environmental Science & Technology, 2016, 50(5): 2546-2555. |
| [4] | Singh K K, Ruhela R, Das A, et al. Separation and recovery of palladium from spent automobile catalyst dissolver solution using dithiodiglycolamide encapsulated polymeric beads[J]. Journal of Environmental Chemical Engineering, 2015, 3(1): 95-103. DOI:10.1016/j.jece.2014.11.002 |
| [5] | Ilyas S, Lee J C. Biometallurgical recovery of metals from waste electrical and electronic equipment: a review[J]. ChemBioEng Reviews, 2014, 1(4): 148-169. DOI:10.1002/cben.v1.4 |
| [6] | Can M, Bulut E, Özacar M. Synthesis and characterization of gallic acid resin and its interaction with palladium(Ⅱ), rhodium(Ⅲ) chloro complexes[J]. Industrial & Engineering Chemistry Research, 2012, 51(17): 6052-6063. |
| [7] | Mack C, Wilhelmi B, Duncan J R, et al. Biosorption of precious metals[J]. Biotechnology Advances, 2007, 25(3): 264-271. DOI:10.1016/j.biotechadv.2007.01.003 |
| [8] | Lloyd J R, Yong P, Macaskie L E. Enzymatic recovery of elemental palladium by using sulfate-reducing bacteria[J]. Applied and Environmental Microbiology, 1998, 64(11): 4607-4609. |
| [9] | Cho C W, Kang S B, Kim S, et al. Reusable polyethylenimine-coated polysulfone/bacterial biomass composite fiber biosorbent for recovery of Pd(Ⅱ) from acidic solutions[J]. Chemical Engineering Journal, 2016, 302: 545-551. DOI:10.1016/j.cej.2016.05.091 |
| [10] | Singh P, Kim Y J, Zhang D B, et al. Biological synthesis of nanoparticles from plants and microorganisms[J]. Trends in Biotechnology, 2016, 34(7): 588-599. DOI:10.1016/j.tibtech.2016.02.006 |
| [11] | Suja E, Nancharaiah Y V, Venugopalan V P. Biogenic nanopalladium production by self-immobilized granular biomass: application for contaminant remediation[J]. Water Research, 2014, 65: 395-401. DOI:10.1016/j.watres.2014.08.005 |
| [12] | Behnamfard A, Salarirad M M, Veglio F. Process development for recovery of copper and precious metals from waste printed circuit boards with emphasize on palladium and gold leaching and precipitation[J]. Waste Management, 2013, 33(11): 2354-2363. DOI:10.1016/j.wasman.2013.07.017 |
| [13] | Muehe E M, Schmidt C, He J, et al. Microbially supported recovery of precious metals and rare earth elements from urban household waste incineration slag[J]. Advanced Materials Research, 2015, 1130: 652-655. DOI:10.4028/www.scientific.net/AMR.1130 |
| [14] | Creamer N J, Baxter-Plant V S, Henderson J, et al. Palladium and gold removal and recovery from precious metal solutions and electronic scrap leachates by Desulfovibrio desulfuricans[J]. Biotechnology Letters, 2006, 28(18): 1475-1084. DOI:10.1007/s10529-006-9120-9 |
| [15] | Nikoloski A N, Ang K L, Li D. Recovery of platinum, palladium and rhodium from acidic chloride leach solution using ion exchange resins[J]. Hydrometallurgy, 2015, 152: 20-32. DOI:10.1016/j.hydromet.2014.12.006 |
| [16] | Zhang Y H, Liu S L, Xie H H, et al. Current status on leaching precious metals from waste printed circuit boards[J]. Procedia Environmental Sciences, 2012, 16: 560-568. DOI:10.1016/j.proenv.2012.10.077 |
| [17] |
商儒, 朱能武, 康乃馨, 等. 生物法回收贵金属铂纳米颗粒及其机制[J]. 环境科学, 2016, 37(7): 2799-2806. Shang R, Zhu N W, Kang N X, et al. Bio-inspired recovery of platinum nanoparticle and its mechanism[J]. Environmental Science, 2016, 37(7): 2799-2806. |
| [18] | Ha C, Zhu N W, Shang R, et al. Biorecovery of palladium as nanoparticles by Enterococcus faecalis and its catalysis for chromate reduction[J]. Chemical Engineering Journal, 2016, 288: 246-254. DOI:10.1016/j.cej.2015.12.015 |
| [19] | Wang N, Zhu L H, Wang D L, et al. Sono-assisted preparation of highly-efficient peroxidase-like Fe3O4 magnetic nanoparticles for catalytic removal of organic pollutants with H2O2[J]. Ultrasonics Sonochemistry, 2010, 17(3): 526-533. DOI:10.1016/j.ultsonch.2009.11.001 |
| [20] | Hou L W, Zhang H, Wang L G, et al. Ultrasound-enhanced magnetite catalytic ozonation of tetracycline in water[J]. Chemical Engineering Journal, 2013, 229: 577-584. DOI:10.1016/j.cej.2013.06.013 |
| [21] | Hou L W, Wang L G, Royer S, et al. Ultrasound-assisted heterogeneous Fenton-like degradation of tetracycline over a magnetite catalyst[J]. Journal of Hazardous Materials, 2016, 302: 458-467. DOI:10.1016/j.jhazmat.2015.09.033 |
| [22] | Saldan I, Semenyuk Y, Marchuk I, et al. Chemical synthesis and application of palladium nanoparticles[J]. Journal of Materials Science, 2015, 50(6): 2337-2354. DOI:10.1007/s10853-014-8802-2 |
| [23] | Xiong L, Chen J J, Huang Y X, et al. An oxygen reduction catalyst derived from a robust Pd-reducing bacterium[J]. Nano Energy, 2015, 12: 33-42. DOI:10.1016/j.nanoen.2014.11.065 |
| [24] |
何洁, 杨晓芳, 张伟军, 等. 纳米Fe3O4-H2O2非均相Fenton反应催化氧化邻苯二酚[J]. 环境科学, 2013, 34(5): 1773-1781. He J, Yang X F, Zhang W J, et al. Catalyzed oxidation of catechol by the heterogeneous Fenton-like reaction of nano-Fe3O4-H2O2 system[J]. Environmental Science, 2013, 34(5): 1773-1781. |
| [25] | Yoo S H, Jang D, Joh H I, et al. Iron oxide/porous carbon as a heterogeneous Fenton catalyst for fast decomposition of hydrogen peroxide and efficient removal of methylene blue[J]. Journal of Materials Chemistry A, 2017, 5(2): 748-755. DOI:10.1039/C6TA07457J |
| [26] | Narayani H, Augustine R, Sumi S, et al. Removal of basic and industrial azo reactive dyes from aqueous solutions via Fenton-like reactions using catalytic non-magnetic Pd-flyash and magnetic Pd-Fe3O4-flyash composite particles[J]. Separation and Purification Technology, 2017, 172: 338-349. DOI:10.1016/j.seppur.2016.08.027 |
| [27] | Li X F, Liu X, Xu L L, et al. Highly dispersed Pd/PdO/Fe2O3 nanoparticles in SBA-15 for Fenton-like processes: confinement and synergistic effects[J]. Applied Catalysis B: Environmental, 2015, 165: 79-86. DOI:10.1016/j.apcatb.2014.09.071 |
| [28] | Ju X H, Igarashi K, Miyashita S I, et al. Effective and selective recovery of gold and palladium ions from metal wastewater using a sulfothermophilic red alga, Galdieria sulphuraria[J]. Bioresource Technology, 2016, 211: 759-764. DOI:10.1016/j.biortech.2016.01.061 |
| [29] | Awual M R, Hasan M M, Znad H. Organic-inorganic based nano-conjugate adsorbent for selective palladium(Ⅱ) detection, separation and recovery[J]. Chemical Engineering Journal, 2015, 259: 611-619. DOI:10.1016/j.cej.2014.08.028 |
| [30] | Huang J L, Lin L Q, Sun D H, et al. Bio-inspired synthesis of metal nanomaterials and applications[J]. Chemical Society Reviews, 2015, 44(17): 6330-6374. DOI:10.1039/C5CS00133A |
| [31] | Gelder E A, Jackson S D, Lok C M. A study of nitrobenzene hydrogenation over palladium/carbon catalysts[J]. Catalysis Letters, 2002, 84(3-4): 205-208. |
| [32] | Kantam M L, Chakravarti R, Pal U, et al. Nanocrystalline magnesium oxide-stabilized palladium(0): an efficient and reusable catalyst for selective reduction of nitro compounds[J]. Advanced Synthesis & Catalysis, 2008, 350(6): 822-827. |
| [33] | Pizarro A H, Molina C B, Rodriguez J J. Decoloration of azo and triarylmethane dyes in the aqueous phase by catalytic hydrotreatment with Pd supported on pillared clays[J]. Rsc Advances, 2016, 6: 113820-113825. DOI:10.1039/C6RA24542K |
 2017, Vol. 38
2017, Vol. 38



