2. 华东师范大学河口海岸学国家重点实验室, 上海 200062;
3. 华东师范大学地理科学学院, 教育部地理信息科学重点实验室, 上海 200241
2. State Key Laboratory of Estuarine and Coastal Research, East China Normal University, Shanghai 200062, China;
3. Key Laboratory of Geographic Information Science, Ministry of Education, School of Geographical Sciences, East China Normal University, Shanghai 200241, China
天然胶体(colloids)指的是至少一维粒径介于1 nm~1 μm之间的固态物质[1, 2].水环境中的胶体可源于火山爆发、岩石风化等自然过程, 也可源于人类活动, 如烟囱粉尘、污水排放等.值得注意的是, 随着纳米技术的发展及纳米材料的大量使用, 这些纳米颗粒不可避免地进入水环境中, 并成为天然胶体的重要组成部分.胶体广泛存在于水环境中, 具有化学异质性, 其粒径小、比表面积大、表面活性基团丰富, 因此易与水环境中的多种污染物相结合[3~6], 进而影响这些污染物在水环境中的赋存、分配、迁移转化和生态效应等一系列环境行为.
天然胶体的粒径分布差异较大, 不同粒径胶体所含的物质组成不尽相同[1], 并且胶体的粒径大小能够决定其理化特性, 进而影响其对水环境中污染物的去向和归宿.例如, 研究发现垃圾渗滤液中Mr>100×103的溶解性有机质(DOM)降解最快, 而邻苯二甲酸酯(PAEs)主要被Mr 1×103~100×103组分所吸附[7]; 土壤中Mr>14×103的DOM对扑草净的迁移作用比其他分级组分大, 这与该分级DOM中较多的芳香组分及不饱和结构有关[8]; 同大粒径DOM相比(Mr 3.5×103~10×103), 小粒径DOM(Mr < 3.5×103)对甲基汞的降解有促进作用[9].然而, 当前有关天然胶体理化性质表征的研究还主要集中于胶体整体方面(即不区分胶体粒径或组分), 对不同粒径胶体中的物质组成、形态结构等知之甚少.因此, 亟需开展水环境中不同粒径天然胶体的理化性质研究, 这是了解不同粒径胶体与污染物环境行为之间相互关系及作用机制的前提和关键.同时, 天然胶体的来源复杂, 因此需要综合应用多种技术来更好地表征其复杂性、异质性和多分散性[10, 11].随着胶体分离及分析技术的发展, 切向流超滤技术(cross-flow ultrafiltration, CFUF)和三维荧光光谱技术(3D EEM)能够有效结合, 目前已被广泛用于不同粒径胶体的分离、组分鉴定及来源辨析[12~15].
黄浦江是上海的重要水道, 流域内人口稠密、经济发达, 上游农业污水及中下游城市生活污水、工业废水的排放成为流域内胶体及众多污染物的重要来源.胶体是水体中污染物的重要载体, 研究流域内典型污水中胶体、尤其是不同粒径胶体的理化性质, 对于深入认识水环境中胶体及其所负载污染物的环境归趋均具有重要意义.因此, 本研究选取黄浦江上游两处受养殖区废水排放影响河流(代表农业污水)及上海市区内的一处污水处理厂进出水(代表生活污水), 采用CFUF技术对采集的水样进行粒径分级, 利用3D EEM重点分析黄浦江流域典型污水中不同粒径胶体的三维荧光光谱特性, 以期为水环境中天然胶体的环境行为以及对痕量污染物的环境归趋作用提供基础数据.
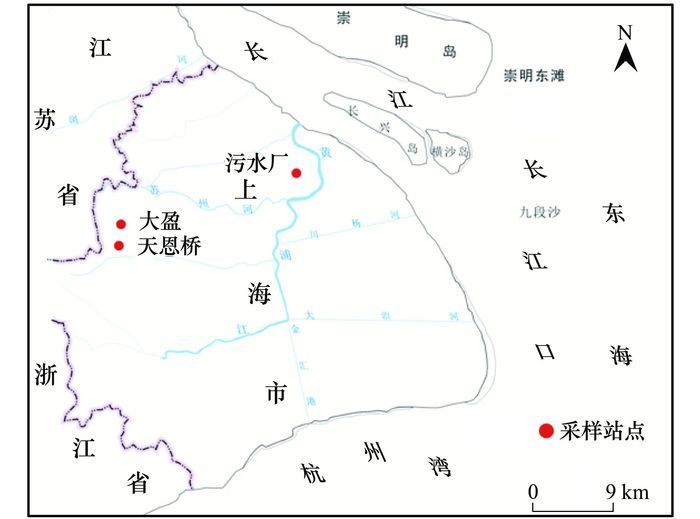
1 材料与方法 1.1 样品采集污水处理厂污水及养殖区污水分别于2013年1月及4月采集回实验室, 采样点分布如图 1所示.养殖区采样点分别为大盈(种畜场)及天恩桥(养猪场).由于水深较浅(1.0~1.5 m左右), 因而选取各采样点表层(30 cm以内)水体作为研究水样.污水处理厂位于上海市区内、黄浦江下游, 水样分别采自污水厂进、出水口处.采样时, 使用洗净后的50 L不锈钢桶进行储存、运输.
|
图 1 黄浦江流域典型污水采样点分布示意 Fig. 1 Sampling sites along Huangpu River |
水样带回实验室后立即用孔径为1 μm的玻璃纤维滤膜(PAUL, USA)进行过滤, 因此过滤所得的水样为粒径 < 1 μm的过滤水.本研究采用CFUF(Pellicon System, Millipore)装置对水中胶体进行分离, 超滤方法参照作者前期工作中所述方法[6], 超滤器内置不同规格的超滤膜(regenerated cellulose, Pellicon 2 PLAC, Millipore).本研究所使用的超滤膜规格包括Mr 1×103(0.5 m2)及Mr 5×103、10×103、300×103(5×10-3 m2)等, 根据超滤膜孔径的不同可以分离得到不同粒径的胶体浓缩液, 粒径范围(Mr)分别为1×103~5×103、5×103~10×103、10×103~300×103、300×103~1 μm.整个分离过程的回收率为72.5%~108.0%.
1.3 三维荧光光谱分析三维荧光光谱分析采用日立(Hitachi)F-4500荧光分光光度计进行测定.三维荧光光谱的扫描波长分别为:激发波长Ex=200~400 nm, 发射波长Em=250~500 nm, 激发波长和发射波长的增量均为3 nm.扫描模式为3D扫描, PMT电压为700 V, 扫描速率为2 400 nm·min-1, 响应时间为2 s, 狭缝宽度为5 nm.所有样品测试前均依据各自的胶体质量浓度进行不同程度的稀释以去除内滤效应对分析结果的影响.利用Origin 9.0软件进行三维荧光光谱图(EEMs)的绘制及相关数据处理(所绘EEMs均为经过扣除Mili-Q超纯水后的矫正结果, 以减少仪器条件和拉曼散射对荧光光谱的影响).根据Coble的研究[16], 天然胶体的荧光峰可分为类蛋白物质及类腐殖质两类特征峰, 其中类蛋白荧光峰包括峰D(Ex=210~230 nm, Em=340~360 nm)和峰T(Ex=270~280 nm, Em=330~370 nm), 类腐殖质荧光峰包括峰A(Ex=210~250 nm, Em=400~460 nm)和峰C(Ex=300~340 nm, Em=400~460 nm).
为了进一步研究不同粒径分级胶体荧光组分的差异, 本研究引入荧光指数FI值、腐殖化指数(humification index, HIX)及生源指数(the index of recent autochthonous contribution, BIX)这3个表征胶体组分来源及特性的指标[17]. FI定义为Ex=370 nm时, Em在450 nm和500 nm下的荧光强度的比值.当FI接近1.9时, 表明荧光组分主要为内源来源; 当FI接近1.4时, 荧光组分主要为陆源来源[18]. HIX最早由Zsolnay等[19]在评价土壤中溶解性有机质的成熟度时引入. HIX定义为Ex=254 nm时, Em为435~480 nm与300~345 nm条件下峰值面积的比值.当HIX为10~16时, 表示荧光组分的腐殖化程度较高、主要为陆源来源, 当HIX < 4时, 则主要为自生源有机质[20]. BIX主要指示的是微生物来源有机质与外源有机质的比例, 用以衡量自生源的贡献率, 定义为Ex=310 nm时, Em为380 nm和430 nm时的荧光强度比值.因此随着BIX增加, 荧光组分中的自生源贡献率随之增加.当BIX>1时, 认为该有机质主要为新近产生的自生源有机质; 当BIX为0.6~0.7时, 认为自生源的有机质较少.
1.4 胶体质量浓度、胶体态有机碳质量浓度测定胶体质量浓度采用称量法进行测定.即:准确量取10 mL的胶体浓缩液置于表面皿中, 并用扎有小孔的铝箔将表面皿包裹, 60℃烘箱烘干后, 利用公式(1) 计算出胶体质量浓度(CC, mg·L-1):
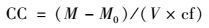
|
(1) |
式中, M0及M分别为烘干前、后表面皿的重量, cf为胶体浓缩倍数(40), V为量取的胶体浓缩液体积.
过滤水、超滤水、胶体浓缩液中的有机碳质量浓度通过TOC分析仪测定(liquiTOC Ⅱ, Elementar, Germany), 胶体态有机碳质量浓度(COC, mg·L-1)则通过公式(2) 计算获得:
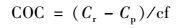
|
(2) |
式中, Cr及Cp分别为胶体浓缩液及超滤水中有机碳质量浓度.
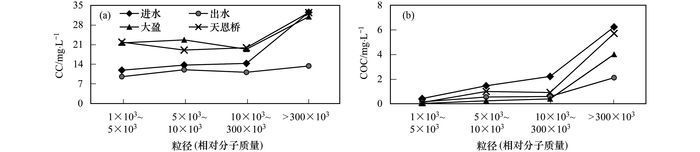
2 结果与讨论 2.1 不同粒径分级胶体的胶体质量浓度(CC)及胶体态有机碳质量浓度(COC)不同粒径(Mr)分级胶体CC及COC值如表 1及图 2所示. 4种水样1×103~5×103、5×103~10×103、10×103~300×103、300×103~1 μm分级胶体CC分别为9.60~21.90、12.05~22.70、11.15~19.90和13.40~32.50 mg·L-1.不同粒径分级胶体CC随粒径增加呈递增趋势[图 2(a)], 但该趋势在污水厂出水中表现得最不明显, 而其他3种污水的Mr 300×103~1 μm分级CC明显高于其他分级, 说明污水厂出水中小颗粒胶体的比重较大, 而其他3种污水以大颗粒胶体的比重较大.此外, 养殖区污水CC大于污水厂进、出水, 其中污水厂出水中各分级CC最低, 并且除Mr 300×103~1 μm分级以污水厂进水稍高, 其他分级的CC值均以养殖区污水较高.说明养殖污水中的胶体质量浓度普遍高于生活污水, 且主要集中在Mr < 300×103的范围内.从各粒径分级CC占全粒径(即Mr 1×103~1 μm)胶体的比值看, 1×103~5×103、5×103~10×103、10×103~300×103和300×103~1 μm胶体占全粒径(Mr)胶体的百分比分别为16.4%~23.5%、19.0%~26.1%、19.8%~24.1%和29.0%~44.9%.其中, 污水厂进水以300×103~1 μm粒径分级胶体占主导(44.9%), 其他3个分级(即1×103~5×103、5×103~10×103和10×103~300×103)CC占全粒径(Mr)胶体比例均为4种水样中最低; 污水厂出水的1×103~5×103、5×103~10×103和10×103~300×103所占比例均为4种水样中最高, 说明污水处理厂对大颗粒胶体(即>300×103)的去除效果较显著.
|
|
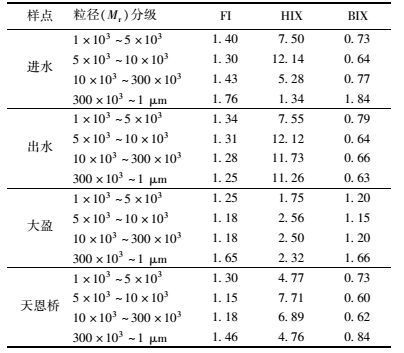
表 1 不同粒径分级胶体的理化性质 Table 1 Physicochemical properties of the different colloidal size fractions |
|
图 2 不同粒径分级胶体的质量浓度(CC)及胶体态有机碳质量浓度(COC) Fig. 2 Colloidal concentration and colloidal organic carbon content of the different colloidal size fractions |
典型污染源水体中超滤水的有机碳质量浓度(UOC)为4.62~6.78 mg·L-1, 其中Mr 1×103~5×103、Mr 5×103~10×103、Mr 10×103~300×103和Mr 300×103~1 μm胶体的COC依次为0.03~0.43、0.24~1.47、0.40~2.22和2.12~6.25 mg·L-1. UOC及各粒径分级胶体COC占水体总有机碳的比例分别为46.7%~60.4%(Mr < 1×103)、0.3%~1.6%(Mr 1×103~5×103)、2.3%~6.9%(Mr 5×103~10×103)、3.7%~8.5%(Mr 10×103~300×103)、23.9%~39.3%(Mr 300×103~1 μm).从图 2(b)可以看出, 各粒径分级胶体的COC随胶体粒径的增加而增加, 其中污水厂进水COC最高, 养殖区污水Mr 300×103~1 μm分级COC明显高于其他3个分级, 而污水厂出水各粒径分级COC相差最小.相关分析结果表明, 各粒径分级胶体CC与其COC之间存在显著正相关关系(R=0.77, P < 0.001), 结合前文分析可知单位体积典型污水中大尺寸胶体的质量浓度大、胶体态有机碳的质量浓度较高.计算结果发现, Mr 300×103~1 μm粒径胶体COC大约是Mr 1×103~5×103粒径胶体的13~137倍, 说明污水厂及养殖区水体中的有机碳主要集中在大尺寸的胶体上.换言之, 能够去除这一粒径分级的胶体对于控制污水中的有机碳浓度具有重要意义.就污水厂进、出水的COC而言, 各粒径分级中有机碳的去除效率基本一致, 在60%~70%之间.
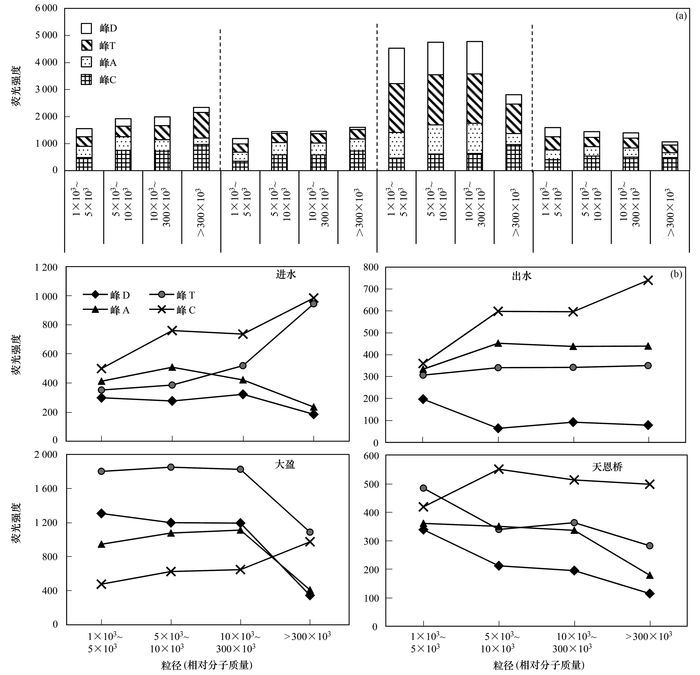
2.2 不同分级胶体样品的三维荧光光谱特性4种污水样品不同粒径分级胶体的EEMs如图 3所示.根据Coble[16]对荧光峰的分类, 本研究中除进水Mr 300×103~1 μm分级胶体(无峰D)外, 4种荧光团均存在, 其荧光峰荧光强度最大值位置分别为Ex/Em=230/352~361 nm(峰D)、Ex/Em=281/331~370 nm(峰T)、Ex/Em=239~251/400~460 nm(峰A)、Ex/Em=311~341/400~451 nm(峰C).一般而言, 类腐殖质荧光峰与腐殖质结构中的羰基和羧基有关[21~23], 且其强度通常都比较大.但受到人类活动污染后, 河流中胶体的类蛋白荧光峰强度会明显增强.类蛋白荧光峰通常与胶体中的芳环氨基酸结构有关[24~26], 其主要来源于生物活动和人为活动的干扰, 其强度可指示水体中的微生物活动及受污染的程度[27].本研究中4种污水中荧光强度变化趋势为大盈>进水>出水≈天恩桥[图 4(a)], 并且可以看出, 峰C为进水、出水及天恩桥污水的主要荧光峰, 峰T为大盈水样的主要荧光峰.以上结果说明污水厂进水经处理后胶体荧光强度有明显降低, 并且不同来源污水的主导荧光峰差异较大, 比如对于不同的农业污水, 其主导荧光峰也有所不同.此外, 4种水样均呈现出较高的类蛋白荧光峰, 表明这些水体受到了人类活动的强烈干扰, 其中大盈水样受干扰的情况最为严重.

|
图 3 不同来源水体中不同粒径分级胶体的EEMs Fig. 3 Fluorescence EEM plots and fluorescence peak positions of the different colloidal fractionations from the different sources |
|
图 4 不同粒径分级胶体4种荧光团的峰值荧光强度 Fig. 4 Fluorescence intensities of peak positions of four selected fluorophores |
此外, 分析4种荧光峰的最大荧光强度发现[图 4(b)], 随胶体粒径的增加所有污水样品中峰D和峰A的荧光强度总体呈减小趋势, 峰C的荧光强度呈增加趋势; 但对于峰T, 随胶体粒径增加, 进水及出水样品中呈增加趋势, 大盈及天恩桥水样中呈减小趋势.结合前人研究, 推测本研究中10×103~300×103分级胶体主要为类腐殖质荧光峰, 类蛋白荧光峰主要存在于Mr 1×103~5×103分级胶体中[28, 29].而Mr 300×103~1 μm分级胶体中的荧光峰较少, 这与黄文丹等研究发现长江口水体中Mr>500×103胶体中的荧光组分较少结论一致[12].相关分析还发现, 峰D、峰T、峰A两两间存在显著正相关关系, 相关系数分别为0.84(P < 0.001, 峰D与峰T)、0.93(P < 0.001, 峰D与峰A)、0.77(P < 0.001, 峰T与峰A), 说明水体受人类活动干扰加剧的同时, 类蛋白荧光物质及腐殖酸亦随之增加, 其来源主要为外源输入, 并且这3种荧光组分存在同源性.
胶体各荧光指数值如表 1所示(包括FI、HIX、BIX). 4种污水的FI值为1.15~1.76, 表明所选胶体既有陆源又有内源类荧光物质存在.并且, Mr 1×103~5×103、5×103~10×103和10×103~300×103分级胶体的FI值较接近1.4(表 1), 而Mr 300×103~1 μm分级胶体(除出水水样外)的FI值较接近1.9, 说明小粒径胶体的荧光物质主要为陆源来源, 而大粒径胶体多来源于生物分解的内源来源.此结论与天然水体中不同粒径分级的胶体分析结果一致[30], 即天然水体中的胶体(1~100×103)主要为陆源来源.由此看出, 典型污水与天然水体不同分级胶体的判源方法相似, 但当胶体粒径较大时(如Mr>300×103), 该分析方法并不适用, 这可能与大粒径胶体中较高的脂肪碳有关.此外, 一般而言, 荧光指数FI值越低, 荧光物质的芳香性越高[31].因此, 从进、出水的FI对比值看, 出水中Mr 10×103~300×103及Mr 300×103~1 μm分级胶体的FI值明显降低, 说明污水处理厂对进水中大粒径胶体(Mr>100×103)的非芳香性组分进行了较好的处理, 从而使得出水中这些粒径分级胶体的芳香性明显提高.从污水厂和养殖区污水的FI对比值看, 养殖区污水较低, 说明养殖区污水中胶体的芳香性较高.
本研究中HIX值为1.34~12.14, 说明所分级胶体的腐殖化程度差异较大, 来源上既有陆源又有内源类荧光物质存在(HIX>16代表DOM具有强腐殖化特征, 以陆源输入为主; 6<HIX < 10代表较强腐殖化特征, 且有较弱自生源特征; 4<HIX < 6代表弱腐殖化特征, 及较强自生源特征; < 4表示自生源为主[32]), 该结论与FI值的分析结果较吻合.相关分析表明, 二者呈显著负相关关系(R=-0.48, P=0.032).从粒径分级的变化趋势上看, Mr 5×103~10×103和Mr 10×103~300×103分级胶体的HIX值相对较高, 表明这两个分级胶体的腐殖化程度相对较高, 该结论与这两个分级胶体中峰A较高的荧光强度值相一致[图 4(b)], 但本研究并未发现HIX值与峰A的最大荧光强度间存在显著相关关系.
4种污水的BIX值为0.60~1.84.可以看出, 除大盈污水及进水的300×103~1 μm分级胶体外, 其它水样大部分分级胶体的BIX值均接近0.6~0.7, 说明这些分级胶体自生源的比率低, 该结论与FI值的分析结果一致.从粒径分级的变化趋势上看, Mr 300×103~1 μm分级胶体的BIX值与其他粒径分级胶体相比有明显增加的趋势(除出水外), 说明大粒径胶体为新近产生的自生源有机质的可能性大.大粒径胶体BIX值较高的原因在于:大粒径胶体所受自然降解过程相较于小粒径胶体弱, 结构中易降解组分所占比重大, 尤其是类蛋白组分.因此, 本研究中出水的BIX值明显低于进水; 生活污水的BIX值稍低于农业污水.
3 结论(1) 黄浦江流域典型污水的CC及COC值均随胶体粒径的增加而呈递增趋势, 其中污水处理厂出水Mr 300×103~1 μm分级的CC与COC值明显下降, 说明污水处理厂对大颗粒胶体(即Mr>300×103)的去除效果较显著, 这对于控制出水中的有机碳浓度具有重要意义.
(2) 黄浦江典型污水不同粒径分级胶体的EEMs表现为类蛋白荧光峰(峰D和峰T)及类腐殖质荧光峰(峰C和峰A), 其中污水厂进水、出水及天恩桥污水以峰C为主要荧光峰, 大盈水样以峰T为主要荧光峰; 不同荧光峰随胶体粒径的变化呈现不同规律, 类腐殖质荧光峰主要存在于Mr 10×103~300×103分级胶体中, 类蛋白荧光峰主要存在于Mr 1×103~5×103分级胶体中, Mr 300×103~1 μm分级胶体中的荧光峰较少.
(3) 光谱分析结果表明, 小粒径胶体陆源来源可能性更大、芳香性及腐殖化程度更高.
| [1] | Lead J R, Wilkinson K J. Aquatic colloids and nanoparticles: current knowledge and future trends[J]. Environmental Chemistry, 2006, 3(3): 159-171. DOI:10.1071/EN06025 |
| [2] | Guo L D, Santschi P H. Ultrafiltration and its applications to sampling and characterisation of aquatic colloids[A]. In: Wilkinson K J, Lead J R (Eds.). Environmental Colloids and Particles: Behaviour, Separation and Characterisation[M]. Chichester: John Wiley & Sons, 2007. 159-222. |
| [3] | Kalmykova Y, Björklund K, Strömvall A M, et al. Partitioning of polycyclic aromatic hydrocarbons, alkylphenols, bisphenol A and phthalates in landfill leachates and stormwater[J]. Water Research, 2013, 47(3): 1317-1328. DOI:10.1016/j.watres.2012.11.054 |
| [4] | Ngueleu S K, Grathwohl P, Cirpka O A. Effect of natural particles on the transport of lindane in saturated porous media: laboratory experiments and model-based analysis[J]. Journal of Contaminant Hydrology, 2013, 149: 13-26. DOI:10.1016/j.jconhyd.2013.02.009 |
| [5] | Nie M H, Yang Y, Liu M, et al. Environmental estrogens in a drinking water reservoir area in Shanghai: occurrence, colloidal contribution and risk assessment[J]. Science of the Total Environment, 2014, 487: 785-791. DOI:10.1016/j.scitotenv.2013.12.010 |
| [6] | Yan C X, Yang Y, Zhou J L, et al. Selected emerging organic contaminants in the Yangtze Estuary, China: a comprehensive treatment of their association with aquatic colloids[J]. Journal of Hazardous Materials, 2015, 283: 14-23. DOI:10.1016/j.jhazmat.2014.09.011 |
| [7] | Zheng Z, Zhang H, He P J, et al. Co-removal of phthalic acid esters with dissolved organic matter from landfill leachate by coagulation and flocculation process[J]. Chemosphere, 2009, 75(2): 180-186. DOI:10.1016/j.chemosphere.2008.12.011 |
| [8] | Chen G, Lin C, Chen L, et al. Effect of size-fractionation dissolved organic matter on the mobility of prometryne in soil[J]. Chemosphere, 2010, 79(11): 1046-1055. DOI:10.1016/j.chemosphere.2010.03.038 |
| [9] | Kim M K, Won A Y, Zoh K D. Effects of molecular size fraction of DOM on photodegradation of aqueous methylmercury[J]. Chemosphere, 2017, 174: 739-746. DOI:10.1016/j.chemosphere.2017.02.033 |
| [10] | Lapworth D J, Stolpe B, Williams P J, et al. Characterization of suboxic groundwater colloids using a multi-method approach[J]. Environmental Science & Technology, 2013, 47(6): 2554-2561. |
| [11] | Yang Y, Colman B P, Bernhardt E S, et al. Importance of a nanoscience approach in the understanding of major aqueous contamination scenarios: case study from a recent coal ash spill[J]. Environmental Science & Technology, 2015, 49(6): 3375-3382. |
| [12] |
黄文丹, 周立旻, 郑祥民, 等. 长江河口不同分子量溶解有机质的三维荧光光谱特征[J]. 光谱学与光谱分析, 2013, 33(4): 1000-1004. Huang W D, Zhou L M, Zheng X M, et al. Spectroscopic characteristics of different molecular weight dissolved organic matter in water from Yangtze River Estuary[J]. Spectroscopy and Spectral Analysis, 2013, 33(4): 1000-1004. |
| [13] |
付佳露, 杨毅, 彭欢, 等. 长江口水环境中纳米颗粒物初探[J]. 环境科学, 2011, 32(7): 1924-1931. Fu J L, Yang Y, Peng H, et al. Study on nanoparticles in Yangtze estuary[J]. Environmental Science, 2011, 32(7): 1924-1931. |
| [14] |
刘瑞霞, 李斌, 刘娜娜, 等. 辽河流域与英国中部河湖水体中溶解有机质的荧光特性[J]. 环境科学学报, 2014, 34(9): 2321-2328. Liu R X, Li B, Liu N N, et al. Fluorescence characteristics of dissolved organic matter in freshwaters from Liaohe Basin and Midland of UK[J]. Acta Scientiae Circumstantiae, 2014, 34(9): 2321-2328. |
| [15] | Yan C X, Nie M H, Lead J R, et al. Application of a multi-method approach in characterization of natural aquatic colloids from different sources along Huangpu River in Shanghai, China[J]. Science of the Total Environment, 2016, 554-555: 228-236. DOI:10.1016/j.scitotenv.2016.02.198 |
| [16] | Coble P G. Characterization of marine and terrestrial DOM in seawater using excitation-emission matrix spectroscopy[J]. Marine Chemistry, 1996, 51(4): 325-346. DOI:10.1016/0304-4203(95)00062-3 |
| [17] | Huguet A, Vacher L, Saubusse S, et al. New insights into the size distribution of fluorescent dissolved organic matter in estuarine waters[J]. Organic Geochemistry, 2010, 41(6): 595-610. DOI:10.1016/j.orggeochem.2010.02.006 |
| [18] | McKnight D M, Boyer E W, Westerhoff P K, et al. Spectrofluorometric characterization of dissolved organic matter for indication of precursor organic material and aromaticity[J]. Limnology and Oceanography, 2001, 46(1): 38-48. DOI:10.4319/lo.2001.46.1.0038 |
| [19] | Zsolnay A, Baigar E, Jimenez M, et al. Differentiating with fluorescence spectroscopy the sources of dissolved organic matter in soils subjected to drying[J]. Chemosphere, 1999, 38(1): 45-50. DOI:10.1016/S0045-6535(98)00166-0 |
| [20] | Huguet A, Vacher L, Relexans S, et al. Properties of fluorescent dissolved organic matter in the Gironde Estuary[J]. Organic Geochemistry, 2009, 40(6): 706-719. DOI:10.1016/j.orggeochem.2009.03.002 |
| [21] | Wu F C, Tanoue E. Isolation and partial characterization of dissolved copper-complexing ligands in streamwaters[J]. Environmental Science & Technology, 2001, 35(18): 3646-3652. |
| [22] |
傅平青, 刘丛强, 尹祚莹, 等. 腐殖酸三维荧光光谱特性研究[J]. 地球化学, 2004, 33(3): 301-308. Fu P Q, Liu C Q, Yin Z Y, et al. Characterization of humic acid by three-dimensional excitation emission matrix fluorescence spectroscopy[J]. Geochimica, 2004, 33(3): 301-308. |
| [23] |
宋晓娜, 于涛, 张远, 等. 利用三维荧光技术分析太湖水体溶解性有机质的分布特征及来源[J]. 环境科学学报, 2010, 30(11): 2321-2331. Song X N, Yu T, Zhang Y, et al. Distribution characterization and source analysis of dissolved organic matters in Taihu Lake using three dimensional fluorescence excitation-emission matrix[J]. Acta Scientiae Circumstantiae, 2010, 30(11): 2321-2331. |
| [24] | Baker A. Fluorescence excitation-emission matrix characterization of river waters impacted by a tissue mill effluent[J]. Environmental Science & Technology, 2002, 36(7): 1377-1382. |
| [25] |
傅平青, 刘丛强, 吴丰昌. 溶解有机质的三维荧光光谱特征研究[J]. 光谱学与光谱分析, 2005, 25(12): 2024-2028. Fu P Q, Liu C Q, Wu F C. Three-dimensional excitation emission matrix fluorescence spectroscopic characterization of dissolved organic matter[J]. Spectroscopy and Spectral Analysis, 2005, 25(12): 2024-2028. DOI:10.3321/j.issn:1000-0593.2005.12.031 |
| [26] | Fu P Q, Wu F C, Liu C Q, et al. Fluorescence characterization of dissolved organic matter in an urban river and its complexation with Hg(Ⅱ)[J]. Applied Geochemistry, 2007, 22(8): 1668-1679. DOI:10.1016/j.apgeochem.2007.03.041 |
| [27] | Leenheer J A, Croué J P. Peer reviewed: characterizing aquatic dissolved organic matter[J]. Environmental Science & Technology, 2003, 37(1): 18A-26A. |
| [28] | Thurman E M. Organic geochemistry of natural waters[M]. Netherlands: Springer, 1985. |
| [29] | Boehme J, Wells M. Fluorescence variability of marine and terrestrial colloids: examining size fractions of chromophoric dissolved organic matter in the Damariscotta River estuary[J]. Marine Chemistry, 2006, 101(1-2): 95-103. DOI:10.1016/j.marchem.2006.02.001 |
| [30] |
刘娜娜, 李斌, 刘瑞霞, 等. 浑太水系水体中不同粒径有机胶体荧光光谱特性[J]. 环境科学, 2014, 35(11): 4103-4110. Liu N N, Li B, Liu R X, et al. Fluorescence characteristics of fractionated colloidal organic matter in freshwater from Hunhe and Taizihe watersheds[J]. Environmental Science, 2014, 35(11): 4103-4110. |
| [31] | Batchelli S, Muller F L L, Baalousha M, et al. Size fractionation and optical properties of colloids in an organic-rich estuary (Thurso, UK)[J]. Marine Chemistry, 2009, 113(3-4): 227-237. DOI:10.1016/j.marchem.2009.02.006 |
| [32] |
黄廷林, 方开凯, 张春华, 等. 利用UV-vis及EEMs对比冬季完全混合下两个不同特征水库溶解性有机物的光学特性[J]. 环境科学, 2016, 37(12): 4577-4585. Huang T L, Fang K K, Zhang C H, et al. Optical characteristics of dissolved organic matter from two different full mixed reservoirs in winter based on UV-vis and EEMs[J]. Environmental Science, 2016, 37(12): 4577-4585. |
 2017, Vol. 38
2017, Vol. 38