苯并三唑(benzotriazole, BTA)是一种新兴污染物, 其年产量达9 000 t, 主要用作防冻液、机场和路面除冰剂[1], 水处理的防腐剂、缓蚀剂和UV稳定剂[2, 3]等. BTA的大量应用, 使之在土壤、水环境中被广泛检出.研究表明其对微生物、无脊椎动物和脊椎动物具有毒害性[4], 且生物降解性有限.由于BTA的广泛应用和毒害性, 研究它在水土环境中的迁移转化过程具有重要的意义, 而吸附对污染物在水-土界面迁移转化具有重要的影响.
土壤溶解性有机质(dissolved organic matter, DOM)广泛存在于土壤环境中, 虽然其含量很少, 但被认为是土壤有机质中具有活性的物质[5]. DOM对有机污染物的影响既可以表现为促进吸附, 减少有机污染物的移动性[6], 又可以表现为抑制吸附, 增加移动性[7~9], 这与污染物和DOM的性质有着密切关系. DOM是一种高度不均匀的混合物, 它的分子大小、亲疏水性、颜色、性状都会随着环境的变化而发生改变[10~12]. Leenheer[11]率先提出可以把DOM按照亲/疏水性分级, 这种分级方法在研究DOM与污染物的相互作用机制时被证明是有效且可行的[13~16].如Chen等[13]的研究表明疏水酸性组分(HOA)和亲水物质(HIM)均能增加扑草津的移动性, 且HIM效果更显著.腐殖土是森林中表土层树木的枯枝残叶经过长时期腐烂发酵后而形成的, 具有保湿保肥的特点, 目前较多应用于园林、盆栽和改善土壤肥力方面.由于腐殖土的广泛存在及其应用, 其中的DOM可能会进入土壤中而影响污染物的吸附和迁移.
当DOM与BTA共存时, 一方面DOM可能会与BTA在溶液中结合, 或与BTA发生竞争吸附, 减少土壤对BTA的吸附; 另一方面DOM与BTA可以发生共吸附和累积吸附, 增加土壤对BTA的吸附.前人对DOM分级的研究多集中在来源于植物秸秆、堆肥以及污泥等中的DOM[10, 13, 15, 17], 然而, 关于腐殖土中的DOM各组分性质研究及这些性质对BTA在土壤上吸附的影响还鲜有报道.本文的研究目为:① 从天然腐殖土中提取DOM, 对DOM按照不同的亲/疏水性分离出不同的5种组分[即疏水酸性组分(HOA)、疏水中性组分(HON)、亲水酸性组分(HIA)、亲水碱性组分(HIB)、亲水中性组分(HIN)]并进行性质表征和分析; ② 研究BTA和DOM不同组分在土壤上的相互作用, 探究DOM的不同组分对BTA在土壤上吸附的影响.
1 材料与方法 1.1 试剂与仪器吸附实验土壤样品购自中国地质科学院地球物理地球化学勘察研究所, 分别为辽宁棕壤[GBW07412a (ASA-1a)]和黑龙江黑土[GBW07458 (ASA-7)]标准土壤样品, 均采自土壤耕作层, 基本理化性质见表 1.
|
|
表 1 标准土壤样品基本理化性质1) Table 1 Physical and chemical characteristics of standard soil samples |
BTA(CAS:95-14-7) 购自日本TCI公司, 纯度≥98%, 分子式C6H5N3, 其lgKow为1.44, 溶解度(25℃)为5.96 g·L-1(来自EPI), pKa分别为1.6和8.6.
FLASH 2000 CHNS/O元素分析仪(美国Thermo公司), TOC仪(3210, 日本岛津公司), Nicolet 6700傅里叶红外光谱仪(美国Nicolet公司), 877Tirino plus自动电位滴定仪(瑞士Metrohm公司), UV-1800紫外分光光度计(日本岛津公司), TU-1901双光束紫外可见分光光度计(北京普希公司), Mastersizer 3000激光粒度仪(英国马尔文公司), RE-52AA旋转蒸发仪(上海亚荣生公司), XAD-8树脂(美国Sigma公司), Amberlyst 15阳离子交换树脂、Amberlyst 21阴离子交换树脂(上海Aladdin公司), 透析袋(截留相对分子质量100, RC膜, 美国联合碳化公司), BT100-1F蠕动泵(保定兰格公司), 甲醇(HPLC级, Thermo Fisher Scientific公司). NaCl、NaOH、HCl、氨水等药品均购自北京化工厂, 分析纯.超纯水为Milli-Q机制造.
1.2 DOM的提取与分级提取DOM的土壤为沂蒙山天然腐殖土.具体为:选取表层由枯枝烂叶腐熟的土壤, 去除杂质, 过2 mm筛, 与去离子水1:10(质量比, 干重)混合后, 于恒温振荡器中, 在25℃ 175 r·min-1条件下振荡24 h, 混合液在3 000 r·min-1条件下离心30 min, 取上清液过0.45 μm滤膜, 滤液为DOM溶液, 即DOMbulk. DOM样品浓度均用溶解性总有机碳DOC含量表示, 用TOC仪测定, 新鲜提取和分级的DOM溶液稀释至相应浓度进行实验, 样品于4℃冰箱中避光保存.
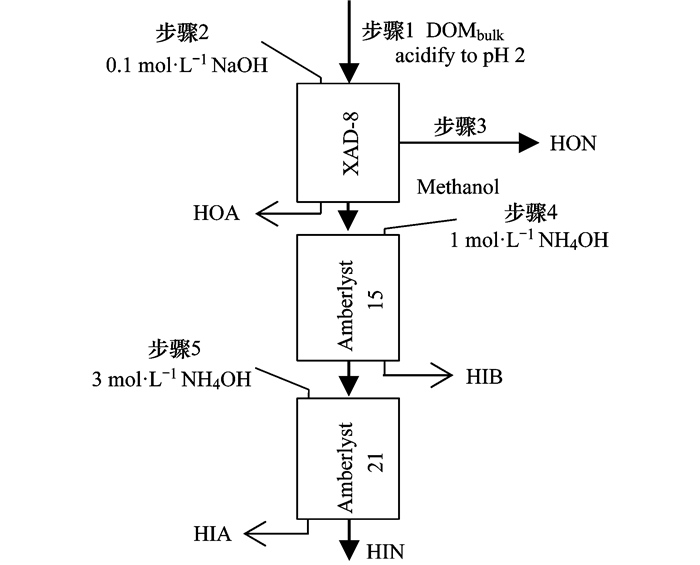
将DOM按照亲/疏水性分级, 主要参照文献[10, 11]的方法.树脂前处理方法见文献[11].分级流程如图 1所示, 首先用6.0 mol·L-1 HCl将DOMbulk溶液的pH值调为2.0, 通过XAD-8树脂柱.疏水组分HOA和HON被吸附在XAD-8树脂上, 用0.1 mol·L-1 NaOH淋洗XAD-8树脂柱得到HOA, 用甲醇索氏提取得到HON, 过量的甲醇用旋转蒸发仪去除.未被XAD-8树脂柱吸附的组分为亲水组分, 依次通过树脂Amberlyst 15和Amberlyst 21, HIB和HIA分别被吸附, 滤出液为HIN.用1 mol·L-1 NH4OH洗脱Amberlyst 15树脂得到HIB.用3 mol·L-1 NH4OH洗脱Amberlyst 21树脂得到HIA.
|
图 1 DOM分级流程示意 Fig. 1 Flow chart of fractionation of DOM |
分级过程中, 树脂柱中的流速均小于10床体积·h-1.得到的DOM组分分别用透析袋去除盐分和杂质来提纯[14, 18].具体为:将DOM置于透析袋内密封后, 浸入去离子水中, 每4 h换一次去离子水, 直到透析袋外溶液的电导率接近去离子水时, 透析完成, 此过程约48 h.此时DOM中的盐分、杂质和相对分子质量<100的DOM组分均被去除.由于DOM相对分子质量较大, <100的DOM组分可忽略不计.分级过程中为防止引入杂质, 树脂柱为带聚四氟乙烯盖的玻璃层析柱, 导管材质为玻璃或聚四氟乙烯, 蠕动泵软管为硅橡胶管.
1.3 吸附实验土壤对BTA的等温吸附实验:称取0.5 g土样于10 mL棕色玻璃瓶中, 加入10 mL含有系列浓度BTA溶液(0~90 mg·L-1)和DOM不同组分溶液(0或40 mg·L-1), 背景溶液为0.01 mol·L-1的NaCl, 为了控制变量, 减少溶液pH变化对吸附的影响, 将溶液初始pH用HCl和NaOH均调为6.0±0.1, 用含聚四氟乙烯垫的铝盖压盖密封, 于25℃, 175 r·min-1条件下水平振荡168 h(动力学数据表明168 h已达到吸附平衡), 在3 000 r·min-1条件下离心15 min, 取上清液供HPLC分析. BTA储备液均用超纯水溶解, 在4℃冰箱中避光冷藏.土壤对BTA的吸附量qe由不加土壤的控制样浓度和反应平衡后液相浓度的差值计算得到(未加入微生物抑制剂, 控制样损失量<1%), 各实验均设置了平行样.
土壤对DOM的等温吸附实验:称取0.5 g土样于10 mL棕色玻璃瓶中, 加入10 mL含有系列浓度的DOM溶液(0~90 mg·L-1)和BTA溶液(0或60 mg·L-1), 其它实验方法同土壤对BTA的等温吸附实验.以不添加DOM样品为对照组, 土壤对DOM的吸附量由不加土壤的控制样与反应后的DOM浓度的差值计算得到.其中已扣除对照实验中土壤溶出的及BTA所贡献的DOM.
透析实验:溶液中DOM对BTA的吸附系数由透析实验得到.透析袋(预实验表明BTA可穿过该透析袋)用蒸馏水煮沸10 min, 然后依次用乙醇和蒸馏水清洗待用. DOM组分大小均>100(在用透析袋去除盐分提纯时, 也同时去除了<100的组分), 不同组分DOM分别用超纯水稀释到40 mg·L-1, 背景溶液为0.01 mol·L-1 NaCl, 取10 mL于透析袋中, 用绳子系紧透析袋两端, 置于40 mL棕色玻璃瓶中, 向玻璃瓶中加入20 mL浓度为60 mg·L-1的BTA溶液, 背景溶液为0.01 mol·L-1 NaCl, 用含聚四氟乙烯内垫的盖子拧紧, 在25℃ 175 r·min-1条件下水平振荡48 h(预实验表明48 h可达到透析平衡, 透析袋吸附的BTA<1%).透析袋内是BTA自由态与BTA-DOM结合态之和, 透析袋外是BTA自由态, 两者之差为BTA-DOM结合态, 吸附系数KDOC是BTA的结合态与自由态的比值.
1.4 DOM的表征冷冻干燥后的DOM粉末用元素分析仪测定C、H、N、O元素含量, 用傅里叶红外光谱仪扫描波长400~4 000 cm-1.样品总酸度用自动电位滴定仪测定[19], 由消耗的电荷密度即消耗NaOH的量计算得到. E4/E6值的测定[20], 用紫外分光光度计分别测定DOM不同组分分别在465 nm和665 nm处的吸光度, 取3次紫外分光光度计读数的平均值的比值为E4/E6值.
1.5 BTA的测定方法BTA的测定采用高效液相色谱仪(日本, 岛津, HPLC LC-20AT), 配有InertSustainSwift C18(25 cm×4.6 mm, 5 μm)色谱柱, 流动相为甲醇和水(体积比40:60, 流速0.7 mL·min-1), 柱温30℃, 检测波长254 nm, 进样体积10 μL, 出峰时间12 min, 检出限0.8 μg·L-1. BTA的标线采用外标的方法, R2达到0.999以上.
1.6 数据分析通常可以用Langmuir模型和Freundlich模型描述土壤的吸附特征[3].由于实验中BTA浓度属于较低范围, 用Langmuir模型拟合等温吸附数据误差较大, 拟合效果不好, 因此本文采用Freundlich模型拟合土壤对BTA的等温吸附数据见公式(1).
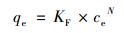
|
(1) |
式中, qe和ce分别为固相吸附量(mg·kg-1)和液相平衡浓度(mg·L-1), KF为Freundlich模型的吸附系数[(mg·kg-1)·(mg·L-1)-N], N值表示非线性程度.
分配系数Kd由公式(2) 计算得到.
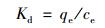
|
(2) |
有机碳标化分配系数Koc由公式(3) 计算得到.
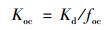
|
(3) |
式中, foc为土壤有机碳含量.
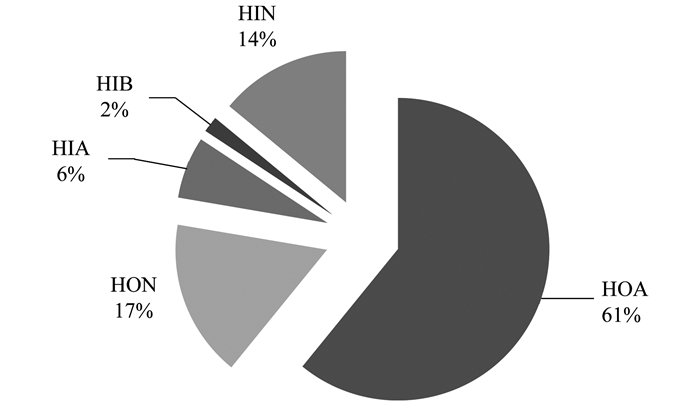
2 结果与讨论 2.1 DOM样品的分级及表征从腐殖土中提取的DOM(未分级的记为DOMbulk), 疏水组分(HOA和HON)占主要部分, 达78%(以C计, 图 2), 亲水组分(HIA、HIB和HIN)占23%.疏水组分所占的比例比以往报道的从废水、秸秆[11, 13]中提取的高, 与从堆肥、厌氧污泥以及再生水中[14, 16, 21, 22]提取的比例相似.各组分中, HOA的含量最高, 占DOMbulk的61%. HIB含量最低, 低于一些文献中报道的数值(10%~16%)[10, 15, 22], 但是也有文献报道某湖水中HIB为3%[23], 甚至Engel等[14]研究的某河流中HIB为0%.总的来说, DOM各组分所占的比例会因来源、腐熟时间等条件的不同发生很大变化[10, 14, 21].
|
图 2 DOM各组分所占比例 Fig. 2 Proportions of isolated DOM fractions |
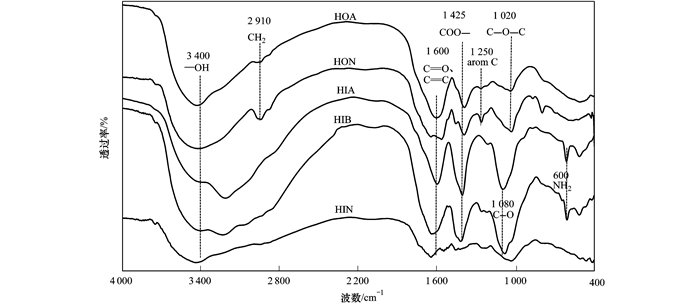
傅里叶红外光谱(图 3)表明, DOM不同组分在3 400 cm-1处均有明显—OH的吸收带[11, 24], 说明DOM各组分均含有较多的羟基.疏水组分HON和HOA在2 910 cm-1和1 440 cm-1处有较明显的吸收带, 表明HON和HOA中含有更多脂肪烷烃类物质[11, 21].疏水组分HOA和HON在1 250 cm-1附近出现吸收带, 显示其含有芳香性碳[10]. DOM各组分在1 600 cm-1和1 425 cm-1均有的羧酸吸收带[10, 11], 但HIA的吸收带较其它组分强烈, 说明HIA含有更多的羧酸类物质. HIA和HIB在600 cm-1附近出现吸收带, 可能是含有酰胺类物质[21].亲水组分(HIA、HIB、HIN)从2 800~3 500 cm-1具有很强的O—H拉伸吸收带, 从1 050~1 200 cm-1具有C—O拉伸带[11], 在1 080 cm-1处有明显的吸收峰, 表明含有较多水溶性多糖类物质[10, 24].
|
图 3 DOM各组分红外光谱 Fig. 3 FTIR spectra of isolated DOM fractions |
DOM不同组分的原子比是不同元素所占质量分数除以各自相对分子质量的比值(表 2). DOM不同组分具有较高的H/C值, 说明它们均具有高的脂肪族特征[15].疏水组分HOA和HON的[(O+N)/C]值较低, 说明二者具有较低极性.这进一步证明本实验中DOM分级的可靠性. HIB、HIA总酸度最高, HIB中含有最多的羟基, 其总酸度主要由羟基提供, HIA中含有最多的羧基, 中性组分(HIN、HON)的总酸度最低. HIB具有最高的N含量以及较低的C/N比, 说明它可能含有更多的肽键.一般认为HIB类似于氨基酸、蛋白质[11, 15]. E4/E6的大小可以反映DOM组成中分子芳香环的缩合度、芳化度和分子量的大小.疏水组分HOA、HON的E4/E6值远大于亲水组分(HIA、HIB、HIN), 说明疏水组分分子量较大、分子结构较复杂、芳香化程度也较高.
|
|
表 2 DOM各组分的化学表征 Table 2 Chemical characterization of isolated DOM fractions |
2.2 DOM对土壤等温吸附BTA的影响
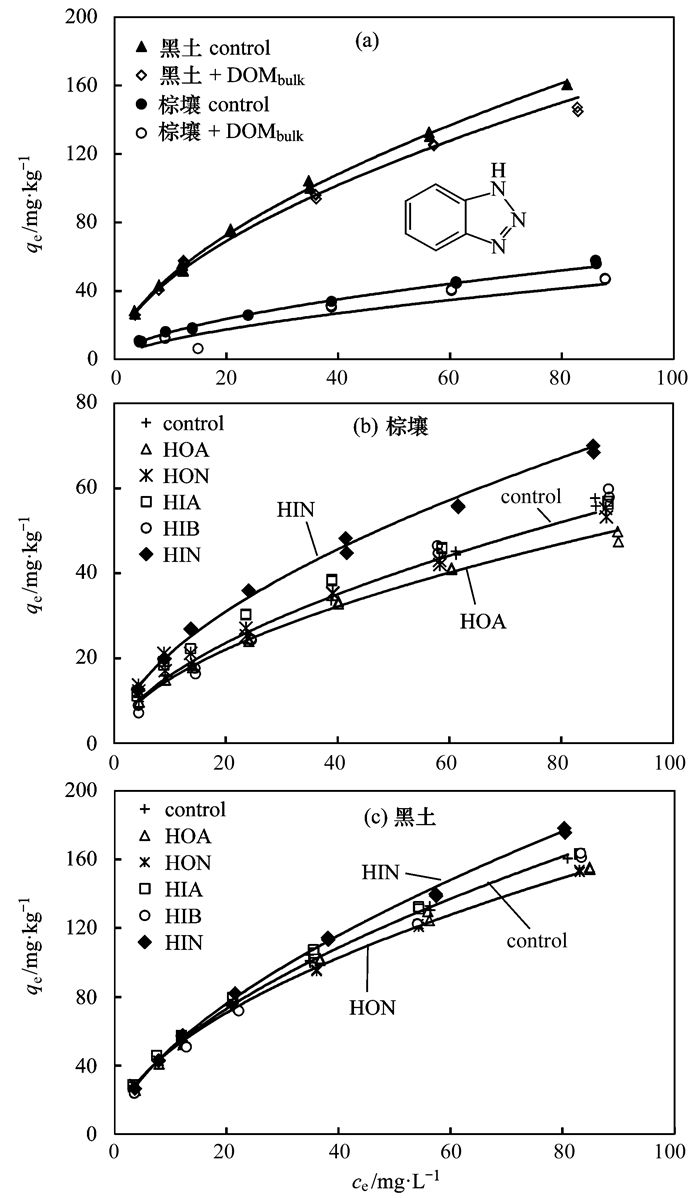
等温吸附实验初始pH为6.0±0.1, 反应平衡后溶液均缓冲到土壤pH值附近(黑土6.14, 棕壤6.80).用Freundlich模型拟合了土壤对BTA的等温吸附数据(图 4和表 3).通过数据差异显著性分析, P值均<0.01, 为非常显著.拟合得到的R2除了棕壤DOMbulk(0.882) 和棕壤HON(0.973) 以外, 其余均在0.995以上, 拟合效果较好.
|
添加DOM 40 mg·L-1, control组未添加DOM 图 4 DOM不同组分对两种土壤等温吸附BTA的影响 Fig. 4 Effects of isolated DOM fractions on BTA sorption in two soils |
|
|
表 3 DOM不同组分存在时两种土壤对BTA吸附的Freundlich模型拟合参数1) Table 3 Fitted parameters of Freundlich model for BTA sorption in two soils with isolated DOM fractions |
对于没有添加DOM的控制组, 因为黑土有机碳(OC)含量是棕壤的1.58倍, 黑土对BTA的吸附能力远大于棕壤.在BTA平衡浓度约为4 mg·L-1时, 黑土的lg Koc为2.47, 棕壤的lg Koc为2.16[Koc由公式(3) 计算得到]. lg Koc的差异说明除了有机质疏水分配作用以外还存在其他作用. Ca2+会促进BTA与土壤的表面络合作用[25], 黑土中的有效Ca2+含量大于棕壤, 导致黑土lg Koc>棕壤lg Koc.
当溶液中添加DOMbulk时, 棕壤和黑土对BTA的吸附均受到了抑制[图 4(a)].其原因是DOMbulk中抑制吸附的疏水组分HOA与HON占78%(图 2); 亲水组分HIN对土壤吸附BTA具有促进作用, 且HIN促进作用最显著, 但对吸附起促进作用的HIN只占14%;DOMbulk的性质是不同组分的综合, 与主要成分疏水组分相似, 因此DOMbulk总体上抑制了棕壤和黑土对BTA的吸附.
DOMbulk存在时, BTA在土壤上的吸附系数实验值为Kd(DOM), 由公式(2) 计算得到, 计算值Kd(DOM)′由DOM各组分存在时, BTA在土壤上的吸附系数即公式(4) 计算得到.公式(4) 假设DOM各组分是独立的, 相互之间没有影响.
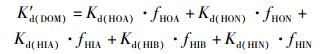
|
(4) |
式中, Kd(HOA)、Kd(HON)、Kd(HIA)、Kd(HIB)、Kd(HIN)分别是HOA、HON、HIA、HIB、HIN组分存在, BTA平衡浓度约为4 mg·L-1和85 mg·L-1时, BTA在土壤上分配系数的实验值; fHOA、fHON、fHIA、fHIB、fHIN分别为HOA、HON、HIA、HIB、HIN在DOMbulk中所占的比例.
当BTA平衡浓度为4 mg·L-1和85 mg·L-1时, 在黑土中, Kd(DOM)′分别为7.20 L·kg-1和1.89 L·kg-1, Kd(DOM)分别为6.96 L·kg-1和1.76 L·kg-1; 在棕壤中, Kd(DOM)′分别为2.39 L·kg-1和0.60 L·kg-1, Kd(DOM)分别为2.09 L·kg-1和0.53 L·kg-1.在相同条件下, 计算值Kd(DOM)′近似于实验值Kd(DOM), 说明在本研究中, DOM不同组分是相互独立的, 可以用DOM不同组分对BTA吸附的影响来预测DOMbulk对BTA的影响, 这与Engel等[14]的研究结果是一致的.
2.3 机制分析前人研究表明, DOM对土壤吸附有机污染物的抑制作用主要通过DOM与污染物在溶液中的结合, 形成络合物[26~28]; DOM与污染物竞争土壤吸附点位[8, 9, 27, 29]; DOM可以减小溶液表面张力, 增加有机污染物的溶解性[13, 30]. DOM对土壤吸附有机污染物的促进作用主要通过共吸附和累积吸附, 增加土壤吸附点位[6, 31].以上因素如何在土壤-DOM-BTA体系中起作用的, 在前人的研究中还未阐明.
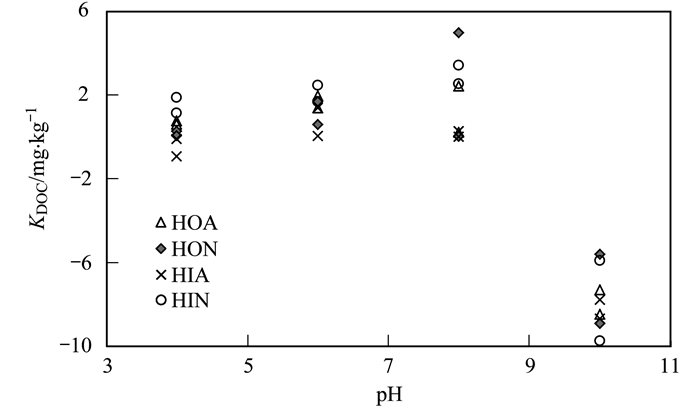
透析实验评估了平衡溶液中DOM组分与BTA的结合系数KDOC.在pH<8.0时, DOM组分与BTA的结合系数KDOC均<6 mg·kg-1(图 5).在pH=10.0时, BTA与DOM均带负电, 具有强的排斥作用, 透析袋内浓度均小于透析袋外浓度(KDOC<-10 mg·kg-1).因为实验条件下DOM组分浓度较低, 且水分子占据吸附点位, 所以DOM不同组分与BTA在溶液中的结合作用较弱. Haham等[18]通过透析实验和红外分析表明, 未发现DOM与磺胺吡啶在溶液中直接的相互作用, 而更多的支持DOM与磺胺吡啶的竞争吸附, 与本研究结果类似.
|
图 5 溶液pH对DOM不同组分吸附BTA的影响 Fig. 5 Effects of solution pH on BTA sorption to isolated DOM fractions |
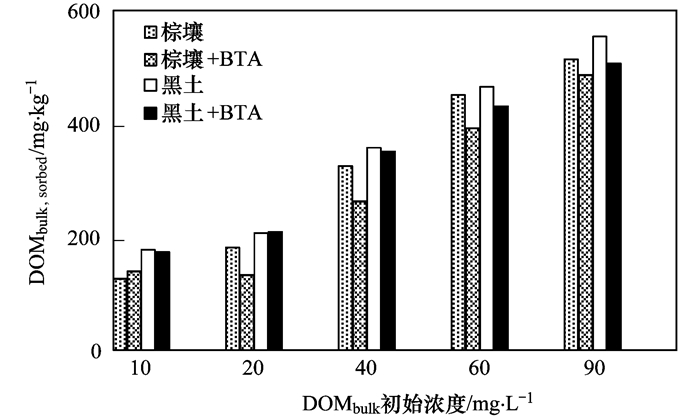
在没有添加外源DOM时, 土壤中均会溶出DOM, 棕壤溶出的DOM为6.0 mg·kg-1, 黑土溶出的DOM较多, 为12.1 mg·L-1, 这是因为黑土的OC含量较高.通常, 随着土壤黏粒和粉砂含量的增加, 土壤固相有机质(SOM)中的腐殖酸(HAs)含N量下降、C/N升高[32], 使得土壤中SOM的芳香度和疏水性随之升高.相比于黑土, 棕壤含有较多黏粒和粉砂, 因此其所含SOM的芳香度和疏水性可能较高, 而黑土中SOM相对更加亲水, 从而黑土中会溶出更多的DOM.随着DOMbulk浓度的升高, 土壤对DOMbulk的吸附量增加(图 6).加入BTA时, 两种土壤对DOMbulk的吸附量均有减少, 说明DOMbulk与BTA之间存在竞争吸附.
|
添加BTA 60 mg·L-1, DOM 10~90mg·L-1 图 6 BTA对两种土壤吸附DOMbulk的影响 Fig. 6 Role of BTA in sorption of isolated DOM fractions to two soils |
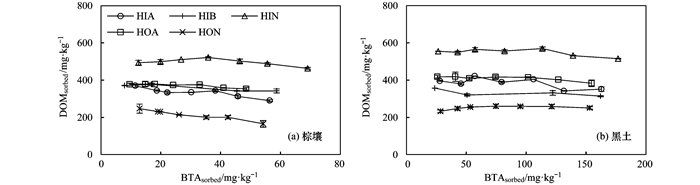
在DOM组分影响BTA的等温吸附实验中, 从土壤吸附BTA和DOM的关系中(图 7), 两种土壤对HIN吸附最强, 其次是HOA, 对HON吸附最弱.一般来说, 土壤对疏水组分的吸附量大于亲水组分[33, 34], 但也与土壤内源DOM含量和性质有关.有研究表明, 内源有机质对土壤吸附外源疏水性DOM有较强的抑制作用[21].黑土OC含量是棕壤的1.58倍(表 1), 但黑土对DOM组分的吸附量只是略大于棕壤(图 6和图 7), 而且吸附在棕壤中DOM组分的标化分配系数Koc是黑土的0.98~1.68倍, 这说明在不考虑有机碳的情况下, 存在其它作用促进棕壤对DOM组分的吸附.从土壤质地来看, 棕壤中黏粒和粉砂含量大于黑土(表 1).有研究表明, DOM中的羧基可以和多种矿物相互作用, 脂肪族的羧基可以插入到黏土层中形成络合物[35], 棕壤中含有更多的黏粒和粉砂, 有利于其对DOM的吸附.
|
添加DOM 40 mg·L-1, BTA 5~90mg·L-1 图 7 BTA和DOM不同组分在棕壤与黑土上吸附的相关性 Fig. 7 Relationship between sorption of BTA and that of isolated DOM fractions to two soils |
HIN含有较少的羟基和羧基, 主要包含多糖类化合物[11, 15], HOA可以看成是低分子量的富里酸[11], 土壤对HIN吸附量最大, 其次是HOA.虽然HIN为亲水组分, HOA为疏水组分, 但从极性指标[(O+N)/C]来看, 二者极性几乎一样, 而HIN的羧酸含量比HOA少很多(表 2).在实验条件下, pH为6~7, HOA表面羧基发生解离, 带负电[14], 与土壤的静电排斥作用影响了土壤对其吸附.一般来说, HIN分子量比HOA小, HOA分子结构较复杂, 分子量较大.棕壤和黑土中均含有一定量的细颗粒(黏粒和粉砂), BTA可以通过颗粒内扩散方式吸附到细颗粒的细小孔隙中[3], 大分子的HOA可以通过吸附到介孔中对孔道造成堵塞[36], 减少了BTA的微孔填充作用.另外, BTA可通过氢键和“π—π”作用吸附到土壤上[3, 37], 而DOM也可通过氢键和“π—π”作用吸附到土壤上, DOM与BTA会竞争土壤上的吸附点位. HIN在土壤上吸附量最大, HIN的吸附增加了土壤中OC含量, 从而增加了土壤中吸附BTA的点位, HIN增加点位的促进吸附大于其与BTA的竞争吸附, 最终表现为促进BTA吸附.
HON主要包含烃类和羰基类化合物[11], 与DOMbulk中其它组分相比, 含有较少的羧基和羟基, 具有最高的含碳量和较高的芳香度. HON在土壤上的吸附量最小(图 7).原因可能是HON使更多的SOM从土壤基质中释放形成DOM[27], 减少了吸附点位, 从而减少了土壤对BTA的吸附.谢黎等[38]研究了3种低分子量有机酸对紫色土吸附菲的影响, 他们认为有机质能够与土壤黏土矿物相互作用, 使SOM释放出来, 形成DOM.吴东明等[21]研究表明内源有机质对疏水性DOM抑制作用更强, 与本研究结果类似. HON与HIN相比, HON分子量较大, 粘度较大, 更容易形成胶体, 活度系数比亲水组分小, 所以土壤对HON吸附量最小. HON对BTA的竞争吸附作用大于产生新点位的促进吸附作用, 所以抑制了土壤对BTA的吸附, 增加了BTA的移动性.
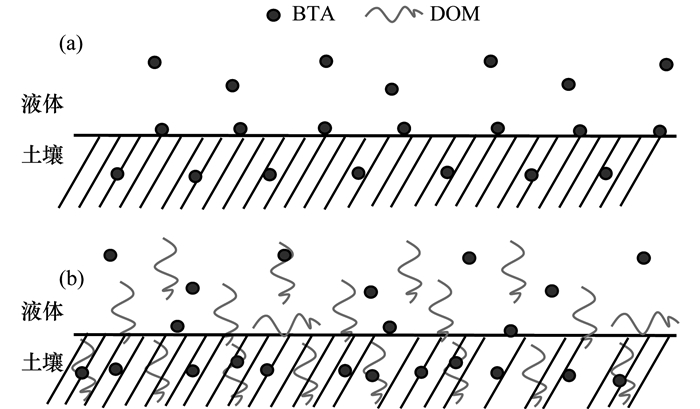
综上所述, DOM可通过分配作用和表面作用吸附到土壤上(图 8), 通过表面作用吸附到土壤上会占据吸附点位和BTA发生竞争吸附.而DOM通过分配作用吸附到土壤上可以增加土壤OC含量, 增加土壤中吸附BTA的点位. HIN增加点位的促进吸附大于HIN与BTA的竞争吸附, 最终表现为促进吸附.土壤SOM对疏水性HON的抑制或者HON使土壤SOM的溶出导致土壤对HON的吸附量最小, 竞争吸附抑制了土壤对BTA的吸附.
|
图 8 DOM对土壤吸附BTA的影响示意 Fig. 8 Scheme of DOM effect on BTA sorption to soil |
由于黑土OC含量高于棕壤, 黑土对BTA和DOM组分的吸附能力均大于棕壤.相对于黑土, 棕壤吸附DOM的标化分配系数Koc较高, 其原因是棕壤中含有较多的对吸附DOM起重要作用的黏粒和粉砂. HIN和HOA极性相似, HOA中羧基会解离, 带负电, 与土壤的排斥作用使土壤对HOA的吸附弱于HIN.因为HON使土壤SOM溶出, 或SOM抑制土壤对外源疏水性DOM的吸附, 所以土壤对HON的吸附最弱.由于水分子占据DOM结合点位, DOM不同组分与BTA在溶液中结合作用较弱. DOMbulk中HIN在土壤上的吸附最强.土壤对HIN的吸附增加了土壤中吸附BTA的点位, 增加点位的促进吸附大于HIN与BTA的竞争吸附, 最终表现为促进吸附. DOMbulk中疏水组分在土壤上的吸附较弱, 产生的新吸附点位较少, 主要通过竞争作用抑制土壤对BTA的吸附. DOMbulk含有78%的疏水组分, 对BTA吸附的影响与疏水组分相似.
| [1] | Giger W, Schaffner C, Kohler H P E. Benzotriazole and tolyltriazole as aquatic contaminants. 1. Input and occurrence in rivers and lakes[J]. Environmental Science & Technology, 2006, 40(23): 7186–7192. |
| [2] | Kim J W, Ramaswamy B R, Chang K H, et al. Multiresidue analytical method for the determination of antimicrobials, preservatives, benzotriazole UV stabilizers, flame retardants and plasticizers in fish using ultra high performance liquid chromatography coupled with tandem mass spectrometry[J]. Journal of Chromatography A, 2011, 1218(22): 3511–3520. DOI: 10.1016/j.chroma.2011.04.006 |
| [3] | Hart D S, Davis L C, Erickson L E, et al. Sorption and partitioning parameters of benzotriazole compounds[J]. Microchemical Journal, 2004, 77(1): 9–17. DOI: 10.1016/j.microc.2003.08.005 |
| [4] | Reemtsma T, Miehe U, Duennbier U, et al. Polar pollutants in municipal wastewater and the water cycle:occurrence and removal of benzotriazoles[J]. Water Research, 2010, 44(2): 596–604. DOI: 10.1016/j.watres.2009.07.016 |
| [5] | 吴文铸, 占新华, 周立祥. 水溶性有机物对土壤吸附-解吸菲的影响[J]. 环境科学, 2007, 28(2): 267–271. Wu W Z, Zhan X H, Zhou L X. Effect of dissolved organic matter on phenanthrene sorption-desorption in soil system[J]. Environmental Science, 2007, 28(2): 267–271. |
| [6] | González-Pradas E, Fernández-Pérez M, Flores-Céspedes F, et al. Effects of dissolved organic carbon on sorption of 3, 4-dichloroaniline and 4-bromoaniline in a calcareous soil[J]. Chemosphere, 2005, 59(5): 721–728. DOI: 10.1016/j.chemosphere.2004.10.050 |
| [7] | Müller K, Magesan G N, Bolan N S. A critical review of the influence of effluent irrigation on the fate of pesticides in soil[J]. Agriculture, Ecosystems and Environment, 2007, 120(2-4): 93–116. DOI: 10.1016/j.agee.2006.08.016 |
| [8] | An C J, Huang G H, Yu H, et al. Effect of short-chain organic acids and pH on the behaviors of pyrene in soil-water system[J]. Chemosphere, 2010, 81(11): 1423–1429. DOI: 10.1016/j.chemosphere.2010.09.012 |
| [9] | Jiang L, Huang J, Liang L, et al. Mobility of prometryne in soil as affected by dissolved organic matter[J]. Journal of Agricultural and Food Chemistry, 2008, 56(24): 11933–11940. DOI: 10.1021/jf8023134 |
| [10] | Chefetz B, Hader Y, Chen Y. Dissolved organic carbon fractions formed during composting of municipal solid waste:properties and significance[J]. Acta Hydrochimica et Hydrobiologica, 1998, 26(3): 172–179. DOI: 10.1002/(ISSN)1521-401X |
| [11] | Leenheer J A. Comprehensive approach to preparative isolation and fractionation of dissolved organic carbon from natural waters and wastewaters[J]. Environmental Science & Technology, 1981, 15(5): 578–587. |
| [12] | Her N, Amy G, McKnight D, et al. Characterization of DOM as a function of MW by fluorescence EEM and HPLC-SEC using UVA, DOC, and fluorescence detection[J]. Water Research, 2003, 37(17): 4295–4303. DOI: 10.1016/S0043-1354(03)00317-8 |
| [13] | Chen G, Lin C, Chen L, et al. Effect of polar-dissolved organic matter fractions on the mobility of prometryne in soil[J]. Journal of Soils and Sediments, 2011, 11(3): 395–405. DOI: 10.1007/s11368-010-0316-1 |
| [14] | Engel M, Chefetz B. Adsorptive fractionation of dissolved organic matter (DOM) by carbon nanotubes[J]. Environmental Pollution, 2015, 197: 287–294. DOI: 10.1016/j.envpol.2014.11.020 |
| [15] | Maoz A, Chefetz B. Sorption of the pharmaceuticals carbamazepine and naproxen to dissolved organic matter:role of structural fractions[J]. Water Research, 2010, 44(3): 981–989. DOI: 10.1016/j.watres.2009.10.019 |
| [16] | Polubesova T, Sherman-Nakache M, Chefetz B. Binding of pyrene to hydrophobic fractions of dissolved organic matter:effect of polyvalent metal complexation[J]. Environmental Science & Technology, 2007, 41(15): 5389–5394. |
| [17] | Chen G, Lin C, Chen L, et al. Effect of size-fractionation dissolved organic matter on the mobility of prometryne in soil[J]. Chemosphere, 2010, 79(11): 1046–1055. DOI: 10.1016/j.chemosphere.2010.03.038 |
| [18] | Haham H, Oren A, Chefetz B. Insight into the role of dissolved organic matter in sorption of sulfapyridine by semiarid soils[J]. Environmental Science & Technology, 2012, 46(21): 11870–11877. |
| [19] | 吴济舟. 溶解性有机质分组及各组分对芘的生物有效性及其吸附解吸的影响研究[D]. 天津: 南开大学, 2012. 30-36. Wu J Z. Fractionation of dissolved organic matter and the impact of the fractions on the bioavailability and sorption-desorption of pyrene[D]. Tianjin:Nankai University, 2012. 30-36. |
| [20] | 刘新超, 李俊, 谢丽, 等. 腐殖酸表征方法研究进展[J]. 净水技术, 2009, 28(3): 6–9, 22. Liu C X, Li J, Xie L, et al. Characterization methods of humic acid:a review[J]. Water Purification Technology, 2009, 28(3): 6–9, 22. |
| [21] | 吴东明, 李勤奋, 武春媛. 铁铝土对溶解性有机质的吸附特性[J]. 环境化学, 2016, 35(4): 639–650. Wu D M, Li Q F, Wu C Y. Adsorption of dissolved organic matter on ferrallitic soils[J]. Environmental Chemistry, 2016, 35(4): 639–650. DOI: 10.7524/j.issn.0254-6108.2016.04.2015112205 |
| [22] | Zhang H, Qu J H, Liu H J, et al. Characterization of isolated fractions of dissolved organic matter from sewage treatment plant and the related disinfection by-products formation potential[J]. Journal of Hazardous Materials, 2009, 164(2-3): 1433–1438. DOI: 10.1016/j.jhazmat.2008.09.057 |
| [23] | Wang L Y, Wu F C, Zhang R Y, et al. Characterization of dissolved organic matter fractions from Lake Hongfeng, Southwestern China Plateau[J]. Journal of Environmental Sciences, 2009, 21(5): 581–588. DOI: 10.1016/S1001-0742(08)62311-6 |
| [24] | 倪文海, 刘欢, 刘振涛, 等. 水稻秸杆腐解过程溶解性有机质红外光谱研究[J]. 土壤, 2013, 45(2): 220–226. Ni W H, Liu H, Liu Z T, et al. Study on Fourier-transform infrared spectra of dissolved organic matters extracted from rice straw at different decay stages[J]. Soils, 2013, 45(2): 220–226. |
| [25] | Bi E P, Schmidt T C, Haderlein S B. Sorption of heterocyclic organic compounds to reference soils:column studies for process identification[J]. Environmental Science & Technology, 2006, 40(19): 5962–5970. |
| [26] | 高鹏, 张照韩, 孙清芳, 等. 溶解性有机质对甲草胺在土壤中吸附行为影响[J]. 哈尔滨工业大学学报, 2012, 44(2): 66–69. Gao P, Zhang Z H, Sun Q F, et al. Effect of dissolved organic matter on sorption behavior of alachlor in soil[J]. Journal of Harbin Institute of Technology, 2012, 44(2): 66–69. DOI: 10.11918/j.issn.0367-6234.2012.02.014 |
| [27] | Ding Q, Wu H L, Xu Y, et al. Impact of low molecular weight organic acids and dissolved organic matter on sorption and mobility of isoproturon in two soils[J]. Journal of Hazardous Materials, 2011, 190(1-3): 823–832. DOI: 10.1016/j.jhazmat.2011.04.003 |
| [28] | 张丰松, 李艳霞, 黄泽春, 等. 雌二醇在土壤/沉积物中的吸附特征及猪粪DOM对吸附的影响[J]. 环境科学, 2012, 33(10): 3542–3546. Zhang F S, Li Y X, Huang Z C, et al. Sorption of 17β-estradiol to soils and sediment and influence of pig manure DOM[J]. Environmental Science, 2012, 33(10): 3542–3546. |
| [29] | Cells R, Barriuso E, Houot S. Effect of liquid sewage sludge addition on atrazine sorption and desorption by soil[J]. Chemosphere, 1998, 37(6): 1091–1107. DOI: 10.1016/S0045-6535(98)00108-8 |
| [30] | 唐东民, 伍钧, 陈华林, 等. 溶解性有机质对芘在土壤中吸附解吸的影响[J]. 环境科学学报, 2010, 30(4): 814–819. Tang D M, Wu J, Chen H L, et al. Effect of dissolved organic matter on the sorption and desorption behavior of pyrene in soil[J]. Acta Scientiae Circumstantiae, 2010, 30(4): 814–819. |
| [31] | Johnson A C, Worrall F, White C, et al. The potential of incorporated organic matter to reduce pesticide leaching[J]. Toxicological & Environmental Chemistry, 1997, 58(1-4): 47–61. |
| [32] | Galantini J A, Senesi N, Brunetti G, et al. Influence of texture on organic matter distribution and quality and nitrogen and sulphur status in semiarid Pampean grassland soils of Argentina[J]. Geoderma, 2004, 123(1-2): 143–152. DOI: 10.1016/j.geoderma.2004.02.008 |
| [33] | Oren A, Chefetz B. Sorptive and desorptive fractionation of dissolved organic matter by mineral soil matrices[J]. Journal of Environmental Quality, 2012, 41(2): 526–533. DOI: 10.2134/jeq2011.0362 |
| [34] | Jones K D, Tiller C L. Effect of solution chemistry on the extent of binding of phenanthrene by a soil humic acid:a comparison of dissolved and clay bound humic[J]. Environmental Science & Technology, 1999, 33(4): 580–587. |
| [35] | Jagadamma S, Mayes M A, Zinn Y L, et al. Sorption of organic carbon compounds to the fine fraction of surface and subsurface soils[J]. Geoderma, 2014, 213: 79–86. DOI: 10.1016/j.geoderma.2013.07.030 |
| [36] | 程和发, 胡二丹, 韦昌富. 矿物微孔对有机污染物吸附的机理和影响因素[J]. 矿物岩石地球化学通报, 2015, 34(2): 250–256. Cheng H F, Hu E D, Wei C F. Sorption of organic contaminants in mineral micropores:mechanism and major controlling factors[J]. Bulletin of Mineralogy, Petrology and Geochemistry, 2015, 34(2): 250–256. |
| [37] | Xu B B, Wu F C, Zhao X L, et al. Benzotriazole removal from water by Zn-Al-O binary metal oxide adsorbent:behavior, kinetics and mechanism[J]. Journal of Hazardous Materials, 2010, 184(1-3): 147–155. DOI: 10.1016/j.jhazmat.2010.08.017 |
| [38] | 谢黎, 陈本寿, 张进忠, 等. 3种低分子量有机酸对紫色土吸附菲的影响[J]. 环境科学, 2016, 37(3): 1032–1038. Xie L, Chen B S, Zhang J Z, et al. Influence of three low-molecular-weight organic acids on the adsorption of phenanthrene in purple soil[J]. Environmental Science, 2016, 37(3): 1032–1038. |
 2017, Vol. 38
2017, Vol. 38


