2. 清华大学环境学院, 环境模拟与污染控制国家重点联合实验室, 国家环境保护环境微生物利用与安全控制重点实验室, 北京 100084;
3. 北京市自来水集团有限责任公司, 北京 100031
2. State Key Joint Laboratory of Environmental Simulation and Pollution Control, State Environmental Protection Key Laboratory of Microorganism Application and Risk Control(MARC), School of Environment, Tsinghua University, Beijing 100084, China;
3. Beijing Waterworks Group Limited Company, Beijing 100031, China
全球淡水资源短缺已成为影响社会经济发展的瓶颈, 为缓解水资源危机, 海水已成为重要的替代水源之一[1].目前, 常用的海水淡化方法主要有蒸馏法、膜法和电渗析[2].其中, 蒸馏法是最为传统和成熟的海水淡化技术, 主要包括低温多效蒸馏(LT-MED)、多级闪蒸(MSF)和压气蒸馏(MVC). LT-MED技术具有净化率高, 对水温不敏感等优点[3], 是主要的海水淡化方法之一, 其工艺是将多台蒸发器串联起来, 后一效的蒸发温度均低于前一效(一级称为一效), 从而可将蒸汽重复利用, 最后得到蒸馏水, 即高质量的产品水.为了确保LT-MED海水淡化装置的正常运行, 一般以混凝、沉淀和过滤作为预处理, 并投加多种药剂(如消毒剂、混凝剂、絮凝剂和阻垢剂等)以改善进水水质, 避免系统受到微生物、化学或物理损伤.氯消毒目前是最常用的预处理消毒剂, 但是氯消毒剂的使用会导致有毒有害的消毒副产物(DBPs)的生成[4~7], 而DBPs的生成浓度及其种类则会受到海水中Br-浓度的影响.
海水中溴离子浓度较高(一般高于45 mg·L-1)[8, 9], 溴离子会在氯化消毒过程中生成次溴酸, 次溴酸的取代活性强于次氯酸, 能与有机物反应生成比氯代消毒副产物具有更高毒性的溴代消毒副产物(Br-DBPs)[10~12].而且, 海水中的有机物主要来源于腐殖质、微生物分泌物、溶解的动物组织和动物的废弃物等, 其种类和含量同样会影响DBPs的生成[13].
本研究在分析海水水质特征的基础上, 研究分析了海水淡化LT-MED工艺三卤甲烷(THMs)、卤乙酸(HAAs)和卤代酚(HPs)的沿程变化规律, 以期为优化海水淡化系统化学药剂的使用和制订浓盐水的处置策略提供数据支持.
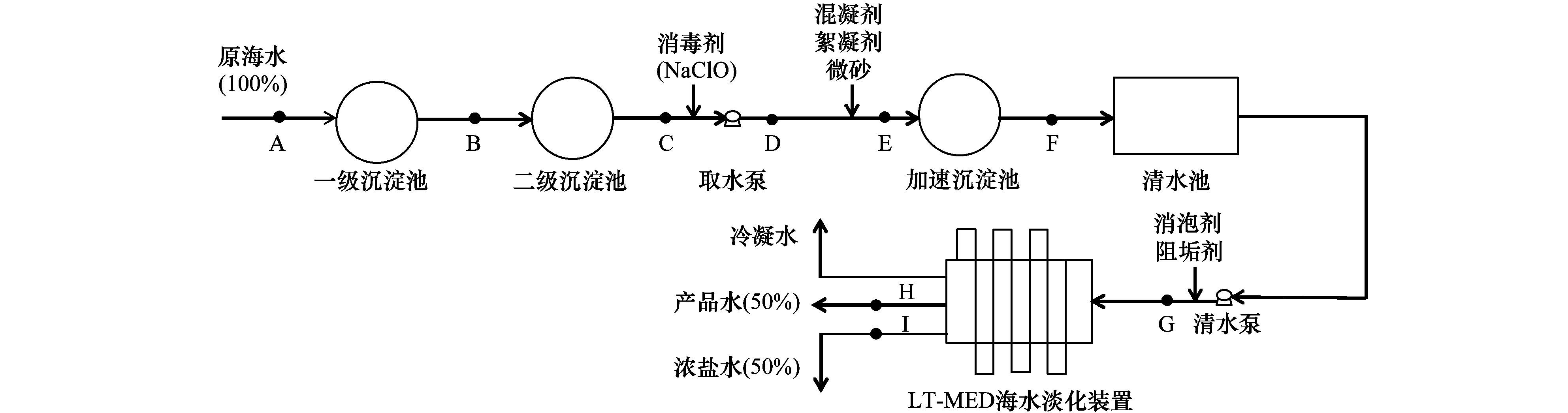
1 材料与方法 1.1 实验水样本实验水样取自天津市某电厂, 工艺流程如图 1所示, 进水为天津渤海湾海水, 设计处理水量2 000 t·h-1, 产水量为1 000 t·h-1, 浓盐水回收率为50%. LT-MED海水淡化装置传热管材料主要采用成本较低的铝和碳钢, 产水比不小于13, 在额定工况下, 装置单机出力不小于25 000 m3·d-1.
该工艺的消毒剂加药浓度为1~2 mg·L-1, 主要成分为5%~10%的NaClO, 以20 m3·h-1连续投加; 混凝剂为聚合硫酸铁; 絮凝剂为阴离子型聚丙烯酰胺(PAM); 消泡剂为0.25‰的磷酸酯类; 阻垢剂为8.5‰的聚磷酸盐, 全部采用连续投加的方式进行投加.对LT-MED海水淡化装置的清洗采用酸洗的方法, 使用2%以内的氨基磺酸.
本实验共有9个采样点(图 1), 分别为原海水(A)、一级沉淀池出水(B)、二级沉淀池出水(C)、取水泵出水(D)、加速沉淀池进水(E)、加速沉淀池出水(F)、海水淡化装置进水(G)、产品水(H)和浓盐水(I).水样取回实验室后, 经0.22 μm滤膜过滤以去除悬浮物, 过滤后的水样保存在4℃冰箱中用于后续测定.
|
图 1 LT-MED海水淡化工艺流程示意 Fig. 1 The schematic diagram of LT-MED for seawater desalination |
溶解性有机碳(DOC)的测定采用Sievers5310C(GE, 美国)型总有机碳分析仪, 254 nm处紫外吸收值(UV254)的测定采用UV-2401PC(Shimadzu, 日本)型紫外-可见分光光度计, 总溶解性固体(TDS)的测定采用SX-650型(上海三信, 中国)笔式电导率/电阻率/TDS/盐度计, 氨氮(NH3-N)的测定采用HI96715型(HANNA, 意大利)氨氮浓度测定仪, Br-的测定采用NaClO氧化-碘量法, 每种水质重复测定3次.
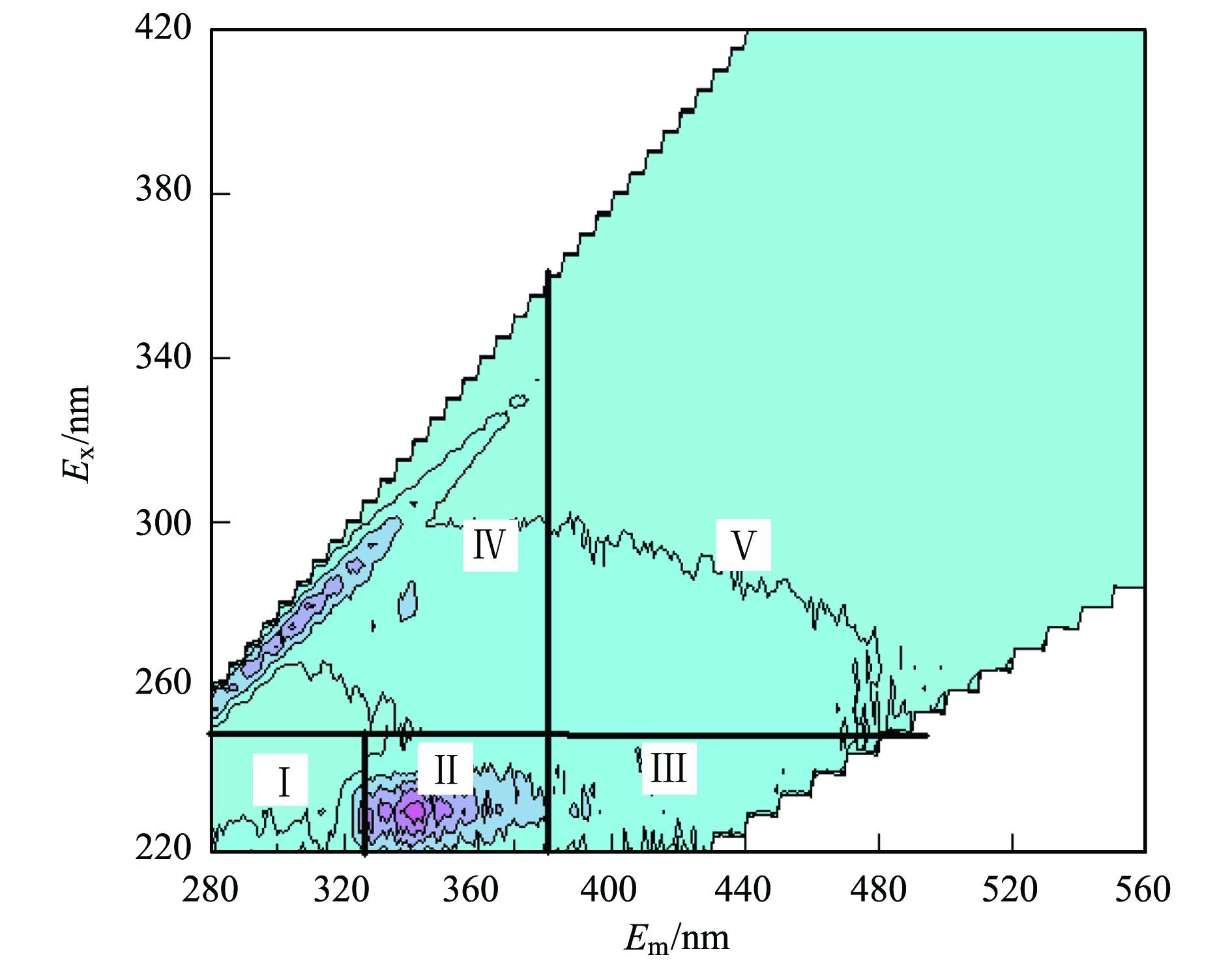
1.3 三维荧光光谱有机物荧光组分分析采用三维荧光光谱分析法.采用F-7000型荧光分光光度计(Hitachi, 日本), 激发光波长(excitation, Ex)范围220~420 nm, 间隔5 nm, 发射光波长(emission, Em)范围240~600 nm, 间隔1 nm.数据采用Matlab和Origin软件进行数据处理, 并以等高线图表征, 以超纯水作为空白校正水的拉曼散射.海水有机物三维荧光光谱如图 2所示, 5个分区分别代表酪氨酸类(Ⅰ区)和色氨酸类(Ⅱ区)芳香族蛋白质、富里酸(Ⅲ区)、溶解性微生物代谢产物(Ⅳ区)和腐殖酸类有机物(Ⅴ区)[14].
|
图 2 海水有机物三维荧光光谱 Fig. 2 Fluorescence spectroscopy of DOM in the seawater |
Br-THMs的测定采用液液萃取-气相色谱-质谱联用(GC/MS)法[15, 16], GC/MS分析采用GCMS-QP2010 Plus型(Shimadzu, 日本)气相色谱质谱联用仪.向110 mL水样中加入110 mL替代物(十氟联苯, 10 μg·mL-1), 颠倒振荡两次, 混匀.再依次加入2.5 mL甲基叔丁基醚(MTBE)、10 g氯化钠, 剧烈振荡4 min进行液液萃取, 垂直静置2 min, 使两相充分分离.用胶头玻璃滴管吸出上层有机相至自动进样瓶, 密封后进行GC/MS分析, 每个水样重复测定3次.
测定的THMs包括:三氯甲烷(CHCl3)、一溴二氯甲烷(CHBrCl2)、二溴一氯甲烷(CHBr2Cl)和三溴甲烷(CHBr3). CHCl3(溶于甲醇, 10.0 mg·L-1)、CHBrCl2(溶于甲醇, 0.954 mg·mL-1)、CHBr2Cl(溶于甲醇, 1.30 mg·mL-1)和CHBr3(溶于甲醇, 1.06 mg·mL-1)标准样品均购自中国计量科学研究院.
利用三卤甲烷标准品配制不同的浓度梯度, 经处理检测后, 得到标准曲线, 相关系数为0.990 4~0.999 3, 表明这4种物质峰面积与浓度之间存在很好的线性关系. CHCl3、CHBrCl2、CHBr2Cl和CHBr3的检出下限分别为0.08、0.03、0.1和0.1 μg·L-1, 4种物质的回收率在96.7%~103.4%之间[17].
1.4.2 溴代卤乙酸(Br-HAAs)Br-HAAs的测定采用液液萃取-衍生化-GC/MS法[18, 19].向50 mL水样中加入30 μL替代物2, 3-二溴丙酸(20 μg·mL-1), 颠倒振荡两次, 混匀; 加入2 mL浓硫酸进行酸化, 使pH<0.5, 抑制卤乙酸电离; 加入18 g无水硫酸钠, 增加HAAs的离子强度, 促使其快速向有机相转移, 强化萃取效果; 加入2 mL含内标1, 2, 3-三氯丙烷的MTBE溶液萃取剂(300 μg·L-1), 剧烈振荡3 min进行液液萃取, 静置5 min使两相充分分离.
吸取1.5 mL上层MTBE有机相转移至衍生瓶中, 加入2 mL 10%的硫酸-甲醇溶液(硫酸:甲醇=1:9), 摇匀密封, 于50℃水浴中进行酯化反应2 h.衍生化结束后将水样冷却至室温, 加入150 g·L-1硫酸钠溶液7 mL, 迅速摇匀后移除水相, 剩余水相<0.3 mL; 缓慢加入1 mL饱和碳酸氢钠溶液, 拧紧瓶盖并间断振荡放气(至少4次), 静置至两相分离.移取上层有机相至2 mL螺纹口样品瓶(美国安捷伦公司产品), 用于GC/MS分析.每个水样重复测定3次.
测定的HAAs包括一氯乙酸(C2H3ClO2)、二氯乙酸(C2H2Cl2O2)、三氯乙酸(C2HCl3O2)、一溴乙酸(C2H3BrO2)、二溴乙酸(C2H2Br2O2)、三溴乙酸(C2HBr3O2)、一溴一氯乙酸(C2H2BrClO2)、二溴一氯乙酸(C2HBr2ClO2)和一溴二氯乙酸(C2HBrCl2O2). C2H2Cl2O2(溶于MTBE, 194 mg·L-1)和C2HCl3O2(溶于MTBE, 137 mg·L-1)购自中国计量科学研究院, C2H3ClO2(溶于MTBE, 1 000 μg·mL-1)、C2H2Br2O2(溶于MTBE, 1 000 μg·mL-1)和C2HBr2ClO2(溶于MTBE, 100 μg·mL-1)购自美国AccuStandard公司, C2H3BrO2(纯度98%)购自德国Dr.Ehrenstorfer公司, C2HBrCl2O2(溶于MTBE, 1 000 μg·mL-1)购自美国Sigma-Aldrich公司, C2HBr3O2(纯度>97%)和C2H2BrClO2(纯度>97%)购自美国Alfa公司.
利用卤乙酸标准品配制不同的浓度梯度, 经处理检测后, 得到标准曲线, 相关系数为0.990 4~0.999 4, 表明这9种物质峰面积与浓度之间存在很好的线性关系. C2H3ClO2、C2H2Cl2O2、C2HCl3O2、C2H3BrO2、C2H2Br2O2、C2HBr3O2、C2H2BrClO2、C2HBr2ClO2和C2HBrCl2O2的检出下限分别为0.6、0.3、0.2、0.2、0.2、0.3、0.1、0.2和0.3 μg·L-1, 9种物质的回收率在93.9%~113%之间[20].
1.4.3 溴代苯酚(BPs)BPs的测定采用固相萃取-衍生化-GC/MS法[21].首先用2 mol·L-1H2SO4调节水样(500 mL)pH至2.0±0.1, 然后将水样通过Waters Oasis HLB(美国)固相萃取小柱.水样中的有机物全部被HLB小柱吸附后, 对HLB小柱抽真空5 min.采用7 mL丙酮-二氯甲烷(丙酮:二氯甲烷=50:50) 洗脱被吸附的有机物, 得到的洗脱液在微弱的氮气流下吹干.
向吹干的残留物中加入有机溶剂丙酮-二氯甲烷(丙酮:二氯甲烷=50:50) 和硅烷化试剂各100 μL, 摇匀密封, 于室温进行硅烷化反应1 h.衍生化结束后冷却至室温, 加入20 μL内标氘代菲标准储备液(5 mg·L-1), 并用丙酮-二氯甲烷溶剂定容至250 μL.移取样品至250 μL内衬管, 并将内衬管置于2 mL螺纹口样品瓶(美国安捷伦公司产品), 用于GC/MS分析.每个水样重复测定3次.
测定的HPs包括2-氯苯酚(2-CP)、3-氯苯酚(3-CP)、4-氯苯酚(4-CP)、2, 4-二氯苯酚(2, 4-DCP)、2, 5-二氯苯酚(2, 5-DCP)、2, 4, 6-三氯苯酚(2, 4, 6-TCP)、2-溴苯酚(2-BP)、4-溴苯酚(4-BP)、2, 4-二溴苯酚(2, 4-DBP)、2, 6-二溴苯酚(2, 6-DBP)和2, 4, 6-三溴苯酚(2, 4, 6-TBP). 2-CP(纯度99.5%)、3-CP(纯度98.6%)、4-CP(纯度99.0%)、2, 4-DCP(纯度99.5%)、2, 5-DCP(纯度99.0%)、2, 4, 6-TCP(纯度99.5%)、2-BP(纯度>98%)、2, 6-DBP(纯度>98%)和2, 4, 6-TBP(纯度99.7%)均购自德国Dr.Ehrenstorfer公司, 4-BP(100 μg·mL-1, 溶于甲苯)和2, 4-DBP(100 μg·mL-1, 溶于甲苯)购自美国AccuStandard公司.
利用卤代酚标准品配制不同的浓度梯度, 经处理检测后, 得到标准曲线, 氯代苯酚的相关系数为0.991 0~0.996 5, 表明这6种物质峰面积与浓度之间存在很好的线性关系, 且氯代苯酚检出下限均为0.02 μg·L-1, 回收率在89%~105%之间[22].溴代苯酚的相关系数为0.999 0~0.999 8, 表明这5种物质峰面积与浓度之间存在很好的线性关系, 2-BP、4-BP和2, 4, 6-TBP的检出下限为0.03 μg·L-1; 2, 4-DBP和2, 6-DBP的检出下限为0.04 μg·L-1, 溴代苯酚的回收率均大于84%[23].
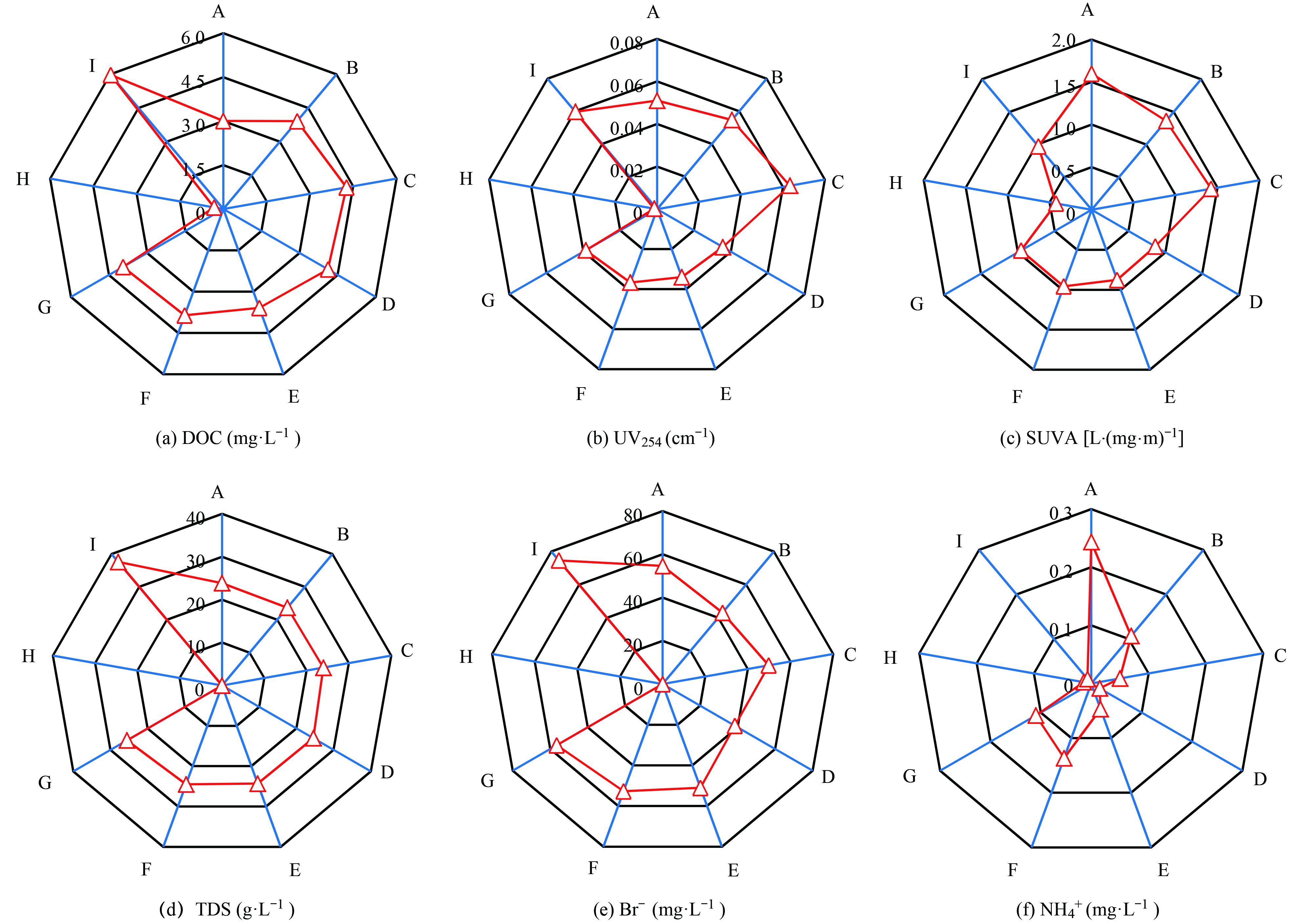
2 结果与讨论 2.1 沿程水质变化特征 2.1.1 常规水质变化特征LT-MED海水淡化工艺沿程常规水质变化如图 3所示.原海水(采样点A)的DOC为3 mg·L-1, 在一级沉淀池出水中(采样点B)有所上升(3.9 mg·L-1), 二级沉淀池出水(采样点C)经氯消毒后, DOC无明显变化, 且其后的沿程加速沉淀池进水(采样点E)、加速沉淀池出水(采样点F)和海水淡化装置进水(采样点G)中DOC都没有明显变化, 而LT-MED海水淡化装置出水即产品水(采样点H)的DOC降至0.3 mg·L-1, 与原海水相比, 降低了89.3%.原海水(采样点A)的UV254为0.051 cm-1, 在一级沉淀池出水(采样点B)和二级沉淀池出水(采样点C)中没有明显变化, 但经氯消毒后, 其UV254降至0.035 cm-1, 与原海水相比, 降低了32.7%, 说明氯消毒可减少水样中含CC双键和CO双键的芳香族化合物[24], 在后续沿程加速沉淀池进水(采样点E)、加速沉淀池出水(采样点F)和海水淡化装置进水(采样点G)中均无明显变化, 经海水淡化装置处理后, 产品水(采样点H)的UV254降至0.001 cm-1, 与原海水相比, 降低了98.1%.比紫外吸收值SUVA(UV254/DOC)可从某种程度上反映水质的芳香性和该处水体中芳香类有机物或消毒副产物前驱物占有机物的质量分数的大小[25].原海水(采样点A)的SUVA为1.6 L·(mg·m)-1, 经氯消毒后(采样点D)降低至0.9 L·(mg·m)-1, 与原海水相比, 降低了43.8%.
原海水(采样点A)的TDS为23.9 g·L-1, 预处理系统对TDS浓度没有影响, 经LT-MED海水淡化装置处理后, 产品水(采样点H)的TDS降至0.005 g·L-1, 去除率达99.98%.原海水(采样点A)的Br-浓度为54.6 mg·L-1, 经氯消毒后(采样点D)的Br-浓度降至38.5 mg·L-1, 降低了29.5%, 这是由于Br-易于被次氯酸氧化成活性更高的次溴酸, 从而生成了毒性更高的Br-DBPs[26~31].在后续沿程投加混凝剂和絮凝剂后, 加速沉淀池进水(采样点E)中Br-上升至51.1 mg·L-1, 经LT-MED海水淡化装置处理后, 产品水(采样点H)中Br-浓度未检出.
原海水(采样点A)的NH4+浓度为0.2 mg·L-1, 经过一级沉淀池和二级沉淀池处理后分别下降至0.1和0.05 mg·L-1.经氯消毒后(采样点D)的NH4+浓度为0.02 mg·L-1, 说明有少量的氨氮参与了氯消毒反应.有氨氮存在情况下, 次氯酸会和氨氮反应生成氯胺[5, 32].后续沿程投加混凝剂和絮凝剂后, 在加速沉淀池进水(采样点E)NH4+浓度上升至0.1 mg·L-1. LT-MED海水淡化装置产品水(采样点H)中NH4+浓度为0.01 mg·L-1, 与原海水相比, 降低了95.8%.
原海水经LT-MED海水淡化装置处理后, 沿程水质指标的浓度全部浓缩到浓盐水(采样点Ⅰ)中, 其中, DOC为6.0 mg·L-1, 是海水本底值的2倍; UV254为0.06 cm-1, 是海水本底值的1.2倍; TDS为37.6 g·L-1, 是海水本底值的1.6倍; Br-浓度为74.6 mg·L-1, 是海水本底值的1.3倍; NH4+浓度为0.01 mg·L-1.
|
图 3 沿程常规水质变化 Fig. 3 Changes of conventional water quality along the process |
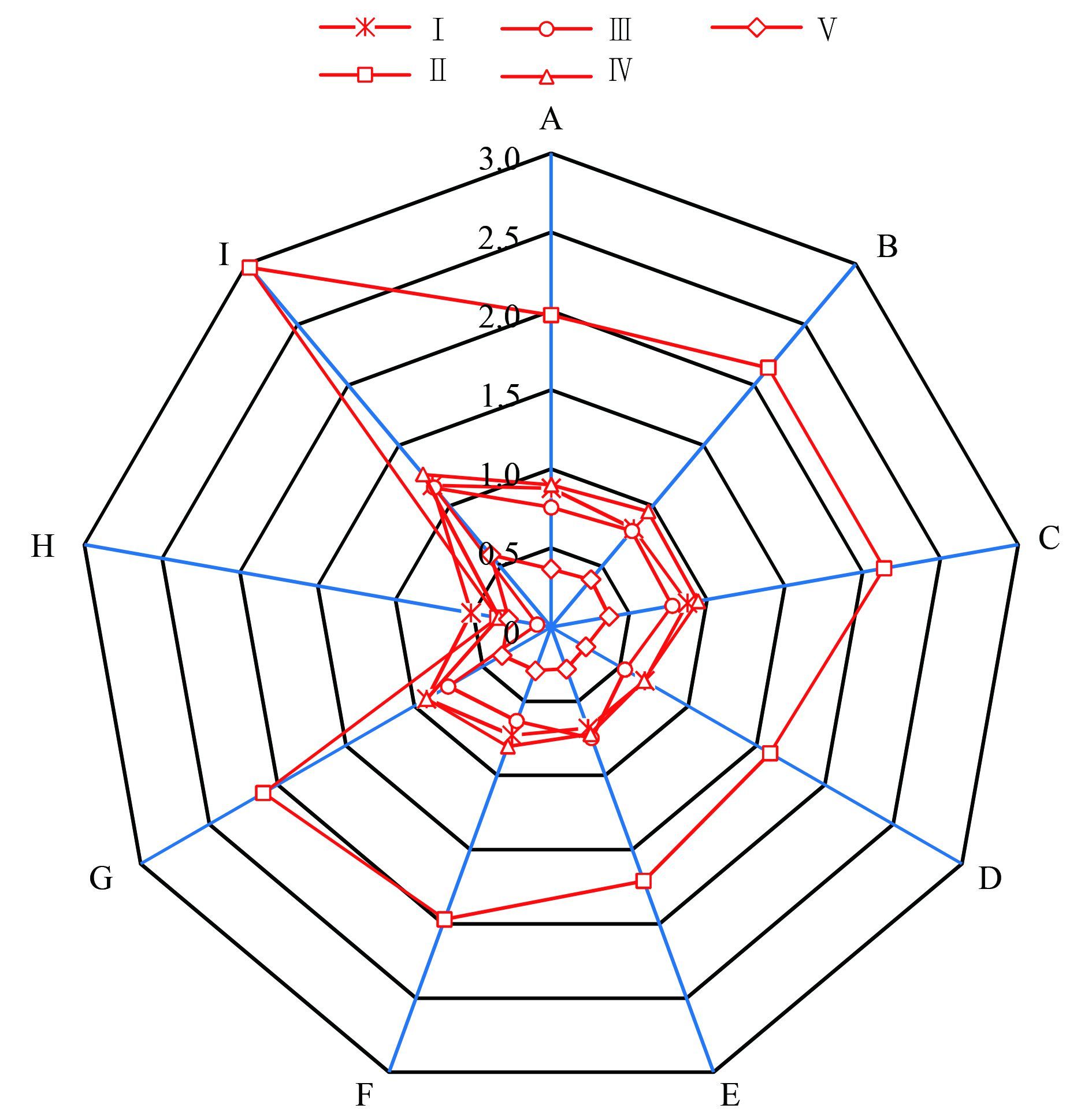
LT-MED海水淡化工艺沿程水样荧光区域体积积分如图 4所示.海水中溶解性有机物主要包括色氨酸类芳香族蛋白质(区域Ⅱ)、富里酸类有机物(区域Ⅲ)和溶解性微生物代谢产物(区域Ⅳ)[33].原海水(采样点A)的色氨酸类芳香族蛋白质占40.48%, 富里酸类有机物和溶解性微生物代谢产物分别占15.52%和18.47%, 在一级沉淀池出水(采样点B)和二级沉淀池出水(采样点C)中没有明显变化.经氯消毒后(采样点D), 色氨酸类芳香族蛋白质、富里酸类有机物和溶解性微生物代谢产物的荧光信号与原海水相比分别降低了19.24%、28.53%和24.75%.在氯消毒过程中, 芳香类和富里酸类有机物是DOM中生成DBPs的主要活性成分.在后续沿程加速沉淀池进水(采样点E)、加速沉淀池出水(采样点F)和海水淡化装置进水(采样点G)中均无明显变化.经海水淡化装置处理后, 产品水(采样点H)中的这3种荧光性DOM的荧光信号与原海水相比分别降低了82.53%、87.98%和62.82%, 而浓盐水(采样点I)中分别增加了50.38%、51.92%和39.84%.
|
图 4 沿程水样荧光区域体积积分 Fig. 4 Volume integral of fluorescence area along the process |
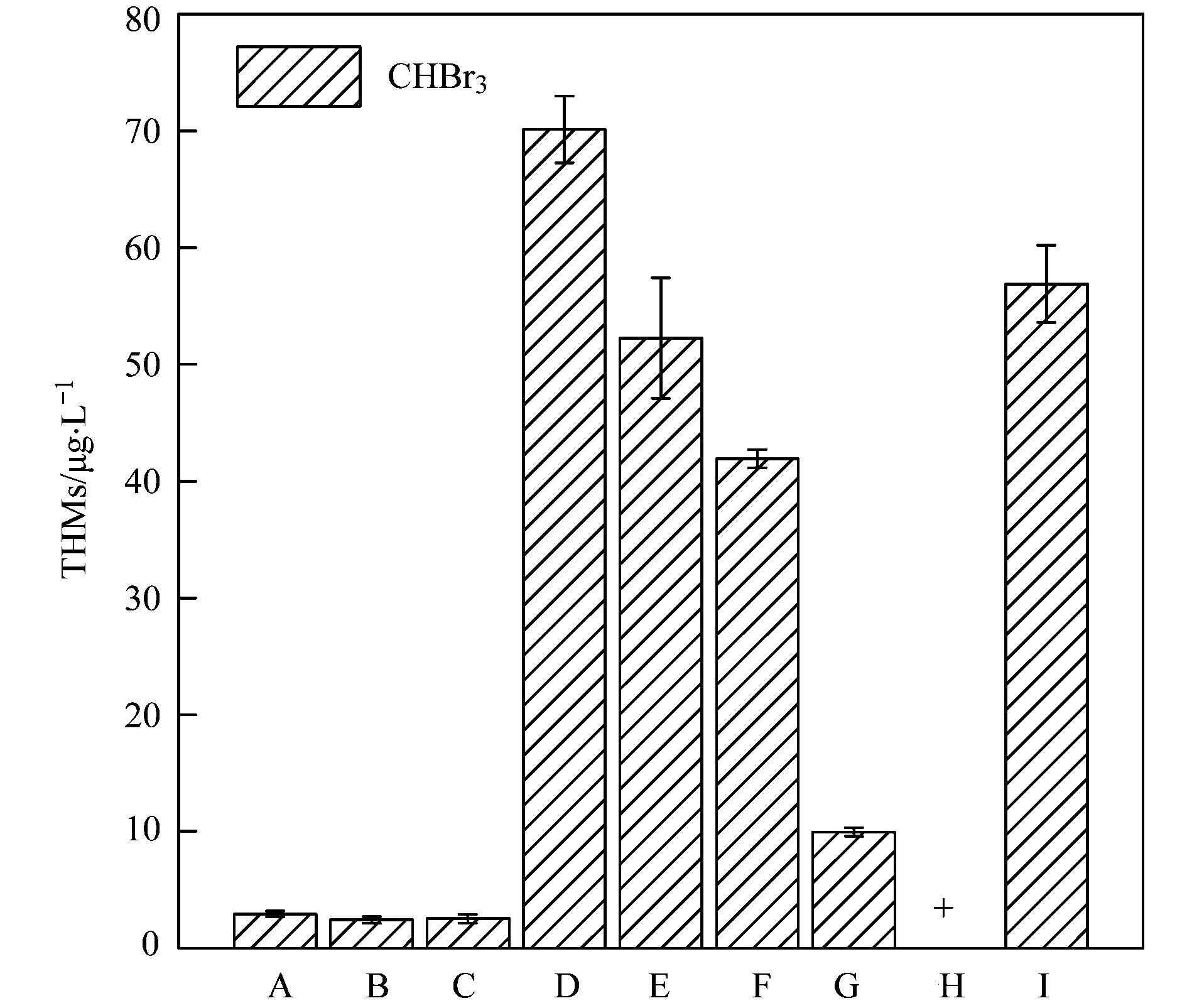
LT-MED海水淡化工艺沿程THMs变化如图 5所示.在沿程中只检出CHBr3, 其余物质均低于检出限, 未检出.原海水(采样点A)CHBr3的浓度为2.9 μg·L-1, 在一级沉淀池出水(采样点B)和二级沉淀池出水(采样点C)中没有明显变化, 但经氯消毒后(采样点D), CHBr3的浓度急剧上升为70.1 μg·L-1, 这是因为溴会首先消耗DOM中可取代的位置, 所以在Br-浓度较高时, 容易生成CHBr3.由于混凝剂和絮凝剂的投加, 加速沉淀池进水(采样点E)中CHBr3的浓度下降为52.2 μg·L-1, 在加速沉淀池出水(采样点F)中无明显变化.海水淡化装置进水(采样点G)中的CHBr3的浓度下降为10 μg·L-1, 这是因为投加了消泡剂和阻垢剂.而经海水淡化装置处理后, 产品水(采样点H)中的CHBr3未检出, 去除率达到了100%.氯消毒预处理过程中生成的CHBr3被截留到了浓盐水(采样点Ⅰ)中, 浓度为56.9 μg·L-1, 是海水中本底CHBr3值的19.6倍.
当海水中有机物含量一定时, THMs的生成量随溴离子浓度的增加而增加, 而且Br-DBPs的比例亦明显增加[34].当存在NH4+时, 会先与次氯酸根反应生成氯胺, 从而降低了氯化消毒副产物的生成[25].高浓度的Br-(54.6 mg·L-1)会被NaClO消毒产生的HOCl氧化成取代活性更强的HOBr, 且会提高氯的氧化反应速率, 同时显著促进氯的消耗[35].此时, 溴以取代作用为主, 而氯以对溴化物的氧化作用为主, 从而促进溴与DBPs前体物的取代反应, 因此会生成大量的Br-DBPs, 相应的反应方程如下式:
HOCl+Br-→HOBr+Cl-
HOBr+DOM→Br-DBPs
|
图 5 海水淡化LT-MED系统的Br-THMs Fig. 5 Br-THMs of the seawater desalination LT-MED system |
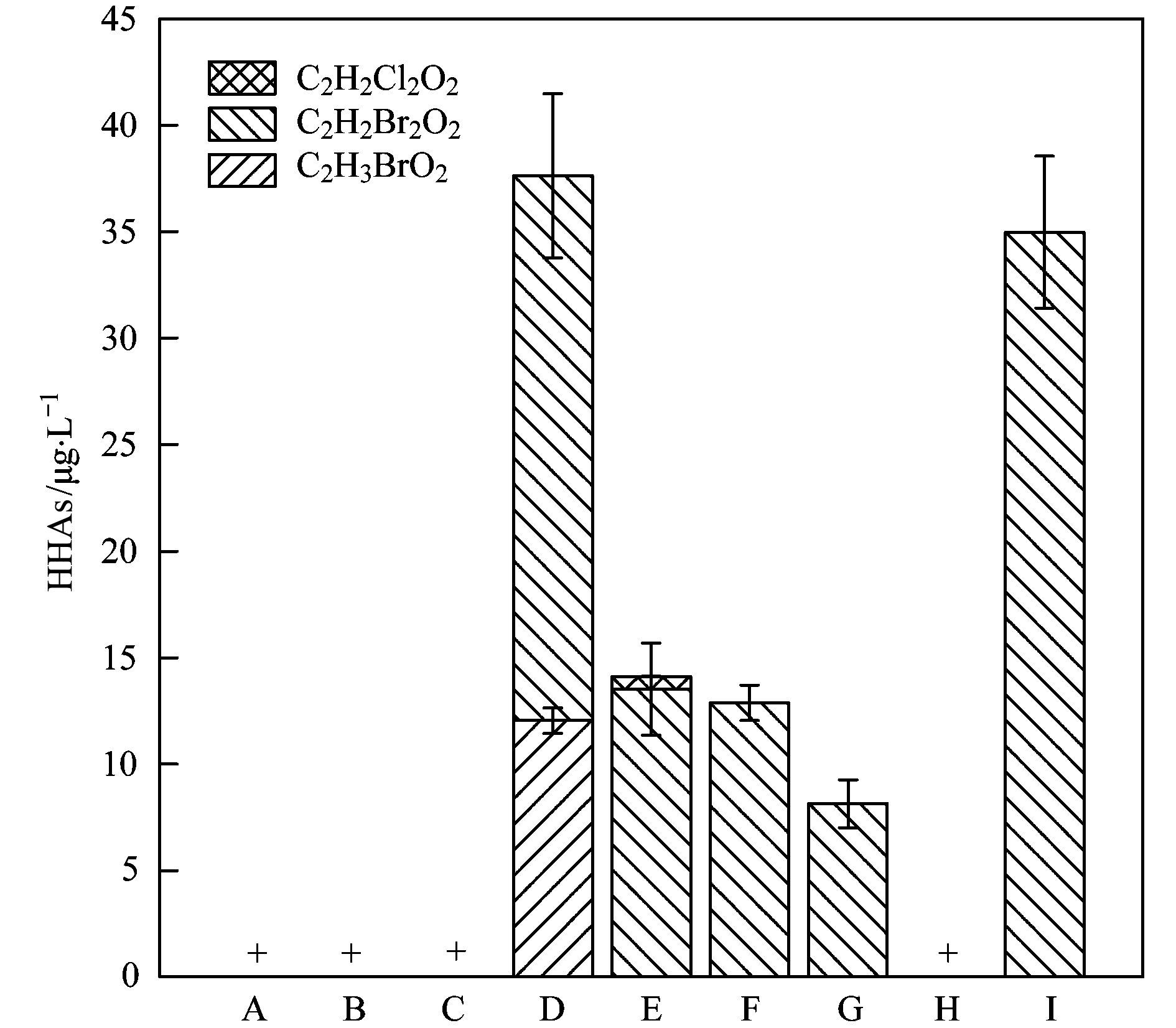
LT-MED海水淡化工艺沿程Br-HAAs的变化如图 6所示.在原海水(采样点A)、一级沉淀池出水中(采样点B)和二级沉淀池出水(采样点C)中都未检测出Br-HAAs.但经氯消毒后(采样点D), HAAs的种类增加至两种, 分别为C2H3BrO2和C2H2Br2O2, 浓度分别为12.0 μg·L-1和25.6 μg·L-1.在氯消毒过程中, 海水中的Br-被HOCl氧化为HOBr, 会首先与DOM反应生成Br-HAAs, 所以在氯消毒之后只检测出Br-HAAs(包括C2H3BrO2和C2H2Br2O2); 与Br-THMs相比, Br-HAAs的生成量较低, 一方面是因为Br-THMs的生成比Br-HAAs更容易[36, 37], 另一方面是因为SUVA值较低, 含疏水性的有机物比例小, 导致HAAs生成潜能较低, 所以HAAs的生成量也比较低[38].
加速沉淀池进水(采样点E)中检测出了新的氯代卤乙酸(Cl-HAAs):C2H2Cl2O2, 浓度为0.6 μg·L-1.由此可见HOBr和HOCl存在竞争的关系, 会有少量的氯代消毒副产物生成.但在高浓度的Br-存在的情况下, 氯代消毒副产物又快速被溴取代, 生成溴代消毒副产物, 使得氯代副产物浓度下降, 溴代副产物浓度升高[39].所以在加速沉淀池出水(采样点F)中只检测到C2H2Br2O2.
|
图 6 海水淡化LT-MED系统的Br-HAAs Fig. 6 Br-HAAs of the seawater desalination LT-MED system |
经LT-MED海水淡化装置处理后, 产品水(采样点H)中的HAAs未检出, 去除率达到了100%.氯消毒预处理过程中生成的HAAs被截留到了浓盐水(采样点I)中, 浓度为35.0 μg·L-1.
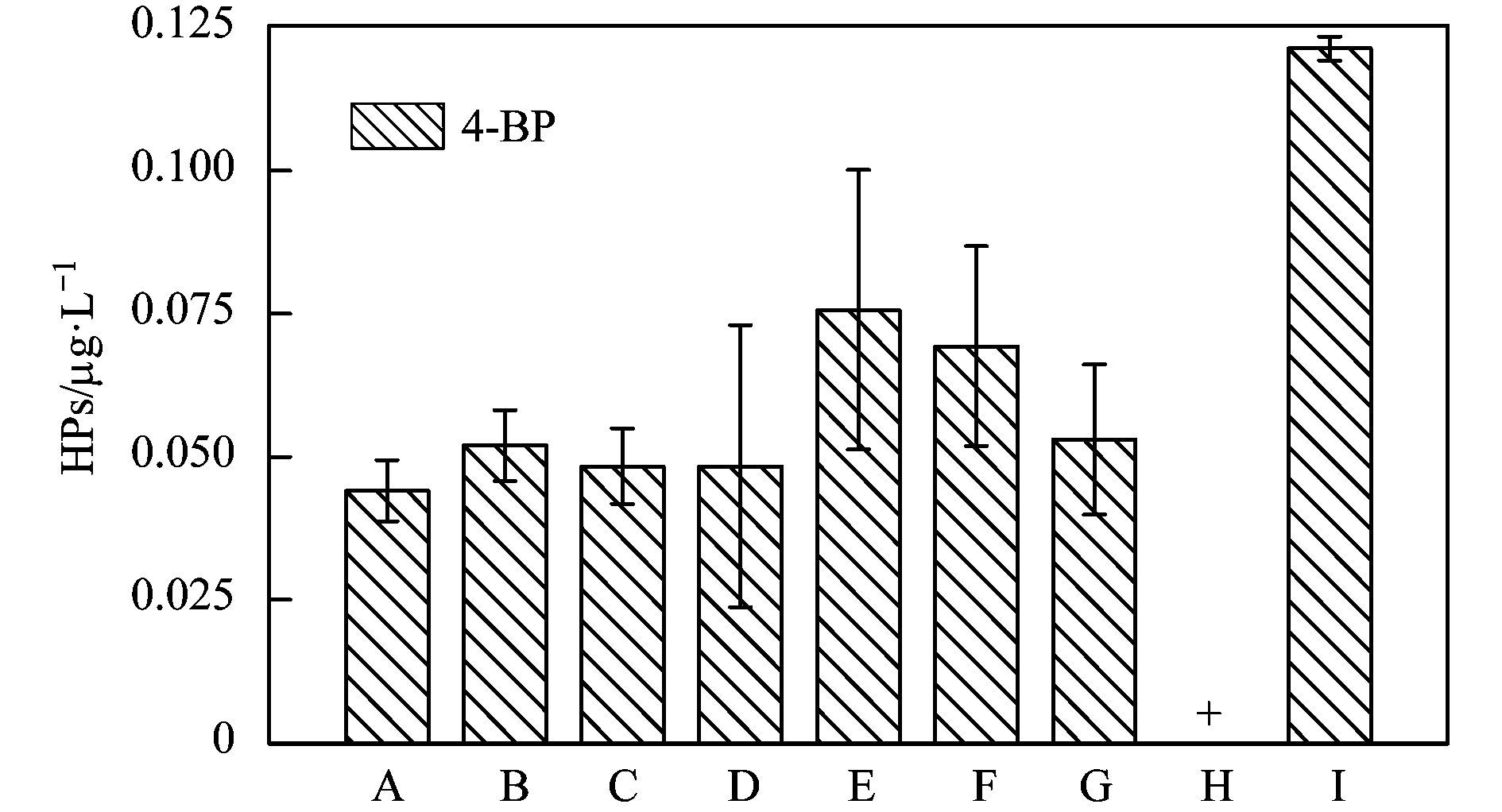
2.2.3 溴代苯酚(BPs)LT-MED海水淡化工艺沿程的BPs变化如图 7所示.海水中的溴代苯酚能够通过多种自然途径形成, 被认为是一种“海洋风味素”[40~42].许多海藻和多毛目环节动物体内都含有溴酚类物质[43]或在代谢过程中会产生酚类物质[44, 45], 从而改变海水中的物质分布, 酚类物质已成为海洋环境的重要污染物之一[46].
|
图 7 海水淡化LT-MED系统的BPs Fig. 7 BPs of the seawater desalination LT-MED system |
本文研究的海水中只检出4-BP, 其余物质均低于检出限, 未检出.当含有浓度较高的Br-(54.6 mg·L-1)时, HOCl会将Br-氧化成为HOBr. HOBr与酚类有机物的反应速率远高于HOCl, 其二级反应速率常数比氯代反应高3个数量级[47], 因此在海水氯消毒过程中, 生成的HPs的主要形态为BPs.
原海水(采样点A)的4-BP的浓度为0.04 μg·L-1, 在一级沉淀池出水(采样点B)、二级沉淀池出水(采样点C)和氯消毒后均无明显变化.由于混凝剂和絮凝剂的投加, 加速沉淀池进水(采样点E)中上升至0.08 μg·L-1且出水(采样点F)中无明显变化.在海水淡化装置进水(采样点G)中, 4-BP的浓度降至0.05 μg·L-1, 这是因为投加了消泡剂和阻垢剂.经LT-MED海水淡化装置处理后, 产品水(采样点H)中的BPs未检出, 去除率达到了100%.氯消毒预处理过程中生成的BPs被截留到了浓盐水(采样点I)中, 浓度为0.1 μg·L-1, 是海水中本底BPs值的2.5倍.
高浓度Br-(54.6 mg·L-1)的存在, 导致生成了活性更强的HOBr, 而溴代苯酚会与HOBr发生反应生成Br-THMs[12], 从而加大了Br-THMs的生成量, 相应的反应方程如下所示:
HOCl+Br-→HOBr+Cl-
HOBr+BPs→Br-THMs
同时, 次溴酸还可与海水中的DOM发生溴代反应, 生成溴代苯酚[48].
3 结论(1) 进水原海水中含有较少的芳香类化合物, SUVA为1.7 L·(mg·m)-1, 其中色氨酸类芳香族蛋白质和富里酸类有机物是海水中的主要荧光性DOM, 经LT-MED海水淡化装置处理后, 5个荧光区域的溶解性有机物均大幅度减少.
(2) 原海水中含有THMs(Br-THMs)和BPs(4-BP), 由于该海水中较高浓度Br-(54.6 mg·L-1)的存在, 使得大部分的DBPs为Br-DBPs.经LT-MED海水淡化装置处理后, 对沿程生成的DBPs去除率为100%, 最终被截留到了浓盐水中.
(3) 在LT-MED海水淡化氯消毒预处理过程中, 会产生多种DBPs, 而浓盐水多采用直接排海的方法, 这会引起海洋生物生态风险, 因此, 在设计海水淡化LT-MED工艺时, 在保证装置正常运行的前提下, 要考虑氯消毒剂等药剂的优化投加和浓盐水的处理与处置问题, 以减少DBPs给水环境健康和生态平衡带来的风险.
| [1] | Ghaffour N, Missimer T M, Amy G L. Technical review and evaluation of the economics of water desalination:current and future challenges for better water supply sustainability[J]. Desalination, 2013, 309: 197–207. DOI: 10.1016/j.desal.2012.10.015 |
| [2] | Dastgerdi H R, Whittaker P B, Chua H T. New MED based desalination process for low grade waste heat[J]. Desalination, 2016, 395: 57–71. DOI: 10.1016/j.desal.2016.05.022 |
| [3] | Qi C H, Feng H J, Lv Q C, et al. Performance study of a pilot-scale low-temperature multi-effect desalination plant[J]. Applied Energy, 2014, 135: 415–422. DOI: 10.1016/j.apenergy.2014.08.096 |
| [4] | Agus E, Voutchkov N, Sedlak D L. Disinfection by-products and their potential impact on the quality of water produced by desalination systems:a literature review[J]. Desalination, 2009, 237(1-3): 214–237. DOI: 10.1016/j.desal.2007.11.059 |
| [5] | Agus E, Sedlak D L. Formation and fate of chlorination by-products in reverse osmosis desalination systems[J]. Water Research, 2010, 44(5): 1616–1626. DOI: 10.1016/j.watres.2009.11.015 |
| [6] | Shi H L, Qiang Z M, Adams C. Formation of haloacetic acids, halonitromethanes, bromate and iodate during chlorination and ozonation of seawater and saltwater of marine aquaria systems[J]. Chemosphere, 2013, 90(10): 2485–2492. DOI: 10.1016/j.chemosphere.2012.09.073 |
| [7] | Kim D, Amy G L, Karanfil T. Disinfection by-product formation during seawater desalination:a review[J]. Water Research, 2015, 81: 343–355. DOI: 10.1016/j.watres.2015.05.040 |
| [8] | Borges E P, Lavorante A F, Reis B F D. Determination of bromide ions in seawater using flow system with chemiluminescence detection[J]. Analytica Chimica Acta, 2005, 528(1): 115–119. DOI: 10.1016/j.aca.2004.07.058 |
| [9] | Heeb M B, Criquet J, Zimmermann-Steffens S G, et al. Oxidative treatment of bromide-containing waters:formation of bromine and its reactions with inorganic and organic compounds-a critical review[J]. Water Research, 2014, 48: 15–42. DOI: 10.1016/j.watres.2013.08.030 |
| [10] | Yang Z, Sun Y X, Ye T, et al. Characterization of trihalomethane, haloacetic acid, and haloacetonitrile precursors in a seawater reverse osmosis system[J]. Science of the Total Environment, 2017, 576: 391. DOI: 10.1016/j.scitotenv.2016.10.139 |
| [11] | Sun Y X, Wu Q Y, Hu H Y, et al. Effect of bromide on the formation of disinfection by-products during wastewater chlorination[J]. Water Research, 2009, 43(9): 2391–2398. DOI: 10.1016/j.watres.2009.02.033 |
| [12] | Albaladejo G J, Ros J A, Romero A, et al. Effect of bromophenols on the taste and odour of drinking water obtained by seawater desalination in south-eastern Spain[J]. Desalination, 2012, 307: 1–8. DOI: 10.1016/j.desal.2012.08.028 |
| [13] | 陈健, 王长生, 张国占, 等. 紫外线消毒技术在给排水中的应用[J]. 中国给水排水, 2002, 18(7): 29–31. Chen J, Wang C S, Zhang G Z, et al. Application of ultraviolet disinfection technology in water and wastewater treatment[J]. China Water & Wastewater, 2002, 18(7): 29–31. |
| [14] | Chen W, Westerhoff P, Leenheer J A, et al. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science and Technology, 2003, 37(24): 5701–5710. DOI: 10.1021/es034354c |
| [15] | EPA Method 551.1, Determination of chlorination disinfection byproducts, chlorinated solvents, and halogenated pesticides/herbicides in drinking water by liquid-liquid extraction and gas chromatography with electron-capture detection[S]. |
| [16] | Huang H, Wu Q Y, Hu H Y, et al. Dichloroacetonitrile and dichloroacetamide can form independently during chlorination and chloramination of drinking waters, model organic matters, and wastewater effluents[J]. Environmental Science & Technology, 2012, 46(19): 10624–10631. |
| [17] | 黄睿, 刘志泉, 闫博引, 等. 基于EPA标准开发同步检测饮用水中三卤甲烷和卤乙酸的方法[J]. 给水排水, 2016, 42(5): 32–36. Huang R, Liu Z Q, Yan B Y, et al. Development of a synchronous assay method for trihalomethane and haloacetic acid in drinking water based on EPA standards[J]. Water & Wastewater Engineering, 2016, 42(5): 32–36. |
| [18] | EPA Method 552.2, Determination of haloacetic acids and dalapon in drinking water by liquid-liquid extraction, derivatization and gas chromatography with electron capture detection[S]. |
| [19] | Xie Y F. Analyzing haloacetic acids using gas chromatography/mass spectrometry[J]. Water Research, 2001, 35(6): 1599–1602. DOI: 10.1016/S0043-1354(00)00397-3 |
| [20] | 郭瑶. 水质卤乙酸类化合物的测定方法研究[D]. 青岛: 青岛理工大学, 2011. |
| [21] | EPA Method 528, Determination of phenols in drinking water by solid phase extraction and capillary column gas chromatography/mass spectrometry (GC/MS)[S]. |
| [22] | Michałowicz J, Stufka-Olczyk J, Milczarek A, et al. Analysis of annual fluctuations in the content of phenol, chlorophenols and their derivatives in chlorinated drinking waters[J]. Environmental Science and Pollution Research, 2011, 18(7): 1174–1183. DOI: 10.1007/s11356-011-0469-5 |
| [23] | Han W, Wang S, Huang H L, et al. Simultaneous determination of brominated phenols in soils[J]. Journal of Environmental Sciences, 2013, 25(11): 2306–2312. DOI: 10.1016/S1001-0742(12)60298-8 |
| [24] | 苗婷婷. 氯及臭氧消毒技术对城市污水水质的影响[D]. 北京: 北京林业大学, 2008. |
| [25] | Hu H Y, Du Y, Wu Q Y, et al. Differences in dissolved organic matter between reclaimed water source and drinking water source[J]. Science of the Total Environment, 2016, 551. |
| [26] | Chang E E, Lin Y P, Chiang P C. Effects of bromide on the formation of THMs and HAAs[J]. Chemosphere, 2001, 43(8): 1029–1034. DOI: 10.1016/S0045-6535(00)00210-1 |
| [27] | Uyak V, Toroz I. Investigation of bromide ion effects on disinfection by-products formation and speciation in an Istanbul water supply[J]. Journal of Hazardous Materials, 2007, 149(2): 445–451. DOI: 10.1016/j.jhazmat.2007.04.017 |
| [28] | Westerhoff P, Chao P, Mash H. Reactivity of natural organic matter with aqueous chlorine and bromine[J]. Water Research, 2004, 38(6): 1502–1513. DOI: 10.1016/j.watres.2003.12.014 |
| [29] | Yang Y, Komaki Y, Kimura S Y, et al. Toxic impact of bromide and iodide on drinking water disinfected with chlorine or chloramines[J]. Environmental Science & Technology, 2014, 48(20): 12362–12369. |
| [30] | Plewa M J, Simmons J E, Richardson S D, et al. Mammalian cell cytotoxicity and genotoxicity of the haloacetic acids, a major class of drinking water disinfection by-products[J]. Environmental and Molecular Mutagenesis, 2010, 51(8-9): 871–878. DOI: 10.1002/em.v51:8/9 |
| [31] | Plewa M J, Muellner M G, Richardson S D, et al. Occurrence, synthesis, and mammalian cell cytotoxicity and genotoxicity of haloacetamides:an emerging class of nitrogenous drinking water disinfection byproducts[J]. Environmental Science & Technology, 2008, 42(3): 955–961. |
| [32] | 邰晓晖, 李轶, WangC S, 等. 操作条件及水质对海水氯消毒过程中消毒副产物生成的影响[J]. 环境工程, 2016, 34(3): 6–10. Tai X H, Li Y, Wang C S, et al. Effects of operating conditions and seawater quality on formation of disinfection by-products (DBPs) during chlorination process[J]. Environmental Engineering, 2016, 34(3): 6–10. |
| [33] | 杨哲, 孙迎雪, 石娜, 等. 海水淡化超滤-反渗透工艺沿程溴代消毒副产物变化规律[J]. 环境科学, 2015, 36(10): 3706–3714. Yang Z, Sun Y X, Shi N, et al. Formation and variation of brominated disinfection by-products in a combined ultrafiltration and reverse osmosis process for seawater desalination[J]. Environmental Science, 2015, 36(10): 3706–3714. |
| [34] | Zhai X D, Liu J F, Zhu X P. Trihalomethane formation of Macao water supply contaminated by seawater intrusion[J]. Journal of Harbin University of Commerce (Natural Sciences Edition), 2006, 22(1): 24–27. |
| [35] | 张华, 曲久辉, 刘会娟, 等. 中水消毒中溴代副产物在总消毒副产物中的比例及其影响因素[J]. 中国科学B辑:化学, 2008, 38(8): 728–736. Zhang H, Qu J H, Liu H J, et al. The proportion of brominated by-products in total disinfection by-products and the influencing factors[J]. Science in China Series B:Chemistry, 2008, 38(8): 728–736. |
| [36] | Zhang H, Qu J H, Liu H J, et al. Proportion of bromo-DBPs in total DBPs during reclaimed-water chlorination and its related influencing factors[J]. Science in China Series B:Chemistry, 2008, 51(10): 1000–1008. DOI: 10.1007/s11426-008-0097-1 |
| [37] | Yang X, Shang C, Huang J C. DBP formation in breakpoint chlorination of wastewater[J]. Water Research, 2005, 39(19): 4755–4767. DOI: 10.1016/j.watres.2005.08.033 |
| [38] | Zhang H, Qu J H, Liu H J, et al. Characterization of isolated fractions of dissolved organic matter from sewage treatment plant and the related disinfection by-products formation potential[J]. Journal of Hazardous Materials, 2009, 164(2-3): 1433–1438. DOI: 10.1016/j.jhazmat.2008.09.057 |
| [39] | 钱洪智. 不同饮用水源水氯化消毒副产物的特征与风险评价[D]. 杭州: 浙江大学, 2013. |
| [40] | Kotterman M, van der Veen I, van Hesselingen J, et al. Preliminary study on the occurrence of brominated organic compounds in Dutch marine organisms[J]. Biomolecular Engineering, 2003, 20(4-6): 425–427. DOI: 10.1016/S1389-0344(03)00072-8 |
| [41] | Haraguchi K, Kotaki Y, Relox Jr J R, et al. Monitoring of naturally produced brominated phenoxyphenols and phenoxyanisoles in aquatic plants from the Philippines[J]. Journal of Agricultural and Food Chemistry, 2010, 58(23): 12385–12391. DOI: 10.1021/jf103001n |
| [42] | Vetter W, Janussen D. Halogenated natural products in five species of antarctic sponges:compounds with POP-like properties[J]. Environmental Science & Technology, 2005, 39(11): 3889–3895. |
| [43] | Chung H Y, Ma W C, Ang Jr P O, et al. Seasonal variations of bromophenols in brown algae (Padina arborescens, Sargassum siliquastrum, and Lobophora variegata) collected in Hong Kong[J]. Journal of Agricultural and Food Chemistry, 2003, 51(9): 2619–2624. DOI: 10.1021/jf026082n |
| [44] | Martens D A. Identification of phenolic acid composition of alkali-extracted plants and soils[J]. Soil Science Society of America Journal, 2002, 66(4): 1240–1248. DOI: 10.2136/sssaj2002.1240 |
| [45] | Vázquez G, Fontenla E, Santos J, et al. Antioxidant activity and phenolic content of chestnut (Castanea sativa) shell and eucalyptus (Eucalyptus globulus) bark extracts[J]. Industrial Crops and Products, 2008, 28(3): 279–285. DOI: 10.1016/j.indcrop.2008.03.003 |
| [46] | Zhu J, Wang Y, Zeng L. An approach to determination of phenolic compounds in seawater using SPME-GC-MS based on SWCNTs coating[J]. Journal of Ocean University of China, 2016, 15(4): 655–659. DOI: 10.1007/s11802-016-2951-7 |
| [47] | Acero J L, Piriou P, von Gunten U. Kinetics and mechanisms of formation of bromophenols during drinking water chlorination:assessment of taste and odor development[J]. Water Research, 2005, 39(13): 2979–2993. DOI: 10.1016/j.watres.2005.04.055 |
| [48] | Taylor C J L. The effects of biological fouling control at coastal and estuarine power stations[J]. Marine Pollution Bulletin, 2006, 53(1-4): 30–48. DOI: 10.1016/j.marpolbul.2006.01.004 |
 2017, Vol. 38
2017, Vol. 38


