药物的大量使用,使得环境中药物活性物质逐渐积累.根据世界卫生组织相关报道,水循环中痕量的药物活性物质已经对人类健康造成潜在风险[1].用于治疗呼吸道、皮肤和眼睛等过敏性疾病的抗组胺药物CTZ[2]在环境中被频繁检出[3, 4],尤其是花粉热季节,地表水和废水中CTZ的浓度均呈上升趋势. Bahlmann等[5]通过液相色谱-串联质谱法测定污水处理厂CTZ的进水最大质量浓度为0.49 μg ·L-1,出水最大质量浓度为0.51 μg ·L-1.亲水性和不易降解性[6, 7]使其在污水处理中得不到很好的去除,最终会随着废水排至环境中.环境中的CTZ容易经土壤进入地下水甚至生物链,从而对人类健康和生态环境造成危害.
生物炭是生物质在缺氧或无氧条件下高温 (一般 < 700℃) 裂解制备的富含碳的物质[8].其自身的比表面积大、多孔结构、丰富的表面官能团和矿物成分等特点[9],使生物炭作为环境友好型材料[10~13]被广泛关注.生物炭不仅可以作为土壤改良剂[14, 15],提高土壤肥力、减少温室气体排放;还可以作为稳定剂控制污染物在土壤环境中的迁移转化及生物有效性[16, 17],消减其环境风险.添加生物炭后,土壤对污染物的吸附能力显著增强.有研究表明[18],土壤中添加400℃碳化温度的松针生物炭质量分数达0.1%时,混合体系中生物炭对多环芳烃吸附占主要贡献.然而目前关于西替利嗪的研究,多集中于其在环境中的潜在风险[19, 20],关于CTZ在土壤及生物炭上的吸附研究鲜见报道.本研究以西替利嗪为目标污染物,陕西黄绵土为供试土壤,采用批实验法,分析添加不同质量比、不同碳化温度核桃壳生物炭的土壤对CTZ的吸附行为及机制,以期为污灌等活动中防止CTZ及其同类污染物进入地下水提供依据.
1 材料与方法 1.1 吸附剂制备土壤样品为陕西黄绵土[中国地质科学院地球物理地球化学勘察研究所,GBW07460(ASA-9)],其基本理化性质为:pH 8.50±0.07,有机质含量 (10.3±0.3) g ·kg-1,阳离子交换量 (9.6±1.3) cmol ·kg-1.
核桃壳生物炭采用限氧控温碳化法[21]制备.具体是将核桃壳浸泡水洗后,以80℃在鼓风干燥箱中烘干后粉碎过40目筛,分别于300、400、500、600和700℃在马弗炉中碳化6 h (标记为W300、W400、W500、W600和W700),冷却至室温后取出.制得的碳化产物用1 mol ·L-1的盐酸浸泡12 h,去除灰分;经抽滤装置用去离子水洗至中性后,于80℃烘干并过40目筛装于棕色瓶中待用.
将土壤和生物炭以不同比例混合,使得生物炭在混合物中的质量分数分别为1%、5%、10%和20%.为了保证混合物的均匀性,手动混合后放入全自动翻转式振荡器 (30 r ·min-1) 振荡3 d后取出.土壤-生物炭混合物分别标记为:1%SWXXX、5%SWXXX、10%SWXXX、20%SWXXX,XXX表示生物炭制备的碳化温度.
生物炭、土壤以及土壤-生物炭混合体系的总C、H、N元素含量用美国有机元素分析仪Thermo Scientific FLASH 2000 CHNS/O测定;比表面积使用美国麦克ASAP 2020测定.
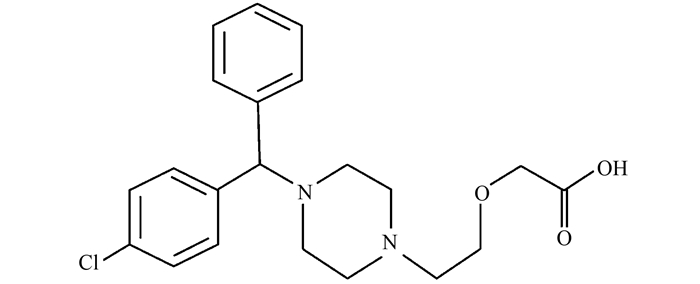
1.2 药品与仪器药品:CTZ (日本TCI公司,纯度≥98%),CAS号为83881-51-0,分子式C21H25ClN2O3,结构式如图 1所示,水中溶解度 (25℃) 为4263 mg ·L-1,辛醇水分配系数lgKow为1.70(由EPI Suite v4.10获得);乙腈 (美国MREDA TECHNOLOGY公司,HPLC级);磷酸二氢钾、无水氯化钙、盐酸和氢氧化钠 (北京化工产,分析纯);实验用水为超纯水 (Milli-Q超纯水机制得).
|
图 1 CTZ分子结构式 Fig. 1 Molecular structure of CTZ |
仪器:高效液相色谱仪 (日本岛津公司,DGU-20A3低容量排气装置,LC-20AT常规溶剂输送泵,SPD-20A高灵敏度紫外-可见检测器,CTO-20A柱温箱);pH计 (德国Sartorius公司,PB-10型号);A-WS台式低速离心机、恒温振荡仪 (上海福玛实验设备有限公司,QYC-2112型号);电子天平 (德国Sartorius公司,BP221S型号);电热恒温鼓风干燥箱 (天津中环实验电炉有限公司,DH-1021-3型号);粉碎机 (天津市泰斯特仪器有限公司);SHB-Ⅲ循环水式多用真空泵 (郑州长城科工贸有限公司);全自动翻转式振荡器 (长沙永乐康YKZ系列).
1.3 实验方法吸附实验中CTZ溶液用超纯水直接配制,背景溶液为0.01 mol ·L-1 CaCl2溶液.等温实验初始pH为6.0±0.1,初始质量浓度范围为5~640 mg ·L-1.
吸附批实验在室温条件下 (25℃) 进行,依据吸附剂的吸附性能,向20 mL的玻璃瓶中分别添加不同质量的吸附剂 (生物炭10~160 mg,土壤1 000 mg,混合物50~1 000 mg),以使得平衡时吸附剂对CTZ的吸附量达到初始量的20%~80%.每个浓度点均有两个平行样和一个控制样.预实验结果表明CTZ在W400~W700和土壤上的吸附动力学平衡时间均为3 d,在W300上的吸附平衡时间为27 d.因此将这些样品放入恒温振荡器振荡3 d (W300和SW300振荡27 d) 以达到吸附平衡.平衡后将样品取出放入低速离心机以3 000 r ·min-1的转速离心15 min达到固液分离.最后取上清液放入2 mL的测样瓶待测.
CTZ的测定采用高效液相色谱仪,配备有4.6 mm×250 mm的反相XDB-C18柱和紫外检测器.检测条件:流动相为乙腈-磷酸二氢钾 (磷酸二氢钾溶液用磷酸调pH至3.0,体积比45 :55),流速1 mL ·min-1,波长276 nm,柱温30℃,进样体积10 μL[22].控制样表明吸附实验过程中的污染物浓度损失可忽略不计,吸附剂对吸附质的吸附量按质量平衡计算.
1.4 数据处理吸附数据采用Freundlich模型[公式 (1)]进行拟合.吸附分配系数Kd根据等式 (2) 计算得出.
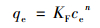
|
(1) |

|
(2) |
式中,qe是吸附平衡时CTZ在吸附剂上的固相吸附量 (mg ·kg-1),ce是吸附平衡时CTZ的液相质量浓度 (mg ·L1),KF是Freundlich吸附常数,n为非线性系数.
2 结果与讨论 2.1 吸附剂的物理化学性质生物炭和土壤的元素组成、BET比表面积、平均孔径、总孔隙体积等表征数据见表 1. W400~W600,C元素含量逐渐增加;H、N元素含量从W300到W700逐渐减少,与以往的研究结果一致[23].通过BET比表面积数据可以发现,W300基本是无孔结构;W400比表面积相比W300增加一个数量级,具有多微孔结构;W700比表面积达到最大,具多微孔和介孔结构.
|
|
表 1 土壤和生物炭的物理化学性质 Table 1 Physicochemical properties of biochars and soil |
为了比较混合后样品物理化学性质的实际测定值与理论计算值的差异,根据质量平衡,混合物样品中C和H元素含量预测值由以下式子计算 (N含量由于低于检测限而未被检测出):

|
(3) |
式中,Emix,the是混合物样品C和H元素含量理论值;Esoil和Ebc分别是土壤和生物炭的C、H元素含量;fsoil和fbc分别是土壤和生物炭在混合物中所占的质量分数. SA的理论值计算方法同上.
混合物C、H元素含量与生物炭添加比例成正相关 (表 2),表明生物炭和土壤混合得较均匀,向土壤中添加生物炭能够增强土壤肥力[24, 25].混合物总C含量理论值与实测值并不完全相同,这可能与土壤和生物炭组分之间的相互作用有关[26]. SW300比表面积的实测值较理论值均偏大,是由于生物炭表面的非碳化有机质组分会被土壤中的矿物去除,使其比表面积变大[27].对于SW400~SW700,随着碳化温度升高,生物炭的非碳化有机质减少,这种比表面积增大效应减弱;另外,随着生物炭添加量增大 (添加质量比为10%和20%),土壤和生物炭组分之间相互作用更加强烈,相互堵塞导致混合后比表面积实测值较理论值偏小.
|
|
表 2 混合样品元素组成和比表面积的理论值与实测值的比较 Table 2 Comparison between the theoretical and experimental values of elemental composition and SA of biochar-soil mixtures |
2.2 生物炭和土壤分别对CTZ的等温吸附
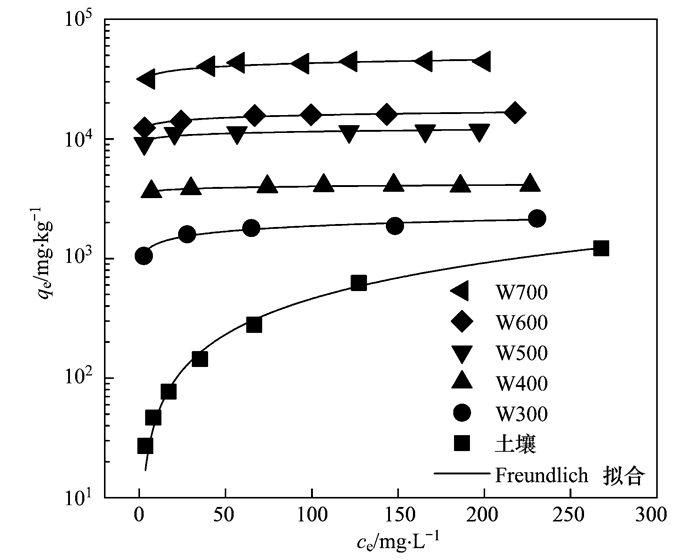
生物炭和土壤分别对CTZ的等温吸附结果用Freundlich模型拟合 (图 2和表 3).土壤对CTZ的吸附基本为线性吸附.W300~W700对CTZ的等温吸附曲线表现为明显的非线性吸附. W400~W700对CTZ的吸附量在该研究的浓度范围内变化量相对较小,表明生物炭对CTZ的吸附量已经达到饱和吸附量.
|
图 2 土壤和生物炭 (W300~W700) 对西替利嗪的等温吸附曲线 Fig. 2 Sorption isotherms of cetirizine to soil and biochars (W300-W700) in aqueous solution |
|
|
表 3 土壤、生物炭以及土壤-生物炭混合体系对CTZ等温吸附的Freundlich模型拟合参数及吸附分配系数Kd值 Table 3 Freundlich isotherm parameters and the sorption distributed coefficient (Kd) of cetirizine on soil, biochars, and biochar-soil mixtures |
生物炭对有机污染物的吸附能力受制备生物炭时的碳化温度控制[28~30],因此采用5种不同碳化温度制备的生物炭,探讨了碳化温度对生物炭性质及吸附能力的影响.从图 2可以看出,高碳化温度下制备的生物炭吸附能力最强.这与以往的研究成果相一致[31],其原因是:随着碳化温度升高,生物炭内部形成更多的孔结构且孔隙逐渐增大,比表面积和总孔隙体积增大,吸附位点增多,从而吸附能力增强[32]. 表 1数据也显示核桃壳生物炭的BET比表面积和总孔隙体积从W300~W700分别增大了268、86倍,表明生物炭对CTZ吸附能力随碳化温度的升高而增强是与其比表面积和孔隙体积的增大有关.
生物炭对CTZ的吸附能力显著强于黄绵土,且当溶液中CTZ浓度低时更为明显. 表 3计算了吸附平衡时溶液中不同浓度CTZ (ce=0.005 Sw和 ce=0.05 Sw,Sw为25℃时CTZ在水中的溶解度) 对应的Kd值,以下分别称Kd(0.005) 和Kd(0.05). W300~W700的Kd(0.005) 是黄绵土的12.48~323.6倍,因此可以添加生物炭到黄绵土中,以增强黄绵土对CTZ的吸附能力.
2.3 土壤-生物炭混合物对西替利嗪的吸附该部分探讨了向黄绵土中分别添加质量比为1%、5%、10%和20%,碳化温度300~700℃的核桃壳生物炭对CTZ吸附作用的影响.吸附平衡后溶液的pH值为7.6±0.2,与土壤吸附CTZ平衡时溶液的pH值一致.从图 3和表 3可以看出,添加W300对黄绵土吸附CTZ能力增强不明显.土壤中添加W300后,虽然总含C量从3.38%增加到14.6%,但比表面积并没有明显增大,因此对CTZ吸附能力没有明显增强.添加W400~W700可显著增强黄绵土对CTZ的吸附能力,相比土壤,20%SW400~20%SW700的Kd(0.005) 分别增大了2.56~50.5倍.添加的生物炭碳化温度越高、添加量越多,其混合体系对CTZ的吸附能力越强,等温曲线的非线性程度越大.添加生物炭后,土壤有机质含量和比表面积增大,对污染物的吸附能力增强[33].黄绵土中添加W400~W700后,比表面积和含碳量均增大 (表 2),对CTZ的吸附能力增强.因此向黄绵土中添加400~700℃碳化温度制备的核桃壳生物炭,以期减少土壤孔隙水中CTZ的浓度,降低其迁移性是可行的.

|
图 3 土壤、生物炭及添加不同质量比生物炭的土壤-生物炭混合物对CTZ的等温吸附曲线 Fig. 3 Sorption isotherms of cetirizine to soil, biochars and biochar-soil mixtures with different biochar addition mass ratios |
假设混合物对CTZ的吸附量是生物炭和土壤分别对CTZ吸附量的总和,则混合物样品对CTZ吸附分配系数的理论值按下面公式计算:
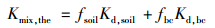
|
(4) |
式中,Kmix,the是混合物样品对CTZ吸附分配系数的理论值;Kd, soil和Kd, bc是土壤和生物炭单独存在时分别对CTZ的吸附分配系数.
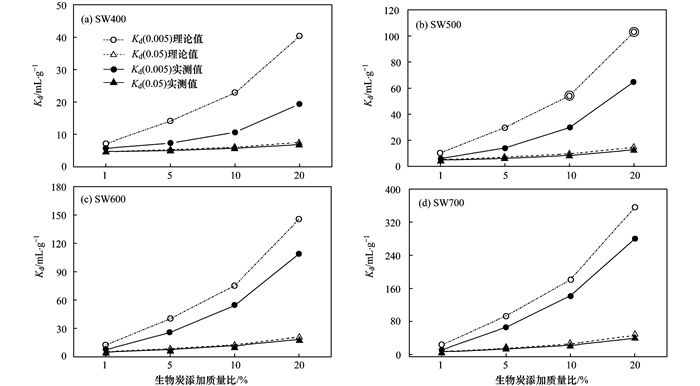
土壤-生物炭混合体系对CTZ吸附分配系数Kd(0.005) 和Kd(0.05) 的理论值与实测值并不相同 (图 4).表明混合体系对CTZ的吸附量并不是简单的生物炭和土壤单独对其吸附量的线性叠加,土壤和生物炭的组分之间发生了一定的作用[34],已经成为一个有机整体.土壤溶解性有机质可能进入生物炭表面或孔隙影响生物炭对CTZ的吸附能力,同时土壤组分会与生物炭吸附位点相互堵塞或竞争[35],使混合物对CTZ吸附能力的实测值偏低.
|
图 4 土壤-生物炭混合物对CTZ吸附分配系数[Kd(0.005) 和Kd(0.05)]理论值和实测值比较 Fig. 4 Comparison between the theoretical and experimental sorption capacity [Kd(0.005), Kd(0.05)] of CTZ by biochar-soil mixtures |
Kd(0.05) 实测值与理论值之间的差异较小,此浓度下预测混合体系吸附CTZ能力的结果较为准确.但Kd(0.005) 实测值与理论值之间的差异较大 (除生物炭添加质量比为1%),且随着生物炭添加量的增大,两者之间的差异越显著,说明生物炭与土壤组分之间的相互作用也随之更加强烈.因此当溶液中CTZ浓度相对较低,添加生物炭的量相对较高时,对混合物吸附CTZ能力的预测相对不可靠.实际应用时需要考虑生物炭和土壤组分之间的相互作用,避免高估添加生物炭后的混合体系对CTZ的吸附能力.
3 结论(1) 核桃壳生物炭吸附CTZ的能力随着其碳化温度的升高而增强;W300~W700对CTZ的吸附分配系数Kd(0.005) 分别是黄绵土的12.5~324倍,这与生物炭本身的多孔结构、比表面积大、含碳量高有关.
(2) 添加W400~W700可显著增强黄绵土对CTZ的吸附能力.且添加的生物炭碳化温度越高、添加量越多,土壤-生物炭混合体系对CTZ的吸附能力越强,这与添加生物炭后比表面积和含碳量增加有关.
(3) Kd(0.05) 实测值与理论值之间的差异较小,但对于Kd(0.005) 两者之间的差异较大 (除生物炭添加质量比为1%),且随着生物炭添加量的增大差异越显著,此时忽略土壤与生物炭组分之间的相互作用会高估混合体系对CTZ的吸附能力.
| [1] | Taheran M, Brar S K, Verma M, et al. Membrane processes for removal of pharmaceutically active compounds (PhACs) from water and wastewaters[J]. Science of the Total Environment, 2016, 547: 60–77. DOI: 10.1016/j.scitotenv.2015.12.139 |
| [2] | van Balen G P, Caron G, Ermondi G, et al. Lipophilicity behaviour of the zwitterionic antihistamine cetirizine in phosphatidylcholine liposomes/water systems[J]. Pharmaceutical Research, 2001, 18(5): 694–701. DOI: 10.1023/A:1011049830615 |
| [3] | Nödler K, Licha T, Bester K, et al. Development of a multi-residue analytical method, based on liquid chromatography-tandem mass spectrometry, for the simultaneous determination of 46 micro-contaminants in aqueous samples[J]. Journal of Chromatography A, 2010, 1217(42): 6511–6521. DOI: 10.1016/j.chroma.2010.08.048 |
| [4] | Fick J, Söderström H, Lindberg R H, et al. Contamination of surface, ground, and drinking water from pharmaceutical production[J]. Environmental Toxicology and Chemistry, 2009, 28(12): 2522–2527. DOI: 10.1897/09-073.1 |
| [5] | Bahlmann A, Carvalho J J, Weller M G, et al. Immunoassays as high-throughput tools:monitoring spatial and temporal variations of carbamazepine, caffeine and cetirizine in surface and wastewaters[J]. Chemosphere, 2012, 89(11): 1278–1286. DOI: 10.1016/j.chemosphere.2012.05.020 |
| [6] | Wennmalm Å, Gunnarsson B. Pharmaceutical management through environmental product labeling in Sweden[J]. Environment International, 2009, 35(5): 775–777. DOI: 10.1016/j.envint.2008.12.008 |
| [7] | Kosonen J, Kronberg L. The occurrence of antihistamines in sewage waters and in recipient rivers[J]. Environmental Science and Pollution Research, 2009, 16(5): 555–564. DOI: 10.1007/s11356-009-0144-2 |
| [8] | Lehmann J, Joesph S. Biochar for environmental management:science and technology[M]. London: Earthscan, 2009. |
| [9] | Tan X F, Liu Y G, Zeng G M, et al. Application of biochar for the removal of pollutants from aqueous solutions[J]. Chemosphere, 2015, 125: 70–85. DOI: 10.1016/j.chemosphere.2014.12.058 |
| [10] | Jin J, Sun K, Wu F C, et al. Single-solute and bi-solute sorption of phenanthrene and dibutyl phthalate by plant-and manure-derived biochars[J]. Science of the Total Environment, 2014, 473-474: 308–316. DOI: 10.1016/j.scitotenv.2013.12.033 |
| [11] | Li H L, Qu R H, Li C, et al. Selective removal of polycyclic aromatic hydrocarbons (PAHs) from soil washing effluents using biochars produced at different pyrolytic temperatures[J]. Bioresource Technology, 2014, 163: 193–198. DOI: 10.1016/j.biortech.2014.04.042 |
| [12] | Knauer K, Sobek A, Bucheli T D. Reduced toxicity of diuron to the freshwater green alga Pseudokirchneriella subcapitata in the presence of black carbon[J]. Aquatic Toxicology, 2007, 83(2): 143–148. DOI: 10.1016/j.aquatox.2007.03.021 |
| [13] | 吴晴雯, 孟梁, 张志豪, 等. 芦苇秸秆生物炭对水中菲和1, 1-二氯乙烯的吸附特性[J]. 环境科学, 2016, 37(2): 680–688. Wu Q W, Meng L, Zhang Z H, et al. Sorption characteristics of phenanthrene and 1, 1-dichloroethene onto reed straw biochar in aquatic solutions[J]. Environmental Science, 2016, 37(2): 680–688. |
| [14] | Beesley L, Moreno-Jiménez E, Gomez-Eyles J L. Effects of biochar and greenwaste compost amendments on mobility, bioavailability and toxicity of inorganic and organic contaminants in a multi-element polluted soil[J]. Environmental Pollution, 2010, 158(6): 2282–2287. DOI: 10.1016/j.envpol.2010.02.003 |
| [15] | Chen B L, Yuan M X. Enhanced sorption of polycyclic aromatic hydrocarbons by soil amended with biochar[J]. Journal of Soils and Sediments, 2010, 11(1): 62–71. |
| [16] | Jones D L, Edwards-Jones G, Murphy D V. Biochar mediated alterations in herbicide breakdown and leaching in soil[J]. Soil Biology and Biochemistry, 2011, 43(4): 804–813. DOI: 10.1016/j.soilbio.2010.12.015 |
| [17] | Yu X Y, Ying G G, Kookana R S. Reduced plant uptake of pesticides with biochar additions to soil[J]. Chemosphere, 2009, 76(5): 665–671. DOI: 10.1016/j.chemosphere.2009.04.001 |
| [18] | Teixidó M, Hurtado C, Pignatello J J, et al. Predicting contaminant adsorption in black carbon (biochar)-amended soil for the veterinary antimicrobial sulfamethazine[J]. Environmental Science & Technology, 2013, 47(12): 6197–6205. |
| [19] | Nham H T T, Greskowiak J, Nödler K, et al. Modeling the transport behavior of 16 emerging organic contaminants during soil aquifer treatment[J]. Science of the Total Environment, 2015, 514: 450–458. DOI: 10.1016/j.scitotenv.2015.01.096 |
| [20] | Valhondo C, Carrera J, Ayora C, et al. Characterizing redox conditions and monitoring attenuation of selected pharmaceuticals during artificial recharge through a reactive layer[J]. Science of the Total Environment, 2015, 512(512-513): 240–250. |
| [21] | Fang Q L, Chen B L, Lin Y J, et al. Aromatic and hydrophobic surfaces of wood-derived biochar enhance perchlorate adsorption via hydrogen bonding to oxygen-containing organic groups[J]. Environmental Science & Technology, 2014, 48(1): 279–288. |
| [22] | 陈有梅, 刘博, 周安宁, 等. 盐酸西替利嗪/蒙脱土纳米复合物的制备及其结构与性能[J]. 复合材料学报, 2010, 27(1): 43–50. Chen Y M, Liu B, Zhou A N, et al. Preparation, structure and properties of cetirizine hydrochloride/montmorillonite nanocomposites[J]. Acta Materiae Compositae Sinica, 2010, 27(1): 43–50. |
| [23] | Sun K, Kang M J, Ro K S, et al. Variation in sorption of propiconazole with biochars:the effect of temperature, mineral, molecular structure, and nano-porosity[J]. Chemosphere, 2016, 142: 56–63. DOI: 10.1016/j.chemosphere.2015.07.018 |
| [24] | Ding Y, Liu Y G, Liu S B, et al. Biochar to improve soil fertility. A review[J]. Agronomy for Sustainable Development, 2016, 36(2): 36. DOI: 10.1007/s13593-016-0372-z |
| [25] | Novak J M, Busscher W J, Laird D L, et al. Impact of biochar amendment on fertility of a southeastern coastal plain soil[J]. Soil Science, 2009, 174(2): 105–112. DOI: 10.1097/SS.0b013e3181981d9a |
| [26] | Liang B Q, Lehmann J, Solomon D, et al. Stability of biomass-derived black carbon in soils[J]. Geochimica et Cosmochimica Acta, 2008, 72(24): 6069–6078. DOI: 10.1016/j.gca.2008.09.028 |
| [27] | Li J F, Li S J, Dong H P, et al. Role of alumina and montmorillonite in changing the sorption of herbicides to biochars[J]. Journal of Agricultural and Food Chemistry, 2015, 63(24): 5740–5746. DOI: 10.1021/acs.jafc.5b01654 |
| [28] | Vulava V M, Cory W C, Murphey V L, et al. Sorption, photodegradation, and chemical transformation of naproxen and ibuprofen in soils and water[J]. Science of the Total Environment, 2016, 565: 1063–1070. DOI: 10.1016/j.scitotenv.2016.05.132 |
| [29] | Zheng H, Wang Z Y, Zhao J, et al. Sorption of antibiotic sulfamethoxazole varies with biochars produced at different temperatures[J]. Environmental Pollution, 2013, 181: 60–67. DOI: 10.1016/j.envpol.2013.05.056 |
| [30] | Chen B L, Chen Z M. Sorption of naphthalene and 1-naphthol by biochars of orange peels with different pyrolytic temperatures[J]. Chemosphere, 2009, 76(1): 127–133. DOI: 10.1016/j.chemosphere.2009.02.004 |
| [31] | Zhang G X, Zhang Q, Sun K, et al. Sorption of simazine to corn straw biochars prepared at different pyrolytic temperatures[J]. Environmental Pollution, 2011, 159(10): 2594–2601. DOI: 10.1016/j.envpol.2011.06.012 |
| [32] | 张振国, 蒋煜峰, 慕仲锋, 等. 生物炭对西北黄土吸附壬基酚的影响[J]. 环境科学, 2016, 37(11): 4428–4436. Zhang Z G, Jiang Y F, Mu Z F, et al. Effect of biochar on adsorption behavior of nonylphenol onto loess soil in northwest China[J]. Environmental Science, 2016, 37(11): 4428–4436. |
| [33] | Ouyang W, Zhao X C, Tysklind M, et al. Typical agricultural diffuse herbicide sorption with agricultural waste-derived biochars amended soil of high organic matter content[J]. Water Research, 2016, 92: 156–163. DOI: 10.1016/j.watres.2016.01.055 |
| [34] | Jin J, Kang M J, Sun K, et al. Properties of biochar-amended soils and their sorption of imidacloprid, isoproturon, and atrazine[J]. Science of the Total Environment, 2016, 550: 504–513. DOI: 10.1016/j.scitotenv.2016.01.117 |
| [35] | 吴蒨蒨. 生物炭增强土壤吸附阿特拉津的作用及机理[D]. 杭州: 浙江大学, 2016. Wu Q Q. Enhanced sorption of atrazine to soils amended with biochars[D]. Hangzhou:Zhejiang University, 2016. |
 2017, Vol. 38
2017, Vol. 38


