2. 南京工业大学环境学院, 南京 211816;
3. 南京沙夫特环境科技有限公司, 南京 210042
2. College of Environment, Nanjing Technology University, Nanjing 211816, China;
3. Nanjing Environmental Safety Tech Co., Ltd., Nanjing 210042, China
邻苯二甲酸酯 (PAEs),又名酞酸酯,是由两个侧链基团 (—COOR) 共享一个苯环的1, 2-苯二甲酸酯类化合物 (见表 1)[1, 2].邻苯二甲酸酯作为塑化剂,其广泛用于有机合成、塑料用品、橡胶、涂料,玩具等行业[3~6].目前全球许多国家的环境介质中普遍检出PAEs[7]. PAEs极易从各种材料或者日常用品中释放出来[8],它们可通过饮食、呼吸、或者皮肤接触暴露于人体和动物体,有多项研究报道PAEs具有毒性以及“三致效应”,例如长期暴露于PAEs可能会产生致癌以及先天性畸形的严重影响[9],且多数PAEs对动物体有明显的内分泌干扰作用,如影响男性精液质量以及内分泌系统紊乱等 (如过早发育或者发育不全,异常肥胖,孩童痴呆等)[10].
|
|
表 1 11种PAEs的理化性质 Table 1 Physical-chemical properties of 11 PAEs |
PAEs潜在的环境风险使得此类化合物受到全球的广泛关注.许多国家和组织已经采取措施控制PAEs的生产和使用,如DEHP、DBP、DEP、DMP、DOP等物质已经被美国、加拿大以及欧盟等列入优先污染物名单中[11],其中DEHP与DBP更是被美国严格禁止用于儿童玩具以及日用品.
污水处理厂 (sewage treatment plants, STP) 是PAEs向环境中排放的一个重要中转站,含PAEs的工业废水以及生活污水都要进入STP进行生化处理. PAEs在STP中的去除过程包括生物降解和污泥吸附.有研究表明,DBP和DEHP由于其较强的吸附能力,使得它们极易吸附于剩余污泥或者活性污泥颗粒中,难以进一步降解[12, 13].但是由于不同PAEs的理化性质存在差异,如PAEs的吸附系数 (lgKoc) 为1.32~5.0,生物降解潜力也不尽相同,使得PAEs在STP中的分布变得复杂.若此类物质无法在STP中有效去除,则二级出水排进地表水后势必对生态系统以及人和动物健康造成威胁,因此关注和研究PAEs在污水处理系统中的分布与归趋,对于环境风险评估以及风险防控具有重要意义.
本文参考经济合作与发展组织 (organization for economic cooperation and development, OECD) 的化学品生物降解性测试导则,首先测定了11种PAEs在环境中的快速生物降解性,然后研究了PAEs在好氧活性污泥中的降解速率和降解动力学,最后采用STP室内模拟、STP现场实测及STP模型预测相结合的方式,研究了PAEs在STP中分布、归趋及暴露水平进行了预测,以期为化学品环境暴露与风险评估提供更有效和真实的基础数据.
1 材料与方法 1.1 仪器与试剂BOD检测仪 (Oxitop OC100,WTW,德国);好氧生化污水处理模拟系统 (KLD4N/SR,德国);可控恒温培养箱 (LOVIBOND,罗威邦,德国);气相色谱串联质谱仪 (GC/MS,Agilent 7890A,安捷伦,美国);5975C三重四级杆质谱检测器 (Agilent 5975 C),毛细管色谱柱 (Agilent,30 m×0.250 mm,0.25μm).总有机碳 (TOC) 分析仪 (N/C 3100,耶拿,德国);
旋转蒸发仪 (BUCHI/R-210,瑞士);氮吹仪 (ANPEL,安谱);水质多参数电极 (HQ 40 d,哈希,美国);电子天平 (梅特勒托利多,瑞士);高速冷冻离心机 (CR22GII,日立,日本);纯水器 (Millii-Q,密里博,美国);移液器 (FINNPIPETTE,赛默飞世尔,美国);恒温磁力搅拌器 (国华,HJ-3);5804高速离心机 (Eppendorf,德国). 16通道固相萃取装置 (Waters,美国);HLB固相萃取柱 (500 mg,6cc,Waters,美国),PSA柱 (1 g,6cc;Waters,美国).
PAEs标准品 (分析纯,百灵威化学).正己烷 (色谱纯,MERCK);二氯甲烷 (色谱纯,MERCK);乙酸乙酯 (色谱纯,MERCK).
实验中的活性污泥采自南京某生活污水处理厂的曝气池.
1.2 PAEs的好氧生物降解实验 1.2.1 呼吸计量法实验 (301F)快速生物降解实验基于OECD 301F方法[14].本实验在500 mL BOD瓶中进行.向瓶中分别添加297 mL培养基,3 mL活性污泥悬浮液 (3 g·L-1) 以及约15 mg PAEs,使活性污泥浓度为30 mg·L-1,PAEs浓度为50 mg·L-1;此外,设置不含受试物的接种物空白对照,含苯甲酸钠程序对照 (苯甲酸钠作为参比物,指示污泥活性).所有瓶子在22℃±2℃下密闭恒温搅拌28 d. 28 d内的氧消耗通过BOD分析仪测定. PAEs的生物降解率R按照式 (1) 计算.
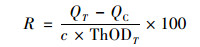
|
(1) |
式中,R为生物降解率 (%);T代表受试物;QT和QC分别为受试物和空白的氧消耗 (mg·L-1);c为受试物浓度 (mg·L-1);ThODT为受试物的理论需氧量 (mg·mg-1).
1.2.2 好氧降解动力学实验将活性污泥悬浮液 (3 g·L-1) 接种于STP模拟系统的曝气罐中,连续充氧曝气,每天加入适量合成污水驯化一个月[15].驯化结束后,将500 mL活性污泥悬浮液转移到离心瓶中,使用高速冷冻离心机 (5 000 r·min-1) 离心5 min后弃去上清液,然后用去离子水重新溶解污泥团,充分混匀分散后重复上述步骤至少3次,从而尽可能洗涤污泥中自身残留的PAEs (经过洗涤的污泥中检出的PAEs化合物浓度<5 μg·L-1).用去离子水将洁净的污泥配制成3 g·L-1的悬浮液.向其中添加11种PAEs,使得PAEs在污泥悬浮液中最终浓度为1 mg·L-1,持续搅拌培养,确保溶解氧达到2 mg·L-1以上,每隔一定时间采样并使用GC/MS方法测定36 h内污泥中PAEs变化.
使用一级动力学方程拟合PAEs浓度随时间的变化曲线,拟合公式如下:
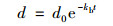
|
(2) |
式中,d为受试物在t时刻的残留率 (%), d0为受试物的初始百分比 (%); kb为速率常数 (s-1);t为时间 (h).
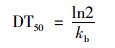
|
(3) |
式中,DT50为降解半衰期 (h).
1.3 模拟生物降解实验将活性污泥悬浮液 (3 g·L-1) 接种于生物降解模拟系统的曝气罐中,连续充氧.实验期间,含有PAEs (1 mg·L-1) 和合成污水的进水 (TOC=100 mg·L-1),以420 mL·h-1的流速进入曝气罐中,平均水力停留时间 (HRT) 约为11.2 h.当化学品去除率达到稳定后,调整进水泵转速,改变水力停留时间分别为12 h和24 h继续测试.实验期间,每天测定曝气罐中活性污泥悬浮固体的浓度,并定期去除多余的污泥,使污泥浓度稳定在3 g·L-1.
1.4 STP模型预测与分析国际针对化学品在污水处理阶段的暴露和归趋评估多采用模型预测.周林军等系统调研了我国的STP工艺和环境场景参数,应用逸度、惠特曼双阻力扩散及一级动力学降解等理论,开发了基于我国典型污水处理工艺和环境参数以及与文献[16]相匹配的C-STP (O) 预测模型[17, 18],用于评估化学品在污水处理阶段的暴露和归趋.
C-STP (O) 将初沉池、曝气池和二沉池按照水相、悬浮颗粒相、污泥相及空气相划分成9箱.模型包括输入、计算、输出这3个过程,输入参数包括化学品固有特性 (如分子量、水溶解度、logKow、蒸气压以及快速生物降解性等) 以及环境场景参数 (模型默认);模型预测生产使用过程中排放的化学品废水经由STP处理后的去除率,包括向水、大气和污泥归趋因子及生物降解去除率.
在本研究中,PAEs的lgKow、lgKoc、亨利常数、水溶解度、蒸气压数据来自OECD echemportal数据库[19],快速生物降解性数据采用2.1节的测定结果;C-STP (O) 模型场景参数使用模型默认参数.
1.5 STP现场采样以及分析 1.5.1 样品中溶解性有机碳测定取STP进水及出水各10 mL,过0.45μm滤膜,加200 μL 0.1 mol·L-1盐酸酸化去除水样中无机碳后,用TOC分析仪测定DOC,每个样品3个平行. pH、溶解氧 (DO) 以及电导率等指标使用水质多参数测定仪测定.
1.5.2 样品中目标物浓度测定水样和污泥样品从江苏淮安市某18家污水处理厂采集.水样和活性污泥均采集3 L于棕色玻璃瓶中.水样提取使用Oasis HLB (500 mg,6 mL) 固相萃取柱萃取,固相萃取柱依次用5 mL二氯甲烷、5 mL甲醇、5 mL超纯水活化;上样结束后使用10 mL二氯甲烷洗脱.将洗脱液在微弱的氮气流中吹干,最后用1 mL正己烷复溶,过0.22μm滤膜后待GC/MS分析.
将采集的活性污泥悬浮液进行离心分离,将污泥风干后研磨成粉末状,称取5.0 g污泥,使用25 mL二氯甲烷超声萃取污泥两次,每次15 min,收集合并萃取液后旋转蒸发至约1.0 mL,使用无水硫酸钠Sep-Pak PSA柱净化.水样以及活性污泥的回收率结果见表 2.
|
|
表 2 11种PAEs的回收率和相对标准偏差 (RSD) Table 2 Recovery and relative standard deviation (RSD) of eleven PAEs |
1.5.3 仪器分析方法
色谱条件:Agilent DB 1701(30 m×250μm×0.25μm) 毛细管色谱柱;流量1.5 mL·min-1,进样口温度:250℃;不分流,隔垫吹扫流量20 mL·min-1;辅助加热器:250℃.
质谱条件:离子源 (EI)230℃;MS四级杆温度150℃.
程序升温流程:60℃保持1 min,以20℃·min-1上升至180℃,保持8 min;以5℃·min-1上升至250℃,保持1 min;以25℃·min-1上升至300℃,保持5 min.
2 结果与讨论 2.1 PAEs的快速生物降解性及生物降解动力学表征采用OECD呼吸计量法 (301F) 同时测定11种邻苯二甲酸酯的快速生物降解性,各物质的生物降解曲线见图 1.从中可见,参比物苯甲酸钠在第6 d开始生物降解率达到60%,并通过10 d观察期,表明污泥活性良好,实验结果有效. 28 d期间11种PAEs发生了不同程度的降解,从表 3可知,8种PAEs 10 d观察期降解率>60%,属于快速生物降解性化学品. DNP和DHP虽然28 d生物降解率超过60%,但10 d观察期未达到60%. DPP在28 d的生物降解率只有43.5%( < 60%).

|
图 1 11种邻苯二甲酸酯的28 d生物降解曲线 Fig. 1 Biodegradation curves of eleven phthalic acid esters in a period of 28 d |
|
|
表 3 11种邻苯二甲酸酯的快速生物降解性及动力学结果 Table 3 Ready biodegradability and first-order kinetic parameter of 11 phthalic acid esters |
根据欧盟和美国的化学品快速生物降解性测试结果外推生物降解速率 (k) 的标准[20],DMP、BMEP、DEP、DBP、DIBP、DNPP、DNHP以及DEHP这8种PAEs 10 d观察期降解率>60%,则k值为0.69 h-1;DPP的k值为0.069 h-1;DNP以及DHP k值为0.23 h-1,具体数据见表 3.
在好氧降解动力学实验中,PAEs残留率随时间变化曲线见图 2. 11种PAEs的一级动力学拟合方程及k见表 3.一级动力学方程拟合相关系数r2均在0.95以上,表明PAEs在活性污泥的生物降解过程符合一级动力学. DBP、DPP、DEP以及DIBP降解速率较快,DT50均在2 h以内;DEHP降解速率相对较慢,降解半衰期DT50为27.7 h. DNPP在30 h内只降解50%,其DT50超过30 h. ZENG等[21]和郑晓英等[22]也研究了微生物对几种PAEs的降解特性,发现DMP、DEP、DNBP以及DIBP在3h内几乎能完全去除,并且降解符合一级动力学,与本研究基本相符.
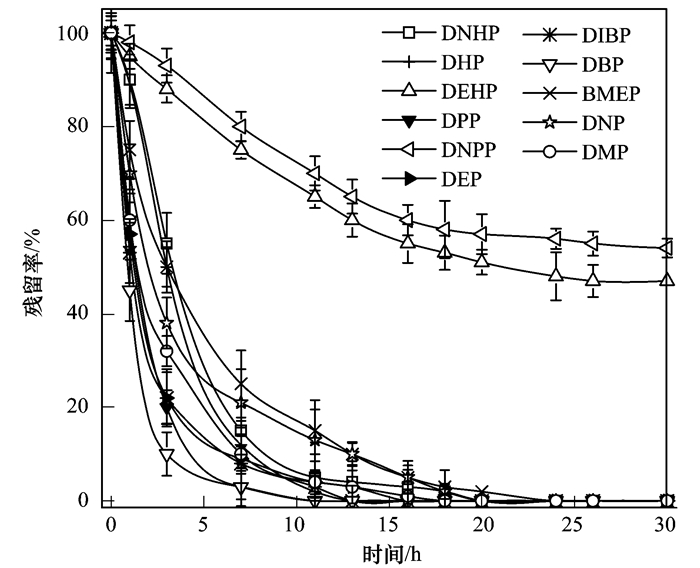
|
图 2 11种邻苯二甲酸酯的残留率随时间变化曲线 Fig. 2 Residual rate over time of eleven phthalic acid esters in kinetic test |
通过比较快速生物降解测试结果外推获得的k与污泥降解动力学实验测定的k可以发现,除DPP、DEHP和DNPP之外,其余8种PAEs两种方法得到的k值相差较小,DPP在快速生物降解测试外推得到的k为0.069 h-1,而降解动力学实验测定的k为0.79 h-1,表明在降解动力学实验中DPP降解速率较快,可能是因为污泥经过了较长时间的驯化,对DPP适应性较好. DEHP和DNPP在快速生物降解测试外推得到的k都为0.69 h-1,而降解动力学实验测定的k分别为0.03 h-1和0.02 h-1,差异产生的原因有待进一步探讨.
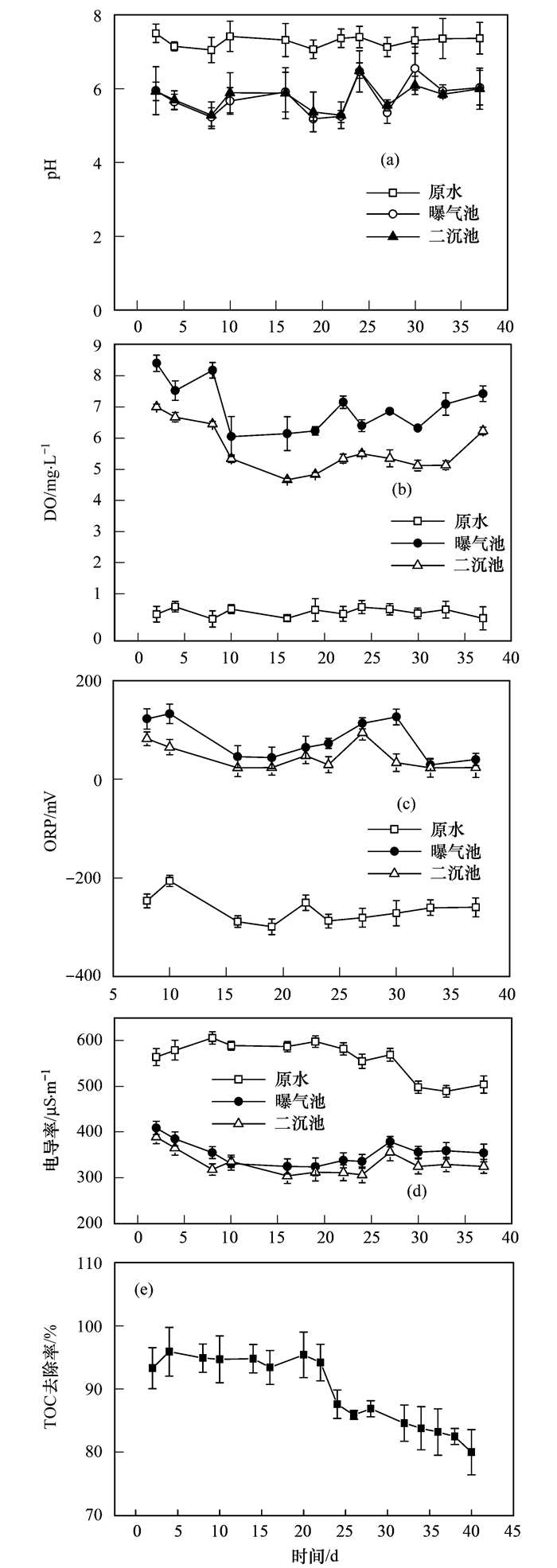
2.2 PAE在好氧污水处理系统中的去除特性在STP模拟系统运行期间,进水、曝气罐水质指标变化情况见图 3.从中可以看出进水的pH维持在6~8,适宜降解PAEs[23];溶解氧保持在4 mg·L-1以上,符合好氧生物降解条件. 37 d的运行周期内,曝气罐中ORP在29.4~132.6 mV间波动,表明活性污泥氧化性良好;二级出水电导率相比进水显著降低,表明经处理后水质明显改善,此外,出水的电导率较低暗示了邻苯二甲酸酯的降解使得水质有一定程度改善.水力停留时间为12 h (24~40 d) 和24 h (0~23 d) 时,系统TOC平均去除率在均能维持在85%、94%左右.以上信息表明,STP模拟系统运行良好.
|
图 3 STP模拟系统中各罐水质 Fig. 3 Curves of water quality parameters of each tank in STP simulated system |
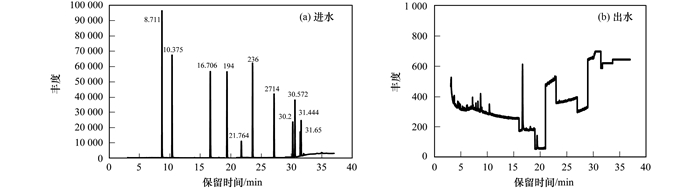
实验期间,定期采集进出水样品以及活性污泥样品,使用GC/MS测定了11种邻苯二甲酸酯类物质的残留浓度,并比较了在不同水力停留时间下目标物的去除率变化情况. 图 4为STP模拟系统中进水和出水样品的色谱图.从中可以发现PAEs在二级出水中未检出,去除效率较高.
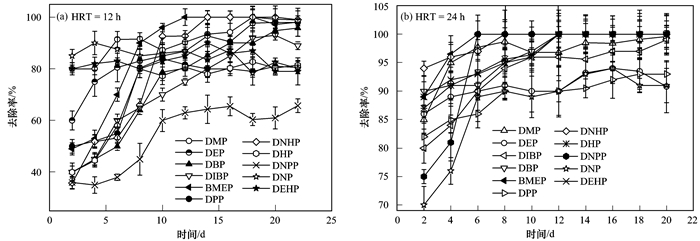
PAEs去除率随时间变化曲线见图 5.当水力停留时间为12 h的时候,DNPP生物去除率为55%~70%,其余10种PAEs在第10 d开始去除率稳定在80%以上;当水力停留时间为24 h的时候,各物质的去除速率明显提高,DNPP降解率也达到90%以上,从第12 d开始二级出水中DBP、BMEP、DNHP、DHP、DNPP、BEHP等6种物质均未检出,表明在HRT=24 h的条件下这6种PAEs能够完全去除.张娅等[24]发现在3DBER-S-Fe系统中提高水力停留时间不仅能提高PAEs化合物的去除率,而且对去除TP、TN这些指标也有很好的效果.
|
图 4 好氧污水处理模拟系统进水和出水中11种PAEs的色谱图 Fig. 4 Chromatograms of the 11 PAEs in influent and effluent of STP simulated system |
|
图 5 模拟测试中11种塑化剂在不同水力停留时间的去除曲线 Fig. 5 Removal rate over time of eleven PAEs in stimulation test |
本文采集了淮安市18乡镇污水处理厂水样,每个厂各采集进、出水以及活性污泥3 L.同时在现场记录了采样点位以及测定了部分水质参数 (pH、溶解氧、电导率以及SS),见表 4.在后续过程中对样品中PAEs浓度进行了分析,评估了PAEs在污水处理厂中的现场暴露水平,并与好氧生化污水模拟系统的测试数据以及STP模型预测结果进行了对比分析.
|
|
表 4 采样点信息以及水质常规参数 Table 4 Information of different sampling points and conventional parameters of water quality |
图 6为18家污水处理厂中进出水的DOC去除率.结果表明18家污水处理厂中有8家的DOC平均去除率低于60%,其余10家去除率均超过60%.此外,在采样过程中监测了18家污水处理厂的进出水固体悬浮物浓度SS后发现,DOC去除率 < 60%的这8家SS去除率也很低,进一步推测这8家污水处理厂运转能力存在一定问题.

|
图 6 18家乡镇污水处理厂的DOC去除率 Fig. 6 DOC removal rate of eighteen townships sewage treatment plant |
11种PAEs中,除DPP未检出外,其余10种目标物在各厂各处理工段水样中均有不同程度检出.其中DMP、DEP、DIBP、DBP以及DEHP浓度较高,原水中浓度范围分别为ND~11 038、ND~2 903、329~2 136、1 269~5 467以及160~1 067 ng·L-1,出水浓度分别为ND~44.0、ND~12.0、60.4~ 594、88.0~823和130~728 ng·L-1.以上5种物质的去除率范围分别为27.6%~100%、84.4%~100%、0%~89.3%、9.33%~96.9%以及8.98%~61.1%.这5种物质的检出率较高从侧面反映出这些化合物在日常工农业生产中的普遍性,由于采样区为经济相对较为落后的乡镇,这些污水处理厂主要位于农田、生活区,据悉当地农民秋冬季大面积种植大蒜,且他们常使用白色塑料薄膜作为幼苗的遮盖物,且PAEs化合物极易从日常用品中释放出来,因此推测原水中的大量的DMP、DBP、DEHP等物质可能来自农业种植使用的塑料薄膜、塑料废品的使用. PAEs经过释放、土壤中的淋溶以及大气沉降等一些列过程进入土壤和水体[25].未被完全去除的PAEs进入收纳水体后,可能对水生生物甚至周边人造成一定程度的不良影响.
2.4 STP模型预测与实验结果比较分析 2.4.1 PAEs在STP中的归趋预测使用C-STP (O)9箱概念模型预测了在HRT分别为12 h和24 h时11种邻苯二甲酸酯在STP中的归趋,各物质在STP模型各箱体中计算得出的分布比例见表 5.从中可以发现,水力停留时间为24 h时,PAEs化合物在STP中的去除率更高.
|
|
表 5 C-STP (O) 模型预测结果/% Table 5 Prediction results of C-STO (O) model/% |
此外,从表 5中还可知,化学品在污水处理系统中的分布同它们的理化性质有着紧密的关联,DPP、DNP和DEHP的lgKoc值最高,分别为4.12、5.67和5.08,在C-STP (O) 模型输出结果中,大约10.4%的DPP吸附于污泥,DNP有40.79%通过吸附,只有50.9%通过降解去除;而DEHP吸附15.5%,降解了77.4%. Huang等[26]认为污泥吸附作用是DEHP在STP中降解的重要机制. Zhang等[27]研究发现,河北省某河流灌溉土壤中检测到的PAEs中,DEHP与邻苯二甲酸二正丁酯 (DnBP) 占63.9%. 11种邻苯二甲酸酯的亨利系数较低,均在2.5 Pa·m3·mol-1以下,它们挥发到大气中的比例均在0.4%以下.因此除DPP、DNP以及DEHP这几种物质吸附于污泥的部分较多,其余8种物质在活性污泥中的去除主要表现为生物降解.
2.4.2 模型预测与现实的STP监测结果比较分析在不同水力停留时间下,将通过C-STP (O) 模型预测结果与好氧生化模拟测试结果及STP现场监测结果进行比较,从表 6中可知,对于PAEs的去除率,预测值和实验值除个别偏差较大 (如DPP、DNPP>20%) 外,其余去除率差异基本在20%以内,符合性较好.当HRT为24 h时,预测值和实验值偏差更小,说明提高水力停留时间,化学品在曝气池中的去除更加稳定和有效.
|
|
表 6 11种PAEs在模拟实验和C-STP (O) 中的去除率比对 Table 6 Comparison between predicted values of C-STP (O) model and simulation experiment data of eleven phthalates |
从表 6还可以发现,DMP、DEP、DBP以及DIBP这几种物质分子量较小,在污水处理厂现场采样的去除率相对较高,分别为88.2%、98.4%、73%和78.8%.其余物质分子量较大的物质去除率下降,可以初步认为,PAEs化合物在STP中的去除率随其分子量增大而减小,其化合物结构的复杂性加大了各个物质的空间位阻效应,这与前文研究结果基本一致.
BMEP、DHP、DEHP以及DNP等几种物质去除率同模型预测值偏差较大,推测可能的原因是在温度较低的冬季取样时,STP中污泥活性相对较低,因此部分化学品去除率受到影响;其次可能是因为各污水处理厂工艺设计以及运行过程中曝气池污泥浓度不同,造成部分PAEs物质去除率存在偏差.本文使用的研究模型是基于O型工艺的C-STP (O) 模型,而污水处理厂现场的处理工艺是A2/O工艺,A2/O工艺相比O型工艺多了厌氧和缺氧过程,这很可能是造成结果偏离的重要原因.此外,从这一结果可以反映出当使用STP模型预测化学品在污水处理厂归趋时的结果具有一定的保守性,这有利于对化学品进行更加科学的暴露与风险评估,使人们提高对此类化学物质的风险控制的警惕性,从而避免它们对生态系统造成不必要的伤害.
3 结论(1) 研究探讨了11种PAEs的好氧生物降解性. 11种物质在28 d内除DPP降解速率较慢以外 (降解率为43.5%),其余物质均能快速生物降解,且降解遵循一级动力学规律.
(2) 在室内模拟去除PAEs研究中发现,11种目标物在较高水力停留时间下能够更好地去除,HRT为24 h时,系统DOC去除率为93%,PAEs总的平均去除率稳定在87.5%~98.6%之间.生物降解以及吸附作用为PAEs去除的最主要原因.
(3) 污水处理厂现场样品检测结果表明,PAEs化合物能够普遍检出,尽管检出浓度较低,但是它们随污水处理厂出水排放进入收纳水体后,可能会对水生态系统造成一定程度的不良影响.
(4) 目前关于这11个物质的环境健康以及生态风险还缺乏坚实的数据支持,在后续研究中需对此类物质开展系统风险评估,并对重点流域的此类污染物进行筛查和监测,从而为此类物质的风险管理提供理论依据和数据支持.
| [1] | Oliver R, May E, Williams J. Microcosm investigations of phthalate behaviour in sewage treatment biofilms[J]. Science of the Total Environment, 2007, 372(2-3): 605–614. DOI: 10.1016/j.scitotenv.2006.10.026 |
| [2] | 张焕云, 吴卓, 戴佳佳, 等. DINP皮肤暴露对小鼠过敏性皮肤炎症的佐剂作用[J]. 中国环境科学, 2015, 35(12): 3804–3809. Zhang H Y, Wu Z, Dai J J. Adjuvant effect of skin DINP exposure on mice with allergic dermatitis[J]. China Environmental Science, 2015, 35(12): 3804–3809. DOI: 10.3969/j.issn.1000-6923.2015.12.035 |
| [3] | Net S, Sempéré R, Delmont A, et al. Occurrence, fate, behavior and ecotoxicological state of phthalates in different environmental matrices[J]. Environmental Science & Technology, 2015, 49(7): 4019–4035. |
| [4] | 蔡婧, 马明, 赵雨薇, 等. 气相色谱-三重四极杆质谱法测定有机肥中邻苯二甲酸酯[J]. 环境化学, 2015, 34(12): 2301–2303. DOI:10.7524/j.issn.0254-6108.2015.12.2015082102 |
| [5] | He J, Lv R H, Jing Z, et al. Selective solid-phase extraction of dibutyl phthalate from soybean milk using molecular imprinted polymers[J]. Analytica Chimica Acta, 2010, 661(2): 215–221. DOI: 10.1016/j.aca.2009.12.029 |
| [6] | Heudorf U, Mersch-Sundermann S, Angerer J. Phthalates:toxicology and exposure[J]. International Journal of Hygiene and Environmental Health, 2007, 210(5): 623–634. DOI: 10.1016/j.ijheh.2007.07.011 |
| [7] | Dalgaard M, Nellemann C, Lam H R, et al. The acute effects of mono (2-ethylhexyl) phthalate (MEHP) on testes of prepubertal Wistar rats[J]. Toxicology Letters, 2001, 122(1): 69–79. DOI: 10.1016/S0378-4274(01)00348-4 |
| [8] | Stales C A, Peterson D R, Parkerton T F, et al. The environmental fate of phthalate esters:a literature review[J]. Chemosphere, 1997, 35(4): 667–749. DOI: 10.1016/S0045-6535(97)00195-1 |
| [9] | Becker K, Seiwert M, Angerer J, et al. DEHP metabolites in urine of children and DEHP in house dust[J]. International Journal of Hygiene and Environmental Health, 2004, 207(5): 409–417. DOI: 10.1078/1438-4639-00309 |
| [10] | Selvaraj K K, Sundaramoorthy G, Ravichandran P K, et al. Phthalate esters in water and sediments of the Kaveri River, India:environmental levels and ecotoxicological evaluations[J]. Environmental Geochemistry and Health, 2015, 37(1): 83–96. DOI: 10.1007/s10653-014-9632-5 |
| [11] | 周文敏. 环境优先污染物[M]. 北京: 中国环境科学出版社, 1999: 11-13. |
| [12] | Amir S, Hafidi M, Merlina G, et al. Fate of phthalic acid esters during composting of both lagooning and activated sludges[J]. Process Biochemistry, 2005, 40(6): 2183–2190. DOI: 10.1016/j.procbio.2004.08.012 |
| [13] | Wang J L, Liu P, Qian Y. Biodegradation of phthalic acid esters by acclimated activated sludge[J]. Environment International, 1998, 22(6): 737–741. |
| [14] | 环境保护部化学品登记中心, 《化学品测试方法》编委会. 化学品测试方法 (降解与蓄积卷)[M]. (第二版). 北京: 中国环境出版社, 2013. 82-101. Environmental Protection Administration State. The guidelines for the testing of chemicals Guidelines for the testing of chemicals (Degradation and Accumulation) (2nd ed.)[M]. Beijing:China Environmental Press, 2013. 82-101. |
| [15] | 环境保护部化学品登记中心, 《化学品测试方法》编委会. 化学品测试方法 (生物系统效应卷)[M]. (第二版). 北京: 中国环境出版社, 2013. 73-85. Environmental Protection Administration State. The guidelines for the testing of chemicals Guidelines for the testing of chemicals (Effects on Biotic Systems) (2nd ed.)[M]. Beijing:China Environmental Press, 2013. 73-85. |
| [16] | 环境保护部办公厅. 关于征求《化学物质风险评估导则》(征求意见稿) 等两项国家环境保护标准意见的函[EB/OL]. http://www.mep.gov.cn/gkml/hbb/bgth/201109/t20110930_217940.htm,2011-09-26. |
| [17] | 周林军, 刘济宁, 石利利, 等. 好氧生化污水处理厂化学品暴露预测模型构建[J]. 环境科学, 2016, 37(1): 228–239. Zhou L J, Liu J N, Shi L L, et al. Development of chemical exposure prediction model for aerobic sewage treatment plant for biochemical wastewaters[J]. Environmental Science, 2016, 37(1): 228–239. |
| [18] | 冯洁, 周林军, 刘济宁, 等. 污水处理厂暴露模型参数及对化学品归趋的影响[J]. 生态与农村环境学报, 2015, 31(2): 262–268. Feng J, Zhou L J, Liu J N, et al. Parameters of exposure models for sewage treatment plants and their impacts on fate of chemicals[J]. Journal of Ecology and Rural Environment, 2015, 31(2): 262–268. DOI: 10.11934/j.issn.1673-4831.2015.02.019 |
| [19] | OECD. eChemPortal[DB/OL]. http://www.echemportal.org,2016-10-06. |
| [20] | US EPA. Interim guidance for using ready and inherent biodegradability tests to derive input data for multimedia models and wastewater treatment plants (WWT) models[EB/OL]. https://www.epa.gov/tsca-screening-tools/interim-guidance-using-ready-and-inherent-biodegradability-tests-derive-input-0,2016-10-06. |
| [21] | Zeng F, Cui K Y, Li X D, et al. Biodegradation kinetics of phthalate esters by Pseudomonas fluoresences FS1[J]. Process Biochemistry, 2004, 39(9): 1125–1129. DOI: 10.1016/S0032-9592(03)00226-7 |
| [22] | 郑晓英, 周玉文, 王俊安. 城市污泥中邻苯二甲酸酯的好氧降解规律研究[J]. 城市环境与城市生态, 2005, 18(6): 26–28. Zheng X Y, Zhou Y W, Wang J A. Aerobic diodegradation of phthalate esters in municipal sludges[J]. Urban Environment & Urban Ecology, 2005, 18(6): 26–28. |
| [23] | Chang B V, Wang T H, Yuan S Y. Biodegradation of four phthalate esters in sludge[J]. Chemosphere, 2007, 69(7): 1116–1123. DOI: 10.1016/j.chemosphere.2007.04.011 |
| [24] | 张娅, 郝瑞霞, 徐鹏程, 等. 3DBER-S-Fe同步脱氮除磷及去除邻苯二甲酸酯的工艺特性[J]. 环境科学, 2016, 37(11): 4268–4274. Zhang Y, Hao R X, Xu P C, et al. Operational characteristics of the simultaneous nitrogen and phosphorus removal and removal of phthalate esters by three-dimensional biofilm-electrode coupled with iron/sulfur reactor[J]. Environmental Science, 2016, 37(11): 4268–4274. |
| [25] | 李彬, 吴山, 梁金明, 等. 珠江三角洲典型区域农产品中邻苯二甲酸酯 (PAEs) 污染分布特征[J]. 环境科学, 2016, 37(1): 317–324. Li B, Wu S, Liang J M, et al. Distribution characteristics and risk assessment of Phthalic acid esters in agricultural products around the Pearl River Delta, South China[J]. Environmental Science, 2016, 37(1): 317–324. |
| [26] | Huang M H, Li Y M, Gu G W. The effects of hydraulic retention time and sludge retention time on the fate of di-(2-ethylhexyl) phthalate in a laboratory-scale anaerobic-anoxic-aerobic activated sludge system[J]. Bioresource Technology, 2008, 99(17): 8107–8111. DOI: 10.1016/j.biortech.2008.03.031 |
| [27] | Zhang Y, Liang Q, Gao R, et al. Contamination of phthalate esters (PAEs) in typical wastewater-irrigated agricultural soils in Hebei, north China[J]. PLoS One, 2015, 10(9): e0137998. DOI: 10.1371/journal.pone.0137998 |
 2017, Vol. 38
2017, Vol. 38


