2. 中国科学院生态环境研究中心饮用水科学与技术重点实验室, 北京 100085
2. Key Laboratory of Drinking Water Science and Technology, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China
铬在环境中是一种常见的重金属污染物,主要来自于电镀、制革、冶金、金属加工、油漆、印染等行业[1].在水体中,其主要以六价铬Cr (Ⅵ) 和三价铬Cr (Ⅲ) 的形态存在,由于Cr (Ⅵ) 具有致癌致畸致突变性,对人体毒性很大[2].另外,在重金属污染大量存在的同时,水环境安全也面临着有机污染物大量排放的潜在威胁,主要特点是量大、成分复杂多变、毒性大、不易处理等[3].在实际电镀废水中,Cr (Ⅵ) 往往与多种有机污染物共存.因此,探讨能够协同去除多种不同污染物的新技术新方法很有必要.
光催化技术利用廉价的太阳能,常温常压就能去除水中污染物,且无二次污染,近年来发展成为一种理想的环境治理技术[4, 5].石墨相氮化碳 (g-C3N4) 是一种新型非金属半导体光催化剂,仅由C和N两种元素组成,使其较其它金属光催化剂具有明显优势,同时该材料带隙窄 (2.7 eV),稳定性好,结构和性能易于调控,是颇具应用前景的可见光催化剂[6],被广泛应用于有机物合成、光降解有机污染物、光解水制氢等各类反应中[7~9]. Ai等[10]利用g-C3N4实现了水体中有机污染物的降解,Ong等[11]利用卤化银与g-C3N4的复合材料将CO2还原为CH4燃料.但是,对于氮化碳协同光催化的研究却相对较少[12].因此,本文以Cr (Ⅵ) 和磺基水杨酸 (SSA) 为模拟污染物,以热解法制备的g-C3N4为光催化剂,开展了协同光催化还原Cr (Ⅵ) 及氧化有机污染物的研究.
1 材料与方法 1.1 实验试剂三聚氰胺[C3N3(NH2)3,99%]购于百灵威科技有限公司;铬酸钾 (K2CrO4)、磺基水杨酸 (C7H6O6S ·2H2O,SSA)、丙酮 (CH3COCH3) 均为分析纯,购于国药集团化学试剂有限公司;二苯碳酰二肼 (C13H14N4O,分析纯) 购于Sigma-Aldrich公司;乙腈 (C2H3N) 为色谱纯.实验用水均为去离子水.
1.2 材料制备热解有机物法利用含氮前驱体受热自身发生缩聚过程来制备氮化碳,是近年来使用最为广泛的制备方法[13~15].具体方法:取一定质量的三聚氰胺置于清洁的坩埚中,加上盖子后放在马弗炉中,以5 ℃ ·min-1的升温速率升至550℃灼烧4 h,自然冷却至室温,得到淡黄色粉末即为石墨相氮化碳 (g-C3N4),研磨成细小微粒备用.
1.3 材料表征采用德国Bruker D8型X射线粉末衍射仪 (XRD) 测定催化剂的晶体结构;采用日本Hitachi H-800型透射电子显微镜 (TEM) 观察催化剂的微观形貌;采用美国Varian Gary 5000型紫外-可见-近红外分光光度计测定氮化碳的紫外可见漫反射光谱 (UV-vis DRS).
1.4 光催化实验方法以Cr (Ⅵ) 和磺基水杨酸 (SSA) 为模拟污染物,考察所制备g-C3N4的催化性能.室温下,将一定质量的g-C3N4投加到100 mL一定浓度比的Cr (Ⅵ) 和SSA混合溶液中,用HCl (0.2 mol ·L-1) 和NaOH (0.1 mol ·L-1) 调节pH,黑暗中搅拌2 h使催化剂与污染物达到吸附-解吸平衡,然后将反应器放在300 W氙灯 (北京中教金源CEL-HXF300型) 下,模拟可见光进行光催化实验,同时循环冷凝水降温.光照过程中,每隔一段时间取样,经0.45 μm的滤膜过滤,用美国Agilent 1260型高效液相色谱 (HPLC) 测定SSA的浓度[16],测定条件为:HYPERSIL C18柱 (250 mm×4.6 mm,5 μm;美国Thermo),检测波长296 nm;流动相为乙腈:水 (40:60),进样量为20 μL,流速为0.8 mL ·min-1.用GB 7467-87二苯碳酰二肼分光光度法测Cr (Ⅵ) 浓度[17],用电感耦合等离子光谱法 (ICP) 测总Cr浓度.光催化效率用c/c0表示,c0代表污染物初始浓度 (mg ·L-1),c代表各取样时间点污染物浓度 (mg ·L-1).
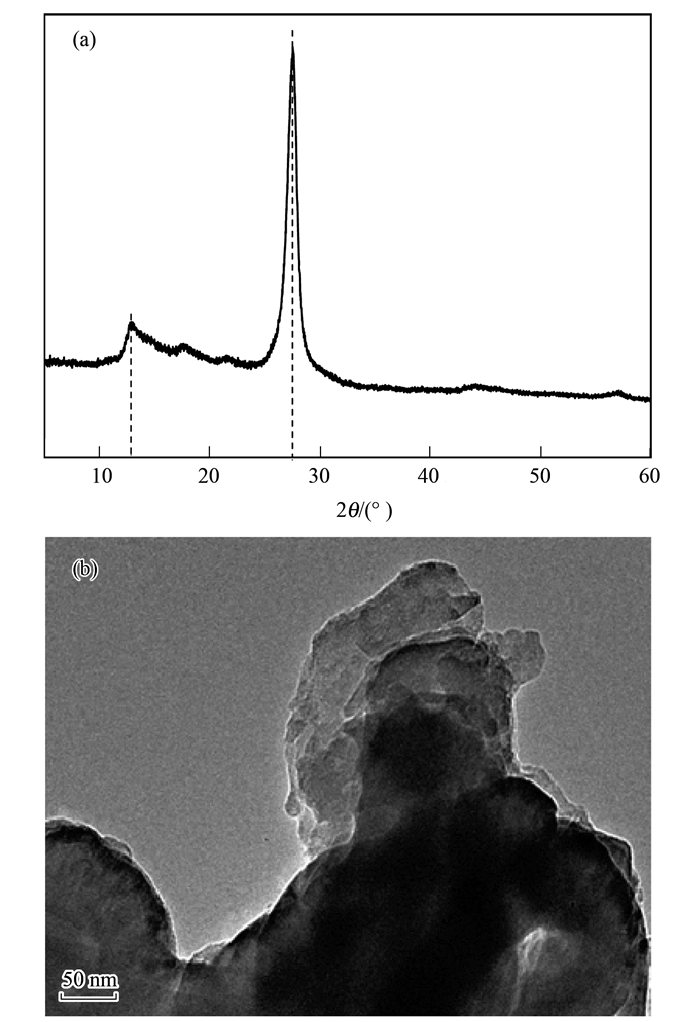
2 结果与讨论 2.1 氮化碳表征通过XRD测定g-C3N4的晶体结构,如图 1(a)所示.可以看到XRD谱图中有两个明显的特征峰. 27.5°出现的强峰是氮化碳层间堆积面 (002) 的特征峰,相对应的层间距为0.326 nm.另一个在13.1°的峰是氮化碳s-三嗪结构形成平面 (100) 的特征峰. g-C3N4的微观形貌通过TEM观察,由图 1(b)可知,g-C3N4呈现无定型的片状结构,且边缘具有折叠层状堆积,表面比较平滑.由此可得,所制备的g-C3N4具有很好的类石墨结构,这与文献[18~20]相符.
|
(a) g-C3N4的XRD谱图;(b) g-C3N4的TEM图 图 1 g-C3N4材料表征 Fig. 1 Characterization of g-C3N4 materials |
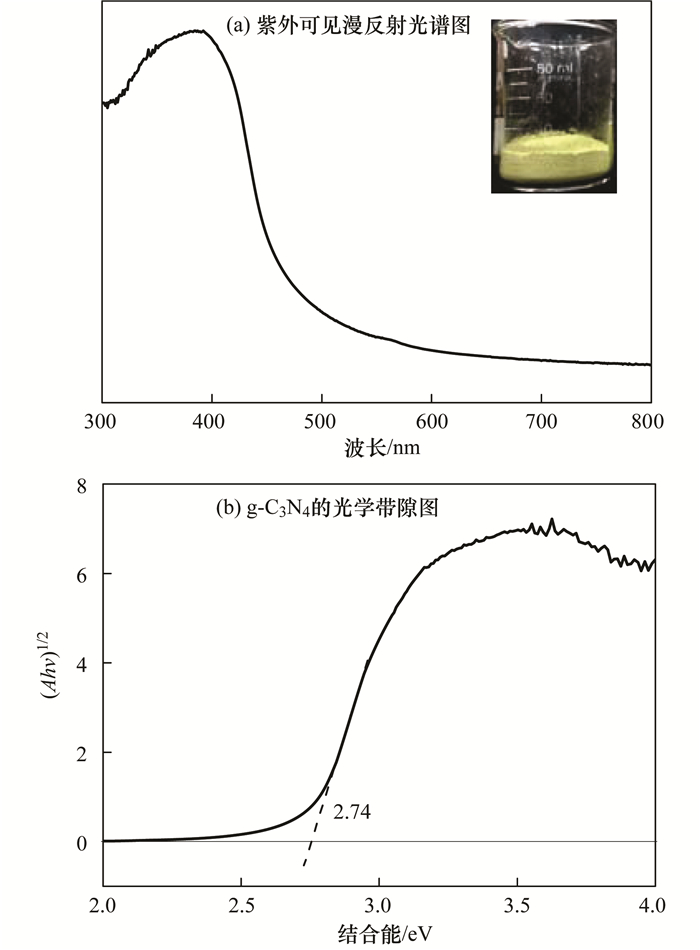
对于半导体光催化剂,光学性质是非常重要的,它可以用来评估催化剂的光吸收能力. 图 2(a)是g-C3N4的紫外可见漫反射光谱图,从中可知它的最大吸收边大约在465 nm,正与所制备出材料[图 2(a)中照片]淡黄色所对应的吸收波长一致.由 (Ahν)1/2对hν作图[图 2(b)]计算得出g-C3N4半导体催化剂的光学带隙为2.74 eV.由DRS图谱结果可知,g-C3N4光学带隙较窄,对可见光有良好的吸收和转化性能.
|
图 2 g-C3N4的光学性质图 Fig. 2 Optical properties of g-C3N4 |
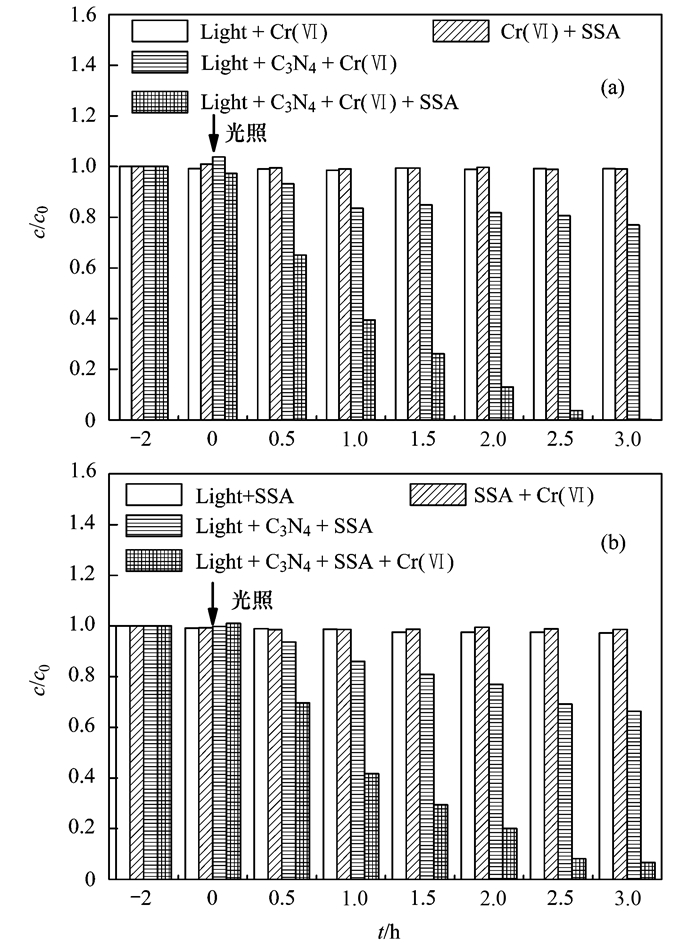
对比研究了g-C3N4光催化还原Cr (Ⅵ)、光催化降解SSA和协同光催化还原Cr (Ⅵ) 及降解SSA的效果,实验结果如图 3所示.黑暗状态吸附-解吸实验表明,催化剂表面吸附对污染物去除的影响可忽略不计.由图可知,不加催化剂直接光照时,Cr (Ⅵ) 不会被还原,SSA也不会被降解;不加催化剂也无光照条件下,Cr (Ⅵ) 和SSA之间并无反应发生;单独还原Cr (Ⅵ) 或单独降解SSA时,g-C3N4对污染物有一定的去除效果,光照3 h后有20%~30%的污染物被还原或被去除;而协同光催化反应中,3 h后Cr (Ⅵ) 和SSA的处理效率可分别达到98.9%和93.4%,是单独光催化反应的3倍以上.由此可见,酸性环境中,通过协同光催化反应可大大提高g-C3N4光催化处理污染物的能力.这是由于光还原和光氧化的同步进行促进了光生电子和空穴的分离,从而加速了电子向电子受体Cr (Ⅵ) 的转移,也提高了空穴的利用率,进一步产生更多的活性自由基,提高了Cr (Ⅵ) 的还原和SSA的降解[12, 21].
|
(a) g-C3N4光催化还原Cr (Ⅵ) 性能评价;(b) g-C3N4光催化氧化SSA性能评价;g-C3N4投加量0.5 g ·L-1,Cr (Ⅵ) 浓度10 mg ·L-1,SSA浓度40 mg ·L-1,pH=2 图 3 g-C3N4光催化性能 Fig. 3 hotocatalytic performance of g-C3N4 |
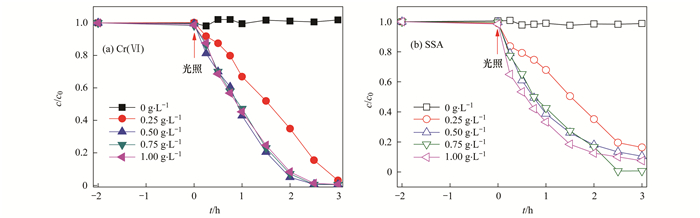
不同g-C3N4投加量对协同光催化效果的影响见图 4.从中可知,光照3 h后,Cr (Ⅵ) 和SSA的处理效果随着催化剂投加量的增加而提高,投加量达到0.5 g ·L-1时,Cr (Ⅵ) 和SSA的去除率最大分别为99.4%和90.5%.这是因为催化剂投加量的增加提高了光生电子和空穴的数量,有利于Cr (Ⅵ) 的还原和SSA的降解.但是催化剂的投加量大于0.5 g ·L-1,处理效果却没有进一步提高,这是因为投加量过大,一定程度上光遮挡效应阻碍了催化剂表面对光的吸收,另一方面投加量过大相应的也增加了光生电子和空穴的复合位点[22],催化剂表面载流子分离与复合达到平衡,反而不利于协同光催化效果.因此,为了合理有效地利用材料,催化剂投加量要控制在合适范围内.
|
Cr (Ⅵ) 浓度10 mg ·L-1,SSA浓度40 mg ·L-1,pH=2 图 4 g-C3N4投加量对协同光催化效果影响 Fig. 4 Effect of the addition amount of g-C3N4 on the simultaneous photocatalysis efficiency |
不同初始pH条件下g-C3N4协同光催化效果见图 5.从中可知,光照反应3 h后,随着pH的降低,即酸性越强协同光催化效果越好.这是因为溶液的pH会影响催化剂的表面电荷形态,酸性条件下氮化碳带正电,而Cr (Ⅵ) 在溶液中以CrO42-负离子团的形式存在,增加了二者之间的静电吸附作用力,有利于光催化还原反应的发生[23];另一方面酸性条件也会促进光载流子与溶液中的H+或O2反应,从而产生更多的活性自由基 (O2·-和·OH),有利于光催化氧化反应的进行[24].

|
g-C3N4投加量0.5 g ·L-1,Cr (Ⅵ) 浓度10 mg ·L-1,SSA浓度40 mg ·L-1 图 5 初始pH对协同光催化效果影响 Fig. 5 Effect of the initial pH on the simultaneous photocatalysis efficiency |
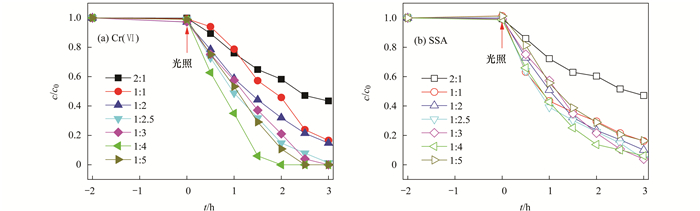
不同初始污染物浓度比[Cr (Ⅵ) :SSA]条件下g-C3N4协同光催化效果见图 6.从中可知,随着初始Cr (Ⅵ) 与SSA浓度比的增加,光催化反应速率逐渐加快,当浓度比为1 :4时,1.5 h光照后,Cr (Ⅵ) 的还原率便可达到99.4%,SSA的降解效率也可达到74.9%.这是因为SSA作为电子给体,其浓度增大可以及时与空穴反应,空穴的有效消耗促进了光生电子-空穴的分离,提高协同光催化效率.当Cr (Ⅵ) 与SSA初始浓度比为1 :5时,光催化反应效率反而降低了,此时Cr (Ⅵ) 与光生电子的反应达到最大平衡,多余的电子很容易与空穴复合,不利于SSA的降解.
|
g-C3N4投加量0.5 g ·L-1,pH=2,Cr (Ⅵ) 浓度均10 mg ·L-1 图 6 初始污染物浓度比对协同光催化效果影响 Fig. 6 Effect of initial contaminant concentration ratio on the simultaneous photocatalysis efficiency |
通过以上实验结果分析可知,室温下,当催化剂投加量为0.5 g ·L-1,pH=2,初始Cr (Ⅵ) 与SSA浓度比为1 :4(10 mg ·L-1 :40 mg ·L-1) 时,光生电子与空穴能够很好地分离和利用,Cr (Ⅵ) 的光还原和SSA的光氧化率最高,g-C3N4的协同光催化效果也达到最优.
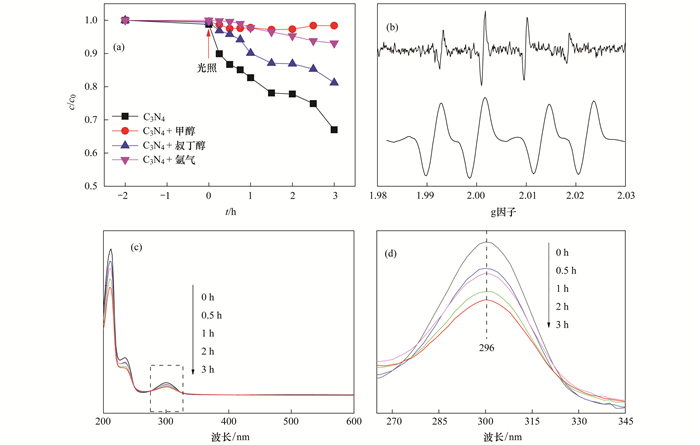
2.6 协同光催化机制为了研究g-C3N4协同光催化反应机制,考察了不同自由基淬灭剂对g-C3N4光催化氧化SSA和光催化还原Cr (Ⅵ) 的影响.研究发现,甲醇可作为空穴淬灭剂,叔丁醇可作为·OH淬灭剂,通氩气制造无氧环境可抑制O2·-的产生[25, 26].由图 7(a)可以看出,不加任何淬灭剂时,SSA的氧化率为33%;当在反应溶液中加入叔丁醇后,光照3小时后,SSA的氧化率与不加叔丁醇相比降低了14%左右,为18.8%;向反应溶液通入氩气时,SSA的氧化率也明显降低,仅为7%;当在反应溶液中加入甲醇后,SSA的氧化率显著降低,甚至几乎无降解.此结果表明,g-C3N4光催化降解SSA反应体系中,·OH、O2·-和空穴自由基均起到了活性氧化作用,其中空穴占主导地位.为了进一步验证该结论,以DMPO作为捕获剂,使用电子自旋共振波谱 (ESR) 测量活性氧化自由基,如图 7(b)所示,水溶液反应体系中,一条强度比为1 :2 :2 :1的四线ESR信号清晰可见,此信号是·OH的特征峰[27].另外,甲醇反应体系中,检测到一条强度比为1 :1 :1 :1的四线ESR信号,此信号是O2·-的特征峰[28],此实验结果验证了上述自由基淬灭实验.另外,采用紫外-可见分光度法 (UV-vis) 对SSA的降解路径进行分析,如图 7(c)所示,从中可知,除了SSA的吸收峰外,没有出现新的吸收峰,并且随着光催化的进行,SSA在296 nm处的特征吸收峰高逐渐衰减,即浓度逐渐降低[图 7(d)].这表明光催化过程中SSA降解路径更倾向于直接矿化,生成其他小分子有机物中间体的几率较低.
|
g-C3N4投加量0.5 g ·L-1,pH=2,SSA浓度均40 mg ·L-1,无Cr (Ⅵ),淬灭剂体积浓度为4% 图 7 g-C3N4光催化氧化SSA反应机制 Fig. 7 Reaction mechanism of g-C3N4 in the photocatalysis oxidation of SSA |
图 8(a)是Cr (Ⅵ) 的自由基淬灭实验结果及光催化过程总Cr含量测定.从中可知,光照3 h后Cr (Ⅵ) 的还原率为29%,向反应溶液中通入氩气抑制O2·-时,Cr (Ⅵ) 的还原率仅仅降低了4%左右,说明Cr (Ⅵ) 的还原主要由光生电子起作用.光催化开始时,没有明显的ESR信号,光催化结束时,在1.979处可以检测到一条明显的ESR信号峰[图 8(b)],此信号是Cr (Ⅲ) 的特征峰,表明Cr (Ⅵ) 最终被还原成Cr (Ⅲ)[12].电感耦合等离子光谱仪 (ICP) 检测总Cr结果显示,光催化还原过程中总Cr量没有发生明显变化,表明吸附沉着于g-C3N4表面的Cr可以忽略,对g-C3N4进一步的光催化反应影响较小.

|
g-C3N4投加量0.5 g ·L-1,pH=2,Cr (Ⅵ) 浓度均10 mg ·L-1,无SSA 图 8 g-C3N4光催化还原Cr (Ⅵ) 反应机制 Fig. 8 Reaction mechanism of g-C3N4 in the photocatalysis reduction of Cr (Ⅵ) |
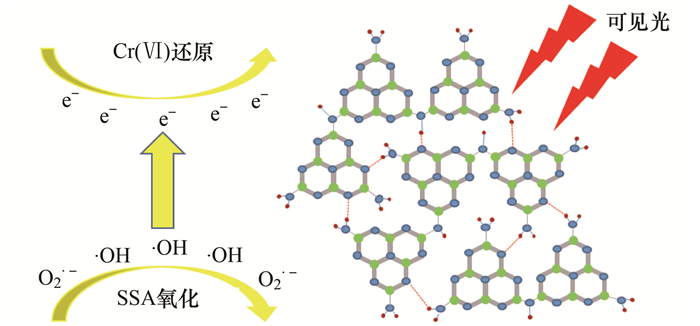
通过以上分析,g-C3N4协同光催化反应机制如图 9所示.在可见光激发下,光生电子与空穴分离并迅速去还原Cr (Ⅵ),同时光载流子与溶液中的H+或O2生成·OH和O2·-自由基,与空穴共同参与SSA的氧化降解.
|
图 9 g-C3N4同步光催化反应示意 Fig. 9 Schematic illustration of g-C3N4 simultaneous photocatalysis |
(1) 利用热解三聚氰胺法成功制备了石墨相氮化碳 (g-C3N4) 光催化剂,该材料对可见光有很好的吸收能力.
(2) 催化剂投加量为0.5 g ·L-1,pH=2,初始Cr (Ⅵ) 与SSA浓度比为1 :4(10 mg ·L-1 :40 mg ·L-1) 时,g-C3N4协同光催化还原Cr (Ⅵ) 及氧化SSA反应达到最优,比单独光还原Cr (Ⅵ) 或光氧化SSA的反应效率提高了3倍以上,此时Cr (Ⅵ) 的还原率为98.9%,SSA的氧化率为93.4%.
(3) 协同光催化体系中,Cr (Ⅵ) 被光生电子还原为Cr (Ⅲ),SSA被O2·-、空穴和·OH共同作用氧化.
| [1] | Sun M, Yan Q, Yan T, et al. Facile fabrication of 3D flower-like heterostructured g-C3N4/SnS2 composite with efficient photocatalytic activity under visible light[J]. RSC Advances, 2014, 4(59): 31019–31027. DOI: 10.1039/C4RA03843F |
| [2] | 王谦, 李延, 孙平, 等. 含铬废水处理技术及研究进展[J]. 环境科学与技术, 2013, 36(12M): 150–156. Wang Q, Li Y, Sun P, et al. The treatment technology and research progress of hexavalent chromium-containing wastewater[J]. Environmental Science & Technology, 2013, 36(12M): 150–156. |
| [3] | 刘文利. 北方某市饮用水体有机物污染状况研究[J]. 工业安全与环保, 2007, 33(8): 19–20. Liu W L. Study on organic compound pollution status of drinking water in one city of North China[J]. Industrial Safety and Environmental Protection, 2007, 33(8): 19–20. |
| [4] | Li G Y, Nie X, Gao Y P, et al. Can environmental pharmaceuticals be photocatalytically degraded and completely mineralized in water using g-C3N4/TiO2 under visible light irradiation?-Implications of persistent toxic intermediates[J]. Applied Catalysis B:Environmental, 2016, 180: 726–732. DOI: 10.1016/j.apcatb.2015.07.014 |
| [5] | Zhang H, Zhao L X, Geng F L, et al. Carbon dots decorated graphitic carbon nitride as an efficient metal-free photocatalyst for phenol degradation[J]. Applied Catalysis B:Environmental, 2016, 180: 656–662. DOI: 10.1016/j.apcatb.2015.06.056 |
| [6] | 楚增勇, 原博, 颜廷楠. g-C3N4光催化性能的研究进展[J]. 无机材料学报, 2014, 29(8): 785–794. Chu Z Y, Yuan B, Yan T N. Recent progress in photocatalysis of g-C3N4[J]. Journal of Inorganic Materials, 2014, 29(8): 785–794. DOI: 10.15541/jim20130633 |
| [7] | Liang F F, Zhu Y F. Enhancement of mineralization ability for phenol via synergetic effect of photoelectrocatalysis of g-C3N4 film[J]. Applied Catalysis B:Environmental, 2016, 180: 324–329. DOI: 10.1016/j.apcatb.2015.05.009 |
| [8] | Zhao Y K, Tang R R, Huang R. Palladium supported on graphitic carbon nitride:an efficient and recyclable heterogeneous catalyst for reduction of nitroarenes and Suzuki coupling reaction[J]. Catalysis Letters, 2015, 145(11): 1961–1971. DOI: 10.1007/s10562-015-1600-x |
| [9] | Zhang J S, Zhang G G, Chen X F, et al. Co-monomer control of carbon nitride semiconductors to optimize hydrogen evolution with visible light[J]. Angewandte Chemie International Edition, 2012, 51(13): 3183–3187. DOI: 10.1002/anie.v51.13 |
| [10] | Ai B, Duan X G, Sun H Q, et al. Metal-free graphene-carbon nitride hybrids for photodegradation of organic pollutants in water[J]. Catalysis Today, 2015, 258: 668–675. DOI: 10.1016/j.cattod.2015.01.024 |
| [11] | Ong W J, Putri L K, Tan L L, et al. Heterostructured AgX/g-C3N4 (X=Cl and Br) nanocomposites via a sonication-assisted deposition-precipitation approach:emerging role of halide ions in the synergistic photocatalytic reduction of carbon dioxide[J]. Applied Catalysis B:Environmental, 2016, 180: 530–543. DOI: 10.1016/j.apcatb.2015.06.053 |
| [12] | Hu X F, Ji H H, Chang F, et al. Simultaneous photocatalytic Cr (Ⅵ) reduction and 2, 4, 6-TCP oxidation over g-C3N4 under visible light irradiation[J]. Catalysis Today, 2014, 224: 34–40. DOI: 10.1016/j.cattod.2013.11.038 |
| [13] | Wang Y, Wang X C, Antonietti M. Polymeric graphitic carbon nitride as a heterogeneous organocatalyst:from photochemistry to multipurpose catalysis to sustainable chemistry[J]. Angewandte Chemie International Edition, 2012, 51(1): 68–89. DOI: 10.1002/anie.201101182 |
| [14] | Wang Y Y, Ibad M F, Kosslick H, et al. Synthesis and comparative study of the photocatalytic performance of hierarchically porous polymeric carbon nitrides[J]. Microporous and Mesoporous Materials, 2015, 211: 182–191. DOI: 10.1016/j.micromeso.2015.02.050 |
| [15] | Dong G H, Ho W, Li Y H, et al. Facile synthesis of porous graphene-like carbon nitride (C6N9H3) with excellent photocatalytic activity for NO removal[J]. Applied Catalysis B:Environmental, 2015, 174-175: 477–485. DOI: 10.1016/j.apcatb.2015.03.035 |
| [16] | Wang C, Zhang X H, Liu H, et al. Reaction kinetics of photocatalytic degradation of sulfosalicylic acid using TiO2 microspheres[J]. Journal of Hazardous Materials, 2009, 163(2-3): 1101–1106. DOI: 10.1016/j.jhazmat.2008.07.064 |
| [17] | GB 7467-1987, 水质六价铬的测定二苯碳酰二肼分光光度法[S]. |
| [18] | Sun J H, Zhang J S, Zhang M W, et al. Bioinspired hollow semiconductor nanospheres as photosynthetic nanoparticles[J]. Nature Communications, 2012, 3: 1139. |
| [19] | Lv H L, Ji G B, Yang Z H, et al. Enhancement photocatalytic activity of the graphite-like C3N4 coated hollow pencil-like ZnO[J]. Journal of Colloid and Interface Science, 2015, 450: 381–387. DOI: 10.1016/j.jcis.2015.03.038 |
| [20] | 孟雅丽, 陈丹, 宋文乔, 等. 类石墨结构氮化碳的合成及其应用[J]. 广州化工, 2010, 38(8): 91–93. Meng Y L, Chen D, Song W Q, et al. Chemical synthesis and application of graphitic carbon nitrides[J]. Guangzhou Chemical Industry, 2010, 38(8): 91–93. |
| [21] | 刘晴, 喻泽斌, 张睿涵, 等. 钯掺TiO2光催化降解全氟辛酸[J]. 环境科学, 2015, 36(6): 2138–2146. Liu Q, Yu Z B, Zhang R H, et al. Photocatalytic degradation of perfluorooctanoic acid by Pd-TiO2 photocatalyst[J]. Environmental Science, 2015, 36(6): 2138–2146. |
| [22] | Gu Q, Gao Z W, Zhao H A, et al. Temperature-controlled morphology evolution of graphitic carbon nitride nanostructures and their photocatalytic activities under visible light[J]. RSC Advances, 2015, 5(61): 49317–49325. DOI: 10.1039/C5RA07284K |
| [23] | 许文泽, 杨春风, 李静, 等. 二氧化钛光催化氧化阿散酸[J]. 环境科学, 2016, 37(1): 193–197. Xu W Z, Yang C F, Li J, et al. Photocatalytic oxidation of p-arsanilic acid by TiO2[J]. Environmental Science, 2016, 37(1): 193–197. |
| [24] | Zhang Y C, Zhang Q, Shi Q W, et al. Acid-treated g-C3N4 with improved photocatalytic performance in the reduction of aqueous Cr (Ⅵ) under visible-light[J]. Separation and Purification Technology, 2015, 142: 251–257. DOI: 10.1016/j.seppur.2014.12.041 |
| [25] | Chen S F, Hu Y F, Meng S G, et al. Study on the separation mechanisms of photogenerated electrons and holes for composite photocatalysts g-C3N4-WO3[J]. Applied Catalysis B:Environmental, 2014, 150-151: 564–573. DOI: 10.1016/j.apcatb.2013.12.053 |
| [26] | 王冉, 周雪峰, 胡学香, 等. Cu2O-Ag-AgBr/MA可见光催化剂的制备及其降解2-氯苯酚的研究[J]. 环境科学, 2014, 35(9): 3417–3421. Wang R, Zhou X F, Hu X X, et al. Synthesis of Cu2O-Ag-AgBr/MA visible photocatalyst and its performance in degradation of 2-chlorophenol[J]. Environmental Science, 2014, 35(9): 3417–3421. |
| [27] | Sun H Q, Zhou G L, Wang Y X, et al. A new metal-free carbon hybrid for enhanced photocatalysis[J]. ACS Applied Materials & Interfaces, 2014, 6(19): 16745–16754. |
| [28] | Hong Y Z, Jiang Y H, Li C S, et al. In-situ synthesis of direct solid-state Z-scheme V2O5/g-C3N4 heterojunctions with enhanced visible light efficiency in photocatalytic degradation of pollutants[J]. Applied Catalysis B:Environmental, 2016, 180: 663–673. DOI: 10.1016/j.apcatb.2015.06.057 |
 2017, Vol. 38
2017, Vol. 38


