2. 苏州科技大学环境生物技术研究所, 苏州 215009
2. Institute of Environmental Biotechnology, Suzhou University of Science and Technology, Suzhou 215009, China
相对于传统的硝化反硝化脱氮技术,全程自养脱氮工艺(completely autotrophic nitrogen removal over nitrite,CANON)[1, 2]以其无添加碳源、 脱氮速率高、 污泥产率低、 节约能源等优点[3, 4]越来越受到人们的关注.CANON工艺是在同一反应器中通过好氧氨氧化菌(AOB)和厌氧氨氧化菌(AnAOB)的协同作用达到自养脱氮的目的,AOB利用溶解氧把部分NH4+氧化为NO2-,AnAOB利用剩余的NH4+和生成的NO2-通过厌氧氨氧化技术进行脱氮[5].在这个过程中,提供溶解氧是实现亚硝化产生NO2-的前提,但是溶解氧同时也会对AnAOB产生抑制作用[6, 7],并且有很多研究者报道由于溶解氧的原因造成硝化菌(NOB)快速增值,使得出水NO3-过高[8, 9].
另外,不同的研究者[10, 11]对CANON工艺的研究发现反应器所需要控制的DO大小存在非常大的差别(0.1~2.53mg·L-1),即使在同样的DO条件下,脱氮效果也会由于AOB活性、 污泥颗粒大小、 NH4+浓度大小等因素而出现明显的波动[9].所以,对DO的有效控制,尤其是低氨氮废水,是实现CANON工艺稳定运行的关键因素.
目前的CANON工艺主要是以压缩空气曝气形式提供溶解氧[12, 13],但是这种供气方式受曝气设备、 曝气管深度、 反应器类型、 填料种类、 污泥形态等因素影响[14],不容易控制溶解氧浓度,易造成NOB的增殖以及AnAOB的抑制,在反应器稳定运行方面存在着一定的欠缺.本实验的目的是研究利用CANON工艺以出水复氧回流的方式处理低氨氮废水的可行性,并对启动及运行过程特性进行分析,以期为CANON工艺处理低氨氮废水提供一个新的运行模式.
1 材料与方法 1.1 接种污泥及配水接种污泥为本课题组培养的成熟的亚硝酸盐型厌氧氨氧化颗粒污泥(粒径1.0~1.5 mm)和部分取自运行稳定的亚硝化反应器中成熟的絮体亚硝化污泥(粒径0.3~0.6 mm),原厌氧氨氧化反应器中脱氮速率为3.5 kg·(m3·d)-1,原亚硝化反应器NH4+-N转化速率为2.1 kg·(m3·d)-1.进水采用人工配水,NO2-按需投加,NH4+以NH4HCO3形式提供,另外添加0.5mol·L-1的NaHCO3维持合适的pH值.基本培养液成分KH2PO4为27mg·L-1,CaCl2为138mg·L-1,MgCl2·6H2O为200mg·L-1,微量元素Ⅰ为1.0 mL·L-1,微量元素Ⅱ为1.25 mL·L-1.微量元素Ⅰ组成: EDTA 5 000mg·L-1,MgCl2·6H2O 5 000mg·L-1.微量元素Ⅱ的组成如表 1所示.
|
|
表 1 微量元素Ⅱ 的组成 Table 1 Composition of trace element Ⅱ |
1.2 连续流实验装置
采用上流式污泥床反应器,如图 1.

|
图 1 实验装置示意 Fig. 1 Schematic diagram of experimental device |
总体积V为0.2 L,下段直径为φ 16 mm,上段直径为φ 20 mm,总高度80 cm,出水口距底部76 cm.由蠕动泵从底部进水,上清液的出水溢流跌入复氧池,在溢流下跌以及复氧池表面扰动过程达到出水复氧的效果,复氧池内的溶解氧基本处于饱和状态,然后经蠕动泵回流至反应器,向反应器内提供溶解氧,反应器的最终出水通过复氧池自然溢出.
1.3 条件控制分别接种成熟的亚硝化污泥20 mL、 厌氧氨氧化污泥30 mL,污泥体积分数25%.原位测定接种污泥的AOB和AnAOB活性.反应器外部用遮光布遮盖避光,避免光照对AnAOB活性的抑制. 反应器温度为32℃,进水pH为7.80~8.20,复氧池中DO为6.50~7.16mg·L-1.
实验过程中HRT为2 h,运行分为3个阶段.第一个是接种污泥活性探究阶段,此阶段进水基质为氨氮和一定量的亚硝酸盐,分别原位考察AOB活性与AnAOB活性.第二个是复氧回流自养脱氮工艺的启动阶段,启动阶段进水基质只有氨氮,通过逐步调节回流量,考察AOB活性与AnAOB活性动态平衡特征.第三个阶段为反应器的稳定阶段,此阶段进水只有氨氮,考察复氧回流模式的CANON工艺处理低氨氮废水的可行性.
1.4 分析监测指标及数据处理方法分析测定项目参照文献[15]: NH4+-N采用纳氏试剂分光光度法,NO2--N采用N-(1-萘基)-乙二胺分光光度法、 NO3--N采用紫外分光光度法.pH采用pHS-3TC型酸度计测定,DO采用便携式溶氧仪Multi 3410.
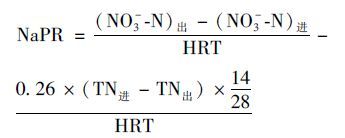
计算公式(1)为AOB活性产生NO2-的能力(nitrite production rate,NiPR),计算公式(2)为AnAOB活性消耗NO2-的能力(nitrite consumption rate,NiCR),计算公式(3)为NOB活性产生NO3-的能力(nitrate production rate,NaPR),计算公式(4)为AOB与AnAOB活性平衡指标的积累速率(nitrite accumulation rate,NAR),公式(5)为总氮去除率(nitrogen removal rate,NRR),进出水总氮为NH4+-N、 NO2--N、 NO3--N的总和,假设损失的总氮都通过ANAMMOX过程产生N2的形式排出.

|
(1) |
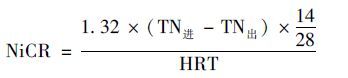
|
(2) |
|
(3) |
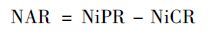
|
(4) |
在第一阶段,首先接种本课题组培养好的成熟絮体亚硝化污泥20 mL,通入压缩空气,维持DO为0.52mg·L-1左右,进出水pH分别为8.08~8.20、 8.00~8.10,在HRT为2 h的情况下稳定运行1 d,其进出水氮浓度见表 2.AOB氧化NH4+产生NO2-的能力NiPR为1.01 kg·(m3·d)-1.
|
|
表 2 接种污泥活性检测 Table 2 Activity detection of inoculated sludge |
在2~4 d,另外接种成熟的厌氧氨氧化颗粒污泥30 mL,HRT为2 h,设定回流流量为0.42 mL·s-1,反应器内部DO<0.01mg·L-1,进出水pH分别为7.95~8.05、 8.08~8.20. 其进出水氮浓度见表 2,接种污泥的AnAOB最大脱氮速率NRR和NO2-消耗速率NiCR分别为1.31 kg·(m3·d)-1、 0.86 kg·(m3·d)-1.
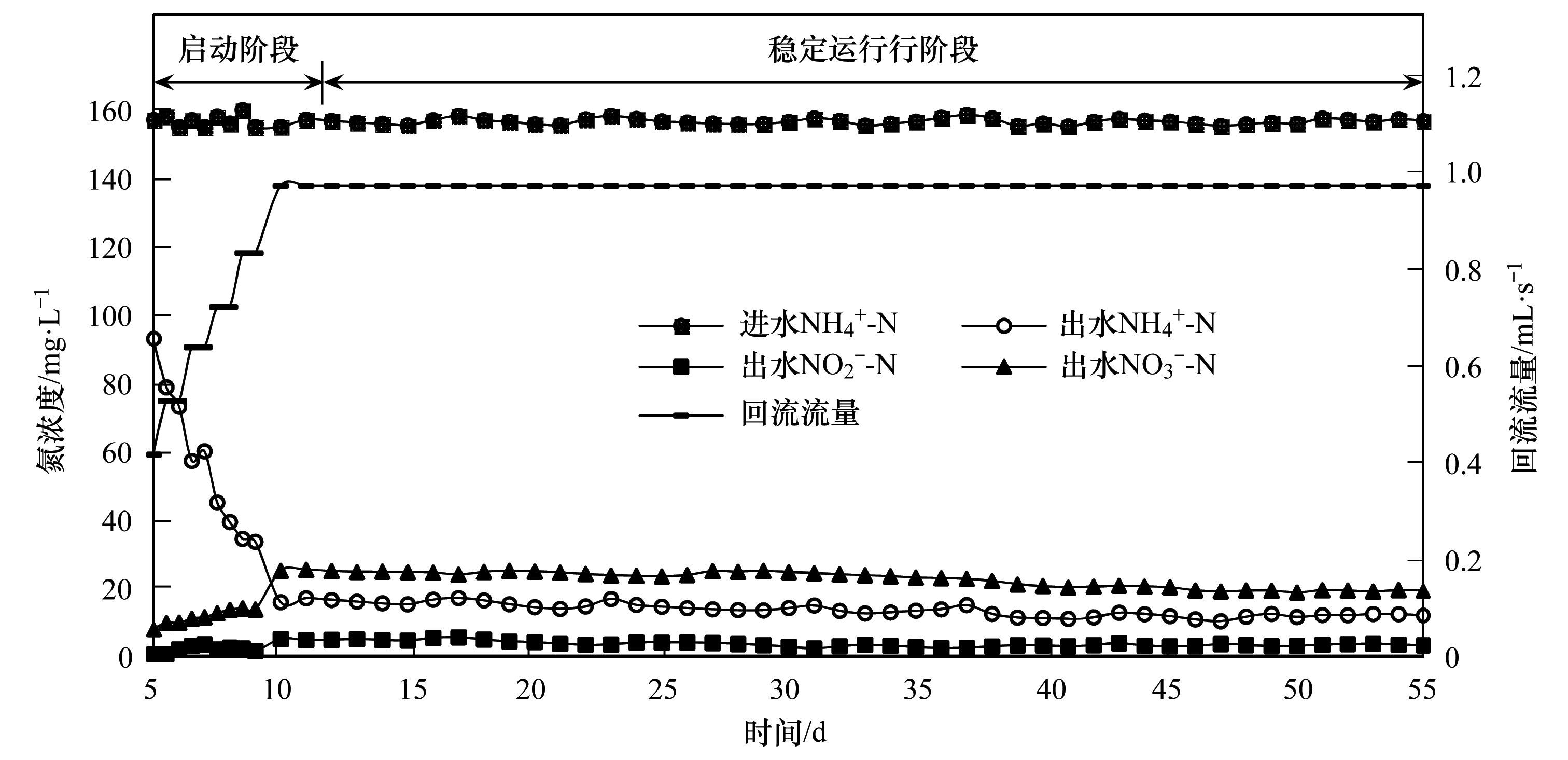
2.2 启动阶段特性分析第二阶段中进水只有157mg·L-1的NH4+-N,进出水pH为8.08~8.20,HRT为2 h.结果见图 2,在5~9 d,回流量从0.42 mL·s-1逐渐提高到0.83 mL·s-1,出水NH4+-N也从90mg·L-1降低到34mg·L-1,过程中出水NO2--N小于5mg·L-1,仅有少量积累,出水NO3--N从8mg·L-1升高到14mg·L-1.在第9 d的时候AnAOB脱氮速率NRR从最初的0.68 kg·(m3·d)-1升高到1.29 kg·(m3·d)-1,基本达到了接种时的水平.
这个过程中没有NO2-的积累,并且没有观察到明显的NOB活性,这主要是由于AnAOB消耗NO2-的速率NiCR比AOB产生NO2-速率NiPR大.另外,复氧回流的方式向反应器提供的溶解氧是有限的,这就有效控制了AOB产生NO2-的速率NiPR,在AOB产生NO2-速率低于AnAOB最大消耗NO2-速率[0.86 kg·(m3·d)-1]之前,NO2-也就无法得到积累. 说明这种复氧回流的方式稳定的控制了AOB的活性,使得NO2-的产生速率NiPR与消耗速率NiCR达到一个平衡状态,同时由于极低的DO有效的抑制了NOB的活性,避免的NO2-的硝化反应.
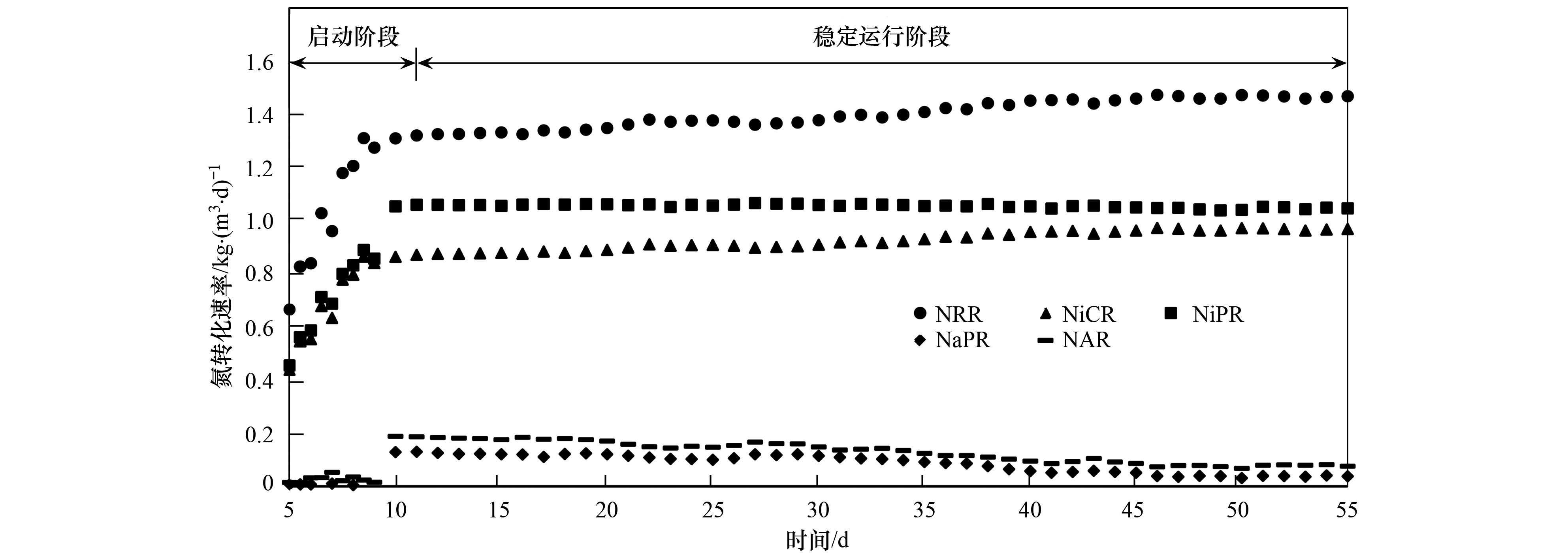
2.3 复氧回流CANON工艺处理低氨氮废水的可行性分析在AnAOB脱氮速率NRR达到接种时的水平之后,系统没有出现NO2-积累和NO3-的过量产生,表明系统中NiPR和NiCR达到一个良好的平衡状态.第三阶段(10~55 d)把回流量提高到0.97 mL·s-1,考察复氧回流运行过程特性. 从图 2可以看出,当回流量提高之后,出水NH4+基本呈现稳定下降的趋势,在进水NH4+-N为157mg·L-1情况下,出水浓度从17mg·L-1降低到12mg·L-1.而出水NO3--N从13.0mg·L-1直接升高到25mg·L-1之后也开始逐渐减小,但是对于出水的NO2--N浓度变化不大,从2mg·L-1升高到5mg·L-1,随后降低到3mg·L-1左右并保持不变. 另外,从图 3可以看出在第三阶段的前期NAR最高达到0.19 kg·(m3·d)-1,NaPR最大也达到了0.13 kg·(m3·d)-1,这说明前期NiPR明显比NiCR大.
|
图 2 实验期间氮浓度变化 Fig. 2 Change of nitrogen concentration during the experiment |
|
图 3 实验期间氮转化速率 Fig. 3 Nitrogen conversion rate during the experiment |
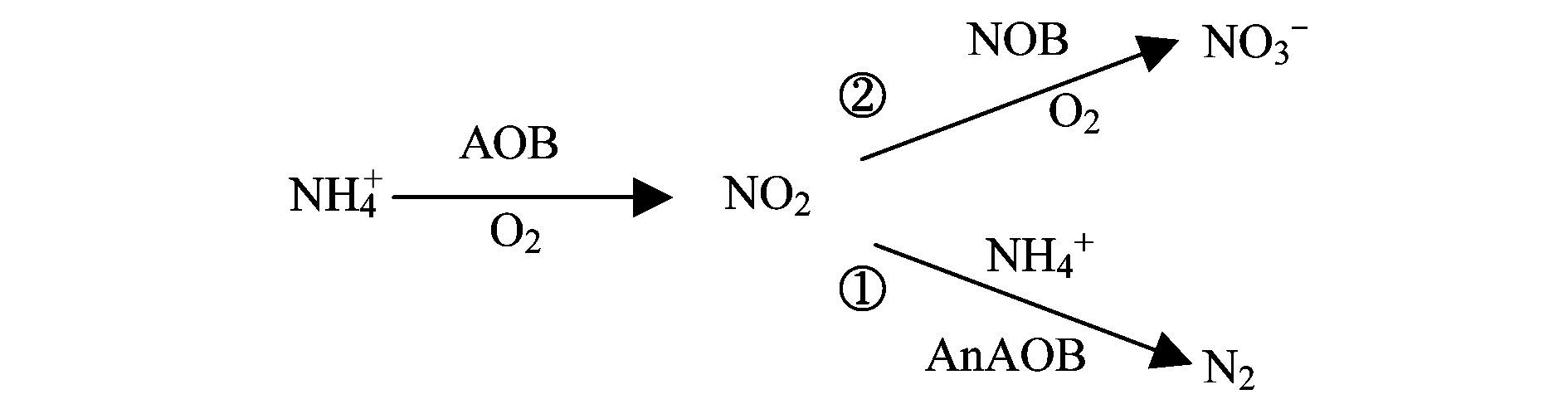
在10~55 d之间,NiPR基本保持着一个恒定值1.06 kg·(m3·d)-1,但是NaPR呈现出逐步降低的趋势,从0.13 kg·(m3·d)-1降低到0.04 kg·(m3·d)-1.这主要是和NO2-转化途径的变化有关.从图 3可以得知AnAOB的NiCR在10~55 d之间从0.87 kg·(m3·d)-1升高到0.98 kg·(m3·d)-1,NRR从1.31 kg·(m3·d)-1升高到1.47 kg·(m3·d)-1.但是这个过程中NO2-的浓度基本上没有什么变化,同时NiPR也保持着一个恒定值,这说明由于NiCR逐渐提高,AOB产生的NO2-从被NOB利用氧化成NO3-的途径(图 4中①过程)逐渐地转变为被AnAOB以ANAMMOX的方式氧化NH4+还原成N2的途径(图 4中②过程).
|
图 4 NO2-的转化途径 Fig. 4 Transformation pathway of NO2- |
CANON工艺成功运行的重要前提是NO2-的积累,而使得NO2-得到积累的关键因素是抑制NOB活性[16]. 从接种污泥的活性可以看出,AOB产生NO2-的速率大于AnAOB消耗NO2-的速率,并且接种污泥中有明显的NOB存在,在DO为0.52mg·L-1时,其转化NO2--N的能力达到0.24 kg·(m3·d)-1.所以抑制NOB对NO2-的转化是反应器稳定运行的重要前提.
在高温条件下(30~35℃),NOB的倍增时间比AOB长,通过控制SRT可以达到抑制NOB活性的目的,但是一般CANON工艺中污泥并不外排,所以以SRT的方式抑制NOB活性是不可取的. 另外,有报道指出高浓度的FA(游离氨)可以抑制NOB的活性,以启动CANON工艺[13, 17],但是Hawkins等[18]的研究表明FA对NOB产生抑制作用的主要是pH而不是FA,在同样的FA(2.1~2.2mg·L-1)水平下,pH从7.1升高到8.0时,NOB的抑制作用从18%升高到60%; 而在同样的pH(pH=8.0)水平下,FA从0.2mg·L-1升高到181mg·L-1时,NOB的抑制作用从69%仅仅升高到73%,这表明FA对NOB的抑制作用不大,并且Liang等[19]研究表明在CANON工艺中无法通过FA达到抑制NOB的目的.所以,在CANON工艺运行过程中通过DO来抑制NOB活性是最常用的手段,因为AOB对O2的亲和力比NOB高[20],两者的溶解氧半饱和常数分别为0.6mg·L-1、 2.2 mg·L-1[21],同时也有研究表明低的DO值(0.31mg·L-1)可以抑制NOB活性[22].但是低的DO并不是都能抑制NOB的活性,这还和AOB的活性有关[18],Joss等[9]的研究发现,在同样的DO条件下(0.2mg·L-1),当AOB活性被部分抑制时,AnAOB活性却被完全抑制,导致NO2-的积累,进而引起NOB的快速增长. 这是由于在相同的DO环境下,当污泥外层的AOB消耗氧的速率减少后,一方面溶解氧对颗粒污泥的渗透深度会增加,导致内部的AnAOB被抑制,另一方面NOB可以利用积累的NO2-和多余的溶解氧进行增长,导致NO3-浓度升高. 这说明低DO值与对NOB活性抑制之间并不是绝对的关系,这还与AOB活性、 污泥粒径大小等因素有关.而本实验中接种污泥含有相对比较多的NOB,更难通过低的DO值(0.2~0.3mg·L-1)来达到抑制NOB活性的目的,而这种情况在一般接种来自污水处理厂的硝化污泥是普遍存在的. 复氧回流方式运行CANON工艺可以把系统内的DO控制在一个极小的值(<0.01 mg·L-1),一方面可以避免对AnAOB的抑制而导致NO2-的积累; 另一方面总溶解氧量的控制使NH4+的好氧氧化仅停留在NO2-阶段. 所以,这种CANON工艺的运行模式可以对NOB活性的抑制提供一个良好的条件.
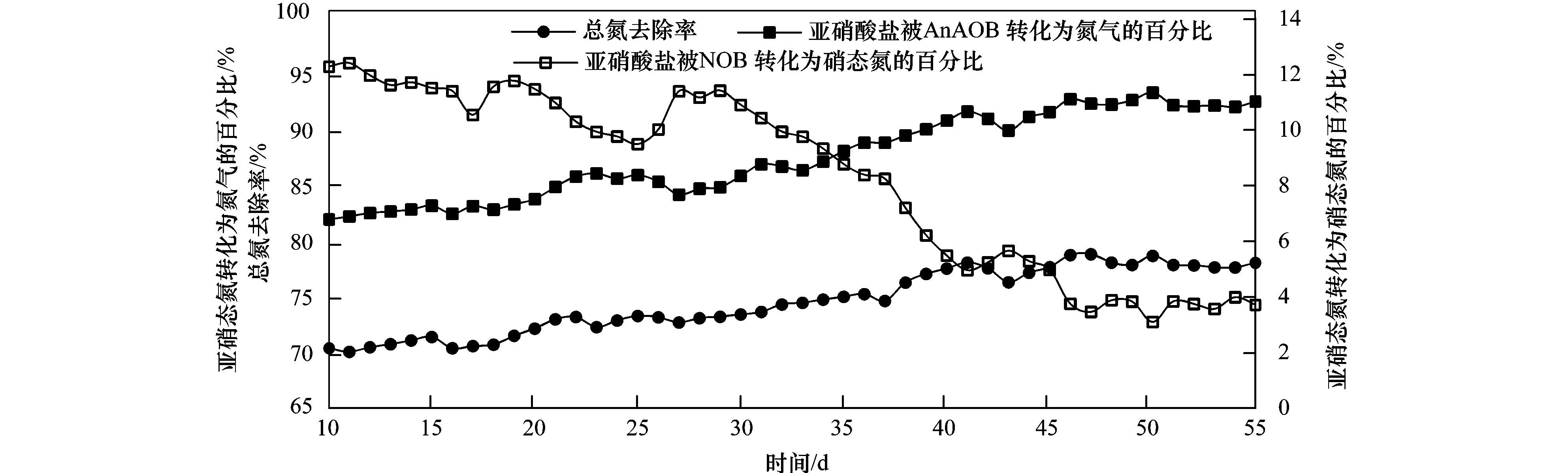
对于CANON工艺,NO2-的转化途径决定了反应器的脱氮效果,NO2-越是趋于图 4中的硝化反应(①过程),那么脱氮效果就会越差,而NO2-越趋于ANAMMOX反应(②过程)脱氮效果越好. 从图 5可以看出,在反应器稳定运行阶段NO2-被NOB利用进行硝化反应的比例处于一个稳定下降的趋势,说明复氧回流的方式有效地抑制了NOB的活性. 在NiPR基本不变的情况下,NO2-的硝化反应比例从12.0%降低到3.8%,ANAMMOX反应比例从82.3%升高到92.2%,总氮去除率也同步增加. 这可以看出,CANON工艺中对NOB活性抑制程度决定了反应器的脱氮效果.
|
图 5 亚硝态氮转化途径的变化 Fig. 5 Change of NO2- transformation pathway |
Jetten等[3]认为CANON工艺稳定运行最重要的前提就是保持目标微生物菌群的稳定,一个是防止AnAOB的恶化,另一个就是防止NOB的积累,有研究表明DO是实现这一目标的主要控制参数[8, 23].
从表 3可以看出,在不同的反应器中成功运行时所要控制的DO大小存在着很大的差异性(0.1~2.53 mg·L-1),这主要与污泥颗粒大小或生物膜厚度有关[27]. 另外,王毅等[28]利用海绵填料对半亚硝化的影响因素的研究中发现,DO低于0.6mg·L-1时已经对AOB产生了抑制作用,导致出水NO2-降低,DO控制在0.95~1.3mg·L-1时NH4+转化率约50%.并且,Hunik等[29]研究发现AOB、NOB的溶解氧半饱和速率为0.16mg·L-1、 0.54mg·L-1,这说明在一般的CANON工艺研究中的AOB、NOB处于一定的抑制状态,如果DO出现异常(偏高)就会使得AOB、NOB潜在的活性激发出来,继而导致出水NO2-、NO3-升高,同时DO长期过高也会对AnAOB产生不可逆的抑制作用[7],最终使CANON工艺反应器崩溃[8, 9, 23]. 所以,对于曝气形式供氧的CANON,稳定的曝气速率是其实现稳定运行的前提,尤其在处理低氨氮废水时. 但是曝气速率受曝气设备的老化、 污泥覆盖等因素影响,Joss等[9]在对德国苏黎世的一个WWTP中运行的CANON反应器研究发现,对曝气设备进行清理会导致曝气量明显增加,使得氧气供应速率超过AOB的耗氧速率,进而对AnAOB产生抑制,NO2-得到积累,而此时也达到了NOB合适的生长环境,在近4个月的运行中NO3--N从15mg·L-1 升高到200mg·L-1,最终导致了反应器的崩溃. 本研究采用出水复氧回流向反应器提供溶解氧,这种方法可以通过控制回流量来有效控制溶解氧的绝对量,当NH4+氧化为NO2-之后,没有多余的溶解氧被NOB利用进行硝化反应,达到完全抑制NOB的作用,同时AnAOB也不会因为DO而受到影响,可以发挥到最大的厌氧氨氧化活性达到一个良好的氮去除速率. 所以,这种复氧回流的方式可以把DO稳定地控制在一个非常小的值(<0.01 mg·L-1).另外,复氧回流可以使得反应器内NiPR与NiCR稳定地处于一个良好的平衡状态,使得反应器中不同菌落之间有一个很好的协同作用,这种CANON工艺的运行模式很好地抑制了NOB活性,为反应器的稳定运行创造了良好的基础.
|
|
表 3 CANON 工艺在不同研究中所控制的 DO 值 Table 3 DO values controlled by CANON process in different researches |
另外,有报道指出CANON工艺还受进水NH4+浓度等的条件影响[11],但是NH4+浓度与DO之间存在着一定的关联性.张肖静等[11]发现,当ALR(氨氮负荷)从0.5 kg·(m3·d)-1升高到0.7 kg·(m3·d)-1以上后,NAR也从60%升高到99%. Third等[2]对CANON反应器的进水氨氮浓度从12mmol·L-1降为5.2mmol·L-1后,其脱氮效率也从92%下降到57%. 所以,ALR(通过改变HRT或进水NH4+浓度)的变化(在游离氨产生抑制作用范围内)本身并不会影响NAR或NRR,而是由于ALR减少引起基质限制使得氨氧化速率降低,继而导致反应器内的溶解氧过剩,DO升高,然后对AnAOB产生了抑制,影响NRR; 同样,在相同的曝气条件下ALR增加会加快氨氧化速率,降低DO,进而抑制了NOB活性使得NAR增加,所以仅仅通过DO的大小并不是都能达到抑制NOB活性的效果. 在本研究中发现,反应器稳定运行过程中其上部沉淀区DO<0.01 mg·L-1,这说明系统内AOB的耗氧速率与溶解氧的供给速率基本保持一致,同时,出水NO2-<5mg·L-1,在此条件下有效地抑制了NOB活性,使得反应器在运行稳定性方面表现了很好的优势.
3.3 复氧回流CANON工艺的经济性分析相对于硝化-反硝化脱氮技术,CANON工艺减少了60%左右的曝气量,在节约能耗方面表现了显著的优势. 而本文研究过程中采用溢流出水复氧回流的方式节约了100%的曝气能耗,使得对低氨氮废水处理的运行成本方面更加经济. 另外,对于利用上流式污泥床反应器处理低水量废水时一般需要内回流增加水力搅动,而复氧回流过程在提供溶解氧的同时也为反应器提供了一定的水力搅动,这使得在不额外增加回流的情况下达到脱氮的目的. 所以,利用CANON工艺以复氧回流的方式处理低氨氮废水是一种经济可靠的运行模式.
4 结论(1) 出水复氧回流可以快速启动并稳定运行CANON工艺,在污泥体积分数为25%,进水NH4+-N为157mg·L-1,HRT为2 h的条件下,经过50 d的运行,总氮去除速率NRR从1.31增加到1.47 kg·(m3·d)-1.反应器内部DO在0.01mg·L-1以下.
(2) 对于CANON工艺,复氧回流的方式有效地控制了反应器内溶解氧的量,对系统中的NOB起到了很好的抑制效果,在稳定运行阶段NaPR只有0.04 kg·(m3·d)-1,占NRR的2.7%,表明系统中的NOB活性被有效抑制.另外,由于反应器内的DO<0.01 mg·L-1,AnAOB活性没有受到溶解氧的影响,启动过程中NiCR可以快速恢复,并在其后运行中有稳定增加的趋势.
(3) 复氧回流CANON工艺运行模式在稳定性方面表现出了很大的优势,在反应器运行50 d中,仅仅通过控制回流量既可以使得NiPR一直维持在1.06 kg·(m3·d)-1附近,其浮动范围在0.01 kg·(m3·d)-1内.表明回流量精确的控制了系统中溶解氧的量,使得NO2-产生速率处于一个稳定的值. 并且有效地避免了DO对AnAOB可能产生的抑制,NiCR有条件稳定增加,使得所积累的NO2-逐步从硝化反应转移到ANAMMOX反应,达到一个更好的脱氮效果.
(4) 相对于常用的上流式污泥床反应器运行的CANON工艺,复氧回流节约了100%的曝气能耗;同时,回流过程也为反应器提供了一定的水力搅动,在低水量的情况下节约了内回流的水力能耗.所以,复氧回流CANON工艺运行模式在低氨氮废水处理方面表现了更加节能、经济的优点.
(5) 复氧回流CANON工艺为ANAMMOX脱氮技术的应用以及CANON工艺启动并稳定运行提供了一个新模式;为CANON工艺中NOB活性的抑制提供了一个新方法.
| [1] | Sliekers A O, Derwort N, Gomez J L, et al. Completely autotrophic nitrogen removal over nitrite in one single reactor[J]. Water Research, 2002, 36(10) : 2475–2482. DOI: 10.1016/S0043-1354(01)00476-6 |
| [2] | Third K A, Sliekers A O, Kuenen J G, et al. The CANON system (Completely Autotrophic Nitrogen-removal Over Nitrite) under ammonium limitation:interaction and competition between three groups of bacteria[J]. Systematic and Applied Microbiology, 2001, 24(4) : 588–596. DOI: 10.1078/0723-2020-00077 |
| [3] | Jetten M S M, Wagner M, Fuerst J, et al. Microbiology and application of the anaerobic ammonium oxidation (‘anammox’) process[J]. Current Opinion in Biotechnology, 2001, 12(3) : 283–288. DOI: 10.1016/S0958-1669(00)00211-1 |
| [4] | Mulder A. The quest for sustainable nitrogen removal technologies[J]. Water Science and Technology, 2003, 48(1) : 67–75. |
| [5] | 王亚宜, 黎力, 马骁, 等. 厌氧氨氧化菌的生物特性及CANON厌氧氨氧化工艺[J]. 环境科学学报, 2014, 34(6) : 1362–1374. Wang Y Y, Li L, Ma X, et al. Bio-characteristics of anammox bacteria and CANON anammox process[J]. Acta Scientiae Circumstantiae, 2014, 34(6) : 1362–1374. |
| [6] | Egli K, Fanger U, Alvarez P J J, et al. Enrichment and characterization of an anammox bacterium from a rotating biological contactor treating ammonium-rich leachate[J]. Archives of Microbiology, 2001, 175(3) : 198–207. DOI: 10.1007/s002030100255 |
| [7] | Strous M, Van Gerven E, Kuenen J G, et al. Effects of aerobic and microaerobic conditions on anaerobic ammonium-oxidizing (Anammox) sludge[J]. Applied and Environmental Microbiology, 1997, 63(6) : 2446–2448. |
| [8] | 李冬, 崔少明, 梁瑜海, 等. 溶解氧对序批式全程自养脱氮工艺运行的影响[J]. 中国环境科学, 2014, 34(5) : 1131–1138. Li D, Cui S M, Liang Y H, et al. The effect of dissolved oxygen on running CANON process in sequencing batch reactor[J]. China Environmental Science, 2014, 34(5) : 1131–1138. |
| [9] | Joss A, Derlon N, Cyprien C, et al. Combined Nitritation-Anammox:advances in understanding process stability[J]. Environmental Science & Technology, 2011, 45(22) : 9735–9742. |
| [10] | 付昆明, 周厚田, 左早荣, 等. 水力停留时间对海绵填料CANON反应器性能的影响[J]. 中国给水排水, 2016, 32(7) : 1–5. Fu K M, Zhou H T, Zuo Z R, et al. Effect of hydraulic retention time on performance of CANON reactor with sponge as carrier[J]. China Water & Wastewater, 2016, 32(7) : 1–5. |
| [11] | 张肖静, 李冬, 梁瑜海, 等. 氨氮浓度对CANON工艺性能及微生物特性的影响[J]. 中国环境科学, 2014, 34(7) : 1715–1721. Zhang X J, Li D, Liang Y H, et al. Effect of ammonia concentration on the performance and microbial characteristics of CANON process[J]. China Environmental Science, 2014, 34(7) : 1715–1721. |
| [12] | 廖德祥, 李小明, 曾光明, 等. 单级SBR生物膜中全程自养脱氮的研究[J]. 中国环境科学, 2005, 25(2) : 222–225. Liao D X, Li X M, Zeng G M, et al. Studies on deammonification process in single SBR biofilm[J]. China Environmental Science, 2005, 25(2) : 222–225. |
| [13] | Zhang X J, Li D, Liang Y H, et al. Performance and microbial community of completely autotrophic nitrogen removal over nitrite (CANON) process in two membrane bioreactors (MBR) fed with different substrate levels[J]. Bioresource Technology, 2014, 152 : 185–191. DOI: 10.1016/j.biortech.2013.10.110 |
| [14] | 羊寿生. 曝气的理论与实践[M]. 北京: 中国建筑工业出版社, 1982. |
| [15] | 国家环境保护总局. 水和废水监测分析方法[M]. (第四版). 北京: 中国环境科学出版社, 2002. |
| [16] | Liu T, Li D, Zeng H P, et al. Biodiversity and quantification of functional bacteria in completely autotrophic nitrogen-removal over nitrite (CANON) process[J]. Bioresource Technology, 2012, 118 : 399–406. DOI: 10.1016/j.biortech.2012.05.036 |
| [17] | Van Hulle S W H, Vandeweyer H J P, Meesschaert B D, et al. Engineering aspects and practical application of autotrophic nitrogen removal from nitrogen rich streams[J]. Chemical Engineering Journal, 2010, 162(1) : 1–20. DOI: 10.1016/j.cej.2010.05.037 |
| [18] | Hawkins S, Robinson K, Layton A, et al. Limited impact of free ammonia on Nitrobacter spp. inhibition assessed by chemical and molecular techniques[J]. Bioresource Technology, 2010, 101(12) : 4513–4519. DOI: 10.1016/j.biortech.2010.01.090 |
| [19] | Liang Y H, Li D, Zhang X J, et al. Stability and nitrite-oxidizing bacteria community structure in different high-rate CANON reactors[J]. Bioresource Technology, 2015, 175 : 189–194. DOI: 10.1016/j.biortech.2014.10.080 |
| [20] | Laanbroek H J, Gerards S. Competition for limiting amounts of oxygen between Nitrosomonas europaea and Nitrobacter winogradskyi grown in mixed continuous cultures[J]. Archives of Microbiology, 1993, 159(5) : 453–459. DOI: 10.1007/BF00288593 |
| [21] | Wiesmann U. Biological nitrogen removal from wastewater[A]. In:Wiesmann U (Ed.). Biotechnics/Wastewater[M]. Berlin Heidelberg:Springer, 1994. 113-154. |
| [22] | Wyffels S, Boeckx P, Pynaert K, et al. Nitrogen removal from sludge reject water by a two-stage oxygen-limited autotrophic nitrification denitrification process[J]. Water Science and Technology, 2004, 49(5-6) : 57–64. |
| [23] | 操家顺, 漆磊, 薛朝霞, 等. 水动力条件对全程自养脱氮工艺启动研究[J]. 工业安全与环保, 2016, 42(3) : 57–61. Cao J S, Qi L, Xue Z X, et al. Study on hydrodynamic conditions on start-up of CANON process[J]. Industrial Safety and Environmental Protection, 2016, 42(3) : 57–61. |
| [24] | Gonzalez-Martinez A, Rodriguez-Sanchez A, Garcia-Ruiz M J, et al. Performance and bacterial community dynamics of a CANON bioreactor acclimated from high to low operational temperatures[J]. Chemical Engineering Journal, 2016, 287 : 557–567. DOI: 10.1016/j.cej.2015.11.081 |
| [25] | Helmer-Madhok C, Schmid M, Filipov E, et al. Deammonification in biofilm systems:population structure and function[J]. Water Science and Technology, 2002, 46(1-2) : 223–231. |
| [26] | 蔡庆, 张代钧, 肖芃颖, 等. 完全自营养脱氮过程中的影响因素[J]. 环境工程学报, 2013, 7(10) : 3895–3900. Cai Q, Zhang D J, Xiao P Y, et al. Influencing factors in completely autotrophic nitrogen removal process[J]. Chinese Journal of Environmental Engineering, 2013, 7(10) : 3895–3900. |
| [27] | Vlaeminck S E, Terada A, Smets B F, et al. Aggregate size and architecture determine microbial activity balance for one-stage partial nitritation and anammox[J]. Applied and Environmental Microbiology, 2010, 76(3) : 900–909. DOI: 10.1128/AEM.02337-09 |
| [28] | 王毅, 金腊华, 朱波, 等. 全程自养脱氮反应器条件下半亚硝化影响因素的探究[J]. 安徽农业科学, 2013, 41(24) : 10095–10097. Wang Y, Jin L H, Zhu B, et al. Research on influencing factors of half-nitrosation in CANON reactor[J]. Journal of Anhui Agricultural Sciences, 2013, 41(24) : 10095–10097. |
| [29] | Hunik J H, Tramper J, Wijffels R H. A strategy to scale up nitrification processes with immobilized cells of nitrosomonas europaea and nitrobacter agilis[J]. Bioprocess Engineering, 1994, 11(2) : 73–82. DOI: 10.1007/BF00389563 |
 2017, Vol. 38
2017, Vol. 38


