2. 中国科学院水生生物研究所, 淡水生态与生物技术国家重点实验室, 武汉 430072
2. State Key Laboratory of Freshwater Ecology and Biotechnology, Institute of Hydrobiology, Chinese Academy of Sciences, Wuhan 430072, China
湖泊富营养化导致浮游植物过量生长、蓝藻水华频发、水质恶化、生物多样性下降、水生态系统失衡,严重威胁了人类饮用水安全,已成为目前最为严重的水环境问题之一[1].一般而言,过量的磷输入是导致湖泊富营养化的关键因素[2].作为湖泊中磷的主要组成部分,有机磷在水环境中起着十分重要的作用,在局部水体中甚至成为营养物质的主要组分[3, 4].同时,有机磷可以转化为无机磷,故将成为潜在的可被生物利用的重要营养源,作为参与湖泊磷循环的主体,其含量在很大程度上决定了水体初级生产力水平[5, 6].最近研究表明,光化学分解是水体中营养盐来源的重要途径之一[7].湖泊水体中的有机磷可以在光照条件下释放溶解态无机磷.由于该反应发生于湖泊水体表层,因此反应产生的溶解态反应磷(SRP)可以快速参与水体循环,对水体富营养化进程具有重要影响[8, 9].然而,相关研究对参与反应的有机磷形态及其驱动力缺乏系统研究.
Fe (Ⅲ)在湖泊水体磷循环方面起着极为重要的作用.一方面,Fe (Ⅲ)可以与SRP反应生成不溶复合物而沉积大量的SRP;另一方面,Fe (Ⅲ)在水体中形成羟基氧化铁胶体也可以吸附一定量的SRP[10].但是值得注意的是,自然条件下,Fe (Ⅲ)易与广泛存在的有机物形成络合物,其能在紫外和太阳光辐射下,会发生一系列的光化学反应,进而影响水体中元素循环[11].在早期的研究中就已经发现,腐殖质-磷-Fe (Ⅲ)络合物,能够在紫外光照射下释放出溶解态磷酸盐[12],但以往的研究却未对其机制进行深入阐明.自然水体中Fe (Ⅲ)-草酸络合物体系在光照条件下能否实现水体中有机磷向无机磷的转化,从而影响水体中磷水平尚不得知.
草甘膦(GLY)是一种膦酸酯形态的有机磷农药,其低毒性和稳定性使其在农业生产中得以广泛应用,可以随地表径流等途径而进入湖泊水体[13].因此,本文以草甘膦为有机磷代表,在对比研究了不同的氧化体系下草甘膦光解释放无机磷过程的基础上,重点分析了太阳光和紫外光照射下自然湖泊中草甘膦在Fe (Ⅲ)-草酸络合物光化学作用下向磷酸根转化的过程,同时考察了环境因素如草酸盐、Fe (Ⅲ)不同浓度配比、pH和草甘膦初始浓度对磷酸根释放过程的影响,并采用活性氧分子探针验证了Fe (Ⅲ)-草酸络合物光化学反应体系中的活性氧物种及其稳态浓度.本研究将有助于系统认识湖泊水体磷素循环,以期为调控水体关键营养元素提供科学依据.
1 材料与方法 1.1 试剂草甘膦为标准品,购自Sigma-Aldrich (美国);氯化铁、盐酸、氢氧化钠、草酸盐钠、抗坏血酸、钼酸铵、磷酸二氢钾、异丙醇均为分析纯,购买自国药集团(上海).实验用的纯水由优普系列超纯水机(UPH-I-40L)提供,湖水为武汉市南湖水.
1.2 实验装置光降解实验在PhchemⅢ型旋转式光化学反应仪(北京纽比特科技有限公司)中进行.反应器主要由一个双层石英冷肼与周围12支石英管构成,光源分别选用500 W的氙灯和300 W的高压汞灯置于石英冷肼内,12支装有反应溶液的具塞石英管(200 mm×Φ50 mm,75 mL)垂直固定在冷肼外侧,将配制好的溶液置于石英反应管中,按照不同要求进行光照实验.光照实验分别使用500 W氙灯和300 W汞灯模拟太阳光和紫外光(UV-Vis)光源,其辐照光谱如图 1所示,氙灯辐照光谱范围为200~1 000 nm,汞灯辐照光谱范围为200~600 nm.

|
图 1 氙灯和汞灯辐照光谱 Fig. 1 Spectral irradiance of xenon lamp and mercury lamp |
为研究自然湖水中的Fe (Ⅲ)-草酸络合物光化学活性对草甘膦形态转化过程的影响,本实验采取武汉市南湖表层水,经多处取样混合后,用0.7 μm滤膜过滤以去除浮游植物和颗粒物后使用.其背景值如表 1所示,由于南湖属于城市湖泊,水质受污严重,因降雨等因素影响,总磷、磷酸根等含量变化较大.基于研究目的,分别设置湖水、湖水+Fe (Ⅲ)、湖水+Fe (Ⅲ)-Oxa、湖水+草甘膦、湖水+草甘膦+Fe (Ⅲ)和湖水+草甘膦+Fe (Ⅲ)-Oxa这6个体系.为便于对比,实验设定湖水中草甘膦初始浓度为1 mg·L-1,Fe (Ⅲ)浓度分别为0、5、10、20、50 μmol·L-1,草酸盐浓度分别为0、20、100、200、400 μmol·L-1;溶液最初pH设定为4.0、6.0、8.0和10.0,用0.1 mol·L-1 HCl和0.1 mol·L-1 NaOH调节pH;不同底物浓度为0.5、1.0、2.0、4.0 mg·L-1.为进一步验证Fe (Ⅲ)-草酸络合物对湖水中有机磷光氧化降解释放磷酸根过程的影响,在湖水+草甘膦+Fe (Ⅲ)-草酸体系中添加·OH猝灭剂异丙醇,异丙醇添加量为0.1 mol·L-1.紫外光光照时间为60 min,每隔10 min取样一次,太阳光照射时间为720 min,每60 min取样一次,每个时间点的样品至少设3个重复,采用钼蓝分光光度法测定样品中的磷酸根浓度.
|
|
表 1 南湖上覆水基本理化指标 Table 1 Physicochemical indexes of overlying water of Nanhu Lake |
1.4 活性物种稳态浓度的测定方法
·OH是环境中有机物间接光解的主要活性物种之一[14].本研究以香豆素作为·OH分子探针,测定体系中·OH的稳态浓度,香豆素可以与·OH形成具有荧光性很强的七-羟基香豆素(7-HOC)[15].根据Louit等[16]的报道,纯水条件下,测定7-HOC的产率为28.6%,由此通过测定7-HOC的荧光强度,即可换算出羟基自由基(·OH)的稳态浓度.取过滤南湖水配制Fe (Ⅲ)浓度和草酸浓度分别为20 μmol·L-1和400 μmol·L-1,香豆素浓度为100 μmol·L-1,将混合液转移至反应管中,分别在紫外和太阳光照下,每间隔5 min取样5 mL,至少3次平行.采用荧光光度计测定其荧光强度,激发波长:332 nm;发射波长:455 nm;扫描波长:300~600 nm.
超氧自由基(O2·-)也是环境中重要的活性氧物种之一[17],其能够实现众多有机物的形态转化.本研究以氯化氮蓝四唑(NBT)为O2·-分子探针,其能够与O2·-反应生成不溶物单甲腊和二甲腊,因此可以通过测定NBT的降解速率来测定水体中O2·-的稳态浓度[18].取过滤南湖水配制Fe (Ⅲ)浓度和草酸浓度分别为20μmol·L-1和400 μmol·L-1,氯化氮蓝四唑浓度为100 μmol·L-1混合液,将混合液转移至反应管中,分别在紫外和太阳光照下,每间隔10 min取样2 mL于比色管中,稀释样品溶液至10 mL,采用紫外分光光度计在258 nm条件下进行测量其吸光值,实验结果至少3组平行,在反应体系中均加入异丙醇0.1 mol·L-1,以消除·OH的影响.
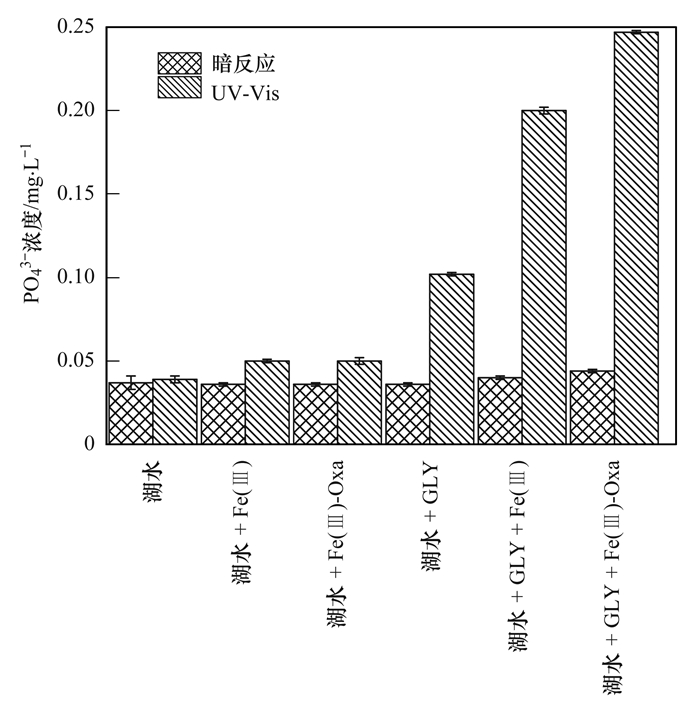
2 结果与讨论 2.1 不同驱动力对湖泊水体中有机磷释放磷的影响本文首先在室内模拟紫外光(UV-Vis)条件下,分别研究了不同处理下有机磷光解对水体中磷水平的贡献.如图 2所示,在暗反应60 min后,湖水处理中磷酸根含量基本不变,表明生物矿化过程对水体中磷水平不明显.经UV-Vis照射60 min后,处理中磷酸根的含量相比暗反应增至0.039 mg·L-1,其主要是湖水中的有机磷经光照分解释放无机磷所致.湖泊水体中的有机磷可以在生物矿化和化学分解作用下转化为无机磷[19, 20],其与水体中的环境因素及有机磷形态具有直接相关性.部分有机磷可以直接光解转化为无机磷,部分有机磷则在水体中的天然光敏物质如NO3-、Fe (Ⅲ)、溶解性有机碳(DOM)等作用下,发生间接光解而释放磷酸根[21].在湖水+Fe (Ⅲ)/湖水+Fe (Ⅲ)-Oxa实验组中,由于外源添加光敏物质产生更多活性氧物质,使湖水中释放的无机磷达到了0.050 mg·L-1.由于湖水样品中有机磷的含量有限,因此,外源添加光敏物质对水体中有机磷光解释放磷酸根的贡献不大.在湖水+草甘膦处理中,随着体系中草甘膦的添加,光照60 min后,体系中磷酸根浓度增加至0.10 mg·L-1,这表明水体中有机磷浓度增加对其光解磷酸根具有重要影响,有机磷含量的增加可以显著提升水体磷酸根水平.在湖水+草甘膦+Fe (Ⅲ)处理中,经光照反应后,磷酸根的含量为0.20 mg·L-1,高于湖水+草甘膦处理,证明天然光敏物质可以加速有机磷向无机磷的转化速率.事实上,Fe (Ⅲ)可以与磷酸根反应生成不溶沉淀从而沉积磷酸根[10],然而,在紫外光照射下,Fe (Ⅲ)存在的主要形态Fe (OH)2+可以光解生成Fe (Ⅱ)和·OH,提供了有机磷光解驱动力--·OH[22],也抑制了Fe (Ⅲ)与磷酸根反应而沉积磷的过程.在自然湖水中,Fe (Ⅲ)更易与水体中的大量小分子有机酸结合生成络合物,在光照条件下,可以快速发生光化学反应,从而影响水体中部分物质的形态转化过程[23].以相同含Fe (Ⅲ)浓度的Fe (Ⅲ)-草酸络合物取代Fe (Ⅲ)的处理中,经60 min光照反应后,磷酸根的含量为0.25 mg·L-1,高于其他对照处理,证明自然水体中的Fe (Ⅲ)-草酸络合物对自然水体中磷的形态转化过程及水体磷水平的贡献率具有较大影响.
|
草甘膦浓度为1.0 mg·L-1,Fe (Ⅲ)浓度20 μmol·L-1,草酸盐浓度为400 μmol·L-1 图 2 不同驱动力对湖水体中草甘膦光解释放磷的影响 Fig. 2 Influence of different driving forces on photochemical release of phosphate under UV-Vis irradiation |

|
(1) |

|
(2) |
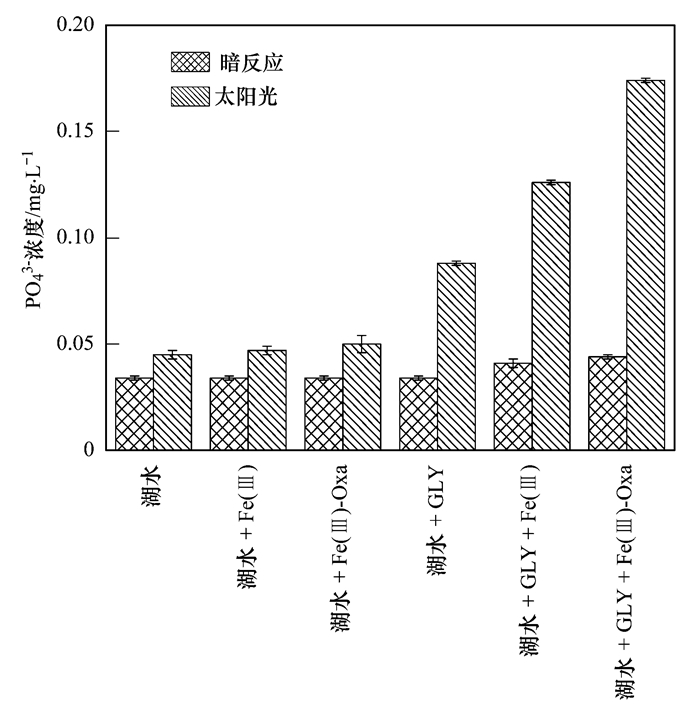
Fe (Ⅲ)和Fe (Ⅲ)-草酸络合物的光响应范围较宽,可以吸收和利用可见光而产生活性氧物种,进而氧化降解水体中的有机物,影响物质的迁移转化[24]. Zhao等[25]的研究结果表明,Fe (Ⅲ)-草酸络合物可以吸收可见光而降解水体中的碘帕醇,但其降解速率低于紫外光.然而由于紫外光只占太阳光的5%,Fe (Ⅲ)-草酸络合物能否吸收和利用太阳光并在短时间内实现水体中有机磷向无机磷的转化及其释放速率尚未可知,因此,本文进一步研究了太阳光照射下不同反应体系中磷酸根的释放情况.研究体系设置与紫外光反应相同,光照时间延长为720 min.从图 3可以看出,在湖水处理中,经太阳光照射720 min后,湖水、湖水+Fe (Ⅲ)、湖水+Fe (Ⅲ)-Oxa、湖水+GLY、湖水+GLY+Fe (Ⅲ)及湖水+GLY+Fe (Ⅲ)-Oxa体系中,磷酸根浓度分别为0.045、0.047、0.050、0.088、0.13和0.18 mg·L-1,均高于暗反应处理,表明光照可以提升水体中磷酸根的释放量.此外,湖水+GLY+Fe (Ⅲ)-Oxa体系中磷酸根的释放量高于其他对照处理,证明太阳光照射下Fe (Ⅲ)-草酸络合物光化学活性对水体磷的释放具有非常重要的影响.
|
草甘膦浓度为1.0 mg·L-1,Fe (Ⅲ)浓度20 μmol·L-1,草酸盐浓度为400 μmol·L-1 图 3 太阳光下不同驱动力对草甘膦光解释放磷的影响 Fig. 3 Influence of different driving forces on photochemical release of phosphate under Sunlight irradiation |
环境因素对Fe (Ⅲ)-草酸络合物光化学反应活性具有极为重要的影响.因此,本研究分别探讨了草酸盐/Fe (Ⅲ)不同浓度配比、pH和草甘膦初始浓度对Fe (Ⅲ)-草酸络合物驱动草甘膦光解释放磷酸根释放过程的影响.由于紫外光照射条件下,磷酸根释放速率显著高于太阳光,因此,本研究重点探讨了紫外光照射下上述环境因素的影响.此外,由于实验采用的自然湖水,而水中磷酸根的初始浓度变化较大,在进行环境因素的影响实验时,磷酸根的初始浓度为0.07~0.09 mg·L-1.
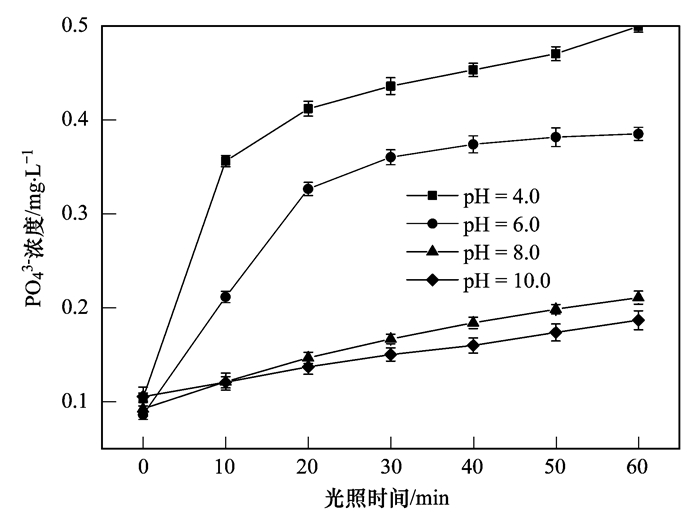
水体pH对有机物的光化学转化过程具有重要影响,其主要通过改变有机物分子和活性物质在水溶液中的存在形态,从而影响其吸收光谱特性,最终影响光化学转化过程[26].本实验首先探究了水体初始pH对草甘膦光解释放磷酸根的影响.在[GLY]=1.0 mg·L-1,[Fe (Ⅲ)]=20 μmol·L-1,[Oxalate]=400 μmol·L-1的条件下,分别测定体系pH为4.0、6.0、8.0和10.0时的磷酸根含量变化.实验结果如图 4所示.经UV-Vis照射60 min后,pH为4.0时,体系内磷酸根的浓度最高,达到了0.46 mg·L-1.随着体系pH的增大,磷酸根的释放量逐渐降低.一方面,pH可以影响草甘膦的直接光解.已有研究表明,升高体系的pH可以显著促进草甘膦光解转化为无机磷[27].但是,另一方面,在Fe (Ⅲ)-草酸络合体系中,pH可以影响Fe (Ⅲ)及Fe (Ⅲ)-草酸络合物的存在形态.当pH过高时,Fe (Ⅲ)易形成Fe (OH)3沉淀,在降低了Fe (Ⅲ)光化学活性的同时,易吸附固定水体产生的磷酸根.且水体中Fe (Ⅲ)-草酸络合物主要以Fe (C2O4)+、Fe (C2O4)2-、Fe (C2O4)33-和Fe (C2O4) H2+形态存在,不同的络合物具有不同的光吸收特性和光化学活性[28, 29].当pH为2~5时,随pH升高,Fe (C2O4)2-的含量逐渐减少,而Fe (C2O4)33-的含量逐渐增多;当pH大于6时,随pH升高,Fe (C2O4)2-、Fe (C2O4)33-的含量逐渐减少[30],进而抑制了Fe (Ⅲ)-草酸络合物的光化学活性,降低了体系中磷酸根的释放量.
|
草甘膦浓度为1.0 mg·L-1,Fe (Ⅲ)浓度20 μmol·L-1,草酸盐浓度为400 μmol·L-1 图 4 初始pH值对湖水体中草甘膦光解释放磷的影响 Fig. 4 Influence of initial pH value on photochemical release of phosphate under UV-Vis irradiation |
在pH=6.0,[GLY]=1.0 mg·L-1,[Fe (Ⅲ)]=20 μmol·L-1的条件下,研究了草酸盐浓度变化对草甘膦光解释放磷酸根过程的影响.草酸盐浓度分别为20、100、200和400 μmol·L-1,实验结果见图 5.经过UV-Vis光照60 min后,草酸盐浓度为20、100、200和400 μmol·L-1的Fe (Ⅲ)-草酸络合物体系中,磷酸根浓度分别为0.32、0.35、0.38和0.40 mg·L-1,表明随着草酸盐浓度的升高,体系中磷酸根的释放量也随着增大.随草酸盐浓度的增加,Fe (C2O4)2-、Fe (C2O4)33-的数量增加[31].在UV-Vis照射下,即可产生更多的活性氧基团,从而促进了草甘膦向磷酸根的形态转化.此外,随着草酸盐浓度的增大,Fe (Ⅲ)的配位数也随着增大,Fe (Ⅱ)的产量也明显增多.由于体系中活性氧基团的产量与Fe (Ⅱ)的含量具有直接相关性,也就有更多的磷酸根产生.在Zou等[32]的报道中,当体系中草酸含量进一步增大时,会抑制Fe (Ⅲ)-草酸络合物的光化学活性,其主要是由于对活性氧物质的竞争所致.

|
图 5 草酸盐浓度对湖水体中草甘膦光解释放磷的影响 Fig. 5 Influence of oxalate concentration on photochemical release of phosphate |
Fe (Ⅲ)/磷比对湖泊水体中磷的存在形态具有极为重要的影响.早期报道已经表明,间隙水中Fe (Ⅲ)与磷的量比大于2.0时,溶液中的溶解态无机磷则会与Fe (Ⅲ)反应而被吸附固定不能进入水体[33].在水柱表层中,溶液中的Fe (Ⅲ)可以光解产生Fe (Ⅱ)[12].一方面,该过程可以抑制Fe (Ⅲ)与磷的沉淀反应过程;另一方面,随着反应体系中Fe (Ⅱ)含量的增多,其可以消耗反应产生的·OH,从而抑制磷的释放效率[34].因此,为探明Fe (Ⅲ)浓度对Fe (Ⅲ)-草酸络合物光解草甘膦释放磷酸根过程的影响,本研究采用Fe (Ⅲ)浓度分别为5、10、20和50 μmol·L-1,草酸浓度为100 μmol·L-1,进行了草甘膦在Fe (Ⅲ)-草酸络合体系中的磷释放量过程研究.结果如图 6所示,UV-Vis照射60 min后,在草酸盐浓度一定的情况下,随Fe (Ⅲ)浓度的增多,磷酸根浓度逐渐增加,Fe (Ⅲ)浓度为50 μmol·L-1时,紫外光照60 min磷酸根浓度为0.28 mg·L-1.这一结果表明Fe (Ⅲ)-草酸络合体系中,Fe (Ⅲ)浓度的增加,可以提升草甘膦光解转化为磷酸根的速率.

|
图 6 铁离子浓度对湖水体中草甘膦光解释放磷的影响 Fig. 6 Influence of Fe (Ⅲ) concentration on photochemical release of phosphate |
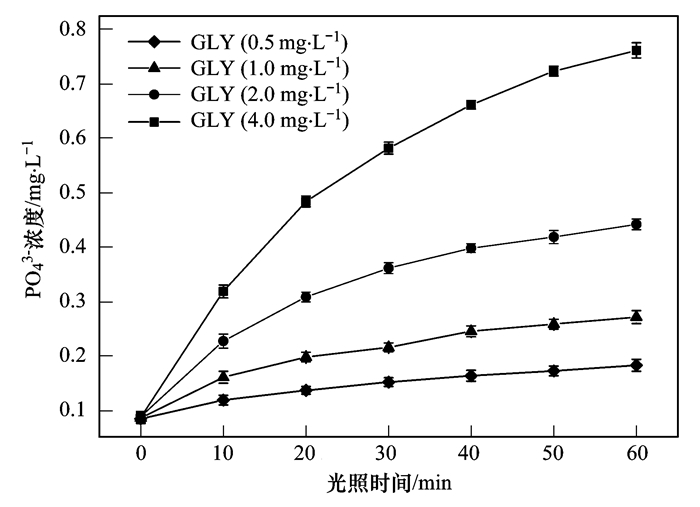
湖泊水体中有机磷通过直接光解和间接光解释放磷酸盐,其浓度直接关系其光解对水体中磷的贡献水平[35].在UV-Vis照射,pH=6.0,[Fe (Ⅲ)]=20 μmol·L-1,[Oxalate]=400 μmol·L-1的体系中,不同草甘膦浓度对其光解释放磷酸根的影响见图 7所示.但是经光照反应后,反应体系中磷酸根浓度显著提升.紫外光照射60 min后,草甘膦的初始浓度为0.50、1.0、2.0和4.0 mg·L-1体系中,磷酸根浓度分别为0.15、0.25、0.42和0.75 mg·L-1,即草甘膦浓度越高,经光照直接分解产生的磷酸根含量也就越多.在自然湖泊上覆水中溶解态有机磷的含量一般较低,但是在湖泊沉积物再悬浮过程中将会有大量的有机磷和大量的光敏物质进入上覆水,在太阳光照下将快速释放出无机磷,且对浅水湖泊而言,当发生再悬浮过程时,其上覆水中有机磷的含量急剧增大,对上覆水无机磷负荷将产生重大影响.这部分溶解态有机磷光解释放磷酸根过程尚未见报道,值得深入研究.
|
Fe (Ⅲ)浓度20 μmol·L-1,草酸盐浓度为400 μmol·L-1 图 7 草甘膦初始浓度对湖水草甘膦光解释放磷的影响 Fig. 7 Influence of initial glyphosate concentration on photochemical release of phosphate under UV-Vis irradiation |
Fe (Ⅲ)-草酸络合物可能发生的光化学反应如公式(3)~(9)所示[36, 37],其主要的活性物种为羟基自由基(·OH)和超氧自由基(O2·-).由于自然水中含有大量的溶解性有机碳、碳酸根、卤离子等物质,对这两种活性氧物质的产量及含量具有极为重要的影响.因此,测定Fe (Ⅲ)-草酸络合物在光诱导下产生的活性氧基团的含量对了解自然水中Fe (Ⅲ)-草酸络合物驱动草甘膦光解释放磷酸根的内在机制具有极为重要的意义.本研究先以香豆素为·OH分子探针,测定体系中·OH的稳态浓度.在本实验条件下,虽然自然湖水中成分复杂,但仍可以采用此方法粗略评估一下不同光照条件下Fe (Ⅲ)-草酸络合物体系中自然水中的·OH稳态浓度.如图 8,在紫外和太阳光下,羟基自由基(·OH)的产生速率可经七-羟基香豆素(7-HOC)的生成速率进行换算,当香豆素的浓度为0.1 mmol·L-1时,仅有6.1%羟基自由基(·OH)被捕获生成7-HOC[38].由以下公式计算:

|
香豆素浓度为0.1 mmol·L-1,Fe (Ⅲ)浓度20 μmol·L-1, 草酸盐浓度为400 μmol·L-1 图 8 紫外和太阳光照下七-羟基香豆素的产率 Fig. 8 Formation rate of 7-hydroxycoumarin under UV-Vis and sunlight irradiation |
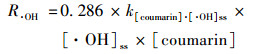
|
式中,R·OH为羟基自由基产生速率[μmol·(L·min)-1],[·OH]ss为羟基自由基稳态浓度(mol·L-1),[coumarin]为反应体系中香豆素浓度(mmol·L-1),k[coumarin]·[·OH]=6.4×109 mol·(L·s)-1[39, 40]为羟基自由基与香豆素的形成速率.
通过对7-HOC荧光强度的测定,证实羟基自由基(·OH)是Fe (Ⅲ)-草酸络合物中的主要活性物种之一.紫外和太阳光下7-HOC的生成速率分别为0.52×10-2 μmol·(L·min)-1和0.03×10-2μmol·(L·min)-1,羟基自由基(·OH)的稳态浓度分别为:紫外光下[·OH]ss=4.74×10-16 mol·L-1;太阳光下[·OH]ss=0.27×10-16 mol·L-1.
根据Liu等[18]的报道,O2·-也是Fe (Ⅲ)-草酸络合物体系中一种重要的活性氧物质.由公式(3),Fe (Ⅲ)-草酸络合物可以光解产生C2O4·-,C2O4·-可以与O2反应生成O2·-,O2·-同样可以降解有机物,使其形态结构发生改变.本研究以氯化氮蓝四唑(NBT)为O2·-分子探针,由以下公式计算:
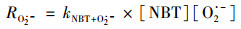
|
式中,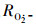

|
(3) |

|
(4) |

|
(5) |

|
(6) |

|
(7) |

|
(8) |

|
(9) |
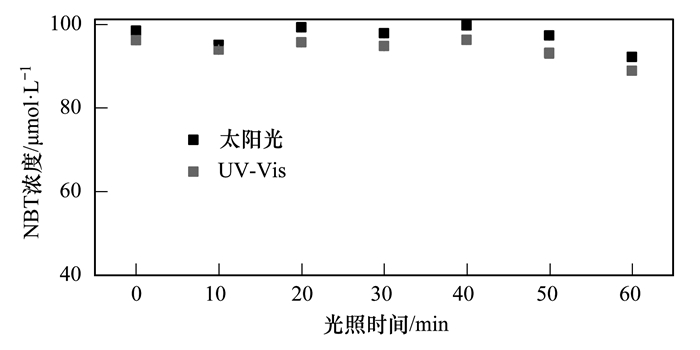
|
氮蓝四唑浓度为100 μmol·L-1,Fe (Ⅲ)浓度20 μmol·L-1,草酸盐浓度为400 μmol·L-1 图 9 紫外和太阳光下氯化氮蓝四唑的降解过程 Fig. 9 Degradation of NBT under UV-Vis and sunlight radiation |
根据活性氧物质稳态浓度的测定结果,·OH是Fe (Ⅲ)-草酸盐光诱导有机物降解的主要活性氧基团.为进一步探讨Fe (Ⅲ)-草酸盐对湖泊有机磷光解释放磷酸根的影响,本文以异丙醇为·OH猝灭剂,研究了紫外光照射条件下添加猝灭剂前后湖水+草甘膦体系与湖水+草甘膦+Fe (Ⅲ)-草酸盐体系中磷酸根的释放情况,异丙醇的初始浓度分别为0.1 mol·L-1和0.5 mol·L-1.从图 10可以看出,在湖水+草甘膦体系,添加0.1 mol·L-1异丙醇光照60 min后,磷酸根浓度由0.14 mg·L-1下降至0.13 mg·L-1,随着异丙醇浓度的提升,磷酸根浓度并未发生显著变化,表明部分磷酸根是由于水体中的草甘膦直接光解所致.就天然湖泊而言,尽管水样中同样含有Fe3+、NO3-等天然光敏物质,其可以在光诱导下产生活性氧基团.然而,水体中的碳酸根、腐殖质等又竞争消耗了产生的自由基,导致了湖水+草甘膦体系中外源添加异丙醇后磷酸根释放量抑制不明显.在湖水+草甘膦+Fe (Ⅲ)-草酸盐体系加入异丙醇,光照60 min后,添加0.1 mol·L-1异丙醇处理,磷酸根浓度由0.28 mg·L-1下降至0.25 mg·L-1,随着异丙醇浓度增加至0.5 mol·L-1,磷酸根浓度进一步降低至0.22 mg·L-1,添加异丙醇对Fe (Ⅲ)-草酸的光催化释放磷酸根有明显的抑制作用,这一结果证明,光照条件下,Fe (Ⅲ)-草酸络合物在有机磷光解释放磷酸根的过程中起着极为重要的作用.

|
草甘膦浓度为1.0 mg·L-1,Fe (Ⅲ)浓度20 μmol·L-1, 草酸盐浓度为400 μmol·L-1 图 10 异丙醇对湖水体中草甘膦光解释放磷酸根的影响 Fig. 10 Influence of isopropanol on photochemical release of phosphate under UV-Vis irradiation in lake water |
(1)本文研究了Fe (Ⅲ)-草酸络合物驱动有机磷光解释放磷酸根的过程.结果表明紫外和太阳光下,Fe (Ⅲ)-草酸络合物增大湖水中磷酸根的释放量.且这一过程显著受到环境因素的影响,一定浓度条件下增大Fe (Ⅲ)和草酸盐的浓度均可以加速这一过程.
(2) ·OH是湖水中Fe (Ⅲ)-草酸络合物光化学反应的主要活性物种,紫外和太阳光照射下,·OH的稳态浓度分别为4.74×10-16 mol·L-1和0.27×10-16 mol·L-1.以异丙醇为·OH猝灭剂,进一步证明Fe (Ⅲ)-草酸络合物在湖水中起着重要作用.
| [1] | Yin H B, Kong M, Fan C X. Batch investigations on P immobilization from wastewaters and sediment using natural calcium rich sepiolite as a reactive material[J]. Water Research, 2013, 47(13) : 4247–4258. DOI: 10.1016/j.watres.2013.04.044 |
| [2] | 郑西来, 张俊杰, 陈蕾. 再悬浮条件下沉积物内源磷迁移-转化机制研究进展[J]. 水科学进展, 2013, 24(2) : 287–295. Zheng X L, Zhang J J, Chen L. Advances in the study of migration and transformation mechanisms of endogenous phosphorus via sediment resuspension[J]. Advances in Water Science, 2013, 24(2) : 287–295. |
| [3] | 霍守亮, 李青芹, 昝逢宇, 等. 我国不同营养状态湖泊沉积物有机磷形态分级特征研究[J]. 环境科学, 2011, 32(4) : 1000–1007. Huo S L, Li Q Q, Zan F Y, et al. Characteristics of organic phosphorus fractions in different trophic sediments of lakes, China[J]. Environmental Science, 2011, 32(4) : 1000–1007. |
| [4] | 熊强, 焦立新, 王圣瑞, 等. 滇池沉积物有机磷垂直分布特征及其生物有效性[J]. 环境科学, 2014, 35(11) : 4118–4126. Xiong Q, Jiao L X, Wang S R, et al. Characteristics and bioavailability of organic phosphorus from different sources of sediments in Dianchi Lake[J]. Environmental Science, 2014, 35(11) : 4118–4126. |
| [5] | Bai X, Ding S, Fan C, et al. Organic phosphorus species in surface sediments of a large, shallow, eutrophic lake, Lake Taihu, China[J]. Environmental Pollution, 2009, 157(8-9) : 2507–2513. DOI: 10.1016/j.envpol.2009.03.018 |
| [6] | 左乐, 吕昌伟, 何江, 等. 微生物对冰封期湖泊沉积物中有机磷降解释放的影响[J]. 环境科学, 2015, 36(12) : 4501–4508. Zuo L, Lv C W, He J, et al. Impacts of microorganisms on degradation and release characteristics of organic phosphorus in lake sediments during freezing season[J]. Environmental Science, 2015, 36(12) : 4501–4508. |
| [7] | Kieber R J, Whitehead R F, Skrabal S A. Photochemical production of dissolved organic carbon from resuspended sediments[J]. Limnology and Oceanography, 2006, 51(5) : 2187–2195. DOI: 10.4319/lo.2006.51.5.2187 |
| [8] | Southwell M W, Kieber R J, Mead R N, et al. Effects of sunlight on the production of dissolved organic and inorganic nutrients from resuspended sediments[J]. Biogeochemistry, 2010, 98(1-3) : 115–126. DOI: 10.1007/s10533-009-9380-2 |
| [9] | Southwell M W, Mead R N, Luquire C M, et al. Influence of organic matter source and diagenetic state on photochemical release of dissolved organic matter and nutrients from resuspendable estuarine sediments[J]. Marine Chemistry, 2011, 126(1-4) : 114–119. DOI: 10.1016/j.marchem.2011.04.005 |
| [10] | Peng J F, Wang B Z, Song Y H, et al. Adsorption and release of phosphorus in the surface sediment of a wastewater stabilization pond[J]. Ecological Engineering, 2007, 31(2) : 92–97. DOI: 10.1016/j.ecoleng.2007.06.005 |
| [11] | Garrido-Ramírez E G, Theng B K G, Mora M L. Clays and oxide minerals as catalysts and nanocatalysts in Fenton-like reactions-A review[J]. Applied Clay Science, 2010, 47(3-4) : 182–192. DOI: 10.1016/j.clay.2009.11.044 |
| [12] | Francko D A, Heath R T. UV-sensitive complex phosphorus:association with dissolved humic material and iron in a bog lake[J]. Limnology and Oceanography, 1982, 27(3) : 564–569. DOI: 10.4319/lo.1982.27.3.0564 |
| [13] | 郭强, 田慧, 毛潇萱, 等. 珠江河口水域有机磷农药水生生态系统风险评价[J]. 环境科学, 2014, 35(3) : 1029–1034. Guo Q, Tian H, Mao X X, et al. Ecological risk assessment of organophosphorus pesticides in aquatic ecosystems of pearl river estuary[J]. Environmental Science, 2014, 35(3) : 1029–1034. |
| [14] | Thakur R S, Chaudhary R, Singh C. Fundamentals and applications of the photocatalytic treatment for the removal of industrial organic pollutants and effects of operational parameters:a review[J]. Journal of Renewable and Sustainable Energy, 2010, 2(4) : 042701. DOI: 10.1063/1.3467511 |
| [15] | Fang X W, Mark G, von Sonntag C. OH radical formation by ultrasound in aqueous solutions part I:the chemistry underlying the terephthalate dosimeter[J]. Ultrasonics Sonochemistry, 1996, 3(1) : 57–63. DOI: 10.1016/1350-4177(95)00032-1 |
| [16] | Louit G, Foley S, Cabillic J, et al. The reaction of coumarin with the OH radical revisited:hydroxylation product analysis determined by fluorescence and chromatography[J]. Radiation Physics and Chemistry, 2005, 72(2-3) : 119–124. DOI: 10.1016/j.radphyschem.2004.09.007 |
| [17] | Gamaley I A, Klyubin I V. Roles of reactive oxygen species:signaling and regulation of cellular functions[J]. International Review of Cytology, 1999, 188 : 203–255. DOI: 10.1016/S0074-7696(08)61568-5 |
| [18] | Liu G M, Zheng S R, Xing X L, et al. Fe (Ⅲ)-oxalate complexes mediated photolysis of aqueous alkylphenol ethoxylates under simulated sunlight conditions[J]. Chemosphere, 2010, 78(4) : 402–408. DOI: 10.1016/j.chemosphere.2009.11.002 |
| [19] | Van Moorleghem C, Schutter N D, Smolders E, et al. Bioavailability of organic phosphorus to Pseudokirchneriella subcapitata, as affected by phosphorus starvation:an isotope dilution study[J]. Water Research, 2013, 47(9) : 3047–3056. DOI: 10.1016/j.watres.2013.03.026 |
| [20] | Zhou Y Y, Song C L, Cao X Y, et al. Phosphorus fractions and alkaline phosphatase activity in sediments of a large eutrophic Chinese lake (Lake Taihu)[J]. Hydrobiologia, 2008, 599(1) : 119–125. DOI: 10.1007/s10750-007-9185-z |
| [21] | Chen Y, Wu F, Lin Y X, et al. Photodegradation of glyphosate in the ferrioxalate system[J]. Journal of Hazardous Materials, 2007, 148(1-2) : 360–365. DOI: 10.1016/j.jhazmat.2007.02.044 |
| [22] | Li D P, Huang Y, Fan C X, et al. Contributions of phosphorus on sedimentary phosphorus bioavailability under sediment resuspension conditions[J]. Chemical Engineering Journal, 2011, 168(3) : 1049–1054. DOI: 10.1016/j.cej.2011.01.082 |
| [23] | 欧晓霞, 王崇, 张凤杰, 等. 三价铁及其络合物光化学行为的研究进展[J]. 环境保护科学, 2010, 36(4) : 33–35. Ou X X, Wang C, Zhang F J, et al. Review of photochemical behavior of Fe (Ⅲ) and their complexes[J]. Environmental Protection Science, 2010, 36(4) : 33–35. |
| [24] | Gulshan F, Yanagida S, Kameshima Y, et al. Various factors affecting photodecomposition of methylene blue by iron-oxides in an oxalate solution[J]. Water Research, 2010, 44(9) : 2876–2884. DOI: 10.1016/j.watres.2010.01.040 |
| [25] | Zhao C, Arroyo-Mora L E, DeCaprio A P, et al. Reductive and oxidative degradation of iopamidol, iodinated X-ray contrast media, by Fe (Ⅲ)-oxalate under UV and Visible light treatment[J]. Water Research, 2014, 67 : 144–153. DOI: 10.1016/j.watres.2014.09.009 |
| [26] | Silva M R A, Trovó A G, Nogueira R F P. Degradation of the herbicide tebuthiuron using solar photo-Fenton process and ferric citrate complex at circumneutral pH[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2007, 191(2-3) : 187–192. DOI: 10.1016/j.jphotochem.2007.04.022 |
| [27] | Romero V, Acevedo S, Marco P, et al. Enhancement of Fenton and photo-Fenton processes at initial circumneutral pH for the degradation of the β-blocker metoprolol[J]. Water Research, 2016, 88 : 449–457. |
| [28] | Zhou D N, Wu F, Deng N S. Fe (Ⅲ)-oxalate complexes induced photooxidation of diethylstilbestrol in water[J]. Chemosphere, 2004, 57(4) : 283–291. DOI: 10.1016/j.chemosphere.2004.05.043 |
| [29] | Hislop K A, Bolton J R. The photochemical generation of hydroxyl radicals in the UV-Vis/Ferrioxalate/H2O2 system[J]. Environmental Science & Technology, 1999, 33(18) : 3119–3126. |
| [30] | Chen Y, Liu Z Z, Wang Z P, et al. Photodegradation of propranolol by Fe (Ⅲ)-citrate complexes:kinetics, mechanism and effect of environmental media[J]. Journal of Hazardous Materials, 2011, 194 : 202–208. DOI: 10.1016/j.jhazmat.2011.07.081 |
| [31] | Matykiewiczová N, Kurková R, Klánová J, et al. Photochemically induced nitration and hydroxylation of organic aromatic compounds in the presence of nitrate or nitrite in ice[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2007, 187(1) : 24–32. DOI: 10.1016/j.jphotochem.2006.09.008 |
| [32] | Zuo Y G, Hoigne J. Formation of hydrogen peroxide and depletion of oxalic acid in atmospheric water by photolysis of iron (Ⅲ)-oxalate complexes[J]. Environmental Science & Technology, 1992, 26(5) : 1014–1022. |
| [33] | Chang Y H, Ou C C, Yeh H W, et al. Photo-catalytic selectivity of anthranilic acid over iron oxide incorporated titania nanoparticles:influence of the Fe2+/Fe3+, ratio of iron oxide[J]. Journal of Molecular Catalysis A:Chemical, 2016, 412 : 67–77. DOI: 10.1016/j.molcata.2015.12.001 |
| [34] | Maranger R, Pullin M J. Elemental complexation by dissolved organic matter in lakes:implications for Fe speciation and the speciation and the bioavailability of Fe and P[A]. In:Findlay S E G, Sinsabaugh R L (Eds.). Aquatic Ecosystems:Interactivity of Dissolved Organic Matter[M]. San Diego:Academic Press, 2003. |
| [35] | Gardolinski P C F C, Worsfold P J, McKelvie I D. Seawater induced release and transformation of organic and inorganic phosphorus from river sediments[J]. Water Research, 2004, 38(3) : 688–692. DOI: 10.1016/j.watres.2003.10.048 |
| [36] | Lee J, Kim J, Choi W. Oxidation of aquatic pollutants by ferrous-oxalate complexes under dark aerobic conditions[J]. Journal of Hazardous Materials, 2014, 274 : 79–86. DOI: 10.1016/j.jhazmat.2014.03.056 |
| [37] | Monteagudo J M, Durán A, López-Almodóvar C. Homogeneus ferrioxalate-assisted solar photo-Fenton degradation of orange II aqueous solutions[J]. Applied Catalysis B:Environmental, 2008, 83(1-2) : 46–55. DOI: 10.1016/j.apcatb.2008.02.002 |
| [38] | Katsumata H, Koike S, Kaneco S, et al. Degradation of reactive yellow 86 with photo-Fenton process driven by solar light[J]. Journal of Environmental Sciences, 2010, 22(9) : 1455–1461. DOI: 10.1016/S1001-0742(09)60275-8 |
| [39] | Zhang J, Nosaka Y. Quantitative detection of OH radicals for investigating the reaction mechanism of various Visible-light TiO2 photocatalysts in aqueous suspension[J]. The Journal of Physical Chemistry C, 2013, 117(3) : 1383–1391. DOI: 10.1021/jp3105166 |
| [40] | Singh T S, Rao B S M, Mohan H, et al. A pulse radiolysis study of coumarin and its derivatives[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2002, 153(1-3) : 163–171. DOI: 10.1016/S1010-6030(02)00272-1 |
| [41] | Bielski B H J, Shiue G G, Bajuk S. Reduction of nitro blue tetrazolium by CO2- and O2- radicals[J]. The Journal of Physical Chemistry, 1980, 84(8) : 830–833. DOI: 10.1021/j100445a006 |
 2017, Vol. 38
2017, Vol. 38


