生物炭作为一类新型环境功能材料,在土壤改良、温室气体减排以及受污染环境修复方面都展现出巨大的应用潜力[1]. 有研究表明,生物炭具有发达的孔隙结构,表面含有大量的官能团和负电荷,对重金属离子有较强的吸附和固定能力[2, 3],并且能够调节土壤理化性质以及通过沉淀、吸附、离子交换、氧化-还原等一系列反应[4, 5],改变重金属元素在土壤中的化学形态和赋存状态[6],抑制其在土壤中可移动性和生物有效性,有效地降低土壤重金属污染程度,减轻重金属对作物生长的毒性作用[7, 8],从而达到修复污染土壤的目的. 在控制和治理土壤镉污染方面具有广阔的应用前景. 同时生物炭的制备原料非常广泛,成本较低,有利于大规模应用修复轻中度重金属污染农田土壤,实现固体废弃物的资源化利用.
目前,生物炭已被应用于修复受污染的土壤和水,由于生物炭是一种粗犷的富碳材料,其所具有的物化性质较为复杂,难以有较突出的化学功能性质,在环境应用中受到了一定的局限性,需要进一步的改进[9, 10]. 因此,近年来研究者主要集中于通过改性处理生物炭,使其结构和表面特征发生改变,从而提高修复功能和改善环境友好效应[11]. 生物炭的改性处理涉及各种方法,如酸处理、碱处理、胺化、表面活性剂改性、矿物吸附剂的浸渍、蒸汽活化和磁性改性[12~16],不同方法改性处理的生物炭已广泛用于对水中目标污染物的吸附/去除,但还缺乏对土壤中污染物的吸附及钝化效应研究[17, 18]. 改性方法的适用性主要由污染物(即:无机/有机、阴离子/阳离子、亲水性/疏水性、极性/非极性)、环境条件、修复目标等方面所决定[17]. 一般来说,改性处理后的生物炭材料能提高原生物炭的吸附能力及环境修复应用的潜力. 因此,本研究采用油菜秸秆生物炭原料,通过酸(HNO3)/碱(NaOH)改性制备的改性炭、KMnO4浸渍处理生物质后在600℃热解制备的MnOx-生物炭复合材料、FeCl3处理生物质后在600℃热解制备的磁性生物炭,应用于原土/外源镉污染的土壤中,探究其对目标污染物的钝化效应,旨在为后期改性生物炭材料应用于污染土壤修复提供一定的前景依据,同时明确生物炭表面含氧官能团、化学组分、物理结构的差异对重金属污染治理效果影响及其钝化机制具有重要意义.
1 材料与方法 1.1 试验材料 1.1.1 供试材料原生物质材料为油菜秸秆,于热解反应器(450℃,30 min)生产,所得到的样本标记为BC. BC-HNO3生物炭是用2 mol ·L-1的HNO3溶液在高温(100℃,24 h)处理制备[19],相应的生物炭质量与液体体积比为:0.1 g ·mL-1,处理后的样品用去离子水洗涤,直到pH值不再变化,然后将样品在烘箱中于105℃过夜干燥,处理后的生物炭样品储存在干燥器中; BC-NaOH生物炭是由2 mol ·L-1 NaOH 24 h处理[20],碱化处理与酸化处理步骤相同; BC-KMnO4生物炭是用2%的KMnO4溶液浸渍生物质处理后,经105℃烘干后移入坩埚中,加盖置于马弗炉中600℃煅烧2 h,相应的生物质质量与液体体积比为:0.1 g ·mL-1[21]; BC-FeCl3生物炭是由1 mol ·L-1的FeCl3溶液浸渍生物质处理后(铁与生物质质量比为0.56 ∶1) ,经105℃烘干后移入坩埚中,加盖置于马弗炉中600℃煅烧2 h[22],生物炭基本理化性质见表 1.
|
|
表 1 生物炭基本理化性质 1) Table 1 Basic physical and chemical properties of biochar |
1.1.2 供试土壤
供试土壤采自绵竹市兴隆镇安仁村4组(31.423 01°N, 104.225 37°E, 海拔629.6 m),土壤类型为灰棕色冲积物发育的潴育水稻土. 根据国际制法,土壤质地为黏壤土(颗粒组成2~0.02 mm 53.6%、0.02~0.002 mm 28.6%、<0.002 mm 17.8%). 基本理化性质见表 2,从中可以看出,试验区土壤镉含量远超过了国家土壤环境质量标准(GB 15618-1995) ,超过三级标准值(1.00 mg ·kg-1,pH<6.5) 3倍.
|
|
表 2 土壤基本理化性质 Table 2 Properties of tested soil |
1.2 试验设计与处理
原状土制备:以供试土壤为原状污染土壤(未添加外源镉),采集的供试土壤经室内风干,用玛瑙研钵研磨,过2 mm孔径尼龙筛,备用. 外源镉污染土壤制备:称取5 kg过2 mm孔径尼龙筛的风干土壤于盆铂中,加入100 mg ·L-1的Cd2+溶液500 mL(用CdCl2 ·2.5H2O配制),混合搅拌均匀,使土壤中外源添加镉含量为10mg ·kg-1,调节含水量为田间最大持水量的65%,室温下平衡30 d后风干,土样制备同上.
静态恒温培养试验于2015年6~9月进行,分别称取过2mm孔径筛的两种镉浓度污染水稻土(未添加外源镉污染的原状土和添加外源镉10 mg ·kg-1的污染土壤)100 g,将5种供试炭材料(BC、BC-HNO3、BC-NaOH、BC-KMnO4、BC-FeCl3)以质量分数2.5%、5%、10%的比例与土壤均匀混合,置于250 mL培养瓶中,共设置16个处理,按照65%的田间持水量添加去离子水到培养瓶中,用保鲜膜封口,并在保鲜膜中间留数个小孔. 将培养瓶置于25℃±1℃的恒温培养箱中培养,培养过程中采用称重法补充蒸发了的水分,使土壤水分维持在田间持水量的65%左右,每处理重复6次,培养周期为90 d. 在培养30 d、90 d后取土壤样品,自然风干后过筛备用.
1.3 样品测定土壤理化性质测定参考文献[23]进行,土壤有机碳测定采用重铬酸钾外加热法[23]测定,土壤中镉全量采用HNO3-HF-HClO4 (2 ∶2 ∶1,体积比)硝化处理,土壤有效态镉含量采用DTPA溶液浸提(GB/T 23739-2009 ),土壤镉形态分组按Tessier连续提取方法[24]测定. 可交换态(Exc-Cd)采用1.0 mol ·L-1 MgCl2(pH=7) 浸提,碳酸盐结合态(Carb-Cd)采用1.0 mol ·L-1NaOAc(用HAc调到pH=5) 浸提,铁锰氧化物结合态(FeMnOx-Cd)采用0.04 mol ·L-1 NH2OH ·HCl加入25%HOAc浸提,有机物结合态(Org-Cd)采用0.02 mol ·L-1HNO3 加入30% H2O2浸提,残渣态(Res-Cd)采用HNO3-HF-HClO4硝化处理. 土壤镉全量和各形态含量采用ICP-MS(型号:Agilent 7700X)测定,上机之前所有浸提液和消化液均通过0.25 μm滤膜. 在分析测试过程中,随机插入国家标准样品(GBW07403 for soil; GBW07603 for plant)以保证试验结果精度,国家标准样品来源于中国标准物质中心(National Research Center for CRM, China).
1.4 数据处理方法数据处理采用Microsoft Excel 2007,数据统计分析采用SPSS 17.0中LSD方法进行显著性检验(P≤0.05) .
2 结果与分析 2.1 改性生物炭对土壤有效态镉含量的影响 2.1.1 对原状土壤有效态镉含量的影响由图 1(a)可知,在原状土壤中添加5种不同的生物炭材料,短期培养30 d,均能有效降低土壤中有效态镉含量. 其中添加10%BC、5%BC-HNO3、各比例的BC-NaOH、10%BC-KMnO4、10%BC-FeCl3对有效态镉含量降低作用分别为37.2%、57.9%、58.8%、44.4%、37.5%较佳. NaOH改性的生物炭材料在短期内(30d)对土壤中有效态镉含量的抑制作用较佳. 由图 1(b)可知,培养90 d,各处理均能有效降低土壤中有效态镉的含量,且比培养30 d抑制效果作用更显著,BC-NaOH、BC-HNO3、BC-KMnO4这3种改性生物炭材料对土壤有效态镉的钝化作用较佳,其中10%BC-HNO3和10%BC-NaOH处理对原状土壤中有效态镉含量降低了52.6%和67.1%,5%和10%BC-KMnO4处理分别降低了73.6%和71.9%. 综上,BC-NaOH材料在短期(30 d)或长期(90 d)培养中对原状土壤有效态镉钝化效果较好,BC-KMnO4材料在长期(90 d)培养中对原状土壤有效态镉的钝化作用与其他4种炭材料相比更佳.

|
每个处理重复3次,不同字母表示各处理间在LSD多重比较(P≤0.05) 达显著性差异,下同 图 1 不同处理对原状土壤有效态镉含量影响 Fig. 1 Effect of different treatments on available Cd content of original soil |
外源污染土壤是在原状土壤中添加10mg ·kg-1外源镉制备的高浓度污染土. 由图 2(a)可知,在外源污染土壤中添加不同比例的5种炭材料,短期培养30 d,BC-HNO3材料对土壤中有效态镉有12%~26%的活化作用,可能是由于外源添加高浓度镉使土壤中活化态Cd2+较多,BC-HNO3材料呈酸性(表 1),可促进土壤中Cd2+的活化. BC-FeCl3材料中添加10%比例的处理显著降低了土壤中有效态镉含量,而添加2.5%、5%处理分别活化了0.375 mg ·kg-1、0.832 mg ·kg-1的土壤有效态镉含量. BC材料中添加2.5%的处理对土壤中有效态镉含量降低效果不显著,而5%和10%比例处理分别降低了0.262 mg ·kg-1和0.814 mg ·kg-1的有效态镉含量. 各比例的BC-NaOH和BC-KMnO4材料有效降低了土壤中有效态镉含量,其中2.5%BC-NaOH处理和10%BC-KMnO4处理对外源污染土壤中有效态镉的含量分别降低至0.622 mg ·kg-1 和0.536 mg ·kg-1最佳. 由图 2(b)可知,随着培养时间的延长,当培养90 d时,BC材料对外源污染土壤有效态镉无显著钝化作用,BC-HNO3材料却活化了3.8%~24.5%的有效态镉含量,其他3种炭材料对外源污染土壤的有效态镉钝化效果较显著. 其中添加BC-NaOH(2.5%、5%和10%)降低了13.1%~27.8%%,BC-KMnO4(2.5%、5%和10%)降低了5.2%~33.5%、BC-FeCl3(2.5%、5%和10%)降低了22.5%~32.5%,由此可见,长期培养(90 d),添加10%的BC-KMnO4对外源污染土壤有效态镉的钝化作用最佳.

|
图 2 不同处理对外源污染土壤有效态镉含量影响 Fig. 2 Effect of different treatments on available Cd content of exogenous contaminated soil |
图 3为培养30/90 d后,5种生物炭材料不同添加量处理对原状土壤中各形态镉的影响. 从图 3(a)可知,培养30 d后,表现为添加各比例(2.5%、5%、10%)的5种炭材料与对照相比,显著降低了土壤中可交换态镉含量,降幅在5.2%~64.8%之间,其中以BC-KMnO4和BC-NaOH材料降低的交换态镉含量较佳,降低幅度与对照相比均大于30%; 除添加5%和10%BC-FeCl3材料降低了2.1%~3.5%碳酸盐结合态镉含量,其余各处理与对照相比,均提升了土壤碳酸盐结合态镉(10% BC-KMnO4最佳)、铁锰氧化物结合态(10%的BC-HNO3最佳)、有机物结合态镉含量(10%的BC最佳). 添加各比例BC-NaOH与其他材料相比对土壤中残渣态镉含量增长较高,在10.5%~31.9%之间.

|
Res表示残渣态镉,Org表示有机结合态镉,Ox表示铁锰氧化物结合态镉,Car表示碳酸盐结合态镉,Exc表示可交换态态镉,下同 图 3 不同处理原状土壤中各形态镉含量百分比 Fig. 3 Ratio of each cadmium speciation to total content of cadmium in different original soil treatments after 30 and 90 days of cultivation |
随着培养时间的延长,不同生物炭处理对原状土壤中各形态镉的影响(90 d培养)见图 3(b),添加各比例(2.5%、5%、10%)的5种炭材料与对照相比,降低了土壤中可交换态镉含量,降幅在3.5%~65.1%; 以添加10%BC-KMnO4降低可交换态镉含量最佳; 添加各比例的BC-NaOH和BC-KMnO4,与对照相比,对土壤碳酸盐结合态镉含量(2.5%的BC-KMnO4最佳)、铁锰氧化物结合态镉含量(10%的BC-NaOH最佳)和有机物结合态的镉含量(2.5%的BC-KMnO4最佳)均有所增长; 添加各比例的BC-FeCl3,与对照相比,降低了19.2%~42.7%的碳酸盐结合态镉含量和19.1%~32%的铁锰氧化物结合态镉含量,却提升了15.1%~70.8%的残渣态镉含量; 添加各比例的BC-HNO3,与对照相比,提升了55.3%~69.1%土壤铁锰氧化物结合态镉含量和近1.11倍的有机物结合态镉含量; 添加5%和10%的BC,与对照相比,提升了近1.13倍的土壤有机物结合态镉含量.
综上,原状土壤中,5种生物炭不同比例添加于土壤中,培养30 d/90 d后均显著降低土壤中可交换态镉含量,其中以BC-KMnO4材料效果最佳.
2.2.2 对外源污染土镉形态的影响图 4为培养30 d/90 d后,5种生物炭不同添加量处理对外源污染土壤中各形态镉的影响. 由图 4(a)可知,在外源污染土壤中培养30 d后,各比例(2.5%、5%、10%)的BC、BC-FeCl3、BC-NaOH和BC-KMnO4处理与对照相比,降低了7.9%~49.5%的土壤可交换态镉含量,以添加10%的BC-FeCl3处理最佳,而添加各比例的BC-HNO3处理与对照相比,提升土壤可交换态镉含量高达11.9%,存在一定的危害风险; 添加各比例的BC、BC-NaOH和BC-KMnO4,与对照相比,提高了土壤碳酸盐结合态镉,以添加10%的BC-KMnO4提高1倍最佳,而添加各比例的BC-HNO3和BC-FeCl3,与对照相比,却降低了3.6%~57.9%的土壤碳酸盐结合态镉的含量,说明BC-HNO3和BC-FeCl3这2种生物炭材料呈酸性,可能会增加土壤中H+,导致碳酸根离子的释放,碳酸盐与镉的结合物易遭到破坏; 添加各比例的BC、BC-HNO3、BC-NaOH和BC-KMnO4,与对照相比,降低2.1%~31.4%的土壤铁锰氧化物结合态和5.4%~55.5%的土壤有机物结合态镉含量; 5种炭材料处理与对照相比,均提高了土壤残渣态的镉含量,其中添加各比例BC-FeCl3对土壤中残渣态镉含量增长较高,涨幅在1.18~1.43倍.

|
图 4 不同处理外源污染土壤中各形态镉含量百分比 Fig. 4 Ratio of each cadmium speciation to total content of cadmium in different exogenous contaminated soil treatments after 30 and 90 days of cultivation |
不同生物炭材料处理对外源污染土壤中各形态镉的影响(90 d培养)见图 4(b),各比例(2.5%、5%、10%)的BC、BC-FeCl3、BC-NaOH和BC-KMnO4处理与对照相比,降低了土壤中可交换态镉含量,降幅在4.7%~47.9%之间,以添加10%的BC-NaOH降低作用最佳,而添加各比例的BC-HNO3在培养90 d后,依旧提升了7.2%~20.2%的土壤可交换态镉含量; 添加各比例BC、BC-NaOH和BC-KMnO4,与对照相比,提高了3.5%~56.4%土壤碳酸盐结合态镉含量,这同样也说明了土壤碳酸盐结合态镉易受H+/OH-的影响; 添加各比例的BC、BC-FeCl3对土壤铁锰氧化物结合态镉含量增加了22.5%~56.6%; 而各比例的BC-FeCl3对土壤有机物结合态镉含量增长了0.34~1.05倍较佳; 5种炭材料与对照相比,对土壤残渣态镉含量均有所增长,以BC-KMnO4处理提高了0.66~0.75倍的土壤残渣态镉含量较佳.
综上,在外源污染土壤中,5种生物炭不同比例添加于土壤中,培养30 d/90 d后土壤中可交换态镉含量除BC-HNO3材料呈增长趋势外,其余4种生物炭材料均显著降低土壤中可交换态镉含量,其中30 d培养以BC-FeCl3材料效果最佳,90 d培养以BC-NaOH材料最佳.
2.3 对土壤pH的影响图 5为不同生物炭材料处理对土壤pH值的影响. 从中可知,添加生物炭及改性炭材料培养30 d和90 d后对土壤pH有一定的影响,表现为添加各比例(2.5%、5%、10%)的BC-NaOH、BC-KMnO4的2种炭材料在培养30 d/90 d后,与对照相比,均显著提高了土壤pH(7.2~8.2) . 原状土壤中,各比例的BC处理在培养30 d后,显著提高了土壤pH(7.0~7.5) ,但培养90 d后,对土壤pH的影响无显著性变化; 外源污染土壤中,各比例的BC处理在培养30 d/90 d后,与对照相比,均显著提高了土壤pH(7.1~7.8) .

|
不同字母表示各处理间在LSD多重比较(P≤0.05) 达显著性差异,下同 图 5 不同处理对土壤中pH的影响 Fig. 5 Influence of different treatments on soil pH after 30 days and 90 days of cultivation |
原状土壤中,添加各比例的BC-HNO3处理在培养30 d/90 d后,显著降低了土壤pH(5.9~6.3) ,各比例的BC-FeCl3处理在培养30 d后,显著降低了土壤pH (5.8~6.7) ,但培养90 d后,显著提高了土壤pH(7.3~7.7) ; 外源土壤中,添加各比例的BC-HNO3和BC-FeCl3处理在培养30 d后,降低了土壤pH(5.8~6.5) ,当培养90 d时,添加BC-HNO3和BC-FeCl3的土壤pH与培养30 d相比,提升了0.2~0.8,2.5%和5%BC-FeCl3处理在培养90 d后,土壤pH值高于对照. 综上,添加原生物炭及改性生物炭材料于低/高镉污染土壤中,各比例(2.5%、5%、10%)的BC、BC-NaOH、BC-KMnO4对土壤pH有一定的提升作用,而BC-HNO3对土壤pH有一定的降低作用.
2.4 对土壤有机碳的影响图 6为添加不同比例(2.5%、5%、10%)的5种生物炭于土培试验中对有机碳的影响. 从中可知,各处理与对照相比,30 d/90 d培养后均增加了土壤中有机碳的含量,在原状土壤中尤以添加10%BC-FeCl3在培养30 d后,对土壤中有机碳含量增长2.38倍最高; 10%的BC在培养90 d后,对土壤有机碳的涨幅较其他处理明显,涨幅近3倍. 在外源污染土壤中,添加10%BC-KMnO4、10% BC-HNO3、10%BC-FeCl3处理在30 d/90 d培养后对土壤中有机碳含量比对照增长2倍多较高.

|
图 6 不同处理对土壤中有机碳(SOC)的影响 Fig. 6 Influence of different treatments on SOC after 30 days and 90 days of cultivation |
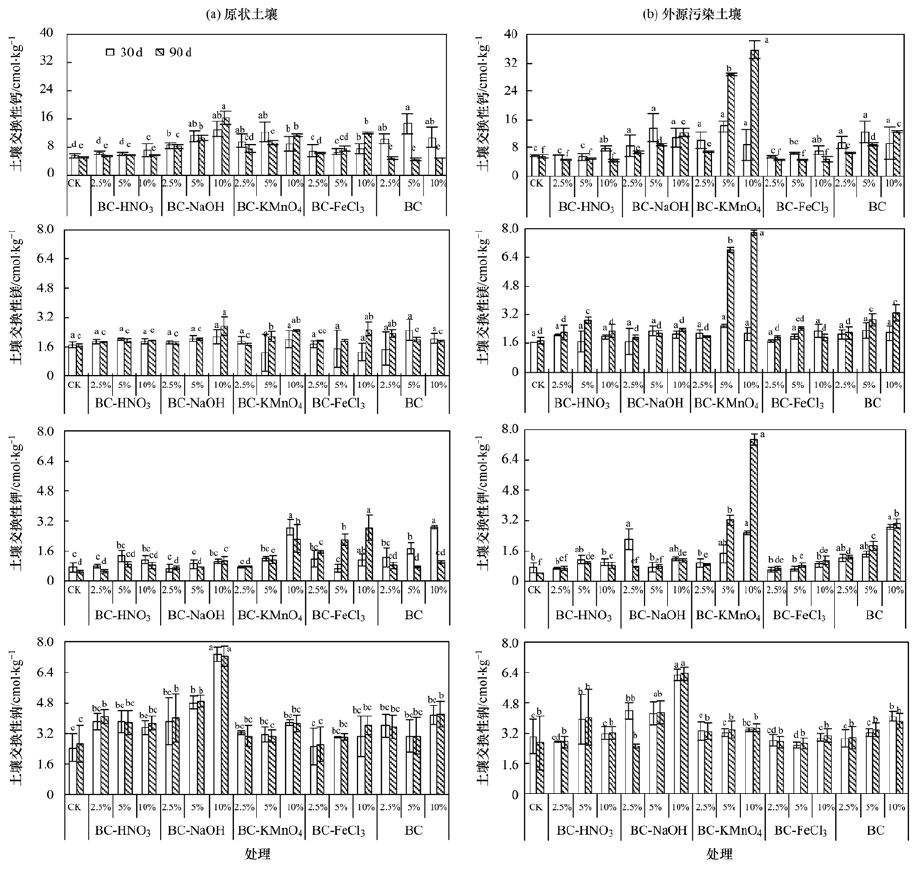
图 7为原生物炭及改性炭于土培试验中对土壤中交换性钙、镁、钾、钠离子含量的影响.
|
图 7 不同处理对土壤中交换性盐基离子的影响 Fig. 7 Influence of different treatments on soil exchangeable Ca2+, Mg2+, K+, Na+ after 30 days and 90 days of cultivation |
土壤中添加BC-NaOH、BC-KMnO4和BC对土壤交换性钙离子含量在培养30 d/90 d与对照相比,均有所增长,其中在原状污染土中以添加BC-NaOH较佳,增长达1.83倍,在外源高浓度镉污染土中以添加BC-KMnO4较佳,增长达2.18倍. 培养30 d时,5种炭材料处理对土壤交换性镁离子含量无显著性影响,但培养90 d后,各处理对土壤中交换性镁离子含量有显著的提升,说明随培养时间的延长,生物炭可增强土壤胶体对镁离子的吸附. 添加BC-NaOH,土壤培养30 d/90 d后都显著提升了交换性钠离子的含量,其中以10%BC-NaOH作用最强,对土壤交换性钠离子含量增长达2.7倍多,而其他炭材料不及BC-NaOH材料,主要由于NaOH改性处理原生物炭,增加了其钠离子含量,从而在土培试验中增加了土壤交换性钠离子的含量. 添加BC-NaOH、BC-KMnO4和 BC在培养30 d后,与对照相比,都显著提高了土壤交换性钾离子含量,随着培养时间的延长(培养90 d),添加BC-KMnO4较对照及其他炭材料表现出显著的增长趋势,以10%BC-KMnO4处理较对照提高作用最强,达4.8倍,说明KMnO4改性处理原生物炭,增加了其钾离子含量,在土培试验中,随着时间的延长,BC-KMnO4炭材料释放出钾离子,增加了土壤交换性钾离子的含量.
2.6 土壤有效态镉与各因素的相关性分析及逐步回归分析将土壤有效态镉含量与土壤pH、有机碳和土壤交换性盐基离子进行相关性分析,由表 3可知,原状土壤中,有效态镉含量与pH、土壤交换性钠离子含量呈显著负相关,相关系数分别为-0.651、-0.305,将各指标进行逐步回归分析,其线性回归方程为:Y= 4.463-0.494 X1(pH),R2=0.443; 外源污染土壤中,有效态镉含量与pH、土壤交换性镁、钾、钠离子含量、有机碳呈显著负相关,相关系数分别为-0.414、-0.452、-0.285、-0.203、-0.321,其线性回归方程为:Y=13.184-0.925 X1(pH)-0.018X2(SOC)-0.277X3(Mg),R2=0.358. 说明在原状土壤中,提高土壤pH和土壤交换性钠离子含量可以有效降低有效态镉的含量; 在外源污染土壤中(高浓度镉污染),不仅pH、土壤交换性钠离子含量是影响土壤有效态镉含量的因素,土壤交换性镁、钾离子含量和有机碳也是影响土壤有效态镉含量的重要因素.
|
|
表 3 土壤有效态镉与土壤理化性质间的相关性分析 Table 3 Correlation analysis of soil available Cd and soil chemical properties |
3 讨论
对生物炭进行改性,将导致其表面性质的变化,包括表面积,表面电荷,官能团,和孔体积及分布. 据报道,利用NaOH、H2O2、H2SO4/HNO3等改性生物炭,能够提高生物炭的比表面积,增加生物炭表面的官能团(如羧基),提高生物炭对污染物的固定能力[25]. Regmi等[26]用KOH改性生物炭后,比表面积达5.01 m2 ·g-1,是未改性生物炭的2.4倍,改性后的生物炭对Cd2+的吸附能力(34 mg ·g-1)高于原生物炭(31 mg ·g-1); Song等[13]将生物质与KMnO4溶液混合处理并置于反应釜煅烧制成MnOx-生物炭炭复合材料(MBC),与原始炭相比,孔径增加(BC:23.7 nm; MBC:92.2 nm),对Cu2+的最大吸附量显著提高(BC:19.6 mg ·g-1; MBC:160.3 mg ·g-1); Mohan等[27]通过制备铁氧化物与生物炭的复合材料,也发现生物炭炭孔容增大(0.01~0.69 cm3 ·g-1),对水中Cd2+的饱和吸附量(7.4 mg ·g-1)大于未经改性的生物炭(0.37 mg ·g-1).
本研究改性处理后生物炭形貌结构发生变化,其微观形貌结构如图 8所示. 改性生物炭的平均孔径在3~11 nm,属于介孔孔径,FeCl3处理扩大了1.52倍原炭的平均孔径,KMnO4、HNO3、NaOH处理扩大了原炭的比表面积、总孔体积,其中BC-KMnO4的比表面积(110.68 m2 ·g-1)和总孔体积(0.087 cm3 ·g-1)最大,分别是 BC的6倍和2.56倍. 5种炭中BC-KMnO4含氧官能团总量较多,阳离子交换能力较强,金属-配体络合作用也较强,BC-FeCl3和BC-HNO3酸性官能团数量较多,羧基和酚羟基显著增加(表 1).

|
图 8 生物炭材料的电镜扫描 Fig. 8 SEM analysis of BCs |
一般认为,添加生物炭材料是降低土壤重金属镉有效性的有效途径之一[28]. 有研究表明,生物炭本身具有高度芳香化的结构,含有大量酚羟基、羧基和羰基,这些基本性质使生物炭具备了良好的吸附特性及稳定性,生物炭对重金属的吸附机制主要有静电吸附作用、离子交换作用、表面矿物组分的吸附作用、阳离子-π作用、表面官能团的作用和沉淀作用,因此可强烈吸附土壤中的重金属并影响其迁移性,可有效降低土壤镉的生物有效性[29]. 将生物炭及4种方法改性处理后的生物炭添加于原状/外源镉污染土壤中进行试验,培养结束后主要表现为:在原状土壤中,均能有效降低土壤有效态镉的含量,其中BC-NaOH和BC-KMnO4材料对原状土中有效态镉的钝化作用超过50%; 在外源污染土壤中,BC材料对土壤有效态镉无显著钝化作用,改性处理后的生物炭BC-NaOH、BC-KMnO4、BC-FeCl3 均可有效降低土壤有效态镉含量,以添加10%的BC-KMnO4降低作用超30%最佳,但BC-HNO3在外源污染土壤中,活化了3.8%~24.5%的有效态镉,这可能是由于外源添加高浓度镉使土壤中活化态Cd2+较多,而BC-HNO3材料呈酸性(表 1),促进了土壤中Cd2+的活化. 综上,BC-KMnO4材料在原状/外源镉污染土壤原位钝化作用较优. 可能由于BC-KMnO4的比表面积和总孔体积在5种材料中最大,进入土壤中,能够有效吸附、固持Cd2+,且MnOx负载于生物炭中,与土壤中Cd2+可形成络合物,或通过阳离子或阳离子π键离子交换作用增强对Cd2+的吸附能力[13]; 同时该材料对土壤理化性质的影响较其他4种材料稳定,可能适宜于抑制有效态镉的释放.
施入生物炭及其改性炭材料后,会通过直接的吸附或络合螯合作用或者通过改变土壤的特性(如 pH值等)间接影响重金属在土壤中的化学形态,进而对重金属在土壤中的迁移性和生物可利用性产生影响[30, 31]. 一般来说,生物炭的施用会降低重金属可交换态的含量,从而降低重金属在土壤中的迁移性和生物可利用性[6]. 高译丹等[33]研究表明,在土壤中添加生物炭材料,可以有效地降低土壤可交换态镉的比例,增加了碳酸盐结合态、铁锰氧化物结合态、有机结合态和残渣态镉的比例,从而降低了土壤重金属的生物有效性. 本研究表明,添加原生物炭及改性生物炭材料,均降低了原状土壤中可交换态镉含量,以BC-KMnO4材料效果最佳. 在外源土壤中,BC-HNO3材料增加了7.2%~20.2%的土壤可交换态镉含量,可能由于BC-HNO3材料呈酸性,会增加土壤中H+,导致土壤中CO32-的释放,碳酸盐与镉形成的络合物易遭到破坏,同时土壤在H+富集状态下易释放出Fe2+/Fe3+、Mn2+等,铁锰氧化物与镉形成的络合物或沉淀也易崩解,释放出活性态镉; 其余4种生物炭材料均降低了土壤中可交换态镉含量. 各处理对土壤中各形态镉含量变化趋势主要表现为降低了土壤中可交换态镉含量,而碳酸盐结合态、铁锰氧化物结合态、有机氧化物结合态和残渣态镉含量呈上升趋于稳定,说明添加生物炭处理土壤后,污染土壤中的活性态镉逐渐向活性较低的化学形态转化,且随着活性形态含量比例趋于稳定,活性较低的化学形态又向活性更低的化学形态缓慢转化[28, 33].
施入生物炭及其改性炭材料后,会影响土壤理化特性(如pH值变化等),间接影响重金属在土壤中的活性. 有研究表明土壤pH值及有机质含量都与有效态铅和有效态镉含量存在负相关关系,提高土壤pH、施入有机钝化剂是抑制土壤重金属活性的有效途径[34, 35]. Houben[6]认为生物炭施用导致pH值的增加进而形成重金属沉淀是其机制之一. Cui等[29]认为生物炭能够提高土壤的pH,增加土壤有机质含量,能够显著影响土壤中重金属的形态和迁移行为,提高重金属离子的稳定性,使土壤中的重金属离子从可交换态向更稳定的状态转化,起到钝化重金属离子的作用. 本研究表明,土壤pH、有机碳含量与土壤有效态镉含量存在负相关关系,提高土壤pH、有机碳含量,可降低土壤有效态镉含量,与以上研究结果一致. 与此同时,本研究还探讨了盐基离子与土壤有效态镉含量的关系,通过相关性分析,土壤交换性钾、钠、镁含量与土壤有效态镉含量存在显著负相关关系,说明盐基离子浓度增大也能一定程度降低土壤有效态镉含量.
综上,在镉污染土壤钝化效应中,BC-KMnO4改性生物炭较佳,可作为原位钝化修复剂; BC-HNO3改性生物炭在高浓度镉污染土壤中使用,可能存在提高土壤镉生物有效态含量及比例的风险.
4 结论(1) 在原状镉污染土壤中,改性生物炭(BC-HNO3、BC-FeCl3、BC-KMnO4、BC-NaOH)均能降低有效态镉含量,尤以BC-KMnO4、BC-NaOH较好,钝化作用超过50%; 改性生物炭材料均降低了可交换态镉含量,添加10%的BC-KMnO4降低可交换态镉含量达65.1%最佳.
(2) 外源高浓度镉污染土壤中,改性生物炭(BC-FeCl3、BC-KMnO4、BC-NaOH)均降低了土壤有效态/可交换态镉含量,以添加10%的BC-KMnO4对有效态镉的钝化作用超30%和添加10%的BC-NaOH降低可交换态镉含量达47.9%为佳; 而BC-HNO3改性生物炭增加了3.8%~24.5%土壤有效态镉含量和7.2%~20.2%土壤可交换态镉含量,具有促进镉生物有效性的风险.
| [1] | Zhang X K, Li Q, Liang W J, et al. Soil nematode response to biochar addition in a chinese wheat field[J]. Pedosphere , 2013, 23 (1) : 98–103. DOI:10.1016/S1002-0160(12)60084-8 |
| [2] | Cantrell K B, Hunt P G, Uchimiya M, et al. Impact of pyrolysis temperature and manure source on physicochemical characteristics of biochar[J]. Bioresource Technology , 2012, 107 : 419–428. DOI:10.1016/j.biortech.2011.11.084 |
| [3] | Jiang T Y, Jiang J, Xu R K, et al. Adsorption of Pb (Ⅱ) on variable charge soils amended with rice-straw derived biochar[J]. Chemosphere , 2012, 89 (3) : 249–256. DOI:10.1016/j.chemosphere.2012.04.028 |
| [4] | Beesley L, Moreno-Jiménez E, Gomez-Eyles J L, et al. A review of biochars' potential role in the remediation,revegetation and restoration of contaminated soils[J]. Environmental Pollution , 2011, 159 (12) : 3269–3282. DOI:10.1016/j.envpol.2011.07.023 |
| [5] | Xu R K, Zhao A Z. Effect of biochars on adsorption of Cu (Ⅱ),Pb (Ⅱ) and Cd (Ⅱ) by three variable charge soils from southern China[J]. Environmental Science and Pollution Research , 2013, 20 (12) : 8491–8501. DOI:10.1007/s11356-013-1769-8 |
| [6] | Houben D.Heavy metal mobility in contaminated soils as affected by plants,amendments and biochar:implications for phytostabilization[D].Belgium:Universite Catholique de Louvain,2013. |
| [7] | Ahmad M, Lee S S, Lim J E, et al. Speciation and phytoavailability of lead and antimony in a small arms range soil amended with mussel shell,cow bone and biochar:EXAFS spectroscopy and chemical extractions[J]. Chemosphere , 2014, 95 : 433–441. DOI:10.1016/j.chemosphere.2013.09.077 |
| [8] | Xing Y, Liu J J, Mcgrouther K, et al. Effect of biochar on the extractability of heavy metals (Cd,Cu,Pb,and Zn) and enzyme activity in soil[J]. Environmental Science and Pollution Research , 2016, 23 (2) : 974–984. DOI:10.1007/s11356-015-4233-0 |
| [9] | Paria S. Surfactant-enhanced remediation of organic contaminated soil and water[J]. Advances in Colloid&Interface Science , 2008, 138 (1) : 24–58. |
| [10] | Vithanage M, Rajapaksha A U, Ahmad M, et al. Mechanisms of antimony adsorption onto soybean stover-derived biochar in aqueous solutions[J]. Journal of Environmental Management , 2015, 151 : 443–449. DOI:10.1016/j.jenvman.2014.11.005 |
| [11] | Ok Y S, Chang S X, Gao B, et al. SMART biochar technology-A shifting paradigm towards advanced materials and healthcare research[J]. Environmental Technology&Innovation , 2015, 4 : 206–209. |
| [12] | Qian K Z, Kumar A, Zhang H L, et al. Recent advances in utilization of biochar[J]. Renewable and Sustainable Energy Reviews , 2015, 42 : 1055–1064. DOI:10.1016/j.rser.2014.10.074 |
| [13] | Song Z G, Fei L, Yu Z H, et al. Synthesis and characterization of a novel MnOx-loaded biochar and its adsorption properties for Cu2+ in aqueous solution[J]. Chemical Engineering Journal , 2014, 242 : 36–42. DOI:10.1016/j.cej.2013.12.061 |
| [14] | Zhang X, Zhang S H, Yang H P, et al. Influence of NH3/CO2 modification on the characteristic of biochar and the CO2 capture[J]. BioEnergy Research , 2013, 6 (4) : 1147–1153. DOI:10.1007/s12155-013-9304-9 |
| [15] | Yakout S M, Daifullah A E H M, El-Reefy S A. Pore structure characterization of chemically modified biochar derived from rice straw[J]. Environmental Engineering and Management Journal , 2015, 14 (2) : 473–480. |
| [16] | Zhang M, Gao B, Varnoosfaderani S, et al. Preparation and characterization of a novel magnetic biochar for arsenic removal[J]. Bioresource Technology , 2013, 130 : 457–462. DOI:10.1016/j.biortech.2012.11.132 |
| [17] | Rajapaksha A U, Chen S S, Tsang D C W, et al. Engineered/designer biochar for contaminant removal/immobilization from soil and water:Potential and implication of biochar modification[J]. Chemosphere , 2016, 148 : 276–291. DOI:10.1016/j.chemosphere.2016.01.043 |
| [18] | Lv H H, Gong Y Y, Tang J C, et al. Advances in preparation and applications of biochar and its composites[J]. Journal of Agro-Environment Science , 2015, 34 (8) : 1429–1440. 吕宏虹, 宫艳艳, 唐景春, 等. 生物炭及其复合材料的制备与应用研究进展[J]. 农业环境科学学报 , 2015, 34 (8) : 1429–1440. |
| [19] | Liu P, Liu W J, Jiang H, et al. Modification of biochar derived from fast pyrolysis of biomass and its application in removal of tetracycline from aqueous solution[J]. Bioresource Technology , 2012, 121 : 235–240. DOI:10.1016/j.biortech.2012.06.085 |
| [20] | Li Y C, Shao J G, Wang X H, et al. Characterization of modified biochars derived from bamboo pyrolysis and their utilization for target component (furfural) adsorption[J]. Energy Fuels , 2014, 28 (8) : 5119–5127. DOI:10.1021/ef500725c |
| [21] | Yu Z H, Xie L K, Liu S, et al. Effects of biochar-manganese oxides composite on adsorption characteristics of Cu in red soil[J]. Ecology and Environmental Sciences , 2014, 23 (5) : 897–903. 于志红, 谢丽坤, 刘爽, 等. 生物炭-锰氧化物复合材料对红壤吸附铜特性的影响[J]. 生态环境学报 , 2014, 23 (5) : 897–903. |
| [22] | Jiang X T, Chi J. Phosphorus adsorption by and forms in Fe-modified biochar[J]. Journal of Agro-Environment Science , 2014, 33 (9) : 1817–1822. 蒋旭涛, 迟杰. 铁改性生物炭对磷的吸附及磷形态的变化特征[J]. 农业环境科学学报 , 2014, 33 (9) : 1817–1822. |
| [23] | Nu R K. Soil agricultural chemical analysis method[M]. Beijing: China Agricultural Science and Technology Press, 2000 . 鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000 . |
| [24] | Tessier A, Campbell P G C, Bisson M. Sequential extraction procedure for the speciation of particulate trace metals[J]. Analytical Chemistry , 1979, 51 (7) : 844–851. DOI:10.1021/ac50043a017 |
| [25] | Uchimiya M, Bannon D I, Wartelle L H. Retention of heavy metals by carboxyl functional groups of biochars in small arms range soil[J]. Journal of Agricultural and Food Chemistry , 2012, 60 (7) : 1798–1809. DOI:10.1021/jf2047898 |
| [26] | Regmi P, Garcia Moscoso J L, Kumar S, et al. Removal of copper and cadmium from aqueous solution using switchgrass biochar produced via hydrothermal carbonization process[J]. Journal of Environmental Management , 2012, 109 : 61–69. DOI:10.1016/j.jenvman.2012.04.047 |
| [27] | Mohan D, Kumar H, Sarswat A, et al. Cadmium and lead remediation using magnetic oak wood and oak bark fast pyrolysis bio-chars[J]. Chemical Engineering Journal , 2014, 236 : 513–528. DOI:10.1016/j.cej.2013.09.057 |
| [28] | 徐楠楠.生物炭对Cd污染土壤钝化修复效应研究[D].吉林:吉林大学,2014.32-36. Xu N N.The effects of biochar on immobilization remediation of soil contaminated by cadmium[D].Jilin:Jilin University,2014.32-36. http://cdmd.cnki.com.cn/article/cdmd-10183-1014281553.htm |
| [29] | Cui L Q, Pan G X, Li L Q, et al. The reduction of wheat Cd uptake in contaminated soil via biochar amendment:a two-year field experiment[J]. BioResources , 2012, 7 (4) : 5666–5676. |
| [30] | Namgay A T, Singh B, Singh B P. Influence of biochar application to soil on the availability of As,Cd,Cu,Pb,and Zn to maize (Zea mays L^)[J]. Australian Journal of Soil Research , 2010, 48 (7) : 638–647. DOI:10.1071/SR10049 |
| [31] | Zhang X K, Wang H L, He L Z, et al. Using biochar for remediation of soils contaminated with heavy metals and organic pollutants[J]. Environmental Science and Pollution Research , 2013, 20 (12) : 8472–8483. DOI:10.1007/s11356-013-1659-0 |
| [32] | Cao Y, Di J M, Shen D, et al. Effects of biochar on soil cadmium forms and cadmium accumulation in peanut kernels[J]. Ecology and Environmental Sciences , 2015, 24 (4) : 688–693. 曹莹, 邸佳美, 沈丹, 等. 生物炭对土壤外源镉形态以及花生籽粒富集镉的影响[J]. 生态环境学报 , 2015, 24 (4) : 688–693. |
| [33] | Gao Y D, Liang C H, Pei Z J, et al. Effects of biochar and lime on the fraction transform of cadmium in contaminated soil[J]. Journal of Soil and Water Conservation , 2014, 28 (2) : 258–261. 高译丹, 梁成华, 裴忠健, 等. 施用生物炭和石灰对土壤镉形态转化的影响[J]. 水土保持学报 , 2014, 28 (2) : 258–261. |
| [34] | Wu M, Xu M G, Xu S H, et al. Effects of organic matter on the stabilization process of added cadmium and lead in red soil and black soil[J]. Journal of Agro-Environment Science , 2011, 30 (3) : 461–467. 吴曼, 徐明岗, 徐绍辉, 等. 有机质对红壤和黑土中外源铅镉稳定化过程的影响[J]. 农业环境科学学报 , 2011, 30 (3) : 461–467. |
| [35] | Guo W J, Liang X F, Lin D S, et al. Adsorption of Cd2+ on biochar from aqueous solution[J]. Environmental Science , 2013, 34 (9) : 3716–3721. 郭文娟, 梁学峰, 林大松, 等. 土壤重金属钝化修复剂生物炭对镉的吸附特性研究[J]. 环境科学 , 2013, 34 (9) : 3716–3721. |
 2016, Vol. 37
2016, Vol. 37


