引用本文

徐彬, 陈天虎, 刘海波, 朱承驻, 陈冬, 邹雪华, 蒋阳 . 热处理天然褐铁矿制备
γ-Fe
2O
3及其NH
3-SCR活性探究[J]. 环境科学,2016, 37(7): 2807-2814.

XU Bin, CHEN Tian-hu, LIU Hai-bo, ZHU Cheng-zhu, CHEN Dong, ZOU Xue-hua, JIANG Yang . Preparation of
γ-Fe
2O
3 Catalyst by Heat Treatment of Natural Limonite for Selective Catalytic Reduction of NO by NH
3[J]. Environmental Science,2016, 37(7): 2807-2814.

热处理天然褐铁矿制备γ-Fe2O3及其NH3-SCR活性探究
徐彬
1
, 陈天虎
1

, 刘海波
1 , 朱承驻
1 , 陈冬
1 , 邹雪华
1 , 蒋阳
2
1.合肥工业大学资源与环境工程学院, 合肥 230009;
2.合肥工业大学材料科学与工程学院, 合肥 230009
收稿日期: 2015-10-19; 修订日期: 2016-01-22.
基金项目:国家自然科学基金项目(41402030,41372045) ;中国博士后科学基金项目(2014M551794) ;中央高校专项科研基金项目(2014HGCH0007)
摘要: 以天然褐铁矿为前驱体,通过热处理制备γ-Fe2O3作为NH3-SCR催化剂.借助XRD、XRF、XPS、NH3-TPD、FR-IR等表征方法,考察反应温度、褐铁矿中的锰氧化物以及H2O和SO2对催化剂选择催化还原NO活性的影响并与α-Fe2O3作对比.结果表明,由于γ-Fe2O3表面比α-Fe2O3具有更强的酸性,使得γ-Fe2O3的脱硝温度窗口(200~350℃)宽于α-Fe2O3(200~300℃),且在活性温度窗口下,催化剂脱硝效率达到99%以上; γ-Fe2O3催化剂中少量MnO2的存在,提高了催化剂低温段(100~200℃)脱硝活性,降低了高温段(400~450℃)脱硝活性; SO2的存在会使γ-Fe2O3的脱硝温度窗口向高温区偏移100℃、体积分数为5%的H2O对脱硝反应的抑制作用很小,但当SO2和5%H2O同时存在,尤其是SO2的体积分数达到0.12%时,硫酸铵盐类的迅速生成会大大降低γ-Fe2O3的脱硝活性;此外,γ-Fe2O3经过NH3-SCR反应后,其磁化率略有降低,催化剂仍然具有磁回收循环利用的潜力.
关键词:
褐铁矿
热处理
γ-Fe2O3
NH3-SCR
H2O
SO2
Preparation of γ-Fe2O3 Catalyst by Heat Treatment of Natural Limonite for Selective Catalytic Reduction of NO by NH3
XU Bin
1
, CHEN Tian-hu
1

, LIU Hai-bo
1 , ZHU Cheng-zhu
1 , CHEN Dong
1 , ZOU Xue-hua
1 , JIANG Yang
2
1.School of Natural Resources and Environment Engineering, Hefei University of Technology, Hefei 230009, China;
2.School of Materials Science and Engineering, Hefei University of Technology, Hefei 230009, China
Abstract: Natural limonite was used as a precursor to prepare γ-Fe2O3 via thermal treatment. The influences of reaction temperature, manganese oxides existing in limonite and coexisting SO2 and H2O on the catalytic reduction activity of the preparedγ-Fe2O3 were evaluated, and the activity of SCR was compared with that of α-Fe2O3, by means of XRD, XRF, XPS, NH3-TPD, FT-IR and so on. The results showed that because the surface acidity of γ-Fe2O3 is stronger, the SCR temperature window of γ-Fe2O3 was 200-350℃ being broader than that of α-Fe2O3 (200-300℃), and in the active temperature window, the NO removal reached over 99%. The existence of MnO2 in the newly formed γ-Fe2O3 slightly decreased the SCR reactivity at lower temperature (100-200℃), while it decreased the SCR reactivity at higher temperature (400-450℃). The existence of SO2 led to the shifting of temperature window by 100℃ from 200-350℃ to 300-450℃, and the volume fraction of 5%H2O only had a tiny negative effect on the SCR reactivity of γ-Fe2O3. However, the coexisting SO2 and H2O, especially when the volume fraction of SO2 reached 0.12%, significantly decreased the SCR reactivity due to the generation of ammonium sulfate. Besides, although the magnetic susceptibility of reacted γ-Fe2O3 experienced a slight decrease compared with the newly prepared γ-Fe2O3, the catalysts could still be used repeatedly by magnetic recycling.
Key words:
limonite
thermaltreatment
γ-Fe2O3
NH3-SCR
H2O
SO2
选择性催化还原脱硝技术发源于20世纪70年代,因其催化效率高、 稳定成为了脱硝技术的主流. 随着传统的V-W-Ti催化剂成本高、 操作温度高以及钒的本征毒性[1]等缺点日益凸显,新型稳定、 经济高效、 环境友好类催化剂的开发和应用研究引起广泛地兴趣.
目前,非钒基催化剂研究热点主要集中在沸石分子筛以及金属氧化物[2]. 分子筛催化剂主要有Cu、 Fe等替代的沸石分子筛[3~5]; 金属氧化物催化剂主要包括FeOx、 CuOx、 MnOx、 CeOx等[6~9]. 在众多非钒基催化剂中,铁系催化剂因其活性组分Fe2O3高效、 稳定、 抗水抗硫性强而被研究较多. 但是,大多的铁系催化剂都是通过商用铁粉或者化学试剂制备而成,其经济性还有待提高. 寻找一种经济、 有效的前躯体和简单易行的Fe2O3制备方法成了铁系催化剂工业化应用的关键. 另一方面,褐铁矿的主要矿物成分为针铁矿(主要成分为α-FeOOH),经过简单的加工就能转变为赤铁矿(α-Fe2O3)或者磁赤铁矿(γ-Fe2O3). 然而,很多褐铁矿资源因其品位较低而未得到充分有效的应用,在选择性催化还原脱硝方面的研究则也不多见. 本课题组前期进行的探索性研究[10]显示褐铁矿在NH3-SCR脱硝方面具有很大的潜力. 本文以天然褐铁矿为前驱体,制备了一系列的γ-Fe2O3,考察其NH3-SCR脱硝性能并与其热处理形成的α-Fe2O3进行对比,同时研究了共存组分 SO2和H2O对γ-Fe2O3催化脱硝的影响. 目的在于揭示以褐铁矿制备铁氧化物催化剂的脱硝性能及其影响因素,以期开发一种经济、 有效、 能可磁回收循环利用的脱硝催化剂,同时也为了推进褐铁矿矿产资源的综合利用提供理论支撑.
1 材料与方法
1.1 催化剂制备
从安徽省新桥硫铁矿采集褐铁矿石,破碎、 研磨、 筛分获得40~60目颗粒作为催化剂制备的前驱体,分别通过以下几个方法制备催化剂:

|
(1) |

|
(2) |

|
(3) |
路径(1) 的制备条件: 在空气气氛中300℃热处理1 h得到α-Fe2O3(样品编号1) ; 路径(2) 的制备条件: 在氢气气氛中450℃还原1 h,然后再置于空气中300℃氧化1 h得到γ-Fe2O3样品(样品编号2) ; 路径(3) 的制备条件: 在空气中300℃热处理脱水1 h后,置于氢气气氛中450℃还原1 h,然后分别在200、 250、 300℃空气中再氧化1 h得到γ-Fe2O3(样品编号3、 4、 5) .
以上所有热处理操作在管式炉内进行,所用的氢气通过氢气发生器提供,流量为100mL·min-1,矿物的用量为2 g.
1.2 催化剂表征
采用NOVA 3000e分析仪77K氮气吸附法表征催化剂的比表面积、 微孔体积和微孔尺寸; 采用英国Bartigton MSZ型双频磁化率仪测量磁化率; 采用丹东浩元DX-2700型X射线衍射仪分析样品的物相; 采用日本岛津XRF-1800对催化剂主要化学组成进行分析; 使用Hiden QIC-20型质谱仪检测催化剂程序升温NH3脱附(NH3-TPD),表征催化剂表面酸度,为了避免H2O的影响,以m/e=15作为NH3的信号; 采用美国Thermo ESCALAB250Xi型X射线光电子能谱仪分析催化剂表面铁锰价态; 采用德国BrukerVERTEX-70型傅立叶变换红外光谱仪进行样品红外光谱分析,分辨率为2 cm-1,扫描时扣除了H2O和CO2的干扰.
1.3 催化剂脱硝活性评价
催化剂NH3-SCR脱硝活性评价在常压连续流动固定床石英管式反应器中进行(图 1),实验装置由配气系统、 催化反应系统、 分析测试系统这3个部分组成. 反应器采用电加热,温度由插入催化剂床层的K型热电偶测量,并由可编程温度控制仪程序控制; 烟气中的水蒸气通过微量注射泵加入去离子水到加热管路中汽化来实现; 模拟烟气由: 0.1%NH3/Ar、 0.1%NO/Ar、 3%O2/Ar,Ar为平衡气体(以上百分数均为气体的体积分数),总流量为300mL·min-1,反应空速为18000 h-1,当考察SO2影响时,通过体积分数为0.5% SO2/Ar来配置,并通过改变平衡气Ar的流量来保持总流量不变.
2 结果与讨论
2.1 前驱体的表征
图 2是褐铁矿前驱体及5种催化剂的XRD图谱,对比标准卡片可以看出褐铁矿前驱体的主要物相为针铁矿(JCPDS81-464) 和石英(JCPDS52-1425) . 此外,XRF结果表明前驱体矿物中主要化学成分的质量分数为: Fe2O3(58.82%)、 SiO2(16.87%)、 Al2O3(4.85%)、 MnO(3.16%)、 烧失量(11.22%). 由此可知,褐铁矿前驱体主要由针铁矿组成,还含有石英等杂质矿物.
2.2 催化剂的表征
2.2.1 催化剂XRD分析
催化剂样品的XRD图谱见图 2,对照标准卡片JCPDS72-2234可知,1号催化剂的主要物相为α-Fe2O3; 对照标准卡片JCPDS25-1402可知,2~5号催化剂的主要物相为γ-Fe2O3.
2.2.2 催化剂比表面积及磁化率
表 1为5种催化剂的比表面积、 孔体积、 孔径以及磁化率数值. 从中可知: α-Fe2O3的比表面积比γ-Fe2O3大,无磁性. 对于γ-Fe2O3,经过预脱水过程制备的3、 4、 5号样品,其比表面积和磁化率都比未经预脱水过程制备的2号样品大. 再对比3、 4、 5号样品,可以看出,随着氧化温度的提高(200、 250、300℃),催化剂的比表面积和磁化率也会随之提高.
表 1
(Table 1)
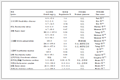
表 1 催化剂的比表面积、 孔体积、 孔尺寸和磁化率
Table 1 Specific surface area,pore volume,pore size and magnetic susceptibility of catalysts
|
编号 | 比表面积/m2·g-1 | 孔体积/cm3·g-1 | 孔径/nm | 质量磁化率×10-8/m3·kg-1 | NH3-SCR 反应后的质量磁化率×10-8/m3·kg-1
|
| 1 | 81.06 | 0.077 | 3.79 | 0 | 0
| | 2 | 23.43 | 0.063 | 10.73 | 29370.63 | 27605.29
| | 3 | 25.44 | 0.075 | 10.47 | 24661.99 | 21263.54
| | 4 | 26.29 | 0.08 | 9.87 | 28625 | 26422.16
| | 5 | 27.21 | 0.086 | 8.8 | 30157.8 | 28903.41 |
|
表 1 催化剂的比表面积、 孔体积、 孔尺寸和磁化率
Table 1 Specific surface area,pore volume,pore size and magnetic susceptibility of catalysts
|
2.2.3 催化剂XPS分析
催化剂表面Fe和Mn的XPS结果如图 3所示. 由于XRF结果表明,催化剂中掺杂量了少量的锰氧化物,而锰氧化物也是SCR的活性组分之一,所以,也有必要分析其价态情况. 在Fe2p曲线中,α-Fe2O3(1号)和γ-Fe2O3(2、 3、 4、 5号)都有两个峰,其中结合能在711 eV左右的峰是由2p3/2电子产生,结合能在725 eV左右的峰则为2p1/2电子,这说明表面的Fe均为+3价态[11]. 从图 3(b)来看,Mn2p曲线也都有两个明显的峰,其中结合能较低的对应着催化剂表面Mn2p3/2电子,较高的为2p1/2电子,这说明催化剂中掺杂的锰氧化物中的Mn均为+4价[12],这些锰氧化物很可能是以MnO2的形式存在.
2.2.4 催化剂NH3-TPD分析
催化剂的NH3-TPD曲线如图 4所示. 从中可知,1~5号催化剂在100℃下均没有NH3脱附峰,说明NH3在催化剂上并没有以物理吸附态的形式吸附[13],而100~400℃之间的脱附峰则来源于催化剂表面B酸和L酸位点对NH3的脱附. NH3在B酸位点上以NH4+形式吸附,而在L酸位上则以配位态的形式吸附[14]. 可以明显看出,γ-Fe2O3对NH3的吸附量要比α-Fe2O3大,即γ-Fe2O3表面酸性要明显强于α-Fe2O3.
2.3 催化剂活性评价
2.3.1 SCR活性
图 5(a)展示了5种催化剂的脱硝活性. 从中可以看出,两种铁氧化物的NO转化率随着温度的升高呈现先增大后减小的变化趋势. 对于α-Fe2O3(1号)催化剂,在200~300℃的温度窗口中,其NO转化率达到了100%,随着烟气温度超过300℃,相应的NO转化率迅速下降,直到450℃几乎降为0; 而γ-Fe2O3(2、 3、 4、 5号)催化剂的活性温度窗口为200~350℃,其NO转化率并没随烟气温度的升高发生骤降,在450℃的烟气温度下,仍然保持了50%以上的NO转化率. 从表 1中的数据可知,α-Fe2O3催化剂的比表面积为81.01 m2·g-1,远高于γ-Fe2O3催化剂(20~30 m2·g-1). 也就是说,α-Fe2O3具有更高的比表面积,但其活性温度窗口却比γ-Fe2O3窄. 这种现象主要和两种铁氧化物的结构密切相关. Cornell等[15]指出: γ-Fe2O3属于反尖晶石结构,所有的铁以三价形式存在,分别以四面体配位的Fe3+和以八面体的Fe3+的结构存在,并含有阳离子的空位,使之具有从外界接受电子和吸附物种并与之成键的能力,而NH3本身具有孤对电子,因而γ-Fe2O3有较强的SCR催化活性. 图 4中NH3-TPD结果也表明γ-Fe2O3的表面酸性比α-Fe2O3活泼,对NH3吸附能力更强,从而具有更高的脱硝效率.
再结合1.1和2.2.2节的内容可以看出,虽然随着氧化热处理温度(200、 250、 300℃)升高,γ-Fe2O3催化剂的比表面积和磁化率均升高,但在各温度段脱硝效率也只是略有升高; 而且通过方法(3) 制备的2号催化剂与方法(2) 制备的3、 4、 5号催化剂在各温度段的脱硝效率几乎没有差别,对比两种催化剂的比表面积和磁化率发现也没有太大差别,由此可见,在通过α-FeOOH制备γ-Fe2O3的过程中,预脱水热处理和氧化热处理温度对催化剂的NH3-SCR脱硝效率没有明显影响. 而从表 1和图 6可看出,5种催化剂的物相在反应前后均没有发生明显变化,反应后的主要物相都仍然是γ-Fe2O3其磁化率略微下降. 由此可知,经450℃氢气还原1 h,再200~300℃空气氧化1 h,可得到高活性、 稳定、 可磁回收的γ-Fe2O3脱硝催化剂.
2.3.2 Mn对催化剂活性的影响
为了探究催化剂中锰氧化物对催化活性的影响,对前驱体进行酸洗处理,具体处理过程为: 配制体积分数为5%的稀盐酸,在50℃下,以1∶100的固液比,浸泡褐铁矿12h,再用去离子水清洗,直至洗出液不使酸性铋酸钠溶液变色为止. 酸洗后的前驱体按照1.1节中描述的热处理方法分别制备α-Fe2O3(1号)和γ-Fe2O3(2、 3、 4、 5号)催化剂. 酸洗后制备的催化剂的脱硝效率如图 7(a)所示,图 7(b)~7(f)为1~5号催化剂酸洗前后脱硝效率对比图. 可以明显的看出,少量的锰氧化物对催化剂总体的脱硝效率的影响表现为: 提高了低温段的脱硝效率(100~200℃),降低了高温段的脱硝效率(400~450℃),这些锰氧化物的存在使催化剂的活性温度窗口向低温偏移了50℃左右.
2.3.3 SO2和H2O对催化脱硝的影响
上述研究结果表明,γ-Fe2O3比α-Fe2O3具有更宽的SCR脱硝温度窗口,且反应后仍有磁性,具有磁分离和循环利用的潜力. 为了探究实际工况中的脱硝活性,以制备过程上比较简单的2号样品为例,探究了SO2和H2O对γ-Fe2O3脱硝反应的影响,其结果如图 5(b)~5(d)所示.
图 5(b)反映了体积分数为0.04%、 0.08%和0.12%的SO2对脱硝效率的影响. 可以看出,随着SO2引入,γ-Fe2O3催化剂的脱硝温度窗口从200~350℃提高至300~450℃. 当烟气温度在300℃以下时,SO2引入对脱硝过程起到抑制作用,且SO2体积分数越高抑制作用越明显; 当烟气温度在300℃以上时,SO2引入反而促进了NO转化. 大量研究表明,SO2对SCR的抑制作用主要原因是: 在低温段,反应过程中生成的硫酸铵(ABS)和硫酸氢铵(AS)沉积在催化剂表面进而导致活性位点被覆盖而失活[16~18]. 但是,当烟气温度高于300℃,ABS和AS会转变为气相,其钝化作用消失,取而代之的是SO42-对催化剂表面的修饰作用. 金属氧化物(如TiO2、 Fe2O3)表面经过SO42-修饰后,其固体酸性质会大大增强,进而提高对NH3的吸附能力,并降低在高温段对NH3的氧化能力,从而提高了反应速率[19~22].
图 5(c)为催化剂在体积分数为5%H2O和不同体积分数SO2体系下NH3-SCR脱硝结果. 从“5%H2O”曲线可以看出,当烟气温度低于300℃时,模拟烟气中引入体积分数为5%的H2O对催化剂有微弱的抑制作用: 200℃、 250℃处的脱硝效率从100%分别降至95.22%、 97.12%,而当烟气温度达到300℃后,H2O对催化剂的活性反应几乎没有影响. 这种微弱的抑制作用很可能是由于H2O与NH3在L酸位上微弱的竞争吸附造成的[23, 24]. 此外,从脱硝数据可以看出,随着SO2体积分数的提高,脱硝活性被抑制得越明显. 进一步对比“0.04%SO2+5%H2O、 0.08%SO2+5%H2O和0.12%SO2+5%H2O”曲线和图 5(b)中“0.04%SO2、 0.08%SO2和0.12%SO2”的曲线可看出: 在200~300℃的烟气温度范围内,H2O会大大促进SO2体系中硫酸铵盐的生成,进而加速了催化活性的降低.
为了进一步证明SO2和H2O对催化效率的影响. 对300℃下,抗水抗硫反应后的样品进行压片红外分析,结果如图 8所示. 其中1635 cm-1和1167 cm-1吸收峰对应着配位在L酸位上的NH3[25, 26]; 1445 cm-1、 1383 cm-1吸收峰分别对应着B酸位上NH4+的非对称振动[27]和SO的拉伸频率[27]; 而1082、 1039 cm-1则是Si—O—Si的吸收峰. 显然,随着反应SO2和H2O的引入,SO2浓度的增加,1445 cm-1和1383 cm-1处的吸收峰明显增加,说明硫酸铵盐在催化剂表面的覆盖量在不断地增加. 此外,硫化金属氧化物的红外光谱一般会在1390~1375 cm-1和1250~900 cm-1,所以,图 8中1039 cm-1和1082 cm-1的吸收峰随着SO2浓度增加而提高,也和反应过程中SO42-的形成有关[27, 28].
图 5(d)为催化剂在体积分数为5%H2O和0.12%SO2的共存于体系下NH3-SCR脱硝结果,反应温度为300℃. 可以看出,当反应时间持续到1400 min,催化剂的脱硝效率还能保持80%左右,可见其抗H2O抗SO2性能比较强.
3 结论
(1) 以取自安徽省新桥的天然褐铁矿为前驱体,经氢气还原空气氧化,可得到高活性、 可磁回收的γ-Fe2O3脱硝催化剂,其活性温度窗口为200~350℃. γ-Fe2O3脱硝活性高于α-Fe2O3,其原因是前者的表面酸度高于后者.
(2) 天然褐铁矿中少量锰氧化物使得催化剂的活性温度窗口整体下降50℃.
(3) 体积分数在0.04%~0.12%范围内的SO2会使得γ-Fe2O3的脱硝活性温度窗口从200~350℃提高至300~450℃; 而体积分数为5%的H2O对γ-Fe2O3的脱硝活性影响非常小: 烟气温度在300℃以下时,有轻微的抑制作用,当烟气温度高于300℃后没有影响; 但当体系中同时存在SO2和H2O时,催化剂脱硝活性被抑制得比较明显,尤其是体积分数为0.12%SO2和5%H2O的共存时,γ-Fe2O3脱硝活性会明显降低.
参考文献
| [1] |
Yang S J, Wang C Z, Chen J H, et al. A novel magnetic Fe-Ti-V spinel catalyst for the selective catalytic reduction of NO with NH3 in a broad temperature range[J].
Catalysis Science & Technology,2012,2
(5)
: 915–917
.
|
|
| [2] |
刘福东, 单文坡, 石晓燕, 等. 用于NH3选择性催化还原NO的非钒基催化剂研究进展[J].
催化学报,2011,32 (7) : 1113–1128.
|
|
| [3] |
Andonova S, Vovk E, Sj blom J, et al. Chemical deactivation by phosphorous under lean hydrothermal conditions over Cu/BEA NH3-SCR catalysts[J].
Applied Catalysis B:Environmental,2014,147
: 251–263
.
|
|
| [4] |
Shi X Y, Liu F D, Xie L J, et al. NH3-SCR performance of fresh and hydrothermally aged Fe-ZSM-5 in standard and fast selective catalytic reduction reactions[J].
Environmental Science & Technology,2013,47
(7)
: 3293–3298
.
|
|
| [5] |
Góra-Marek K, Brylewska K, Tarach K A, et al. IR studies of Fe modified ZSM-5 zeolites of diverse mesopore topologies in the terms of their catalytic performance in NH3-SCR and NH3-SCO processes[J].
Applied Catalysis B:Environmental,2015,179
: 589–598
.
|
|
| [6] |
姚桂焕, 张琦, 秦烨, 等. 低温磁性铁基SCR烟气脱硝的实验研究[J].
环境科学,2009,30 (10) : 2852–2857.
|
|
| [7] |
Yao X J, Zhang L, Li L L, et al. Investigation of the structure, acidity, and catalytic performance of CuO/Ti0.95Ce0.05O2 catalyst for the selective catalytic reduction of NO by NH3 at low temperature[J].
Applied Catalysis B:Environmental,2014,150-151
: 315–329
.
|
|
| [8] |
周爱奕, 毛华峰, 盛重义, 等. 碱土金属钙沉积对Mn-Ce/TiO2低温SCR催化剂脱硝性能的影响[J].
环境科学,2014,35 (12) : 4745–4751.
|
|
| [9] |
Ma Z R, Wu X D, Si Z C, et al. Impacts of niobia loading on active sites and surface acidity in NbOx/CeO2-ZrO2 NH3-SCR catalysts[J].
Applied Catalysis B:Environmental,2015,179
: 380–394
.
|
|
| [10] |
邹雪华, 陈天虎, 张萍, 等. 天然针铁矿热处理产物的结构特征[J].
硅酸盐学报,2013,41 (10) : 1442–1446.
|
|
| [11] |
Liu C X, Yang S J, Ma L, et al. Comparison on the performance of α-Fe2O3 and γ-Fe2O3 for selective catalytic reduction of Nitrogen Oxides with ammonia[J].
Catalysis Letters,2013,143
(7)
: 697–704
.
|
|
| [12] |
Li J H, Chen J J, Ke R, et al. Effects of precursors on the surface Mn species and the activities for NO reduction over MnOx/TiO2 catalysts[J].
Catalysis Communications,2007,8
(12)
: 1896–1900
.
|
|
| [13] |
Long R Q, Yang R T. Selective catalytic reduction of NO with ammonia over Fe3+-exchanged mordenite (Fe-MOR):catalytic performance, characterization, and mechanistic study[J].
Journal of Catalysis,2002,207
(2)
: 274–285
.
|
|
| [14] |
Chmielarz L, Dziembaj R, Grzybek T, et al. Pillared smectite modified with carbon and manganese as catalyst for SCR of NOx with NH3. Part Ⅱ. Temperature-programmed studies[J].
Catalysis Letters,2000,70
(1-2)
: 51–56
.
|
|
| [15] |
Cornell R M, Schwertmann U.
The Iron Oxides:structure, properties, reactions, occurences and uses[M].(2nd ed.). Weinheim: Wiley-VCH, 2003 : 740 -741.
|
|
| [16] |
Li P, Liu Z Y, Li Q C, et al. Multiple roles of SO2 in selective catalytic reduction of NO by NH3 over V2O5/AC catalyst[J].
Industrial & Engineering Chemistry Research,2014,53
(19)
: 7910–7916
.
|
|
| [17] |
Qi G, Yang R T, Chang R. MnOx-CeO2 mixed oxides prepared by co-precipitation for selective catalytic reduction of NO with NH3 at low temperatures[J].
Applied Catalysis B:Environmental,2004,51
(2)
: 93–106
.
|
|
| [18] |
Xie G Y, Liu Z Y, Zhu Z P, et al. Simultaneous removal of SO2 and NOx from flue gas using a CuO/Al2O3 catalyst sorbent:Ⅱ. Promotion of SCR activity by SO2 at high temperatures[J].
Journal of Catalysis,2004,224
(1)
: 42–49
.
|
|
| [19] |
Si Z C, Weng D, Wu X D, et al. Modifications of CeO2-ZrO2 solid solutions by nickel and sulfate as catalysts for NO reduction with ammonia in excess O2[J].
Catalysis Communications,2010,11
(13)
: 1045–1048
.
|
|
| [20] |
赵宇峰, 赵博, 禚玉群, 等. SO2对于铁基硫酸盐的NH3选择性还原NO催化活性的影响[J].
中国电机工程学报,2011,31 (23) : 27–33.
|
|
| [21] |
Ma L, Li J H, Rui K, et al. Catalytic performance, characterization, and mechanism study of Fe2(SO4)3/TiO2 catalyst for selective catalytic reduction of NOx by ammonia[J].
The Journal of Physical Chemistry C,2011,115
(15)
: 7603–7612
.
|
|
| [22] |
Huang H L, Lan Y, Shan W P, et al. Effect of sulfation on the selective catalytic reduction of NO with NH3 Over γ-Fe2O3[J].
Catalysis Letters,2014,144
(4)
: 578–584
.
|
|
| [23] |
Liu F D, He H. Selective catalytic reduction of NO with NH3 over manganese substituted iron titanate catalyst:reaction mechanism and H2O/SO2 inhibition mechanism study[J].
Catalysis Today,2010,153
(3-4)
: 70–76
.
|
|
| [24] |
Pan S W, Luo H C, Li L, et al. H2O and SO2 deactivation mechanism of MnOx/MWCNTs for low-temperature SCR of NOx with NH3[J].
Journal of Molecular Catalysis A:Chemical,2013,377
: 154–161
.
|
|
| [25] |
Lietti L, Forzatti P, Ramis G, et al. Potassium doping of vanadia/titania de-NOxing catalysts:surface characterisation and reactivity study[J].
Applied Catalysis B:Environmental,1993,3
(1)
: 13–35
.
|
|
| [26] |
Jin R B, Liu Y, Wu Z B, et al. Relationship between SO2 poisoning effects and reaction temperature for selective catalytic reduction of NO over Mn-Ce/TiO2 catalyst[J].
Catalysis Today,2010,153
(3-4)
: 84–89
.
|
|
| [27] |
Chen J P, Yang R T. Selective catalytic reduction of NO with NH3 on SO42-/TiO2 superacid catalyst[J].
Journal of Catalysis,1993,139
(1)
: 277–288
.
|
|
| [28] |
Shen B X, Liu T. Deactivation of MnOx-CeOx/ACF catalysts for low-temperature NH3-SCR in the presence of SO2[J].
Acta Physico-Chimica Sinica,2010,26
(11)
: 3009–3016
.
|
|











 2016, Vol. 37
2016, Vol. 37


