2. 西南大学资源环境学院, 重庆 400715;
3. 重庆市农业资源与环境研究重点实验室, 重庆 400715
2. College of Resources and Environment, Southwest University, Chongqing 400715, China;
3. Chongqing Key Laboratory of Agricultural Resources and Environment, Chongqing 400715, China
纳米TiO2是应用最早的纳米材料之一,已经被广泛应用于各领域数十年[1, 2, 3, 4, 5],其在生产、 使用和废物处理过程中必将进入环境[6]. 土壤和沉积物是环境污染物的汇聚场所,进入环境的纳米TiO2最终也汇入土壤或沉积物中[7, 8]. 有研究预测纳米TiO2在污泥处理的土壤中的含量以42-89 μg ·(kg ·a)-1的速度增加[9],全球范围内预计到2025年高风险区域土壤中纳米TiO2的含量可达到20 g ·kg-1[9, 10]. 并且,利用纳米TiO2的光催化作用降解土壤中有机农药和处理重金属污染也是目前正在探索的土壤修复新方法之一. 由于具有催化活性,理论上可能改变重金属的价态和存在状态,一些研究显示,纳米TiO2对土壤中Zn、 Pb、 Cu、 Cd等有一定固定作用[11, 12]. 因此关于纳米TiO2的安全应用及对土壤环境的生态风险问题已成为关注的焦点. 有研究显示纳米TiO2颗粒影响Cu2+在不同类型土壤中的迁移[13]. 但目前关于纳米TiO2对其他重金属的迁移转化的影响还知之甚少. 重金属的形态变化是反映其迁移转化的重要指标,因此,本研究以三峡水库典型消落区土壤为对象,通过室外的模拟淹水实验,分析两种晶型的纳米TiO2颗粒对土壤中重金属形态变化的影响,以期为纳米TiO2的安全应用及其环境风险预测提供科学依据.
1 材料与方法 1.1 纳米TiO2颗粒与供试土壤锐钛矿颗粒(-100 nm)和金红石颗粒(<25 nm)颗粒均购自阿拉丁试剂公司(Aladdin),纯度均为99.8%.
供试土壤采自三峡水库干流重庆市忠县石宝寨(N30°25′5.5″,E108°10′5.5″)消落区,海拔153 m处,该消落区淹没面积较大,且随水库水位而变化,占重庆市消落区总面积的1/10,土壤类型是西南地区典型的紫色土,每年4-9月为落干期,其余时间为淹水期. 样品风干后粉碎,过2 mm和0.149 mm筛,混合均匀备用. 土壤基本的理化性质和Cr、 Zn、 Pb、 Cu、 Cd含量如表 1.
| 表 1 供试土样的基本特性 Table 1 Physicochemical properties of soil for test |
用超纯水配制300 mL 0.2 g ·L-1和0.4 g ·L-1的纳米TiO2颗粒悬液,超声30 min. 称30 g 土样(0.149 mm),加到纳米TiO2颗粒悬液中,摇匀,土样中纳米TiO2颗粒的添加量分别为2 g ·kg-1和4 g ·kg-1,金红石处理组编号为R2(2 g ·kg-1)和R4(4 g ·kg-1),锐钛矿处理组编号为T2(2 g ·kg-1)和T4(4 g ·kg-1),以不加纳米TiO2处理为对照,每个处理重复3次. 实验采用磨口硼硅玻璃瓶,加盖,置于室外环境中,60 d后,分离上覆水,测定水样中Cr、 Pb、 Zn、 Cd和Cu的浓度,土样冻干后粉碎,过筛(0.149 mm),混合均匀. 采用改进的BCR连续提取法[14]分析样品中各形态Cr、 Pb、 Zn、 Cd和Cu的含量,具体步骤见表 2.
| 表 2 各形态重金属的提取方法 Table 2 Extraction method of various forms of heavy metals in soil |
实验采用超纯水(Minipore 18.2 MΩ ·cm),所用试剂均为优级纯,样品采用电感耦合等离子体质谱ICP-MS(Thermo,iCAP-Q)测定. 实验过程采用空白实验、 标准工作曲线、 加标回收、 标准物质(GBW 07406)进行质量控制,回收率在90.6%-106.8%之间.
2 结果与分析 2.1 上覆水中各重金属元素的浓度淹水60 d后,上覆水中各重金属元素的浓度如表 3. 与对照相比,添加纳米TiO2颗粒处理后,上覆水中Cr浓度均明显升高(P<0.05),且均随纳米TiO2颗粒浓度的增加而升高,4 g ·kg-1处理组Cr浓度均大幅升高,说明两种纳米TiO2颗粒均促进土壤中Cr的释放,提高水体污染风险,且浓度越高风险越大. 上覆水中Pb浓度仅R4处理组明显升高,表明4 g ·kg-1金红石促进土壤中Pb的释放. 与Cr和Pb不同的是,T2和T4处理组上覆水中Zn浓度明显低于对照组,说明锐钛矿纳米TiO2抑制土壤Zn的溶出,具有一定的固定作用. 此外,上覆水中Cd浓度均非常低,差异也较小,可能是由于土壤中Cd含量很低或纳米TiO2对土壤Cd影响很小;各处理 组Cu含量与对照相比也没有明显的变化,显示纳米TiO2对土壤Cu释放的影响很小.
| 表 3 上覆水中各重金属元素的浓度 1)/μg ·mL-1Table 3 Concentrations of heavy metal elements in overlying water/μg ·mL-1 |
经过反复淹水和落干过程,三峡水库消落带土壤重金属含量相对较稳定. 淹水60 d后,与原样相比,对照组各重金属元素的总量均略有降低,但没有明显的差异(表 4). 与对照相比,4g ·kg-1纳米TiO2颗粒处理组Cr含量均明显下降,分别降低30.20%和30.85%,这与上覆水中该处理组Cr浓度急剧升高是一致,R4和T4处理组上覆水中Cr浓度显著升高,进一步证明土壤中Cr释放到水中. 金红石颗粒组土壤Pb含量呈下降趋势,但没有达到显著水平. 锐钛矿颗粒处理组土壤Zn呈升高趋势,且T4处理组明显高于对照组. 此外,土壤中Cd和Cu均没有明显变化.
 | *表示P<0.05(与对照相比),下同 图 1 土壤中各形态铬的含量 Fig. 1 Contents of different speciation of chromium in soil |
| 表 4 土壤中各重金属元素的总量变化 /mg ·kg-1Table 4 Changeof the total amounts of heavy metals in soils/mg ·kg-1 |
从形态分布来看,供试土壤Cr主要以残渣态和可氧化态形式存在(图 1),两种形态占总量的95%以上. 值得注意的是,两种纳米TiO2颗粒均促进土壤中这两种形态Cr的释放,R4和T4处理组可氧化态Cr含量分别下降58.79%和67.40%,残渣态含量分别下降20.08%和18.11%,土壤Cr的活性增强,环境风险增大. 纳米TiO2处理组酸可交换态和可还原态Cr与对照相比没有明显变化,说明释放出来的可氧化态和残渣态Cr没有转化成其他形态,全部进入水中.
土壤中Pb主要以残渣态存在(图 2),所占比例为51.77%-61.87%,且淹水后略有升高,其次是可还原态,淹水后,可还原态Pb含量均明显低于原样,但纳米TiO2对这两种形态Pb均没有明显的影响. 土壤中酸可交换态和可氧化态Pb含量的变化规律类似,仅R4处理组明显低于对照组,其他处理组都没有明显的变化,值得注意的是,虽然R4处理组土壤中总Pb含量下降没有达到显著水平,但实际上仍有少量Pb释放到水中,只是本研究采用的土壤中酸可交换态和可氧化态Pb含量相对较低,所以对总量变化影响较小.
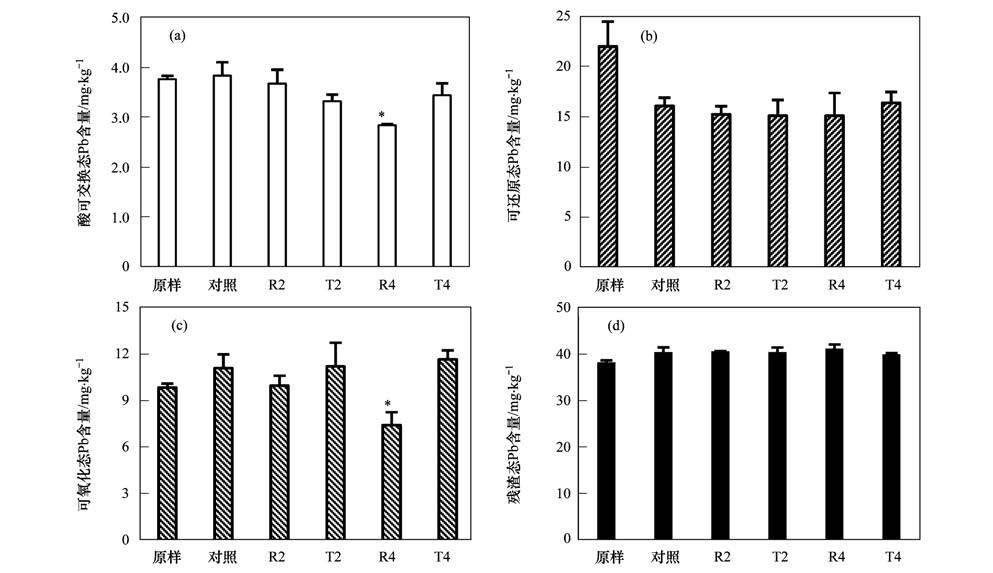 | 图 2 土壤中各形态铅的含量 Fig. 2 Contents of different speciation of lead in soil |
土壤中4种形态Zn的含量分布相对比较均匀(图 3),淹水后呈现酸可交换态和可还原态向可氧化态和残渣态转化的趋势,纳米TiO2颗粒对酸可交换态、 可还原态和残渣态Zn含量的影响不明显;可氧化态Zn淹水后也呈升高趋势,其中锐钛矿颗粒处理组(T2和T4)达到显著水平(P<0.05),分别比对照高42.65%(T2)和44.25%(T4),说明锐钛矿颗粒促进了可氧化态Zn的形成,使部分溶解的Zn转化成可氧化态滞留在土壤中,这也是T2和T4处理组上覆水Zn含量明显低于对照组,且土壤中Zn总量高于对照组的主要原因.
 | 图 3 土壤中各形态锌的含量 Fig. 3 Contents of different speciation of zinc in soil |
此外,供试土壤Cd含量较低,各形态的含量变化不明显,纳米TiO2对Cu的形态和总量也没有明显的影响(图 4).
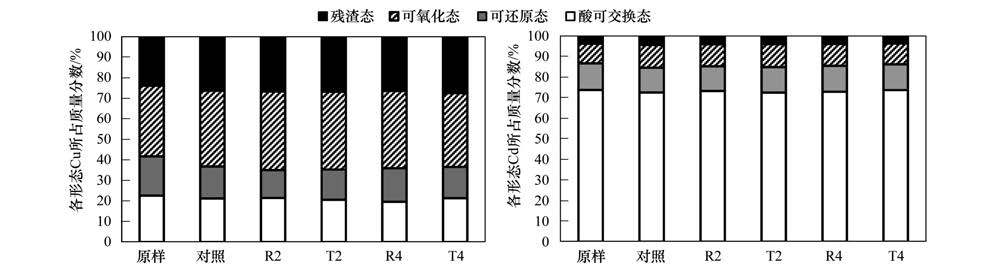 | 图 4 土壤中各形态铜和镉的比例 Fig. 4 Proportions of different speciation of copper and cadmium in soil |
综合上覆水、 土壤重金属总量和各形态的含量变化可以看出,土壤重金属总量的变化能反映出不同处理之间的变化趋势,上覆水的变化能够较准确地反映出不同处理之间的差异,各形态含量的变化才能判断纳米TiO2对土壤重金属的影响过程.
土壤中重金属的存在形态与pH、 氧化还原电位、 铁锰氧化物、 有机质、 微生物等因素有关. 本研究土壤淹水后处于还原条件,通常在还原条件下,重金属和土壤中的硫容易形成硫化物沉淀,因此一般残渣态含量会升高. 本研究中Pb、 Zn和Cu也有类似的规律,各处理组残渣态含量均略有升高. 但Cr的变化差异较大,各处理组残渣态含量均降低,其中对照组和2g ·kg-1纳米TiO2处理组(R2和T2)的变化与陈英旭等[15]的研究结果相似,还原条件下土壤中铬有从残渣态逐渐向有机结合态(可氧化态)转化的趋势. 但4g ·kg-1纳米TiO2处理组(R4和T4)残渣态和可氧化态都大幅降低,并且对应的上覆水中Cr浓度大幅升高,说明4g ·kg-1纳米TiO2处理促进残渣态和可氧化态Cr的溶出,这可能与Cr的价态变化有关. 纳米TiO2与铬可以发生复杂化学反应,Cr(Ⅵ)可被纳米TiO2光催化还原成Cr(Ⅲ)[16, 17, 18, 19, 20, 21, 22],但在Mn2+存在时,不仅能使催化剂中毒[23],还能氧化Cr(Ⅳ)[Cr(Ⅵ)光催化还原的中间产物]而阻碍Cr(Ⅵ)的还原[24]. Mn2+是土壤中普遍存在的元素,阻碍Cr(Ⅵ)的光催化还原过程是可能的. 此外,Cr(Ⅵ)的光催化反应还受pH、 有机物等多种因素的影响[25, 26]. 土壤是一个复杂的体系,纳米TiO2与土壤中铬是直接发生反应,还是通过改变土壤环境条件间接导致其溶出,还需进一步研究确定.
可氧化态重金属一般氧化环境下易分解释放,还原条件下有利于其积累,因而一般在还原条件下,可氧化态重金属含量会升高. 本研究中除了R4和T4处理组可氧化态Cr含量明显降低外,金红石颗粒处理组可氧化态Pb含量也随颗粒浓度升高而降低,其中R4处理明显降低,表明金红石颗粒抑制了可氧化态Pb的形成,其他各处理组可氧化态含量均呈上升趋势. 与Cr类似,金红石颗粒对可氧化态Pb的抑制可能与其价态变化有关,Pb的价态有+4和+2,结合土壤可氧化态Cr和Pb的结果,推测在本实验条件下,纳米TiO2可能促进土壤中低价的Cr和Pb向高价转化,起了光催化氧化的作用,高价态Cr和Pb的活性和溶解性均高于低价态,毒性也高于低价态,因此纳米TiO2颗粒在提高土壤Cr和Pb的迁移性的同时可能也提高了生态毒性,特别是Cr. 此外,与之相反的是,锐钛矿颗粒处理显著提高了可氧化态Zn的含量,将淹水过程释放出来的可还原态和酸可交换态Zn部分转化成可氧化态而截留在土壤中,相应的上覆水中Zn浓度显著低于对照组也证明了锐钛矿颗粒抑制土壤Zn的溶出,降低水体污染风险. 其原因可能是由于纳米TiO2颗粒易与土壤中有机胶体类物质(如腐殖质)结合,因其具有较强的吸附作用,从而提高土壤中有机物对溶出Zn2+的捕获能力,由此可以推测锐钛矿颗粒比金红石颗粒的吸附作用更强,本研究中纳米TiO2对Hg2+的吸附作用的结果证明了这一推测,锐钛矿颗粒对Hg2+的吸附作用远高于金红石颗粒[27].
土壤中可还原态重金属的含量均没有明显的变化,虽然纳米TiO2对土壤Fe和Mn形态影响的研究结果显示,2 g ·kg-1金红石颗粒和4 g ·kg-1锐钛矿颗粒促进了少量可还原态Fe和Mn的转化[28],但并没有影响到本研究中5种重金属铁锰氧化物结合态的释放,对氧化态Hg的影响更大[29],这可能与本研究中几种重金属可还原态含量相对较低有关,而该土壤中氧化态汞的含量较高. 酸可交换态重金属的含量变化,除了R4处理组酸可交换Pb含量有明显降低以外,其他处理组与对照相比均没有明显变化.
4 结论本实验条件下,纳米TiO2对土壤Cr、 Zn、 Pb、 Cu和Cd的形态转化存在较大的差异. 对Cr的影响最大,锐钛矿和金红石两种晶型均可促进土壤中残渣态和可氧化态Cr的释放,提高其生态风险;金红石型纳米TiO2促进土壤中可氧化态和酸可交换态Pb的释放;在采用纳米TiO2材料对Cr和Pb污染土壤进行修复时需要特别注意. 而锐钛矿颗粒对土壤中Zn具有一定的固定作用;两种纳米TiO2颗粒对土壤中Cu和Cd则几乎没有影响.
| [1] | Lomer M C E, Thompson R P H, Commisso J, et al. Determination of titanium dioxide in foods using inductively coupled plasma optical emission spectrometry[J]. The Analyst, 2000, 125(12): 2339-2343. |
| [2] | Contado C, Pagnoni A. TiO2 in commercial sunscreen lotion: flow field-flow fractionation and ICP-AES together for size analysis[J]. Analytical Chemistry, 2008, 80(19): 7594-7608. |
| [3] | Reijnders L. Cleaner nanotechnology and hazard reduction of manufactured nanoparticles[J]. Journal of Cleaner Production, 2006, 14(2): 124-133. |
| [4] | He X J, Hwang H M. Engineered TiO2 nanoparticles: their fate and effects in natural aquatic environments[M]. Titanium Dioxide: Chemical Properties, Applications and Environmental Effects. New York: Nova Science Publishers, 2014. 1-20. |
| [5] | Nur Y, Lead J R, Baalousha M. Evaluation of charge and agglomeration behavior of TiO2 nanoparticles in ecotoxicological media[J]. Science of the Total Environment, 2015, 535: 45-53. |
| [6] | Gottschalk F, Sun T Y, Nowack B. Environmental concentrations of engineered nanomaterials: review of modeling and analytical studies[J]. Environmental Pollution, 2013, 181: 287-300. |
| [7] | Sun P D, Zhang K K, Fang J, et al. Transport of TiO2 nanoparticles in soil in the presence of surfactants[J]. Science of the Total Environment, 2015, 527-528: 420-428. |
| [8] | Chekli L, Roy M, Tijing L D, et al. Agglomeration behaviour of titanium dioxide nanoparticles in river waters: a multi-method approach combining light scattering and field-flow fractionation techniques[J]. Journal of Environmental Management, 2015, 159: 135-142. |
| [9] | Gottschalk F, Sonderer T, Scholz R W, et al. Modeled environmental concentrations of engineered nanomaterials (TiO2, ZnO, Ag, CNT, fullerenes) for different regions[J]. Environmental Science & Technology, 2009, 43(24): 9216-9222. |
| [10] | Ge Y, Priester J H, Van De Werfhorst L C, et al. Potential mechanisms and environmental controls of TiO2 nanoparticle effects on soil bacterial communities[J]. Environmental Science & Technology, 2013, 47(24): 14411-14417. |
| [11] | 丁园, 刘燕红, 郝双龙, 等. 化学改良剂对红壤中铜、镉吸附行为的影响[J]. 江西农业大学学报, 2010, 32(4): 824-828. |
| [12] | 孟丽华. 胶体二氧化钛对水土环境重金属污染控制研究[D]. 合肥: 中国科学技术大学, 2009. 1-44. |
| [13] | 方婧, 周艳萍, 温蓓. 二氧化钛纳米颗粒对铜在土壤中运移的影响[J]. 土壤学报, 2011, 48(3): 549-556. |
| [14] | 张朝阳, 彭平安, 宋建中, 等. 改进BCR法分析国家土壤标准物质中重金属化学形态[J]. 生态环境学报, 2012, 21(11): 1881-1884. |
| [15] | 陈英旭, 何增耀, 吴建平. 土壤中铬的形态及其转化[J]. 环境科学, 1994, 15(3): 53-56. |
| [16] | Wang L M, Wang N, Zhu L H, et al. Photocatalytic reduction of Cr (VI) over different TiO2 photocatalysts and the effects of dissolved organic species[J]. Journal of Hazardous Materials, 2008, 152(1): 93-99. |
| [17] | 陈心满, 徐明芳. UV/TiO2光催化还原Cr(Ⅵ)过程中吸附作用的影响及其消除[J]. 环境科学, 2006, 27(5): 913-917. |
| [18] | 付宏祥, 吕功煊, 李树本. Cr(Ⅵ)离子在TiO2表面的光催化还原机理研究[J]. 化学物理学报, 1999, 12(1): 112-116. |
| [19] | Akkan Ş, Altın I, Koç M, et al. TiO2 immobilized PCL for photocatalytic removal of hexavalent chromium from water[J]. Desalination and Water Treatment, 2015, 56(9): 2522-2531. |
| [20] | Paul M L, Samuel J, Roy R, et al. Studies on Cr (Ⅳ) removal from aqueous solutions by nanotitania under visible light and dark conditions[J]. Bulletin of Materials Science, 2015, 38(2): 393-400. |
| [21] | Ravishankar T N, Muralikrishna S, Kumar K S, et al. Electrochemical detection and photochemical detoxification of hexavalent chromium (Cr(Ⅵ)) by Ag doped TiO2 nanoparticles[J]. Analytical Methods, 2015, 7(8): 3493-3499. |
| [22] | Song R, Bai B, Jing D W. Hydrothermal synthesis of TiO2-yeast hybrid microspheres with controllable structures and their application for the photocatalytic reduction of Cr (Ⅵ)[J]. Journal of Chemical Technology and Biotechnology, 2015, 90(5): 930-938. |
| [23] | Burns R A, Crittenden J C, Hand D W, et al. Effect of inorganic ions in heterogeneous photocatalysis of TCE[J]. Journal of Environmental Engineering, 1999, 125(1): 77-85. |
| [24] | Elovitz M S, Fish W. Redox interactions of Cr (Ⅵ) and substituted phenols: products and mechanism[J]. Environmental Science & Technology, 1995, 29(8): 1933-1943. |
| [25] | 傅宏祥, 吕功煊, 李树本. 有机物存在下Cr6+离子的光催化还原[J]. 物理化学学报, 1997, 13(2): 106-112. |
| [26] | 杨永凡, 费学宁. TiO2光催化去除废水中重金属离子的研究进展[J]. 工业水处理, 2012, 32(7): 9-14. |
| [27] | 周雄, 张金洋, 王定勇, 等. 纳米TiO2吸附HgCl2水溶液中Hg (Ⅱ)[J]. 环境科学, 2016, 37(1): 220-227. |
| [28] | 张金洋, 王定勇, 李楚娴, 等. 纳米TiO2对土壤中Al、Fe和Mn释放及形态的影响[J]. 水土保持学报, 2015, 29(2): 238-241. |
| [29] | 张金洋, 李楚娴, 王定勇, 等. 纳米TiO2对底泥中汞释放及活化的影响[J]. 环境科学, 2014, 35(12): 4567-4572. |
 2016, Vol. 37
2016, Vol. 37


