矿化垃圾具有比表面积大,水力渗透性能好的特性,其上附着经高浓度渗滤液长期驯化得到的优势微生物[1, 2]. 矿化垃圾构建的准好氧生物反应床,能大大提高氨氮和总氮的去除效果,具有较好的脱氮效果[3, 4, 5, 6]. 而脱氮过程会有伴随强温室气体N2 O的产生[7],与CO2相比N2 O虽然属于痕量气体,但其百年增温潜势约是CO2的300倍,同时,N2 O还能消耗平流层臭氧,对人体及其他生物产生毒性,被认为21世纪最主要的臭氧层破坏物质[8, 9]. 影响准好氧矿化垃圾反应器(SAARB)处理效率的因素有很多,比如水力负荷、 温度、 回灌频率、 渗滤液COD等[10, 11, 12]. 盐度也是影响其处理效率的一个重要因素. 盐度过高会导致微生物细胞渗透压的改变,对微生物的生长起抑制作用,从而影响微生物的新陈代谢和生物处理效率[13]. 特别是沿海地区和含盐工业废水排放的地区,高盐度的影响更为严重[14]. 盐度对于N2 O的产生也有影响,目前的研究主要集中于污水处理过程. 刘甜甜等[15]对具有短程生物脱氮污泥实验得出,盐度的突变会导致亚硝酸型反硝化过程N2 O峰值出现时间延后并且浓度增加. 王珊珊等[16]对好氧颗粒污泥全程硝化过程中通过控制进水盐度得出,随着进水盐度的增加溶解态N2 O和释放态N2 O产生量在硝化过程中均呈现先上升后下降的趋势. 此外,尚会来等[17]通过实验得出盐度7.5 g ·L-1的生活污水硝化过程中N2 O产量是未调节盐度的2.85倍,且盐度过高波动会导致污水硝化过程中N2 O产量和转化率的大幅升高. 然而盐度对矿化垃圾处理渗滤液过程中N2 O产生的影响研究并不多,特别是SAARB处理渗滤液过程中更为少见.
基于以上研究背景,本研究在实验室内构建SAARB,通过调节回灌渗滤液盐度(7、 10、 15、 20、 30 g ·L-1,以NaCl计),分析不同盐度条件下SAARB对回灌渗滤液的处理效果以及N2 O产生规律的影响,以期为SAARB处理高盐度废水提供一定的理论依据,为填埋场N2 O减排提供一定的理论及工程指导.
1 材料与方法 1.1 实验材料 1.1.1 渗滤液渗滤液取自某生活垃圾填埋场渗滤液调节池. 具体理化性质见表 1. 根据不同阶段要求,渗滤液进行配比.
| 表 1 渗滤液理化性质 Table 1 Physical and chemical characteristics of leachate |
矿化垃圾取自某生活垃圾填埋场,填埋龄为8 a. 样品在经过48 h风干后,人工分拣出大的塑料袋、 玻璃瓶、 石块、 橡胶等大颗粒物质,2 mm过筛处理后备用. 矿化垃圾基本物理化学性质见表 2.
| 表 2 装填垃圾的物理化学特性 Table 2 Physical and chemical characteristics of aged refuse |
实验将矿化垃圾装填于有机玻璃柱内,模拟SAARB. 有机玻璃柱规格为高度1 000 mm,内径150 mm,壁厚5 mm. 反应器底部设置渗滤液收集口和通风管,顶部设置渗滤液回灌口和气体采样口. 填埋柱自下而上依次为50 mm渗滤液储存层,50 mm砾石层,800 mm矿化垃圾填埋层,50 mm细沙层用于均匀布水,以及50 mm自由空间以贮存气体. 实验装置如图 1所示.
 | 图 1 实验装置示意 Fig. 1 Schematic diagram of experimental apparatus |
实验采用如图 2所示实验操作流程进行. 实验开始前采用容积负荷渐增法[18]对反应器进行驯化. 渗滤液回灌前采用空气压缩机(35 L ·min-1)对反应器底部通气导管进行曝气,时间为5 min,保证反应器内部空气完全置换. 然后用蠕动泵回灌,回灌周期为1 d,回灌量为每次0.5 L,回灌时间为10 min,回灌速率为0.05 L ·min-1. 回灌24 h后排空底部渗滤液并收集100 mL作为样品进行测定,同时采用50 mL注射器抽取顶部气体测定N2 O浓度. 每个水平在至少6周期稳定后进行下一水平的实验. 反应器进水是将渗滤液进行1 ∶5稀释,并通过添加NaCl以调节进水盐度,同时添加渗滤液调节进水渗滤液COD和NH+4-N浓度在一定范围内,并控制适宜的pH,回灌采取盐度从低到高的顺序进行. 实验在25-30℃的室内进行.
 | 图 2 实验操作流程 Fig. 2 Experimental operation process during a single cycle |
实验每天采集渗滤液和气体样品进行测定. N2 O的测定采用Shimaduz GC 2010 Plus气相色谱仪分析,色谱柱为Porapak Q (30 m×0.53 mm×20 μm),检测器为电子捕获监测器ECD,载气为99.99%的高纯氮气. 操作参数为:定量六通阀进样,进样量1 mL,柱流量1.0 mL ·min-1,分流比为20,柱温60℃,SPL进样口温度150℃,ECD检测器温度340℃. 渗滤液分析指标和方法见表 3.
| 表 3 渗滤液监测指标及方法 Table 3 Leachate monitoring indexes and methods |
N2 O气体产生量按公式:
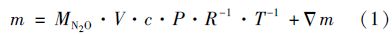
式中,m为N2 O产生量(以N计),单位为μg; c为N2 O产生量(体积分数); V为一个周期内产生的气体体积(L),实际以柱内上部预留空间体积计算; MN2O为N2 O摩尔质量(28 g ·mol-1); P为大气压力(atm); T为气体温度(K); R为理想气体常数[0.082 L ·atm ·(K ·mol)-1]; Δ m为取气损失量(以N计),单位为μg.
渗滤液中COD、 NH+4-N、 TN去除率按公式:

不同盐度条件下反应器在稳定运行后出水水质如图 3-5所示.
 | 图 3 出水COD随进水盐度变化趋势 Fig. 3 COD of effluent leachate as a function of influent salinity |
由图 3可知,随着进水盐度的增加,出水COD浓度逐渐升高,去除率逐渐下降,COD去除率由最初的95%下降到89%. 这是由于7 g ·L-1盐度时对微生物的抑制作用不明显,进水盐度突然增至10 g ·L-1时,微生物不能立即适应而出现COD去除率下降的现象. 后续,随着进水盐度的提高,COD去除率稳定在90%左右,可见系统内的异养微生物逐渐适应了较高的盐度环境,虽然进水COD浓度有小范围波动,但整个实验周期COD去除率始终在85%以上. 刘甜甜等[15]在同类研究中表明,盐度对各菌群的抑制强度中对碳氧化菌的抑制强度最弱. 较高的COD去除率表明进水渗滤液中有机碳源得到了充分利用,这也与盐度对反硝化菌等异养菌的抑制程度相关. 上述变化可以看出盐度的增加对SAARB去除有机物的能力存在一定的影响,但影响不大,此外在一定的盐度浓度范围内经过一定时间的驯化,
不适应高盐度环境的微生物淘汰,耐盐微生物可以通过自身渗透压调节生理作用来保护细胞体内原生质或平衡自身渗透压,逐渐恢复活性[19, 20],使系统仍能达到较高的COD去除率,这也与渗滤液中有机物大部分为易生物降解有机物有关.
由图 4可知,不同进水盐度条件下,出水NH+4-N和TN变化趋势基本一致. 随着进水盐度的增加,出水NH+4-N、 TN浓度均呈逐渐上升,去除率均呈逐渐下降的趋势. 出水NH+4-N、 TN去除率分别由7 g ·L-1盐度时的98.23%、 91.48%降至30 g ·L-1时的31.75%、 34.24%. 由于反应器在间歇曝气密封后相当于一个准好氧生物反应床,张爱平等[21]研究发现准好氧矿化垃圾床系统内存在大量的亚硝化菌、 硝化菌、 厌氧反硝化菌和好氧反硝化菌,并由此表明准好氧矿化垃圾床处理渗滤液的生物脱氮机制为同步硝化反硝化,主要发生在反应床的表层和底部. 本实验只对下层出水进行了水质测定,所测水质已经在反应柱内发生了充分的硝化、 反硝化作用. 盐度7 g ·L-1时,NH+4-N、 TN去除率较高,表明反应柱内的硝化、 反硝化菌群能很快适应低盐环境,并未对脱氮效果产生明显影响. 当进水盐度为10 g ·L-1时,去除率分别降至70.16%和69.99%,随着后续进水盐度(15-30 g ·L-1)的增加,去除率均显著下降,基本处于50%以下. 这主要是由于盐度的变化使矿化垃圾体内丰富的生物类群受到不同程度的抑制作用,随着盐度升高,系统内脱氮微生物的受抑制作用增强,盐度的突然增大使不能适应高盐环境的微生物被淘汰,适应环境的脱氮微生物生存下来,并成为优势菌群,此过程也是一个菌群优化的过程. 盐度对硝化细菌的抑制机制为:盐度的增加,硝化细菌受到外界环境的胁迫,会提高自身渗透压或者通过分泌溶解性微生物产物和胞外聚合物来保护自身,细胞用于维持自身新陈代谢的能量减少,导致硝化菌酶受到影响; 此外,适应高盐环境酶系统的形成一方面需要能量,另一方面也需要时间,从而使其硝化能力变弱[21, 22]. 而反硝化细菌对有毒有害物质的敏感性比硝化细菌低得多[23, 24]. 结合图 5可以看出,在进水NH+4-N相同时,随着盐度增加,出水NH+4-N去除率大幅降低的同时出水NO-x-N呈现增加趋势. 在盐度为30 g ·L-1时,出水水质才出现明显的NO-2-N、 NO3--N积累现象. 由于进水C/N始终大于5,根据同类研究表明此时C源并不是反硝化脱氮的限制因素[25].
 | 图 4 出水NH+4-N和TN随盐度变化趋势 Fig. 4 NH+4-N and TN concentrations of leachate as a function of salinity |
可见NaCl盐度对硝化细菌和反硝化细菌均有抑制作用,且对硝化菌的抑制作用远大于反硝化菌. 这与Pronk等[26]和王淑莹等[27]在NaCl盐度对活性污泥系统脱氮性能的影响研究结果一致.
 | 图 5 出水NO3--N和NO-2-N随盐度变化趋势 Fig. 5 NO3--N and NO-2-N concentrations of leachate as a function of salinity |
不同盐度条件下,反应器密闭 24 h后,顶部预留空间气体中 N2 O产生量变化如图 6所示.
 | 图 6 N2 O产生量随盐度变化趋势 Fig. 6 Production of N2 O as a function of salinity |
由图 6可知,在进水其他条件相同时,随着盐度的增加,反应器中N2 O产生量呈增加趋势. 在7-15 g ·L-1的盐度范围内N2 O产生量较少,平均产生量在18.16-66.92 μg之间,占TN去除总量的0.08‰-0.28‰; 盐度为20 g ·L-1时平均产生量为232.31 μg±65.36 μg,占TN去除总量的1.63‰; 30 g ·L-1高盐度条件下其N2 O平均产生量最高,为1 397 μg±369.88 μg,占TN去除总量的8.87‰,是回灌低盐度条件下的6-117倍. 可见N2 O的产生量与回灌渗滤液盐度负荷呈显著的正相关. 分析原因可能是盐度对硝化和反硝化微生物不同的抑制强度造成NO-2-N的积累,而NO-2-N的积累不论对硝化过程还是反硝化过程均是导致N2 O产生的关键因素[28, 29]. 在进水盐度7-20 g ·L-1时未出现明显NO-2-N积累现象,但由于盐度增加对硝化过程的抑制作用增强,使硝化过程N2 O产生量增加; 同时反硝化过程受抑制作用增强,反硝化过程N2 O产生量也增加,此外氧化亚氮还原酶(Nos)受盐度抑制作用增强[30],使反硝化过程N2 O去除量减少,从而使反应器内N2 O产生量增加. 而盐度为30 g ·L-1时出现了较高的NO-2-N、 NO3--N积累. 氨氧化细菌生成的部分NO-2-N及硝酸盐还原菌生成的NO-2-N无法进一步发生反硝化去除. 而NO-2-N的积累也会导致氨氧化细菌产生异构亚硝酸盐还原酶以NO-2-N为电子受体,导致N2 O的产生. 同时盐度对Nos存在抑制作用,使硝化和反硝化过程中产生的N2 O无法进一步被还原,从而导致30 g ·L-1盐度时较其他盐度条件下N2 O的积累与释放量增加显著.
2.3 单周期N2O产生规律分析以上实验结果分析可知,SAARB在对渗滤液的回灌处理中进水盐度的改变是影响渗滤液脱氮效果及N2 O释放的重要因素. 为进一步探究盐度对N2 O释放的影响规律,特选不同盐度条件下一个回灌周期,探究SAARB内的N2O产生量随时间的动态变化规律(图 7).
 | 图 7 N2 O产生量随时间变化趋势 Fig. 7 Production of N2 O as a function of time |
由图 7可知,随着进水盐度的增加,一个周期内N2O产生量和产生特征随时间变化趋势上存在一定的差异. 盐度为7 g ·L-1时,初始N2 O产生量最高为19.61 μg,然后随时间急剧下降,4 h后N2 O产生量已低于仪器的检出限. 盐度在10-20 g ·L-1范围时,N2 O产生量变化基本一致,呈现先缓慢升高后逐渐降低的趋势. 30 g ·L-1盐度时,反应器内N2 O产生量呈现先骤然升高后缓慢降低的趋势. 反应至10 h时,N2 O产生量达最高,为16 620.23 μg,24 h后,N2 O产生量明显高于其他盐度条件,为6 900.40 μg. 分析原因是反应器经过曝气后,O2充足条件下进行回灌,回灌的渗滤液首先与矿化垃圾表层接触发生硝化反应,从而使反应器产生N2 O. 随着O2的消耗以及渗滤液的下渗,反应器内存在缺氧-厌氧环境,硝化、 反硝化反应同时进行[21]. 随后由于O2的进一步消耗以及NH+4-N的降低,硝化过程产生的N2 O虽有减少,但反硝化过程在对NO-x-N的反硝化过程中也会产生部分N2 O[31],使反应器内N2 O在一定时间内呈升高趋势; 同时存在反硝化微生物产生的Nos使N2 O作为反硝化的中间产物被还原为N2的过程. 后期由于反硝化作用的持续进行以及硝化作用的进一步减弱,使反应器内N2 O浓度达到峰值后开始逐渐降低.
不同盐度条件下N2 O产生量峰值具有较大差异,盐度为30 g ·L-1时N2 O产生量的最大值为16 620.23 μg,是低盐度7 g ·L-1条件的790倍. 低盐度7 g ·L-1条件下,N2 O峰值出现的时间为4 h; 高盐度条件下(10-30 g ·L-1)N2 O峰值出现在10-12 h之间,与低盐度相比,存在峰值延后的现象,与刘甜甜等[15]和Tsuneda等[30]等的研究报道一致. 分析原因是随着进水盐度增加,硝化、 反硝化作用所受抑制程度不同造成的. 随着进水盐度的增加,硝化作用受抑制强度高,使硝化过程产生副产物N2 O浓度依次升高,虽然反硝化作用受抑制强度低,但其产生中间产物N2 O也呈升高趋势,而反硝化初期,由于Nos的合成滞后而使N2 O不能迅速被还原成N2,造成N2 O积累[32]. 因此N2 O峰值随进水盐度增加呈增加趋势; 而已合成的Nos随盐度增加所受抑制也逐渐增加,N2 O还原作用逐渐减弱,致使N2 O单周期内峰值出现的时间呈现延后趋势.
3 结论(1)盐度对SAARB回灌渗滤液的处理效果有一定影响. COD的去除率随进水盐度的增加而降低,但始终维持在85%以上. 与COD去除效率相比,盐度对氮污染物的去除效果有较大影响,NH+4-N、 TN的去除率分别由最初的98.23%、 91.48%降至31.75%、 34.24%. 同时在高盐度条件下(30 g ·L-1)时,反应器出水出现了明显的NO-2-N积累现象.
(2)随着进水盐度的增加,N2 O产生量显著增加. 当进水盐度为30 g ·L-1时N2 O产生量可达到(1 397±369.88) μg,占TN去除量的8.87‰,同时单周期内N2 O产生量也呈增高趋势,产生量峰值也出现延后趋势.
(3)通过本研究发现,回灌渗滤液存在高盐度环境时,反应器脱氮效果会受到明显抑制,N2 O产生量骤然增加,也就意味着垃圾填埋场的高盐渗滤液回灌可能贡献了N2 O的产生,间接影响全球温室效应.
| [1] | 赵由才, 柴晓利, 牛冬杰. 矿化垃圾基本特性研究[J]. 同济大学学报(自然科学版), 2006, 34 (10): 1360-1364. |
| [2] | 石磊, 张全, 牛冬杰, 等. 矿化垃圾反应床处理渗滤液的微生物学特性[J]. 同济大学学报(自然科学版), 2007, 35 (8): 1085-1089. |
| [3] | 张爱平, 刘丹, 何水晶. 基于准好氧矿化垃圾床的渗滤液脱氮研究[J]. 水处理技术, 2008, 34 (7): 36-38, 42. |
| [4] | He Y, Zhao Y C, Zhou G M, et al. Field assessment of stratified aged-refuse-based reactor for landfill leachate treatment[J]. Waste Management & Research, 2011, 29 (12): 1294-1302. |
| [5] | Xie B, Zhou L, Chong H, et al. Nitrogen removal through different pathways in an aged refuse bioreactor treating mature landfill leachate[J]. Applied Microbiology Biotechnology, 2013, 97 (20): 9225-9234. |
| [6] | Hassan M, Xie B. Use of aged refuse-based bioreactor/biofilter for landfill leachate treatment[J]. Applied Microbiology and Biotechnology, 2014, 98 (15): 6543-6553. |
| [7] | Kampschreur M J, Temmink H, Kleerebezem R, et al. Nitrous oxide emission during wastewater treatment[J]. Water Research, 2009, 43 (17): 4093-4103. |
| [8] | De Graaff M S, Zeeman G, Temmink H, et al. Long term partial nitritation of anaerobically treated black water and the emission of nitrous oxide[J]. Water Research, 2010, 44 (7): 2171-2178. |
| [9] | Ravishankara A R, Daniel J S, Portmann R W. Nitrous oxide (N2 O): The dominant ozone-depleting substance emitted in the 21st century[J]. Science, 2009, 326 (5949): 123-125. |
| [10] | 苏艳萍, 刘丹, 张爱萍, 等. 准好氧矿化垃圾处理渗滤液的工艺参数研究[J]. 四川环境, 2008, 27 (2): 35-38. |
| [11] | 何水晶, 李启彬, 刘忠鹏. 准好氧矿化垃圾床处理渗滤液的试验研究[J]. 环境科学与技术, 2009, 32 (7): 152-155. |
| [12] | 李贵芝, 刘丹, 李启彬, 等. 准好氧矿化垃圾生物反应床的最佳工况研究[J]. 环境科学与技术, 2012, 35 (3): 34-37. |
| [13] | Zhao W, Wang Y Y, Liu S H, et al. Denitrification activities and N2 O production under salt stress with varying COD/N ratios and terminal electron acceptors[J]. Chemical Engineering Journal, 2013, 215-216 : 252-260. |
| [14] | Loncnar M, Zupan Dč i Dč M, Bukovec P, et al. Fate of saline ions in a planted landfill site with leachate recirculation[J]. Waste Management, 2012, 30 (1): 110-118. |
| [15] | 刘甜甜, 彭永臻, 王淑莹, 等. 盐度对垃圾渗滤液短程脱氮性能及其N2 O产量的影响[J]. 化工学报, 2012, 63 (10): 3269-3276. |
| [16] | 王珊珊, 梁红, 高大文. 盐度对好氧颗粒污泥硝化过程中N2 O产生量的影响[J]. 环境科学, 2014, 35 (11): 4237-4243. |
| [17] | 尚会来, 彭永臻, 张静蓉, 等. 盐度对污水硝化过程中N2 O产量的影响[J]. 环境科学, 2009, 30 (4): 1079-1083. |
| [18] | 刘丹, 张爱平, 陈锦文. 准好氧生物反应器处理渗滤液系统的驯化研究[J]. 中国给水排水, 2007, 23 (19): 80-82, 86. |
| [19] | Chen M X, Wang W C, Feng Y, et al. Impact resistance of different factors on ammonia removal by heterotrophic nitrification-aerobic denitrification bacterium Aeromonas sp. HN-02[J]. Bioresource Technology, 2014, 167 : 456-461. |
| [20] | 王子超. 盐度和重金属对序批式生物反应器性能及微生物群落结构影响的研究[D]. 青岛: 中国海洋大学, 2014. |
| [21] | 张爱平, 刘丹, 韩智勇, 等. 准好氧矿化垃圾床处理渗滤液的脱氮菌群研究[J]. 环境科学研究, 2011, 24 (1): 102-109. |
| [22] | Dinçer A R, Kargi F. Salt inhibition kinetics in nitrification of synthetic saline wastewater[J]. Enzyme and Microbial Technology, 2001, 28 (7-8): 661-665. |
| [23] | 屈晋云, 刘波, 万馥君, 等. 针对硝化菌抗盐机理的研究[J]. 环境科学与技术, 2012, 35 (9): 108-111. |
| [24] | Yuan C Y, Li C X, Wang Y, et al. Study on the salinity domestication and mechanism of nitrite nitrogen removal of Acinetobacter lwoffii[J]. Advanced Materials Research, 2015, 1092-1093 : 641-644. |
| [25] | 李鹏章, 王淑莹, 彭永臻, 等. COD/N与pH值对短程硝化反硝化过程中N2 O产生的影响[J]. 中国环境科学, 2014, 34 (8): 2003-2009. |
| [26] | Pronk M, Bassin J P, De Kreuk M K, et al. Evaluating the main and side effects of high salinity on aerobic granular sludge[J]. Applied Microbiology and Biotechnology, 2014, 98 (3): 1339-1348. |
| [27] | 王淑莹, 唐冰, 叶柳, 等. NaCl盐度对活性污泥系统脱氮性能的影响[J]. 北京工业大学学报, 2008, 36 (6): 631-635. |
| [28] | Alinsafi A, Adouani N, Béline F, et al. Nitrite effect on nitrous oxide emission from denitrifying activated sludge[J]. Process Biochemistry, 2008, 43 (6): 683-689. |
| [29] | Ali T U, Ahmed Z, Kim D J. Estimation of N2 O emission during wastewater nitrification with activated sludge: effect of ammonium and nitrite concentration by regression analysis[J]. Journal of Industrial and Engineering Chemistry, 2014, 20 (4): 2574-2579. |
| [30] | Tsuneda S, Mikami M, Kimochi Y, et al. Effect of salinity on nitrous oxide emission in the biological nitrogen removal process for industrial wastewater[J]. Journal of Hazardous Materials, 2005, 119 (1-3): 93-98. |
| [31] | 汤洁, 方天儒, 侯克怡, 等. 盐碱区不同开发年限水田温室气体排放规律及影响因素[J]. 环境科学, 2014, 35 (12): 4727-4734. |
| [32] | Letey J, Valoras N, Focht D D, et al. Nitrous oxide production and reduction during denitrification as affected by redox potential[J]. Soil Science Society of America Journal, 1981, 45 (4): 727-730. |
 2016, Vol. 37
2016, Vol. 37


