2. 中国海洋大学海洋化学理论与工程技术教育部重点实验室, 青岛 266100
2. Key Laboratory of Marine Chemistry Theory and Technology, Ministry of Education, Ocean University of China, Qingdao 266100, China
磷是影响藻类生长、 水体富营养化的重要营养元素之一,而沉积物是海洋中氮、 磷等营养盐蓄积、 释放的重要场所[1, 2]. 桑沟湾位于山东半岛东端,北、 西、 南为陆地环绕,湾口向东,为半封闭海湾,平均水深约7.5 m,是我国北方重要的水产品基地,主要养殖品种有贝类和海带等,其生物活动影响营养盐在沉积物-水界面的通量[3, 4],同时,风浪扰动可引起沉积物再悬浮[5],影响着沉积物中磷源的释放,对水体营养化水平也有重要的贡献. 养殖水体底质与上覆水的物质交换是初级生产者营养要素的主要来源之一,已有的研究表明桑沟湾养殖水域表层沉积物起“磷源”的作用[5],影响养殖生物的生长繁殖. 与非养殖区相比,养殖海域的沉积物组成及理化性质的时空分布均存在显著特点[4, 6, 7],而沉积物对磷的吸附特性与其组成及理化性质有密切的联系[1, 8, 9, 10]. 另外沉积物与磷的结合形式多样复杂[11, 12, 13],对沉积物中磷的形态分析有助于认识沉积物内源磷负荷机制和沉积物-水界面磷的交换机制,但在海水养殖环境中,结合沉积物表面特性及吸附过程中磷的形态变化研究磷的吸附机制的报道较少. 因此从以上入手研究养殖海域沉积物界面上磷的迁移行为是很有必要的.
本研究在室内模拟条件下,考察了桑沟湾表层沉积物对磷的吸附动力学和热力学等温线,采用酸碱电位滴定技术测定了沉积物的表面电荷性质,与表面络合理论相结合,探讨了固体表面电荷和表面羟基位对吸附的影响; 同时利用连续提取法[13, 14],对桑沟湾表层沉积物吸附磷前后的样品分别进行磷赋存形态分析,讨论了磷在沉积物-水界面的迁移、 转化机制. 以上结果有助于为桑沟湾养殖环境质量控制提供技术支撑,促进桑沟湾水产养殖业的稳定、 健康发展.
1 材料与方法 1.1 样品采集与预处理实验所用沉积物样品于2011年4月(春季)、 8月(夏季)分别取自桑沟湾养殖区,取回后冷冻保存. 使用前室温解冻、 自然风干,研磨,分别过40、 200目尼龙筛,封于聚乙烯袋中备用. 采用X射线粉末衍射法测定沉积物矿物组成,灼烧法测定有机质(OM)含量[15],其部分理化性质列于表 1. 实验所用天然海水(NSW)取自青岛石老人海域,经陈化后,抽滤过0.45 μm滤膜,调节pH至8.0. 其中无机磷含量小于0.001 mg ·L-1.
|
|
表 1 沉积物样品的组成 Table 1 Compositions of the sediment samples |
采用批量法,称取一系列(0.500 0±0.000 2) g沉积物样品于100 mL磨口带塞锥形瓶中,然后加入40 mL 1.0 mg ·L-1的磷溶液(由KH2PO4和NSW配制,调整pH=8.0),于(25±1)℃恒温水浴振荡器中150 r ·min-1振荡,定时取样,离心分离,用磷钼蓝分光光度法[16]测定上清液磷的浓度,根据吸附前后水样中磷的浓度差,计算磷在t时间段内的吸附量Qt(mg ·g-1),绘制吸附动力学曲线. 根据所确定的吸附平衡时间,过程同上,改变磷酸盐初始浓度(0-2.0 mg ·L-1)进行吸附等温线测定.
以上实验均在相同条件下作2个平行样. 空白实验表明器壁吸附可以忽略不计.
1.2.2 表面酸碱性质测定实验采用瑞士万通809自动电位滴定仪进行测定. 准确称取0.1 g沉积物样品(过200目筛),加入40 mL 0.7 mol ·L-1 NaNO3溶液,水化充分后进行滴定. 滴定过程中通N2,排除CO2的干扰,温度控制在(25.0±0.2)℃. 等量等当点滴定法控制酸碱加入量,所使用的NaOH和HNO3溶液均为标定后的标准溶液. 先滴加HNO3至pH=3左右(酸量滴定),然后用NaOH滴定至pH=10左右(碱返滴定),再用HNO3返滴定至第一次酸量滴定的pH(酸返滴定). 以第二次滴酸的体积换算滴定过程所需要的酸,消除了基体溶解带来的误差. 借助FITEQL 4.0软件,采用恒定容量模型对表面酸碱反应平衡常数进行计算.
1.2.3 沉积物中磷形态的分离提取称取一系列(0.500 0±0.000 2) g沉积物样品于100 mL磨口带塞锥形瓶中,然后加入40 mL浓度为16.0 mg ·L-1的磷溶液,于(25±1)℃恒温水浴振荡器中振荡48 h后平衡,离心分离,吸附磷后的沉积物样品烘干备用.
分别称取5份(0.150 0±0.000 2) g沉积物原样及以上吸附后的沉积物样品于50 mL离心管中,进行如下逐级分离提取[13, 14]:分别用MgCl2溶液、 柠檬酸钠-连二亚硫酸钠-碳酸氢钠混合溶液(CDB)、 醋酸钠-醋酸缓冲液、 盐酸溶液提取无机磷中的弱吸附态磷(Ex-P)、 铁结合态磷(Fe-P)、 自生和生物磷灰石碳酸钙结合磷(ACa-P)、 原生碎屑及其它无机磷(DAP); 然后将提取无机磷后的沉积物在550℃下灰化,用盐酸提取有机磷(OP).
2 结果与讨论 2.1 吸附动力学沉积物对磷的吸附通常包括快吸附过程和慢吸附过程. 图 1为P在桑沟湾1号站位沉积物样品(8月,过200目筛)的吸附动力学曲线. 在初始2 h内吸附较快,之后吸附量增长缓慢,到36 h时吸附反应基本达到平衡,为保证吸附充分,平衡时间确定为48 h.

|
图内曲线为快慢二段一级动力学方程拟合曲线 图 1 1号站位沉积物对P的动力学吸附曲线 Fig. 1 Sorption kinetic curve for phosphorus onto 1 sediment |
利用伪二级动力学方程(1)和快慢二段一级动力学方程(2)对吸附动力学曲线进行拟合.
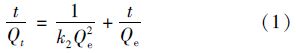
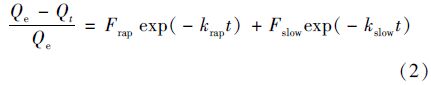
|
|
表 2 1号站位沉积物对P的动力学吸附拟合参数 Table 2 Fitted kinetic parameters of phosphorus sorption onto 1 sediment |
对1、 2、 3号站位沉积物样品(40目)分别进行磷的吸附热力学实验. 由图 2可见,磷初始浓度较低时,研究范围内样品对磷的吸附存在负吸附现象,原因是天然沉积物中存在内源磷,即原先结合在沉积物上的磷 (NAP),当介质中磷浓度小于某一临界值时,这部分磷就会释放进入介质,吸附等温线符合Langmuir交叉型等温式[2].
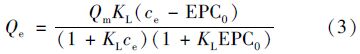
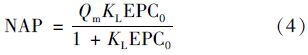

|
图 2 不同季节、 粒度的沉积物对P的吸附等温线 Fig. 2Phosphorus sorption isotherms of different particle size fractions from various sediments in different seasons |
拟合计算结果见表 3,拟合相关系数r2在0.986-0.998之间,3个站位在4、 8月沉积物样品对磷的最大吸附量Qm在0.047 1-0.123 0 mg ·g-1之间,春、 夏季均表现为3号站位最大,1号最小,NAP值在0.010 6-0.016 1 mg ·g-1之间,EPC0在0.059 6-0.192 7 mg ·L-1,3个站位的EPC0在春季均明显高于夏季,且均大于相应上覆水中磷浓度(约0.006 5-0.058 9 mg ·L-1)[5, 6],因此可以认为桑沟湾沉积物有向上覆水中释放磷的能力,即充当“磷源”的作用,与蒋增杰等[5]的研究结论一致.
|
|
表 3 4、 8月沉积物对P的等温吸附曲线拟合参数 Table 3 Fitted isotherm parameters of thesorption of phosphorus in April and August |
沉积物对磷的吸附行为受沉积物组成的影响. 由XRD结果(表 1)可见,1号站位样品赤铁矿、 黏土矿物、 方解石及有机质含量相对较少,以上组分作为沉积物中的吸附活性组分对磷的吸附性能起着重要作用,因此可认为是导致1号站位的Qm最小的原因之一. Qm与沉积物中具有较高比表面积的Fe、 Al氧化物有密切的关系,铁氧化物含大量的表面羟基位,并且可以粘附于黏土矿物表面,对磷具有较强的吸附能力[19, 20]; 黏土矿物是由硅(铝)氧四面体片和金属-氧(羟基)八面体片构成的层状结构,表面存在大量的Si—OH、 Al—OH等基团,具有较大表面积,且常带有不饱和电荷,对水体中磷元素有较好的吸附能力[21]; 方解石对磷的吸附作用较强且迅速[22]. 除此之外,有机质作为沉积物重要的组成部分,在沉积物吸附磷的过程中也有重要作用:腐殖质能和铁、 铝形成有机无机复合体,抑制铁、 铝氧化物结晶,从而增强对磷的吸附[9, 19],另外有机质还可以释放出氢离子,引起沉积物表面基团质子化而有利于磷的吸附[23]. 但由于有机质结构复杂,除了能促进磷的吸附之外,部分有机质也可以抑制磷的吸附,例如富里酸聚阴离子与磷酸盐阴离子可产生吸附竞争,促进磷的释放[23].
作为养殖海域的桑沟湾,春季(4月)海带、 贝类处于生长阶段,2011年5月桑沟湾发生大规模赤潮,造成海带腐烂,贻贝、 牡蛎及滩涂贝发生大规模死亡[24]. 死亡的残体、 碎屑变成水体中悬浮有机颗粒物,沉于沉积物表层,以致本实验中2、 3号站位夏季样品中有机质含量比春季高(表 1),对磷的吸附有一定的促进作用[9, 19],另外,生物残体中微生物的作用也是增强沉积物吸附磷的重要因素[25],以上可能是磷最大吸附量表现为夏季大于春季的原因之一. 1号站位在湾外,受到海浪的不断冲击,沉降有机颗粒发生再悬浮,可能是导致其夏季样品中有机质含量比春季低(表 1)的原因.
为了了解粒度对沉积物吸附磷的影响,选用8月沉积物样品,过200目筛,进行对比吸附实验(图 2),以Langmuir交叉型模型拟合的结果见表 3. 各站位沉积物样品对磷的Qm均表现出过40目筛小于过200目筛的沉积物样品. 随着沉积物颗粒粒径的减小,比表面增大,可以提供大量的沉积物矿物表面,为磷提供吸附位点,吸附量增大[19, 26].
2.3 沉积物的表面酸碱性质沉积物的表面电荷量受沉积物中铁锰氧化物、 腐殖酸等组分的影响. 这些成分表面所带的可离子化功能团如—OH、 —SH、 —COOH等,在水溶液中,通过不同程度的加质子[式(5)]或脱质子[式(6)]反应改变沉积物的表面电荷量[27].
将沉积物样品看作均一表面 ≡SOH ,在沉积物 ≡SOH 表面上可以发生两种反应:
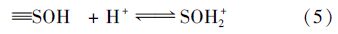
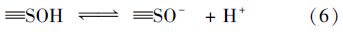
图 3是1、 2、 3号三站位沉积物样品(8月)分别进行酸碱电位滴定所得滴定曲线及pH-Ht图(Ht表示酸的总浓度). 表 4是应用恒定容量模式(CCM),以FITEQL 4.0程序对滴定曲线进行拟合的结果. 由于沉积物组成复杂,不可能准确地区分不同表面活性位的数量,假定极限pH值条件下,所有的有效表面位被吸附的H+或OH-占据,即完全离子化,此时吸附或释放的最大质子量即为表面羟基位浓度Hs,由碱返滴定的实时Gran图,确定等价点处消耗碱的体积,按照公式(7)计算Hs.


|
图 3 不同站位沉积物样品电位滴定曲线及pH-Ht图 Fig. 3Titration curves and pH vs.Ht plots of the sediments from different sites |
|
|
表 4 沉积物电位滴定曲线拟合结果 Table 4 Fitting result for titration curve of the sediments samples |
由图 3可见,3个站位沉积物对pH均表现出一定的缓冲作用,零净质子电荷点PZNPC在pH=6左右,在零净质子电荷点时带有一定量负电荷. pH决定着水体中磷酸根和沉积物表面羟基的存在形态[28, 29]:pH=8时,沉积物表面荷负电,表面羟基趋于脱去质子,表面净电荷量随1、 2、 3号站位依次减小,而介质中磷酸根离子主要以HPO42-形式存在(pKa1=2.12,pKa2=7.20,pKa3=12.36),沉积物表面的负电荷会阻滞其对水体中同样荷负电的磷酸根离子的吸附,与前文中磷吸附能力的研究结果一致. 虽然此时静电吸附难以发生,磷酸根离子可以通过范德华力以及置换沉积物表面的羟基进行配体交换,后者将形成单齿或双齿形态的表面络合物. KL随Hs计算的增大而增大,说明随着表面羟基位浓度的增大,表面吸附活性增强,沉积物对磷的吸附能力增强. 然而随Hs计算的增大,Qm却没有表现出增加的趋势,说明磷在沉积物上的吸附量除受沉积物表面羟基位浓度影响外,还与羟基类型等相关:沉积物中金属氧化物的裸露晶面及晶面上金属离子的分布与配位情况影响着表面羟基的数量和类型,进而影响其配体交换反应的活性,对磷在沉积物上的吸附产生显著的影响. 如:单配位羟基Lewis酸性比双配位羟基高、 更易于参与配体交换反应,而三配位的羟基则只具有质子酸碱反应活性[28]. 由于沉积物中铁铝氧化物除了通过配体交换,还可以通过范德华力等作用进行吸附,也会导致Qm随着Hs计算的变化较为复杂.
2.4 沉积物中不同磷的形态对1、 2、 3号三站位8月沉积物原样(吸附前样品)和吸附16.0 mg ·L-1磷溶液后样品进行磷形态分析. 由图 4可见,在该3个站位原样中,总磷(TP)含量在16.12-21.12 μmol ·g-1之间,其中3号站位含量最大,2号最小; 作为TP主要部分的无机磷(IP)占TP的84%-89%. 吸附后样品中,TP含量在21.07-27.13 μmol ·g-1之间,3号站位含量最大,2号最小,其中IP占TP的88%-91%,与原样相比,IP含量显著增多. Ex-P主要是指沉积物中的Fe、 Mn氧化物或氢氧化物以及黏土矿物等颗粒表面吸附的磷,很容易释放进入水体[13]; 原样中Ex-P含量最少,含量在0.72-1.07 μmol ·g-1之间; 吸附后的样品中Ex-P含量显著增多,在4.15-5.36 μmol ·g-1之间. Fe-P包括铁铝结合态磷和Fe2O3胶膜包裹的磷酸铁及磷酸铝(闭蓄态磷),亲和力较强[13]; 原样中Fe-P含量在1.47-3.56 μmol ·g-1之间,占IP的10%-20%,3号站位的Fe-P含量最多,2号最少. 吸附后样品的Fe-P含量在3.04-5.33 μmol ·g-1之间,占IP的16%-23%,比吸附前有所增加. 沉积物中铁氧化物含有大量可吸附磷的活性羟基位,沉积物中的Fe-P被认为比其它自生矿物(如碳酸氟磷灰石)结合P更容易转化,在吸附过程中具有重要作用[13, 30].

|
图 4 不同沉积物吸附前后磷形态分布 Fig. 4 Contents of Ex-P,Fe-P,ACa-P,DAP,OP from sediments before and after adsorption |
ACa-P是指自生成因和生物成因的自生磷灰石磷,以及与自生碳酸钙共同沉淀的磷(包括生物残骸),或者沉积物早期成岩过程中内生过程形成或生物成因的钙结合态磷[14]; 3个站位原样中所含ACa-P相差不大. DAP主要来源于流域内风化侵蚀产物中磷灰石矿物晶屑等[14]; 3号站位沉积物原样含DAP最多,2号最少. 吸附前后ACa-P与DAP的含量变化不大. OP主要来自陆源排放物质及海洋浮游生物的排泄物或死亡残体,该部分磷一般不能直接被植物利用. 3号站位含OP稍高一些,1号最少,OP与有机质含量及种类有密切的联系.
吸附磷前后的沉积物相比,吸附后样品中Ex-P、 Fe-P含量明显增多,其中Ex-P含量变化最大,占总磷变化量的75%-77%,表明吸附到沉积物中的磷主要以Ex-P、 Fe-P的形式呈现. Ex-P容易在沉积物表面进行可逆性的吸附和解吸,Ex-P的形成主要通过物理吸附为主,过程迅速且可逆,Fe-P主要是通过化学吸附,这种吸附一般不可逆,由此可见,研究范围内,沉积物对磷的吸附中物理吸附和化学吸附同时存在,但物理吸附为主.
3 结论(1)桑沟湾表层沉积物对磷的吸附可用快慢二段一级动力学方程描述,等温线符合Langmuir交叉式; 夏季沉积物样品的Qm大于春季样品,粒级较小的沉积物吸附能力较强.
(2)1、 2、 3号站位沉积物样品的表面电荷量依次减少. 随表面电荷量的减少,Qm增大,KL随表面羟基位浓度的增大而增大. 沉积物表面羟基位的数量影响表观吸附量,表面位点的类型等由于反应活性的差异对吸附能力也有重要的作用.
(3)3个站位不同形态磷的含量不同,受所处地域的影响. 原样中总磷(TP)含量在16.12-21.12 μmol ·g-1之间,IP占TP的84%-89%. 吸附磷后的样品与原样比较,吸附后的样品中Ex-P、 Fe-P含量明显增多,其中Ex-P含量变化最大,沉积物对磷的吸附过程中,物理吸附和化学吸附同时存在,以物理吸附为主.
| [1] | Jalali M, Peikam E N. Phosphorus sorption-desorption behaviour of river bed sediments in the Abshineh river, Hamedan, Iran, related to their composition[J]. Environmental Monitoring and Assessment, 2013, 185 (1): 537-552. |
| [2] | 王圣瑞, 金相灿, 赵海超, 等. 长江中下游浅水湖泊沉积物对磷的吸附特征[J]. 环境科学, 2005, 26 (3): 38-43. |
| [3] | 孙珊, 刘素美, 任景玲, 等. 桑沟湾养殖海域营养盐和沉积物-水界面扩散通量研究[J]. 海洋学报, 2010, 32 (6): 108-117. |
| [4] | 蔡立胜, 方建光, 董双林. 桑沟湾养殖海区沉积物-海水界面氮、 磷营养盐的通量[J]. 海洋水产研究, 2004, 25 (4): 57-64. |
| [5] | 蒋增杰, 王光花, 方建光, 等. 桑沟湾养殖水域表层沉积物对磷酸盐的吸附特征[J]. 环境科学, 2008, 29 (12): 3405-3409. |
| [6] | 万玲. 春季桑沟湾海域贝类养殖营养盐对海水中营养盐的影响研究[J]. 环境科学与管理, 2012, 37 (6): 62-66. |
| [7] | 杨茜, 杨庶, 宋娴丽, 等. 桑沟湾夏、 秋季悬浮颗粒物的沉降通量及再悬浮的影响[J]. 海洋学报, 2014, 36 (12): 85-90. |
| [8] | Zhu H W, Wang D Z, Cheng P D, et al. Effects of sediment physical properties on the phosphorus release in aquatic environment[J]. Science China Physics, Mechanics & Astronomy, 2015, 58 (2): 1-8. |
| [9] | Wang S R, Yi W L, Yang S W, et al. Effects of light fraction organic matter removal on phosphate adsorption by lake sediments[J]. Applied Geochemistry, 2011, 26 (3): 286-292. |
| [10] | Wei S Y, Tan W F, Liu F, et al. Surface properties and phosphate adsorption of binary systems containing goethite and kaolinite[J]. Geoderma, 2014, 213 : 478-484. |
| [11] | Jin X D, He Y L, Kirumba G, et al. Phosphorus fractions and phosphate sorption-release characteristics of the sediment in the Yangtze River estuary reservoir[J]. Ecological Engineering, 2013, 55 : 62-66. |
| [12] | Peryer-Fursdon J, Abell J M, Clarke D, et al. Spatial variability in sediment phosphorus characteristics along a hydrological gradient upstream of Lake Rotorua, New Zealand[J]. Environmental Earth Sciences, 2015, 73 (4): 1573-1585. |
| [13] | 朱媛媛. 东、 黄海沉积物中各形态磷的分布特征及其生物地球化学初步研究[D]. 青岛: 中国海洋大学, 2009. |
| [14] | Ruttenberg K C. Development of a sequential extraction method for different forms of phosphorus in marine sediments[J]. Limnology and Oceanography, 1992, 37 (7): 1460-1482. |
| [15] | Jin X C, Wang S R, Pang Y, et al. The adsorption of phosphate on different trophic lake sediments[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2005, 254 (1-3): 241-248. |
| [16] | GB 17378. 4-2007, 中华人民共和国国家标准海洋监测规范 第4部分: 海水分析[S]. |
| [17] | 江永春, 吴群河. 磷的沉积物-水界面反应[J]. 环境技术, 2003, (增刊): 16-19. |
| [18] | Lookman R, Freese D, Merckx R, et al. Long-term kinetics of phosphate release from soil[J]. Environmental Science & Technology, 1995, 29 (6): 1569-1575. |
| [19] | Wang S R, Jin X C, Bu Q Y, et al. Effects of particle size, organic matter and ionic strength on the phosphate sorption in different trophic lake sediments[J]. Journal of Hazardous Materials, 2006, 128 (2-3): 95-105. |
| [20] | Brinkman A G. A double-layer model for ion adsorption onto metal oxides, applied to experimental data and to natural sediments of Lake Veluwe, The Netherlands[J]. Hydroboiogia, 1993, 253 (1-3): 31-45. |
| [21] | 张宪伟, 潘刚, 王晓丽, 等. 内蒙古段黄河沉积物对磷的吸附特征研究[J]. 环境科学, 2009, 30 (1): 172-177. |
| [22] | Sø H U, Postma D, Jakobsen R, et al. Sorption of phosphate onto calcite; results from batch experiments and surface complexation modeling[J]. Geochimica et Cosmochimica Acta, 2011, 75 (10): 2911-2923. |
| [23] | 赵海超, 王圣瑞, 张莉, 等. 有机质含量及其组分对洱海沉积物磷吸附-释放影响[J]. 环境科学学报, 2014, 34 (9): 2346-2354. |
| [24] | 张继红, 王巍, 韩婷婷, 等. 桑沟湾春季营养盐分布特征及赤潮暴发诱因[J]. 水产学报, 2012, 36 (1): 132-139. |
| [25] | Jin C W, Du S T, Dong W Y, et al. Aquatic plant debris improve phosphorus sorption into sediment under anoxic condition[J]. Environmental Science and Pollution Research, 2013, 20 (11): 8237-8244. |
| [26] | Fan J Y, He X Y, Wang D Z. Experimental study on the effects of sediment size and porosity on contaminant adsorption/desorption and interfacial diffusion characteristics[J]. Journal of Hydrodynamics, 2013, 25 (1): 20-26. |
| [27] | 汤鸿霄. 环境水质学的进展——颗粒物与表面络合(上)[J]. 环境科学进展, 1993, 1 (1): 25-41. |
| [28] | Yang X F, Wang D S, Sun Z X, et al. Adsorption of phosphate at the aluminum (hydr) oxides-water interface: Role of the surface acid-base properties[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2007, 297 (1-3): 84-90. |
| [29] | Jalali M, Matin N H. Sorption of phosphorus in calcareous paddy soils of Iran: effects of soil/solution ratio and pH[J]. Environmental Earth Sciences, 2015, 73 (5): 2047-2059. |
| [30] | Huerta-Diaz M A, Tovar-Sánchez A, Filippelli G, et al. A combined CDB-MAGIC method for the determination of phosphorus associated with sedimentary iron oxyhydroxides[J]. Applied Geochemistry, 2005, 20 (11): 2108-2115. |
 2016, Vol. 37
2016, Vol. 37


