2. 安徽新华学院土木与环境工程学院, 合肥 230088
2. College of Civil and Environmental Engineering, Anhui Xinhua University, Hefei 230088, China
农业汇流区输出的氮磷是造成河、 湖、 库、 海湾水体发生富营养化的主要因素[1, 2]. 农业源头溪流是一类特殊的生态系统,不仅具有河流和湿地的双重特征,同时也具有排涝泄洪的水利工程作用. 作为连接农田与下游水体的重要通道,农田溪流水体沉积物起着氮磷等生源要素源、 汇的功能,特别是其具有的较浅水深和较高面积/体积比,控制着流域非点源污染物向受纳水体的输出负荷[3, 4],从而对农业非点源氮磷污染影响起到一定的调控作用. 近年来,有关源头溪流、 农业排水沟渠等小型河流水环境和水生态问题,已成为环境科学、 环境水文地质学等学科领域研究的热点[5, 6, 7, 8]. 目前,围绕农田溪流、 排水沟渠等开展的农业非点源氮磷污染调控和管理研究,主要集中在非点源氮磷污染特征、 氮磷截留净化的基本机制、 环境效应和生态功能等方面[9, 10, 11, 12, 13],虽然也有学者探讨了源头农业区不同类型水塘沉积物的磷形态及其吸附特征[14, 15, 16],但从整个溪流水系统层面分析沉积物的磷形态及其时空变化性,进而评估沉积物磷释放风险,则还显得较为不足.
巢湖是水体富营养化严重的大型淡水湖泊. 随着汇水区点源污染控制的逐步加强,周边农业区域非点源氮磷污染负荷成为影响巢湖水环境改善和水体富营养化控制的重要因素. 巢湖流域河流水系较为发达,各等级农业源头溪流的数量更是数不胜数. 毫无疑问,为数众多的溪流水系统沉积物的源或汇作用,对于处在最下游的巢湖水体生态环境质量有着极为重要的影响. 本研究拟以巢湖主要入湖河流南淝河的最大支流——二十埠河汇流区内的某一典型农业源头溪流系统为对象,从水塘、 支流、 干流及干流中深潭等溪流的几种主要构成模式角度,解析沉积物的磷形态及其释放风险,以期为巢湖流域农业汇流区溪流水系统磷素污染控制提供参考.
1 研究区概况 1.1 土地利用特征合肥市位于巢湖西半湖北侧,江淮分水岭南部,属于亚热带季风性湿润气候区. 年平均气温15.7℃,降水量近1 000 mm. 南淝河是巢湖的主要入湖河流之一,全长约70 km,流域总面积约1 464 km2,河流的中、 上游位于合肥市城区内. 作为南淝河主要支流的二十埠河,发源于长丰县三十头乡南部,全长27.0 km,流域面积136 km2,汇水区主要位于合肥市北部至东部方向的郊外及城郊结合部. 本研究在二十埠河位于合肥东北部城郊的磨店乡境内,筛选一个具有明显多水塘-支渠系统特征的农田溪流为对象,开展溪流水系统沉积物的磷形态分析及释放风险评估. 溪流水系统的大致构成情况,见图 1.

|
图 1 研究区农田溪流水系统示意 Fig. 1 Sketch map of agricultural headwater stream system in the study area |
所选溪流干流总长约7.0 km,流域中、 上游主要用地类型为耕地和林地,且在汇水区两侧边缘岗坡上分布多个小村庄及2所高校; 下游地区,特别是靠近与二十埠河交汇处附近地区,已为合肥市城市建设用地. 根据溪流水系统的基本构造形态和河床结构特征,笼统地将溪流水系统划分为水塘、 支流、 干流等3个类型. 鉴于干流上分布大量深潭,且深潭水动力学特性与一般渠段存在较大的差异,为此考虑将干流进一步区分为一般干流渠段和深潭两种模式,即按照水塘、 支流、 干流和深潭等4种典型溪流构成模式,解析溪流水系统沉积物磷形态及污染特征.
1.2 溪流水质状况实地调查发现,在桥梁Ⅱ下方约10 m处,有较为明显的高校生活污水和少量食品加工业废水排入,导致溪流水质在感官上明显较桥梁Ⅱ上方水体差些. 鉴于桥梁Ⅱ上、 下方溪流水质差异明显,为便于表述,不妨以桥梁Ⅱ为界,将整个溪流水系统简单地划分为上、 下游. 2015年3-6月在干流上安排19个水质采样点(其中上游7个、 下游12个),逐月采集水样,得到水质指标的统计结果,见表 1.
|
|
表 1 溪流水质理化指标 Table 1 Physicochemical index for surface water quality of the studied headwater stream |
根据农田溪流水系统的基本形态和构造特征,考虑在汇水区内水塘、 支流、 干流及干流深潭等4种溪流基本构成模式上,分别筛选出17、 16、 14和13个采样点位,并以GPS定位,分别于2014年10月和2015年4月,分两次在相同坐标点周边1 m2范围内采集表层沉积物样. 实验室自然风干后,剔除枯枝碎叶,研磨后过100目尼龙筛,装入贴有标签的自封袋备用.
2.2 样品的分析测定总磷(TP)和无机磷(IP)采用欧洲标准测试委员会框架下发展的SMT法测定. 易交换态磷(Ex-P)、 铁铝结合态磷(Fe/Al-P)及碎屑磷(Ca-P)采用三步连续提取方法[17]分析测定. 每提取一次,将离心管放入离心机中以4 000 r ·min-1的转速离心20 min,取上清液,采用钼锑抗分光光度法测定磷含量. 除最后一步提取外,前两步提取所得残渣均使用去离子水清洗两次,再进行下一步的提取. 沉积物中有机质(OM)含量采用灼烧法测定,pH值采用笔式pH计测定(水土比5 ∶1).
2.3 沉积物磷吸附指数的确定对于每个沉积物样,分别称取4份1.000 g 干样于50 mL聚乙烯离心管中,其中1个离心管加入20 mL 0.01 mol ·L-1 CaCl2溶液,作为1个空白,其余3个离心管分别加入 20 mL 75mg ·L-1的KH2PO4溶液(配制在0.01mol ·L-1 CaCl2中)作为3个平行试验,并分别加入2 滴氯仿以抑制微生物活动. 20℃下振荡24 h后,放入4 000 r ·min-1转速的离心机离心20 min,再以0.45 μm孔径的滤膜进行过滤. 滤液中磷浓度以钼锑抗比色法测定,由初始浓度与滤液中磷浓度的差值,计算1.000 g 沉积物吸附磷的量[18]. 然后,再按下式计算吸附指数PSI:
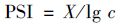
采样SPSS 18.0和Excel统计软件,开展数据分析和相应图形的绘制.
3 结果与分析 3.1 沉积物磷形态及其变化特征 3.1.1 沉积物磷形态含量整个溪流水系统沉积物的pH值变化范围为6.27-8.53,平均值为7.44; OM变化为1.83%-8.99%,平均值为4.79%. 沉积物中各形态磷含量的统计结果见表 2. 总的来看,支流和干流沉积物TP及各形态磷含量的时空变化性相对较小一些. 流域水系沉积物的TP含量变化范围为137.517-1 709.229 mg ·kg-1,均值为532.245 mg ·kg-1,这与国内一些农业源头区情况很相似. 如卫新锋等[19]在对河套灌区各级沟渠表层沉积物的调查中,得到绝大部分沟渠表层沉积物TP含量在600 mg ·kg-1左右,明显高于本研究的水塘和支流,而与干流和深潭含量大体相当. 李红芳等[15]在对农业小流域源头区12个池塘底泥磷含量的研究中,得到由农田改建的人工塘、 人为影响大的山边塘和人为影响小的山边塘TP含量平均值分别为700、 610和350 mg ·kg-1. 显然,本研究中水塘TP含量与人为影响小的山边塘相近,干流与人为影响大的山边塘相当,深潭则与农田改建的人工塘相同.
|
|
表 2溪流水系统沉积物各形态磷含量 Table 2 Statistical results of phosphorus fractions contents in the sediments |
由表 2可见,4种溪流构成模式中沉积物的TP含量由小到大的排序为:水塘<支流<干流<深潭. 这里,位于溪流干流的深潭TP相对较高,可能与深潭水面相对较宽、 水深相对较浅,使得溪流挟带泥沙容易沉降下来有很大的关系. 汇水区内水塘共计数十个,但大部分为近年新开挖的人工养鱼塘,水底沉积物较少. 从外观上看,有些水塘底泥甚至与当地土壤母质相差无几,这可能正是表 2中水塘沉积物磷含量偏低的主要原因. 为了解该流域土壤磷素含量背景水平,笔者曾在距离溪流较远的两处陆域岗坡上,各挖掘了1个直径约40 cm、 深度为60 cm的深坑,并在坑底3个不同方向各采集1份土样(共计6份),分析测得相应的TP、 Ex-P、 Fe/Al-P、 Ca-P和OP平均含量,分别为128.763、 6.324、 34.020、 10.034和48.038 mg ·kg-1. 表 2中水塘底部沉积物TP含量最低值为137.517 mg ·kg-1,与上述背景值十分接近. 显然,与一般河流、 湖泊相比,研究区的Ca-P含量处于相对较低水平,这可能与当地土壤母质构成有一定的关系. 事实上,刘洋等[20]在距离本研究区不远的巢湖北岸六叉河农业小流域多个水塘沉积物磷形态分析中,也得到了较低水平的Ca-P含量,相应的田塘、 旱塘、 山塘、 村塘和河塘的钙镁结合态磷(Ca/Mg-P)平均含量分别为8.6、 9.1、 35.7、 39.5和70.1 mg ·kg-1,水塘沉积物TP含量介于286.3-651.3 mg ·kg-1之间. 刘成等[21]在靠近合肥方向的巢湖西半湖北侧重污染汇流湾区沉积物磷形态分析中,得到Ca-P含量为8.2-65.8 mg ·kg-1.
Ex-P是可以被水生植物直接利用的磷形态,是造成水体富营养化的重要磷素. 总体上,深潭Ex-P含量较高,水塘最低. 整个溪流水系统中Ex-P变异系数明显偏大,表明Ex-P有着较显著的时空差异性. 由表 2可见,Fe/Al-P含量高低排序为:深潭>干流>支流>水塘. 4种溪流构成模式的Fe/Al-P含量都高于Ex-P、 Ca-P,其变异系数相对稳定.
总体上,溪流沉积物中的磷素以无机磷IP为主,平均占TP含量的63.53%-72.43%. 各形态磷含量高低排序为:IP>OP>Fe/Al-P>Ca-P>Ex-P,且在空间分布上,各种磷形态含量基本都表现出相似的变化特征,即深潭>干流>支流>水塘. 这里,水塘与支流的OP含量明显低于深潭和干流. 整个溪流水系统沉积物的OP含量平均值仅为95.172-255.966 mg ·kg-1,显著低于巢湖周围池塘的平均水平(414.480 mg ·kg-1)[22]. 根据实地调查,OP含量最低点出现在上游源头人为活动影响较小的新开挖水塘,最大值则出现在溪流与二十埠河交汇处上游不远处的深潭中. 调查发现,该深潭靠近合肥城区,且在深潭上方不远处有一处较为明显的生活污水和类似生活污水的食品加工废水排放口存在,时常有污水汇入,这可能正是该点位包括OP在内的各形态磷含量明显偏高的主要原因.
3.1.2 磷形态空间分布特征总体上,不同水塘沉积物磷含量差异较大,其中Ex-P、 Fe/Al-P、 OP和TP都表现出下游平均含量高于上游,而Ca-P则为上游偏高. TP最高含量(917.233 mg ·kg-1)出现在下游一个底泥发黑发臭的废弃小型水塘中,相应的Ex-P、 Fe/Al-P、 Ca-P和OP含量分别为9.529、 158.683、 178.106和399.219 mg ·kg-1; TP含量最低值(137.517 mg ·kg-1)出现在上游新开挖水塘,其Ex-P、 Fe/Al-P、 Ca-P和OP含量分别为1.090、 19.708、 4.964和26.665 mg ·kg-1.
支流中,上、 下游的Ex-P和OP含量相当,Fe/Al-P和TP含量则是下游高于上游,而Ca-P含量则表现为下游低于上游. TP最高含量(852.768 mg ·kg-1)出现在下游左侧一个较大支流上,相应的Ex-P、 Fe/Al-P、 Ca-P和OP含量分别为2.095、 18.033、 30.759和97.827 mg ·kg-1. TP含量最低的采样点位于上游源头处左侧小支流上,该支流虽然两侧都是农田、 菜地,但由于地形坡度稍大,使得农田、 菜地径流携带的磷素直接进入干流,而在支流中沉积较少. 该采样点Ex-P、 Fe/Al-P、 Ca-P、 OP和TP含量分别为2.296、 28.080、 46.498、 96.990和241.888 mg ·kg-1.
干流沉积物中,除Ca-P以外,其余各形态磷都表现为上游平均含量低于下游,这与表 1的溪流水质状况相一致. 可能是受到生活污水的影响,TP含量最大值(1 030.814 mg ·kg-1)出现在上游河段一个离村落较近的采样点,其Ex-P、 Fe/Al-P、 Ca-P和OP含量分别为11.461、 53.835、 117.278和260.738 mg ·kg-1.
相比较而言,在干流大小不一的深潭中,各形态磷含量在上、 下游空间分布的差异性最大,上、 下游TP平均值分别为618.590 mg ·kg-1和826.931 mg ·kg-1,TP含量最大值(1 709.229 mg ·kg-1)出现在下游与二十埠河交汇处上方的深潭中,这也是整个溪流水系统中TP含量最高的点位.
3.1.3 不同季节磷形态变化特征由于Ex-P、 Fe/Al-P和OP可以直接或间接地被水生植物吸收利用,因此往往成为水环境保护和水污染控制中颇受关注的磷素指标. 图 2展示了2014年秋季和2015年春季,4种溪流构成模式中Ex-P、 Fe/Al-P、 OP和TP含量变化情况. 可以看出,Ex-P和TP的春季含量都较对应的秋季高些,Fe/Al-P和OP都仅在支流中出现春季高于秋季.

|
图 2 Ex-P、 Fe/Al-P、 OP和TP的季节变化 Fig. 2 Seasonal variations of Ex-P,Fe/Al-P,OP and TP contents in sediments |
深潭中,无论是春季还是秋季,13个采样点位之间Ex-P含量差异均最为显著. 这除了与溪流上、 下游氮磷污染来源不同有关外,深潭中水生植物生长情况的差异性可能也是不容忽视的因素. Fe/Al-P常作为指示沉积物质量的重要指标之一. 活泼的铁氧化物对磷的快速吸附和释放控制着孔隙水中PO43-的浓度,从而直接影响沉积物-水界面磷的交换. 总体上,干流和深潭的沉积物Fe/Al-P含量表现为秋季高于春季、 水塘则是秋季略高于春季,这除了与水生植物的吸收利用影响有关外,还可能缘于春季时水温相对较高,沉积物中微生物活性相对较强,促进了生物扰动和矿化作用,导致水体耗氧增多,从而促使沉积物中 Fe/Al-P 的释放[23].
加拿大安大略省环境和能源部根据沉积物中污染物对于底栖生物的生态毒性效应,制定了环境质量评价标准,即将TP=600 mg ·kg-1作为沉积物已受污染,但多数底栖生物可以承受的最低等级阈值; 将TP=2 000 mg ·kg-1作为底栖生物群落遭受明显损害的严重级别标准[24]. 根据该标准可以判定,深潭在春季和秋季、 干流仅在春季达到最低污染等级,水塘和支流沉积物则均没有达到污染程度. 而根据文献[25]的沉积物污染等级划分标准,即TP>1 300 mg ·kg-1,重污染水平; 500 mg ·kg-1<TP<1 300 mg ·kg-1,中等污染水平; TP<500 mg ·kg-1,轻污染水平. 由图 2可以判定,水塘沉积物处于轻度污染,支流、 干流和深潭在春季时均处于中等污染水平,而秋季时则仅有干流和深潭达到中等污染程度.
当然,这里有关沉积物的磷形态及其变化性,还仅是基于2014年秋季和2015年春季两次采样获得的分析结果,由于采样次数不多,加之未能考虑其他季节的影响,因此可能还不足以真实反映溪流水系统沉积物的磷素变化规律.
3.2 生物有效性磷的变化特征底泥的生物有效性磷主要指底泥中可释放并能在一定条件下被水生植物吸收利用的潜在活性磷,一般包括Ex-P和Fe/Al-P. 实际上,有机磷可以经过磷酸酶水解、 细菌降解或光解等作用后转化成生物有效性磷,从而维持浮游生物的生长[26]. 因此,往往将Ex-P、 Fe/Al-P和OP称为广义生物有效性磷. 不同季节下,水塘、 支流、 干流及干流深潭中沉积物的生物有效性磷及其占TP百分比情况,见表 3.
|
|
表 3 生物有效性磷含量及占TP百分比 Table 3 Bio-available phosphorus contents and its proportion in TP |
可以看出,溪流水系统沉积物的生物有效性磷占TP比重约13.64%-22.18%,明显高于乌梁素海(2%-7%)[27],但低于湖北喻家湖(29.77%-35.06%)[28],显著低于重污染的巢湖十五里河表层沉积物(50.18%)[29]. 溪流水系统沉积物的广义有效磷占TP比重41.72%-64.26%,高于南四湖(19.91%-60.35%)[30]和黄河口临近海域表层沉积物(9.10%-17.51%)[31],表明该溪流沉积物中潜在的磷可释放性较大. 总的来看,秋季时干流和深潭的生物有效性磷、 广义有效性磷占TP比重高于春季,而支流和水塘沉积物则春、 秋季基本相当. 无论是生物有效性磷,还是广义生物有效性磷,在含量大小方面都表现出如下特点,即深潭>干流>支流>水塘.
3.3 溪流水系统的聚类与方差分析 3.3.1 聚类分析根据春、 秋两季沉积物各形态磷含量数据信息,对水塘、 支流、 干流和深潭等4种溪流主要构成模式,开展相似程度的聚类分析(CA),结果见图 3. 可以看出,2014年秋季和2015年春季,4种溪流构成形式产生了两种明显不同的聚类结果. 即,2014年秋季各形态磷含量相对较高的干流和深潭归为了一类,含量相对较低的支流和水塘归为另一类,而且两类之间界线清晰; 2015年春季,可能由于农业活动的增强,特别是作物施肥,以及降雨量增多,使得田间支流沉积物中各形态磷含量增加,于是出现水塘单独归为一类,而干流、 深潭和支流归为另一类的结果. 尽管如此,2015年春季各形态磷含量相对较高的干流和深潭依旧明显归属于同一个子类.

|
图 3 溪流水系统聚类结果 Fig. 3 Results of clustering among different stream styles |
上述聚类结果表明,作为直接接纳汇流区非点源污染负荷的代表性田间水系统,毛沟、 农沟等支流沉积物的磷形态及其含量的季节动态变化性明显强于水塘、 干流和深潭. 据调查,由于汇流区中下游大部分水塘都为近两年新开挖的养鱼塘,水体相对较为封闭,一般不直接接纳周边非点源径流的汇入. 虽然有时需要利用溪水的补给,但为防止鱼群脱逃,补水工作一般都安排在非降雨期间,这就使得水塘沉积物磷形态及其含量未出现明显的季节性波动.
3.3.2 方差分析虽然聚类分析从综合分析层面获得了水塘、 支流、 干流和深潭等的聚簇集合,但无法揭示不同溪流构成形式之间差异明显的具体指标. 方差分析(ANOVA)是用于两个及两个以上样本均数差别的显著性检验. 不妨选择Ex-P、 Fe/Al-P、 Ca-P、 OP、 IP、 TP、 pH和OM作为因素变量,并以各指标均值作为水平,利用最小显著性差异法(LSD法)对溪流水系统开展差异性分析,从而识别不同溪流形态之间差异性较为明显的指标类型,结果见表 4.
由表 4可见,2014年秋季和2015年春季,4种溪流构成形式之间差异性指标大不相同. 2014年秋季,干流与水塘、 支流之间,以及深潭与水塘、 支流之间差异性指标偏多,而干流与深潭之间仅在OM方面有所不同. 2015年春季,深潭与水塘之间差异明显的指标有5个,与支流仅在OP方面存在明显差异性; 干流、 支流与水塘之间都是在少部分指标上差异明显,支流与干流则仅在pH方面存在明显的差异性. 显然,上述结果与聚类分析结论是一致的.
|
|
表 4 溪流水系统4种构成模式的方差分析 Table 4 Results of the ANOVA analysis on the 4 stream styles |
目前,磷吸附指数PSI常用于描述沉积物对于磷的固定或吸附能力. 其中,PSI值越小,表示沉积物对磷的固定能力越弱,即磷素向上覆水释放的风险程度越高; PSI值越大,则表示沉积物对磷的固定能力越强,磷素向上覆水释放的风险越低. 本研究区溪流水系统不同构成形式的沉积物PSI及其变化情况见图 4.

|
图 4 各采样点 PSI变化特征 Fig. 4 Changes of PSI corresponding to each stream style |
从图 4可知,水塘、 支流、 干流和深潭在相同季节下的PSI值颇为接近,意味着溪流水系统沉积物的磷释放风险相差不大. 由秋季时溪流水系统沉积物的PSI显著高于春季,表明2015年春季沉积物对于磷的固定能力相对弱一些,也就是沉积物磷素向上覆水释放的风险程度更高. 究其原因,笔者以为这可能是因为春季(4月)水温较秋季(10月)稍高,水底微生物活性较强,生物化学反应相对较为活跃,使得沉积物中磷素经由间隙水向上覆水体释放的可能性增大,导致春季磷释放风险提高.
溪流水系统PSI的变化范围为26.47-69.88(mg ·L-1) ·(100 g ·μmol)-1,其中2014年秋季和2015年春季PSI平均值分别为59.98(mg ·L-1) ·(100 g ·μmol)-1和34.56 (mg ·L-1) ·(100 g ·μmol)-1,甚至低于部分湖泊水体. 如黄清辉等[32]得到太湖沉积物 PSI 平均值为54.7(mg ·L-1) ·(100 g ·μmol)-1; 卢少勇等[18]在对北京市6个城市湖泊表层沉积物的研究中,得到PSI变化范围及其平均值,分别为14.9-83.3 (mg ·L-1) ·(100 g ·μmol)-1、 34.5(mg ·L-1) ·(100 g ·μmol)-1; 于淑玲等[33]得到的小兴凯湖表层沉积物PSI变化范围为9.78-197.53(mg ·L-1) ·(100 g ·μmol)-1,平均值高达59.77(mg ·L-1) ·(100 g ·μmol)-1. 换言之,2015年春季该溪流水系统沉积物的磷释放风险较高,甚至高于一些富营养化湖泊水体. 水体沉积物磷的潜在释放风险往往取决于两个方面,一是沉积物本身的吸附能力强,含有较高的可释放磷素; 二是沉积物本身的磷吸附能力不强,不利于吸附,因而释放风险较大. 本研究中溪流水系统沉积物的磷素含量普遍不高,计算得到的沉积物PSI值也略偏低,意味着沉积物对磷的缓冲能力不强,也就是沉积物的磷吸附能力偏弱,磷素易释放进入水体. 毫无疑问,对于河流水系较为发达,并且农业生产用地占绝大多数的巢湖流域而言,这种相对较低的沉积物磷吸附能力对于地处下游的巢湖水环境保护和富营养化控制,显然是不利的.
3.4.2 磷吸附指数PSI的影响因素表 5展示了PSI与各形态磷及OM、 pH的相关关系. 不难看出,PSI与Ex-P、 pH均呈极显著负相关关系,而与IP呈显著负相关性. 也就是,Ex-P、 IP含量越高或pH越大,PSI越小,即沉积物向上覆水释放磷的风险越高. 众所周知,沉积物中较高的Ex-P、 IP含量,将会增大沉积物与上覆水的浓度梯度,从而促使沉积物中相关磷的释放,Ex-P、 IP与PSI表现出的负相关性,正好反映这种潜在的相互作用关系. 而就pH的影响来看,碱性环境条件下沉积物对于PO43-的可吸附点位数目减少,从而导致磷素由沉积物向上覆水释放的可能性增大. 故此,Ex-P、 IP、 pH是溪流水系统沉积物吸附磷的主要影响因素.
|
|
表 5 沉积物各指标的相关性分析 Table 5 Correlation analysis among the indexes of the sediments |
这里,pH与Ex-P呈极显著正相关,而与Fe/Al-P呈现极显著负相关,表明pH对Ex-P、 Fe/Al-P存在截然相反的作用关系,从而增强了PSI变化的复杂性. 有研究表明,有机质分解过程中形成的有机胶体(即腐殖质)可以形成一种胶膜,覆盖在黏粒矿物、 氧化铁、 铝以及碳酸钙等无机物的表面,从而减弱无机物对于磷的固定[34],而且有机质中富里酸聚阴离子与磷酸盐阴离子还可能产生吸附竞争,促进磷的释放[35]. 不仅如此,腐殖质还可能和铁、 铝等形成有机无机复合体,进而为无机磷提供吸附位点,从而增强对磷的吸附[36]. 但也有研究表明,沉积物中有机质的分解将会消耗大量的溶解氧,这一过程将促使沉积物中Fe/Al-P向孔隙水释放PO43-[37]. 这种看似截然相反的作用效果,无疑增大了OM与PSI相互关系的复杂性.
4 结论(1)整个溪流水系统沉积物的TP含量变化范围为137.517-1 709.229 mg ·kg-1,平均值为532.245 mg ·kg-1. 其中,4种构成模式中的IP平均含量为237.273-445.912 mg ·kg-1,约占TP的63.53%-72.43%,整个溪流沉积物的各形态磷含量高低排序为:IP>OP>Fe/Al-P>Ca-P>Ex-P.
(2)溪流水系统沉积物的各形态磷含量表现出相同的变化趋势,即深潭>干流>支流>水塘. 在溪流的4种构成模式中,Ex-P和TP的春季含量都高于秋季,而Fe/Al-P和OP都仅在支流中出现春季高于秋季.
(3)溪流水系统沉积物的生物有效性磷占TP比重约13.64%-22.18%,在含量大小方面都表现出相同的变化特征,即深潭>干流>支流>水塘.
(4)统计分析表明,2014年秋季和2015年春季,溪流水系统的4种构成模式表现出两种明显不同的聚类结果,而且彼此之间差异性指标也大不相同.
(5)水塘、 支流、 干流和深潭在相同季节下的PSI值颇为接近,且都表现出春季明显低于秋季的变化特征,表明春季沉积物中磷素向上覆水释放的风险程度更高; 根据相关分析,得出Ex-P、 IP、 pH是溪流水系统沉积物吸附磷的主要影响因素.
| [1] | 马健荣, 邓建明, 秦伯强, 等. 湖泊蓝藻水华发生机理研究进展[J]. 生态学报, 2013, 33 (10): 3020-3030. |
| [2] | 郭茹, 杨京平, 梁新强, 等. 太湖苕溪流域氮磷的生物学阈值评估[J]. 环境科学学报, 2013, 33 (10): 2756-2765. |
| [3] | Alexander R B, Smith R A, Schwarz G E. Effect of stream channel size on the delivery of nitrogen to the Gulf of Mexico[J]. Nature, 2000, 403 : 758-761. |
| [4] | Peterson B J, Wollheim W M, Mulholland P J, et al. Control of nitrogen export from watershed by headwater streams[J]. Science, 2001, 292 (5514): 86-90. |
| [5] | Sugiyama S, Hama T. Effects of water temperature on phosphate adsorption onto sediments in an agricultural drainage canal in a paddy-field district[J]. Ecological Engineering, 2013, 61 : 94-99. |
| [6] | Madison A M, Ruark M D, Stuntebeck T D, et al. Characterizing phosphorus dynamics in tile-drained agricultural fields of eastern Wisconsin[J]. Journal of Hydrology, 2014, 519 : 892-901. |
| [7] | 李如忠, 杨继伟, 钱靖, 等. 合肥城郊典型源头溪流不同渠道形态的氮磷滞留特征[J]. 环境科学, 2014, 35 (9): 3365-3372. |
| [8] | Cooper R J, Rawlins B G, Krueger T, et al. Contrasting controls on the phosphorus concentration of suspended particulate matter under baseflow and storm event conditions in agricultural headwater streams[J]. Science of the Total Environment, 2015, 533 : 49-59. |
| [9] | Baken S, Verbeeck M, Verheyen D, et al. Phosphorus losses from agricultural land to natural waters are reduced by immobilization in iron-rich sediments of drainage ditches[J]. Water Research, 2015, 71 : 160-170. |
| [10] | Kröger R, Moore M T. Phosphorus dynamics within agricultural drainage ditches in the lower Mississippi Alluvial Valley[J]. Ecological Engineering, 2011, 37 (11): 1905-1909. |
| [11] | 毛战坡, 王世岩, 周晓玲, 等. 六岔河流域多水塘-沟渠系统中土壤养分空间变异特征研究[J]. 水利学报, 2011, 42 (4): 425-430. |
| [12] | 单保庆, 李楠, 唐文忠. 江淮农村生态型排水系统构建及截污作用研究[J]. 环境科学, 2012, 33 (11): 3797-3803. |
| [13] | 李如忠, 董玉红, 钱靖. 基于TASCC的典型农田溪流氨氮滞留及吸收动力学模拟[J]. 中国环境科学, 2015, 35 (5): 1502-1510. |
| [14] | 付强, 尹澄清, 马允. 源头农业区不同类型水塘中水体沉积物磷吸附容量[J]. 环境科学, 2005, 26 (4): 70-76. |
| [15] | 李红芳, 刘锋, 杨凤飞, 等. 农业小流域源头区池塘底泥磷形态和吸附特征[J]. 生态与农村环境学报, 2014, 30 (5): 634-639. |
| [16] | Nguyen L, Sukias J. Phosphorus fractions and retention in drainage ditch sediments receiving surface runoff and subsurface drainage from agricultural catchments in the North Island, New Zealand[J]. Agriculture, Ecosystems and Environment, 2002, 92 (1): 49-69. |
| [17] | 朱广伟, 秦伯强. 沉积物中磷形态的化学连续提取法应用研究[J]. 农业环境科学学报, 2003, 22 (3): 349-352. |
| [18] | 卢少勇, 王佩, 王殿武, 等. 北京六湖泊表层底泥磷吸附容量及潜在释放风险[J]. 中国环境科学, 2011, 31 (11): 1836-1841. |
| [19] | 卫新锋, 欧阳威, 郝芳华, 等. 河套灌区沟渠表层沉积物对磷的吸附[J]. 农业工程学报, 2010, 26 (9): 94-100. |
| [20] | 刘洋, 付强, 陆海明, 等. 农业流域中不同类型水塘沉积物磷素状态及其环境意义[J]. 环境化学, 2013, 32 (12): 2307-2314. |
| [21] | 刘成, 邵世光, 范成新, 等. 巢湖重污染汇流湾区沉积物营养盐分布与释放风险[J]. 环境科学研究, 2014, 27 (11): 1258-1264. |
| [22] | 马秀玲, 孙庆业, 伍红琳, 等. 巢湖周围池塘沉积物中磷的赋存形态及空间差异[J]. 安徽农业科学, 2010, 38 (2): 1075-1078. |
| [23] | 苏玉萍, 林佳, 林婉珍, 等. 亚热带深水库沉积物-水界面磷释放受控因子的研究[J]. 农业环境科学学报, 2008, 27 (4): 1465-1470. |
| [24] | 李任伟. 沉积物污染和环境沉积学[J]. 地球科学进展, 1998, 13 (4): 398-402. |
| [25] | Wang S R, Jin X C, Zhao H C, et al. Phosphorus fractions and its release in the sediments from the shallow lakes in the middle and lower reaches of Yangtze River area in China[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2006, 273 (1-3): 109-116. |
| [26] | Baldwin D S, Beattie J K, Coleman L M, et al. Hydrolysis of an organophosphate ester by manganese dioxide[J]. Environmental Science & Technology, 2001, 35 (4): 713-716. |
| [27] | 吕昌伟, 何江, 孙惠民, 等. 乌梁素海沉积物中磷的形态分布特征[J]. 农业环境科学学报, 2007, 26 (3): 878-885. |
| [28] | 鲁群, 李秀, 李湘梅. 湖泊底泥中磷形态及分布特征研究[J]. 环境工程, 2014, 32 (4): 135-139. |
| [29] | 李如忠, 李峰, 周爱佳, 等. 巢湖十五里河沉积物氮磷形态分布及生物有效性[J]. 环境科学, 2012, 33 (5): 1503-1510. |
| [30] | An W C, Li X M. Phosphate adsorption characteristics at the sediment-water interface and phosphorus fractions in Nansi Lake, China, and its main inflow rivers[J]. Environmental Monitoring and Assessment, 2009, 148 (1-4): 173-184. |
| [31] | 李悦, 乌大年, 薛永先. 沉积物中不同形态磷提取方法的改进及其环境地球化学意义[J]. 海洋环境科学, 1998, 17 (1): 15-20. |
| [32] | 黄清辉, 王子健, 王东红, 等. 太湖表层沉积物磷的吸附容量及其释放风险评估[J]. 湖泊科学, 2004, 16 (2): 97-104. |
| [33] | 于淑玲, 李晓宇, 张继涛, 等.小兴凯湖表层底泥磷吸附容量及潜在释放风险[J]. 中国环境科学, 2014, 34 (8): 2078-2085. |
| [34] | 赵海超, 王圣瑞, 张莉, 等. 有机质含量及其组分对洱海沉积物磷吸附-释放影响[J]. 环境科学学报, 2014, 34 (9): 2346-2354. |
| [35] | Kastelan-Macan M, Petrovic M. The role of fulvic acids in phosphorus sorption and release from mineral particles[J]. Water Science and Technology, 1996, 34 (7-8): 259-265. |
| [36] | Gerke J, Hermann R. Adsorption of orthophosphate to humic-Fe-complexes and to amorphous Fe-oxide[J]. Zeitschrift für Pflanzenernãhrung und Bodenkunde, 1992, 155 (3): 233-236. |
| [37] | Spears B M, Carvalho L, Perkins R, et al. Sediment phosphorus cycling in a large shallow lake: spatio-temporal variation in phosphorus pools and release[J]. Hydrobiologia, 2007, 584 (1): 37-48. |
 2016, Vol. 37
2016, Vol. 37


