地表水体富营养化是当前我国所面临的最为严重的水环境问题之一[1]. 磷被认为是造成地表水体富营养化的关键限制性因子之一[2, 3, 4]. 地表水体中磷来源包括外源输入和内源释放[3]. 进入地表水体的外源磷可以沉积于底泥中; 当外界环境条件发生改变时,原先沉积于底泥中的磷可以被重新释放出来,成为地表水体中磷的内源[2, 3, 4]. 特别是,当外源磷输入得到控制之后,底泥磷释放会成为地表水体中磷的重要来源[3]. 因此,控制底泥磷释放对于地表水体富营养化防治而言是非常重要的.
污染底泥磷释放控制技术主要分为异位控制技术和原位控制技术这2大类[5, 6, 7, 8, 9]. 与异位控制技术相比,原位控制技术成本较低,可避免底泥疏浚过程中底泥再悬浮引起大量磷向上覆水体的释放,可避免疏浚底泥输送过程和处理过程中的二次污染问题,无需要额外的场地,亦无需疏浚底泥的处置设施或设备[5]. 目前,原位控制技术已经受到了人们的广泛关注并成为底泥磷释放控制技术研究的热点[5, 6, 7, 8, 9].
底泥磷释放原位控制技术主要包括硝酸盐原位处理[10]、 铝盐钝化[11]、 原位物理覆盖[12]、 底层水人工供氧[13, 14]和吸附剂原位钝化技术[15, 16, 17, 18, 19, 20, 21, 22, 23]等. 其中,底泥吸附剂原位钝化技术,即通过向底泥添加吸附剂以增强底泥对磷的固定能力并降低底泥中磷向上覆水体迁移的风险,或将吸附剂放置于底泥-水界面上方以降低底泥中磷向上覆水体迁移的风险,是一种极具应用前景的底泥磷释放原位控制技术[15, 16, 17, 18, 19, 20, 21, 22, 23].
应用吸附剂原位钝化技术控制水体底泥磷释放的一个关键问题是寻找合适的吸附剂材料作为底泥钝化剂. 目前,国内外的研究人员已经考察了给水处理厂废弃污泥(WTRs)[15, 16, 17]、 镧改性黏土(Phoslock®)[18, 19]、 镧改性沸石[20]、 铝改性沸石[21]、 纳米二氧化钛膜负载多孔性陶瓷滤料[22]和海泡石[23]等吸附剂材料作为钝化剂对底泥磷释放的控制效果. 为推动底泥吸附剂原位钝化技术的发展,进一步研究开发新的钝化剂仍然是非常必要的.
锆氧化物或氢氧化物是一种化学性质稳定、 无毒且不溶于水的无机固体材料,它对水中的磷酸盐具备很强的亲和力[24, 25, 26]. 将锆氧化物或氢氧化物作为钝化剂预计可以有效控制底泥磷的释放. 但由于锆氧化物或氢氧化物价格相对较高,应用其作为钝化剂控制底泥磷释放的成本预计较高. 为降低成本,将锆氧化物或氢氧化物负载到价格低廉的多孔性固体材料上是非常必要的.
高岭土是由硅氧四面体和铝氧八面体组成的层状铝硅酸盐矿物[27, 28, 29]. 高岭土来源广泛、 价格低廉、 对环境无污染且具备较大的比表面积[27, 28, 29],适合作为锆氧化物或氢氧化物的载体. 如果将锆氧化物或氢氧化物负载到高岭土上,所制备得到的锆改性高岭土预计是一种安全、 高效且相对经济的底泥钝化剂. 目前国内外关于利用锆改性高岭土原位改良技术(即将锆改性高岭土直接添加到底泥中)控制底泥磷释放的研究尚鲜见报道. 为此,本研究通过实验考察了锆改性高岭土对水中磷酸盐的吸附性能,分析了吸附磷酸盐后锆改性高岭土的磷形态分布特征,探讨了厌氧条件下锆改性高岭土原位改良技术对重污染河道底泥磷释放通量的削减效果,并考察了锆改性高岭土添加对底泥吸附水中磷酸盐的影响,以期为应用锆改性高岭土原位改良技术控制重污染河道底泥磷释放提供理论依据和技术支撑.
1 材料与方法 1.1 实验材料与方法实验所用高岭土购自中国国药集团化学试剂有限公司,CAS编号: 1332-58-7. 采用彼得森抓斗式底泥采样器从上海市金山工业区红光村一条重污染河道采集表层底泥作为实验用泥. 底泥的pH和有机质含量采用土壤理化性质标准分析方法进行测定[30]. 采用文献[31]的方法对底泥中各种形态无机磷含量进行分析,该方法将底泥中的无机磷分为弱吸附态磷(NH4Cl-P)、 氧化还原敏感态磷(BD-P)、 金属氧化物结合态磷(NaOH-P)和钙结合态磷(HCl-P)等4种形态,分别采用1 mol ·L-1 NH4Cl、 0.11 mol ·L-1 Na2S2O4/0.11 mol ·L-1 NaHCO3、 1 mol ·L-1 NaOH和0.5 mol ·L-1 HCl溶液进行提取. 采用文献[32]的方法对底泥中残渣态磷(Res-P)含量进行分析. 供试底泥的理化性质见表 1. 底泥磷释放控制模拟实验所用的上覆水采自上海市一条干净河道,该河道河水的理化性质采用文献[33]推荐的方法进行测定,结果见表 2. 实验所用的氧氯化锆(ZrOCl2 ·8H2O)、 NaOH、 HCl和KH2PO4 等化学试剂均为分析纯,均购自中国国药集团化学试剂有限公司.
| 表 1 底泥磷释放控制模拟实验所用底泥的理化性质
Table 1 Physical and chemical properties of sediments used in microcosm incubation experiments
|
| 表 2 底泥磷释放控制模拟实验所用上覆水的理化性质
Table 2 Physical and chemical properties of overlying water used in microcosm incubation experiments
|
分别称取10 g高岭土置于5个锥形瓶中,再分别向上述锥形瓶中加入1、 2、 3、 4和5 g ZrOCl2 ·8H2O,再向每个锥形瓶中加入200 mL的去离子水. 采用磁力搅拌器搅拌30 min,使氧氯化锆得到充分溶解,并且使高岭土处于悬浮状态. 采用2 mol ·L-1的氢氧化钠溶液调节混合液的pH值至10. 将锥形瓶密封后置于20℃恒温空气振荡器中以150 r ·min-1的速度振荡20 h. 反应完成后分离固液混合物,并用去离子水清洗固体材料,直到清洗液的pH值为7左右,再将固体置于60℃的烘箱内烘干,最后将固体取出、 破碎、 研磨后即得到锆改性高岭土.
1.2.2 不同沉淀pH值条件下锆改性高岭土的制备分别称取10 g高岭土置于5个锥形瓶中,再分别称取5 g ZrOCl2 ·8H2O加入到上述锥形瓶中,再向每个锥形瓶中加入200 mL的去离子水. 采用磁力搅拌器搅拌30 min,使氧氯化锆得到充分溶解,并且使高岭土处于悬浮状态. 采用2 mol ·L-1的氢氧化钠溶液将上述锥形瓶中混合液的pH值分别调节至8、 9、 10、 11和12. 后续实验步骤同1.2.1节.
1.2.3 锆改性高岭土表征采用美国伊达克斯有限公司生产的型号为Genesis的X射线能量分散谱仪(EDAX)对高岭土和锆改性高岭土(制备时ZrOCl2·8H2O和高岭土质量比为0.5 ∶1、 沉淀pH值为10)表面的化学成分进行测定.
1.3 锆改性高岭土对水中磷酸盐的吸附实验通过批量吸附实验考察锆改性高岭土对水中磷酸盐的吸附性能. 实验步骤为: 采用KH2PO4和去离子水配制磷酸盐溶液,并用0.1 mol ·L-1 的HCl 和0.1 mol ·L-1 的NaOH 溶液将磷酸盐溶液的pH 值调节至7; 称取25 mg锆改性高岭土置于锥形瓶中,再移取50 mL磷酸盐溶液加入到锥形瓶中,密封后置于20℃、 转速为150 r ·min-1的恒温振荡器中振荡; 24 h后将锥形瓶中的固液混合物进行分离,最后用钼锑钪分光光度法测定上清液中磷酸盐的残留浓度. 锆改性高岭土对水中磷酸盐的单位吸附量(qe,单位为mg ·g-1)通过以下公式进行计算:
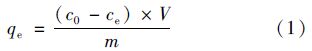
准确称取0.1 g锆改性高岭土置于离心管中,并加入25 mL磷酸盐溶液(初始磷酸盐质量浓度为100 mg ·L-1、 pH值为7),密封后置于转速为200 r ·min-1、 温度为20℃的恒温振荡器中. 反应24 h后,进行固液分离,再采用钼锑钪分光光度法测定上清液中磷酸盐的残留浓度. 离心管中的固体材料用去离子水清洗3遍后,采用文献[31]方法对它的NH4Cl-P、 BD-P、 NaOH-P和HCl-P含量进行分析,采用文献[32]方法对它的Res-P含量进行分析. 实验设置3组平行,NH4Cl-P、 BD-P、 NaOH-P和Res-P含量的标准偏差均小于5%,HCl-P含量的标准偏差小于10%.
1.5 底泥磷释放控制模拟实验采用1 L的棕色试剂瓶(直径10 cm)作为反应器进行底泥磷释放控制模拟实验. 称取200 g混合均匀的新鲜底泥置于棕色试剂瓶中,使底泥均匀铺设于瓶底. 对棕色试剂瓶中底泥采用以下3种方案进行处理: 方案①为底泥不进行任何处理,作为对照组; 方案②为将10 g高岭土加入底泥中,使高岭土和底泥混合均匀; 方案③为将10 g锆改性高岭土加入底泥中,使锆改性高岭土和底泥混合均匀(相当于向每m2底泥-水界面下底泥添加1 274 g锆改性高岭土). 将脱氧后的河水(采用亚硫酸钠进行脱氧)采用虹吸的方法加入到上述棕色试剂瓶,使上述棕色试剂瓶完全充满,加水过程中尽量避免扰动底泥使之出现上浮现象. 加水完成后将上述棕色试剂瓶密封培养. 每隔一定时间,从反应器中取出一定体积的上覆水,并测定上覆水中溶解氧(DO)浓度、 pH值和溶解性磷酸盐磷(SRP)浓度,同时向反应器中加入经过脱氧的河水直至反应器充满,密封后继续培养. 上覆水中的DO浓度采用溶氧仪进行测定,pH值采用梅特勒S20K精密pH 计进行测定,SRP浓度采用钼锑钪分光光度法进行测定. 模拟实验期间底泥磷释放通量采用以下公式进行计算[34]:
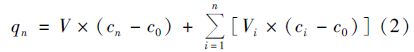

底泥磷释放控制模拟实验结束后取出各反应器中底泥,自然风干,研磨破碎,制备得到未改良底泥(没有掺杂锆改性高岭土)和改良底泥(掺杂了锆改性高岭土). 通过批量吸附实验考察了未改良和改良底泥对水中磷酸盐的吸附性能. 实验步骤为: 配制初始磷质量浓度(以P计)分别为0、 0.2、 0.3、 0.4、 0.5、 1、 2、 4、 6和8 mg ·L-1的磷酸盐溶液,并将它们的pH值调节至7; 量取25 mL磷酸盐溶液置于锥形瓶中,再称取0.1 g底泥加入到锥形瓶中,密封后置于25℃、 转速为150 r ·min-1的恒温振荡器中振荡; 24 h后将锥形瓶中的固液混合物进行分离,最后用钼锑钪分光光度法测定上清液中磷酸盐的残留浓度. 实验设置2组平行.
2 结果与讨论 2.1 锆改性高岭土表征采用EDAX仪对高岭土和锆改性高岭土(制备时ZrOCl2 ·8H2O和高岭土质量比为0.5 ∶1、 沉淀pH值为10)表面的化学成分进行分析,结果发现,高岭土表面的化学成分平均质量分数为: O(46.3%)、 Al(26.9%)和Si(26.9%); 锆改性高岭土表面的化学成分平均质量分数为: O(44.5%)、 Al(23.2%)、 Si(23.5%)和Zr(8.8%). 这证实了高岭土经锆改性后它的表面负载了锆氧化物.
2.2 锆改性高岭土对水中磷酸盐的吸附性能 2.2.1 锆负载量对锆改性高岭土吸附水中磷酸盐的影响图 1为锆负载量对改性高岭土吸附水中磷酸盐的影响. 从中可见,当溶液磷酸盐初始质量浓度(c0)为20 mg ·L-1(以PO43-计)、 溶液体积(V)为50 mL、 溶液pH值为7、 吸附剂投加浓度(质量浓度)为0.5 g ·L-1、 反应温度(T)为20℃、 反应时间(t)为24 h时,本研究所用的高岭土对水中磷酸盐的单位吸附量仅为0.46 mg ·g-1. 这说明本研究所用的高岭土对水中磷酸盐的吸附能力有限. 由图 1还可见,锆改性高岭土对水中磷酸盐的单位吸附量明显高于高岭土,并且其对水中磷酸盐的单位吸附量随锆负载量的增加而增加. 这说明锆改性可提高高岭土对水中磷酸盐的吸附能力,且吸附能力随锆负载量的增加而增加.
 | 图 1 锆负载量对改性高岭土吸附水中磷酸盐的影响
Fig. 1 Adsorption of phosphate from water on zirconium-modified
kaolin clay as a function of its zirconium loading amount
|
高岭土是由硅氧四面体和铝氧八面体组成的层状铝硅酸盐矿物,它的表面带负电荷[27, 28, 29]. 因此,高岭土很难通过静电吸引作用吸附去除水中带负电荷的磷酸盐阴离子. 锆改性高岭土对水中磷酸盐的吸附主要归功于改性高岭土中锆氧化物. 当溶液pH值为7时,水中磷酸盐主要以H2PO4-和HPO42-形式存在[36]. 锆氧化物表面存在以下反应[26]:
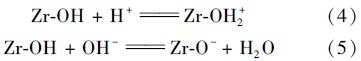
锆氧化物的零电荷点约为6.9[37]. 当溶液pH为 7时,锆氧化物表面带负电荷,此时锆氧化物表面的羟基与水中磷酸根阴离子之间的配位体交换反应是锆氧化物吸附水中磷酸盐起主要作用,详细的化学方程式见公式(6)和(7)[25, 26, 36]. 因此,锆改性高岭土吸附水中磷酸盐的机制主要是配位体交换作用. 当锆改性高岭土锆负载量增加时,锆改性高岭土中锆氧化物或氢氧化物表面的羟基数量增加,导致水中通过配位体交换作用被锆改性高岭土所吸附去除的磷酸盐越多.
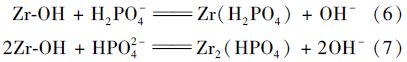
图 2为不同沉淀pH值条件下制备得到的锆改性高岭土对水中磷酸盐的吸附性能. 从中可见,当c0为20 mg ·L-1(以PO43-计)、 V为50 mL、 m/V为0.5 g ·L-1、 T为20℃和t为24 h时,锆改性高岭土对水中磷酸盐的吸附能力随沉淀pH值由8增加到10而急剧增加; 当沉淀pH由10值增加到11时,锆改性高岭土对水中磷酸盐的吸附能力保持不变; 当沉淀pH值由11增加到12时,锆改性高岭土对水中磷酸盐的吸附能力则明显下降. 图 2实验结果表明,用于除磷的锆改性高岭土的最佳沉淀pH值为10-11.
 | 图 2 不同沉淀pH值条件下制备得到的锆改性高岭土对水中磷酸盐的吸附
Fig. 2 Adsorption of phosphate from water on zirconium-modified
kaolin clay prepared under different precipitation pH values conditions
|
当沉淀pH值由8增加到10时,锆改性高岭土中锆氧化物或氢氧化物表面的羟基数量增加,从而有利于锆改性高岭土中锆氧化物或氢氧化物与水中磷酸盐之间发生配位体交换作用,进而导致锆改性高岭土对水中磷酸盐吸附能力的增加. 当沉淀pH值由11增加到12时,锆改性高岭土中锆氧化物或氢氧化物表面的羟基数量可能减少,从而可能不利于锆改性高岭土中锆氧化物或氢氧化与水中磷酸盐之间发生配位体交换作用,进而导致锆改性高岭土对水中磷酸盐吸附能力的下降.
2.2.3 锆改性高岭土对水中磷酸盐的吸附等温线图 3为锆改性高岭土(制备时ZrOCl2 ·8H2O和高岭土质量比为0.5 ∶1、 沉淀pH值为10)对水中磷酸盐的吸附等温线. 从中可见,当c0为4-20 mg ·L-1(以PO43-计)、 V为50 mL、 m/V为0.5 g ·L-1、 T为20℃和t为24 h时,锆改性高岭土对水中磷酸盐的单位吸附量随水中磷酸盐平衡浓度的增加而增加直至达到吸附饱和. 从图 3还可以看出,当水中磷酸盐平衡浓度较低时,锆改性高岭土对水中磷酸盐的单位吸附量较高. 当水中磷酸盐平衡质量浓度为0.859 mg ·L-1时,锆改性高岭土对水中磷酸盐的单位吸附量达到了10.3 mg ·g-1. 湖泊、 水库和河流等天然地表水体的上覆水和间隙水中磷酸盐浓度通常较低. 因此,锆改性高岭土对水中磷酸盐吸附等温线的这种特性是有利于应用锆改性高岭土去除天然地表水体上覆水和间隙水中的磷.
 | 图 3 锆改性高岭土对水中磷酸盐的吸附等温线 Fig. 3 Adsorption isotherm of phosphate from water on zirconium-modified kaolin clay prepared under precipitated pH value 10 conditions |
Langmuir和Freundlich等温吸附模型经常被用于描述吸附剂对吸附质的等温吸附行为. Langmuir等温吸附方程见公式(8)[32]:
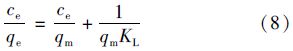
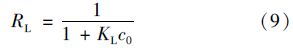

采用Langmuir和Freundlich等温吸附模型对图 3实验数据进行拟合,拟合结果见表 3. 从中可见,Langmuir和Freundlich等温吸附模型的拟合相关系数R2分别为0.998和0.790. 这说明,与Freundlich等温吸附模型相比,Langmuir等温吸附模型更适合用于描述锆改性高岭土对水中磷酸盐的吸附等温行为. Langmuir模型假定吸附剂对水中吸附质的吸附属于单分子层吸附[38]. Langmuir模型对图 3实验结果的拟合结果说明锆改性高岭土对水中磷酸盐的吸附属于单分子层吸附. 根据Langmuir等温吸附模型计算得到的锆改性高岭土(制备时ZrOCl2 ·8H2O和高岭土质量比为0.5 ∶1、 沉淀pH值为10)对水中磷酸盐的最大吸附量为17.5 mg ·g-1(以PO43-计),等同于5.7 mg ·g-1(以P计). 根据计算确定的锆改性高岭土中单位质量锆氧化物(ZrO2)对水磷酸盐的吸附量为109 mg ·g-1(以PO43-计)或35.6 mg ·g-1(以P计). 计算得到的分离因子RL大于0并且小于1,这说明锆改性高岭土对水中磷酸盐的吸附属于优惠吸附.
| 表 3 锆改性高岭土对水中磷酸盐等温吸附模型参数和拟合相关系数 Table 3 Isotherm model parameters and correlation coefficients for phosphate adsorption onto zirconium-modified kaolin clay prepared under precipitated pH value 10 conditions |
图 4为吸附磷酸盐后锆改性高岭土的磷形态分布特征. 从中可见,吸附磷酸盐后锆改性高岭土中各形态磷占总磷的比例从大到小依次为: NaOH-P(72.2%)>BD-P(14.6%)>Res-P(11.8%)>Liable-P(0.8%)或HCl-P(0.6%). 这说明吸附磷酸盐后锆改性高岭土中磷主要以NaOH-P(72.2%)、 BD-P(14.6%)和Res-P(11.8%)等形态存在,以Liable-P和HCl-P等形态存在的磷可以忽略不计. Liable-P 即弱吸附态磷,主要指很松散地被吸附到固体材料表面的磷[17]. BD-P是指对氧化还原敏感的磷[17]. NaOH-P 是指金属氧化物结合态磷,pH较高条件下该形态磷容易释放出来[17]. HCl-P是指与钙镁结合的磷,pH较低条件下该形态磷容易释放出来[17]. 厌氧和通常pH(5-9)条件下,Liable-P和BD-P很容易被重新释放出来,而NaOH-P和HCl-P则是较为稳定的,它们不容易被重新释放出来[17, 18]. Res-P是指永久性结合态磷,它们很难被重新释放出来[18]. 因此,被锆改性高岭土所吸附的磷酸盐大部分以较为稳定的NaOH-P和稳定的Res-P形态存在(这两部分磷占总磷的84.0%),厌氧和pH 5-9条件下不容易被重新释放出来.
 | 图 4 吸附磷酸盐后锆改性高岭土的磷形态分布特征
Fig. 4 Phosphorus fractionation of the phosphate-adsorbed zirconium-modified kaolin clay
|
图 5为厌氧条件时底泥无任何处理、 底泥添加高岭土和底泥添加锆改性高岭土作用下上覆水中SRP浓度随时间变化的曲线. 底泥磷释放控制模拟实验开始时各反应器上覆水中DO质量浓度位于0.09-0.14 mg ·L-1之间,实验终了时各反应器上覆水DO质量浓度位于0.53-1.07 mg ·L-1之间,这说明各反应器中上覆水DO浓度处于非常低的水平. 这说明底泥磷释放控制模拟实验进行期间各反应器中上覆水和底泥均处于厌氧状态. 模拟实验开始时各反应器中上覆水的pH值为7.98,实验终了时各反应器上覆水pH值位于6.66-6.91之间. 这说明反应器中底泥会略微降低了上覆水的pH值. 由图 5可见,当底泥培养时间由0 d增加到171 d时,底泥无任何处理情况下反应器中上覆水SRP质量浓度由0.041 mg ·L-1增加到4.95 mg ·L-1. 这说明厌氧条件下本研究所采用的重污染河道底泥会释放出来大量的磷进入上覆水中. 厌氧条件下,底泥中Fe(Ⅲ)化合物容易被转化为Fe(Ⅱ)化合物,Mn(Ⅲ/Ⅳ)化合物容易被转化为Mn(Ⅱ)化合物,使得底泥中与Fe(Ⅲ)和Mn(Ⅲ/Ⅳ)结合的磷脱离底泥进入间隙水中,进而通过扩散作用进入上覆水中,从而导致上覆水中SRP浓度随底泥培养时间的增加而增加[19]. 根据公式(2)和(3)计算得到开始时刻到第171 d期间厌氧条件下底泥的SRP平均释放速率为3.37 mg ·(m2 ·d)-1.
 | 图 5 原始底泥、 高岭土改良底泥和锆改性高岭土改良底泥的磷释放规律
Fig. 5 Kinetics of phosphorus release from the raw sediment,
kaolin clay-amended sediment and zirconium-modified
kaolin clay-amended sediment
|
由图 5还可见,当底泥培养时间由0 d增加到171 d时,底泥添加高岭土情况下反应器中上覆水SRP质量浓度由0.041 mg ·L-1增加到4.94 mg ·L-1. 这说明厌氧条件下高岭土改良底泥会释放出大量磷进入上覆水中. 与底泥无任何处理组相比,底泥添加高岭土组反应器上覆水中SRP浓度差异不明显,这说明向底泥中添加高岭土不能有效控制底泥磷的释放. 这主要是因为本研究所采用的高岭土对水中磷酸盐吸附能力很差的缘故. 根据公式(2)和(3)计算得到开始时刻到第171 d期间厌氧条件下高岭土改良底泥的SRP平均释放速率为3.40 mg ·(m2 ·d)-1.
由图 5还可以看出,当底泥培养时间为0-171 d时,底泥添加锆改性高岭土情况下反应器中上覆水SRP质量浓度处于0.010-0.083 mg ·L-1之间. 底泥添加锆改性高岭土组反应器上覆水中SRP质量浓度明显低于底泥无任何处理组,亦明显低于底泥添加高岭土组. 这说明锆改性高岭土添加可以有效控制底泥磷的释放. 对于底泥添加锆改性高岭土组,厌氧条件下底泥释放出大量的磷进入间隙水中,位于改良底泥中锆改性高岭土会迅速吸附间隙水中的磷,从而导致模拟期间上覆水中的磷质量浓度处于较低的水平. 被锆改性高岭土所吸附的磷大部分以较稳定的NaOH-P和稳定的Res-P形态存在,厌氧和通常pH(5-9)条件下很难被重新释放出来.
2.5 锆改性高岭土添加对底泥吸附水中磷酸盐的影响图 6为未改良和改良底泥对水中磷酸盐的吸附等温线. 从中可见,当初始磷质量浓度为0 mg ·L-1时,未改良和改良底泥对水中磷酸盐的单位吸附量为负值. 这说明当初始磷质量浓度为0 mg ·L-1时未改良和改良底泥均会释放出磷酸盐; 当初始磷质量浓度大于等于0.2 mg ·L-1时,未改良和改良底泥对水中磷酸盐的单位吸附量为正值,且未改良和改良底泥对水中磷酸盐的单位吸附量随初始磷质量浓度的增加而增加. 这说明当水中初始磷质量浓度大于等于0.2 mg ·L-1时未改良和改良底泥均会吸附水中的磷酸盐,且吸附能力随初始磷质量浓度的增加而增强; 锆改性高岭土改良底泥对水中磷酸盐的吸附能力明显强于未改良底泥. 这说明采用锆改性高岭土对底泥进行改良明显增强了底泥的吸磷能力.
 | 图 6 未改良和改良底泥对水中磷酸盐的吸附等温线 Fig. 6 Adsorption isotherm of phosphate on the original and amended sediments |
当磷浓度较低时,底泥对水中磷的等温吸附行为可以采用线性吸附模型进行描述[40]. 线性吸附模型的数学表达式为[40]:
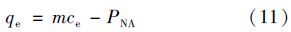

线性吸附模型对图 6(a)实验数据的拟合结果见表 4. 从中可见,锆改性高岭土改良底泥对磷的吸附效率明显高于未改良底泥,而磷吸附-解吸平衡浓度明显低于未改良底泥,这表明锆改性高岭土改良底泥中磷释放的可能性明显低于未改良底泥,采用锆改性高岭土对底泥进行改良降低了底泥磷释放的可能性.
| 表 4 未改良和改良底泥对水中磷酸盐等温吸附模型拟合参数 1) Table 4 Fitting parameters of the isotherm models for phosphate adsorption onto the unamended and amended sediments |
当磷浓度较高时,底泥对水中磷的等温吸附行为可以采用Langmuir和Freundlich等温吸附模型进行描述,它们的数学表达式分别见公式(8)和(10). Langmuir和Freundlich模型对图 6(b)实验数据的拟合结果见表 4. 从中可见,未改良和改良底泥对水中磷酸盐的吸附等温数据均可以采用Langmuir和Freundlich等温吸附模型进行描述. 计算得到的Langmuir模型分离因子RL值和Freundlich模型常数1/n值均大于0.1小于1,这说明未改良和改良底泥对水中磷酸盐的吸附属于优惠吸附. 根据Langmuir等温吸附模型确定的未改良底泥和锆改性高岭土改良底泥对水中磷酸盐的最大单位吸附容量(以P计)分别为249 mg ·kg-1和501 mg ·kg-1. 锆改性高岭土改良底泥吸附磷的KF值明显大于未改良底泥,这说明采用锆改性高岭土对底泥进行改性明显增强了底泥的吸磷能力.
2.6 锆改性高岭土原位改良技术控制底泥磷释放的长效性评估本研究的实验结果已经表明,向底泥添加锆改性高岭土短期内(171 d内)可以有效控制底泥磷的释放(详见2.5节). 为评估锆改性高岭土原位改良技术控制底泥磷释放的长效性,进一步采用数学模型方法计算了锆改性高岭土原位改良技术控制底泥磷释放的有效持续时间. 锆改性高岭土原位改良技术控制底泥磷向上覆水释放的有效持续时间(T,单位为d)主要取决于底泥磷释放速率[JD,单位为mg ·(m2 ·d)-1]、 锆改性高岭土对水中磷的最大单位吸附容量(qm,单位为mg ·g-1)和锆改性高岭土的添加量[M,单位(以底泥-水界面面积计)为kg ·m-2]等,可以采用公式(13)进行计算.
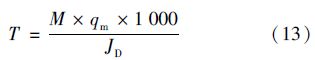
通过前期实验数据,假定底泥溶解性磷酸盐磷释放速率为3.37 mg ·(m2 ·d)-1、 锆改性高岭土对水中溶解性磷酸盐磷的最大单位吸附容量为5.7 mg ·g-1,向底泥添加10 g锆改性高岭土(相当于向每m2底泥-水界面下底泥添加1 274 g锆改性高岭土)理想情况下控制底泥溶解性磷酸盐磷释放的有效持续时间约为6 a. 这说明锆改性高岭土原位改良技术控制底泥磷释放的有效持续时间是比较长的.
3 结论(1)锆改性高岭土对水中磷酸盐的吸附能力随改性所用锆投加量的增加而增加. 随着制备吸附剂时沉淀pH由8增加至12,锆改性高岭土对水中磷酸盐的吸附能力先增强再下降,最优沉淀pH为10-11. 沉淀pH值为10时制备得到的锆改性高岭土对水中磷酸盐的吸附平衡数据可以采用Langmuir模型加以描述.
(2)大部分被锆改性高岭土中锆所吸附的磷酸盐以金属氧化物结合态(NaOH-P)和残渣态(Res-P)形式存在,低溶解氧情况下不容易被重新释放出来.
(3) 低溶解氧情况下,重污染河道底泥会释放出大量的溶解性磷酸盐磷进入上覆水体; 向重污染河道底泥添加锆改性高岭土可以极大地削减底泥中磷向上覆水体迁移的通量.
(4)采用锆改性高岭土对底泥进行改良不仅增强了底泥对水中磷的吸附能力,而且降低了底泥的磷吸附-解吸平衡浓度.
| [1] | 杨永琼, 陈敬安, 王敬富, 等.沉积物磷原位钝化技术研究进展[J].地球科学进展, 2013, 28 (6): 674-684. |
| [2] | 刘超, 朱淮武, 王立英, 等.滇池与红枫湖沉积物中磷的地球化学特征比较研究[J].环境科学学报, 2013, 33 (4): 1073-1079. |
| [3] | 史静, 俎晓静, 张乃明, 等.滇池草海沉积物磷形态、空间分布特征及影响因素[J].中国环境科学, 2013, 33 (10): 1808-1813. |
| [4] | 揣小明, 杨柳燕, 程书波, 等.太湖和呼伦湖沉积物对磷的吸附特征及影响因素[J].环境科学, 2014, 35 (3): 951-957. |
| [5] | 李安定, 张义, 周北海, 等.富营养化湖泊沉积物磷原位控制技术[J].水生生物学报, 2014, 38 (2): 370-374. |
| [6] | 寇丹丹, 张义, 黄发明, 等.水体沉积物磷控制技术[J].环境科学与技术, 2012, 35 (10): 81-85. |
| [7] | 胡赐明, 夏晗婷, 曹静, 等.富营养水体底泥原位控磷技术研究进展[J].杭州师范大学学报(自然科学版), 2011, 10 (1): 71-76. |
| [8] | 张岳, 王佳, 刘嘉裕, 等.富营养水体沉积物磷素释放机理及控制技术研究进展[J].杭州师范大学学报(自然科学版), 2014, 13 (1): 53-59. |
| [9] | Zamparas M, Zacharias I.Restoration of eutrophic freshwater by managing internal nutrient loads.A review[J].Science of the Total Environment, 2014, 496: 551-562. |
| [10] | Yamada T M, Sueitt A P E, Beraldo D A S, et al.Calcium nitrate addition to control the internal load of phosphorus from sediments of a tropical eutrophic reservoir: Microcosm experiments[J].Water Research, 2012, 46 (19): 6463-6475. |
| [11] | Rydin E.Inactivated phosphorus by added aluminum in Baltic Sea sediment[J].Estuarine, Coastal and Shelf Science, 2014, 151: 181-185. |
| [12] | Xu D, Ding S M, Sun Q, et al.Evaluation of in situ capping with clean soils to control phosphate release from sediments[J].Science of the Total Environment, 2012, 438: 334-341. |
| [13] | Katsev S, Dittrich M.Modeling of decadal scale phosphorus retention in lake sediment under varying redox conditions[J].Ecological Modelling, 2013, 251: 246-259. |
| [14] | Schauser I, Lewandowski J, Hupfer M.Decision support for the selection of an appropriate in-lake measure to influence the phosphorus retention in sediments[J].Water Research, 2003, 37 (4): 801-812. |
| [15] | Wang C H, Bai L L, Pei Y S.Assessing the stability of phosphorus in lake sediments amended with water treatment residuals[J].Journal of Environmental Management, 2013, 122: 31-36. |
| [16] | Wang C H, Liang J C, Pei Y S, et al.A method for determining the treatment dosage of drinking water treatment residuals for effective phosphorus immobilization in sediments[J].Ecological Engineering, 2013, 60: 421-427. |
| [17] | Wang C H, Qi Y, Pei Y S.Laboratory investigation of phosphorus immobilization in lake sediments using water treatment residuals[J].Chemical Engineering Journal, 2012, 209: 379-385. |
| [18] | Meis S, Spears B M, Maberly S C, et al.Sediment amendment with Phoslock® in Clatto Reservoir (Dundee, UK): Investigating changes in sediment elemental composition and phosphorus fractionation[J].Journal of Environmental Management, 2012, 93 (1): 185-193. |
| [19] | Meis S, Spears B M, Maberly S C, et al.Assessing the mode of action of Phoslock® in the control of phosphorus release from the bed sediments in a shallow lake (Loch Flemington, UK)[J].Water Research, 2013, 47 (13): 4460-4473. |
| [20] | 李佳, 詹艳慧, 林建伟, 等.镧改性沸石对太湖底泥-水系统中磷的固定作用[J].中国环境科学, 2014, 34 (1): 161-169. |
| [21] | Gibbs M, Özkundakci D.Effects of a modified zeolite on P and N processes and fluxes across the lake sediment-water interface using core incubations[J].Hydrobiologia, 2011, 661 (1): 21-35. |
| [22] | Zhang Y, He F, Xia S B, et al.Adsorption of sediment phosphorus by porous ceramic filter media coated with nano-titanium dioxide film[J].Ecological Engineering, 2014, 64: 186-192. |
| [23] | Yin H B, Kong M, Fan C X.Batch investigations on P immobilization from wastewaters and sediment using natural calcium rich sepiolite as a reactive material[J].Water Research, 2013, 47 (13): 4247-4258. |
| [24] | Chitrakar R, Tezuka S, Sonoda A, et al.Selective adsorption of phosphate from seawater and wastewater by amorphous zirconium hydroxide[J].Journal of Colloid and Interface Science, 2006, 297 (2): 426-433. |
| [25] | Su Y, Cui H, Li Q, et al.Strong adsorption of phosphate by amorphous zirconium oxide nanoparticles[J].Water Research, 2013, 47 (14): 5018-5026. |
| [26] | Liu H L, Sun X F, Yin C Q, et al.Removal of phosphate by mesoporous ZrO2[J].Journal of Hazardous Materials, 2008, 151 (2-3): 616-622. |
| [27] | 张永利, 朱佳, 史册, 等.高岭土的改性及其对Cr(Ⅵ)的吸附特性[J].环境科学研究, 2013, 26 (5): 561-568. |
| [28] | 翟由涛, 杭小帅, 干方群.改性高岭土对废水中磷的吸附性能及机理研究[J].土壤, 2012, 44 (1): 55-61. |
| [29] | 王小波, 王艳, 卢树昌, 等.改性高岭土对水体中氮磷去除效果的研究[J].农业环境科学学报, 2010, 29 (9): 1784-1788. |
| [30] | 中国科学院南京土壤研究所.土壤理化分析[M].上海: 上海科学技术出版社, 1978. |
| [31] | Wang S R, Jin X C, Zhao H C.Phosphorus fractions and its release in the sediments from the shallow lakes in the middle and lower reaches of Yangtze River area in China[J].Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2006, 273 (1-3): 109-116. |
| [32] | Yang M J, Lin J W, Zhan Y H, et al.Adsorption of phosphate from water on lake sediments amended with zirconium-modified zeolites in batch mode[J].Ecological Engineering, 2014, 71: 223-233. |
| [33] | 国家环境保护总局.水和废水监测分析方法[M].(第四版).北京: 中国环境科学出版社, 2002. |
| [34] | 王改, 黄廷林, 周真明, 等.扬州古运河沉积物污染物释放强度与特征研究[J].环境污染与防治, 2012, 34 (11): 25-29. |
| [35] | 胡佶, 张传松, 王修林, 等.东海春季赤潮前后沉积物-海水界面营养盐交换速率的研究[J].环境科学, 2007, 28 (7): 1442-1448. |
| [36] | Zong E M, Wei D, Wan H Q, et al.Adsorptive removal of phosphate ions from aqueous solution using zirconia-functionalized graphite oxide[J].Chemical Engineering Journal, 2013, 221: 193-203. |
| [37] | Stankovic J B, Milonji DćS K, Zec S P.The influence of chemical and thermal treatment on the point of zero charge of hydrous zirconium oxide[J].Journal of the Serbian Chemical Society, 2013, 78 (7): 987-995. |
| [38] | Huang W Y, Li D, Liu Z Q, et al.Kinetics, isotherm, thermodynamic, and adsorption mechanism studies of La(OH)3-modified exfoliated vermiculites as highly efficient phosphate adsorbents[J].Chemical Engineering Journal, 2014, 236: 191-201. |
| [39] | Yan L G, Yang K, Shan R R, et al.Kinetic, isotherm and thermodynamic investigations of phosphate adsorption onto core-shell Fe3O4@LDHs composites with easy magnetic separation assistance[J].Journal of Colloid and Interface Science, 2015, 448: 508-516. |
| [40] | 姜霞, 王秋娟, 王书航, 等.太湖沉积物氮磷吸附/解吸特征分析[J].环境科学, 2011, 32 (5): 1285-1291. |
 2015,Vol. 36
2015,Vol. 36


