2. 重庆理工大学化学化工学院, 重庆 400054;
3. 重庆市农业资源与环境研究重点实验室, 重庆 400715
2. College of Chemistry and Chemical Engineering, Chongqing University of Technology, Chongqing 400054, China;
3. Chongqing Key Laboratory of Agricultural Resources and Environment, Chongqing 400715, China
拦坝建库截流形成的水环境被认为是有利于汞活化、 甲基化和生物累积的场所[1]. 在水库环境中,水体中多种赋存形态汞通过活化、 甲基化进程,形成亲脂强生物神经毒性的甲基汞. 水体中甲基汞通过食物链吸收传递和以生物富集放大系数104~107逐级放大,最终富集在高营养层次鱼类和哺乳动物体内[3].
研究表明,水库中水体表底层温差大,持续时间长,呈现季节性分层的现象[4, 5],抑制了上、 下层水体物质的对流交换,一方面造成氮磷等营养物质在底层滞留,另一方面导致溶解氧、 氧化还原电位等重要水环境参数发生改变[5],进而影响着溶解态和颗粒态汞在水库中的扩散沉降,沉积态汞向间隙水溶出向上覆水体扩散重新入水体的释放过程[6]. 因此,探讨大型水库各形态汞的迁移转化特征,无疑是研究水库敏感汞效应的重要环节.
长寿湖水库是长江支流重要大型水库,位于重庆西南130 km,于1957年建成,兼具饮用、 养殖、 发电、 旅游、 防洪功能. 水库流域面积3248 km2,龙溪河为主要供水河流,平均库容7.48×109 m3,水力停留时间0.38 a,最大水深40 m,平均水深15 m. 20世纪90年代,由于在长寿湖水库大规模开展网箱、 网栏养鱼,大量投放饲料,并投放化肥、 鸡粪等,导致水体污染,水体富营养化严重. 尽管2004年4月后,已全面拆除水库的网箱、 拦网养殖,水质已有所改善,但目前水体仍呈中到富营养化状态. 因此,开展长寿湖水库水体和沉积物间隙水中不同形态汞的浓度及其空间分布特征研究,探讨其迁移转化规律,以期为进一步研究汞在水体中的环境化学行为具有重要意义.
1 材料与方法 1.1 采样点布设本次调查于2013年9月~2014年7月在长寿湖水库选取了5个采样点,采样点布设见图 1. 采样点S1 (E 107°15′29″,N 29°55′3″) 位于水库大坝前,为长寿湖水库出水口. S2 (E 107°16′23″,N 29°59′3″)位于水库西部,为龙溪河入水口,龙溪河流经垫江县和梁平县,河两岸分布密集村落和大片果园. S3 (E 107°18′58″,N 29°58′21″) 位于水库北部回水区,水力交换时间长. S4 (E 107°20′19″,N 29°57′5″)位于水库东部,为另一主要支流入水口,两岸果园分布广泛,村落分布较少. S5 (E 107°17′45″,N 29°56′30″)位于水库中部,北部岛屿分布成片果园,西部和南部岛屿旅游业发达. 分别于2013年9月25日,2014年1月8日、 4月24日、 7月13日,在S1~S5采样点分层采集垂直断面水样和沉积物间隙水样. 水体水样测定了总汞(THg)、 溶解态汞(DHg)、 颗粒态汞(PHg)、 活性汞(RHg)和总甲基汞(TMeHg)、 溶解态甲基汞(DMeHg)、 颗粒态甲基汞(PMeHg)浓度,沉积物间隙水测定溶解态汞(DHg)、 溶解态甲基汞(DMeHg)浓度.
 | 图 1 重庆长寿湖水库采样点分布示意
Fig. 1 Sampling Location in Changshou Reservior
|
Nisiki采样器在S1~S5样点,从表层到底层按每4 m深度取一个样. 采集的水样一部分注入高硼硅玻璃样品瓶,用于分析THg、 RHg、 TMeHg,另一部分用0.45 μm滤膜(Millipore)过滤后注入高硼硅玻璃样品瓶,用于分析DHg、 DMeHg. 水样放入冷藏样品箱,运至实验室后存放冰箱中0~4℃保存,1周内完成各形态汞的分析.
1.2.2 沉积物间隙水采集SWB-1型便携式不扰动湖泊沉积物采样器采集S1-S5样点的沉积物柱,确保界面水清澈,沉积物未被扰动[8]. 仔细抽取界面水后,沉积物样品在氮气氛围的厌氧条件下在现场分割. 表层以下10 cm按1 cm间距分割,10 cm以下部分按2 cm间距分割,将样品封存入经过酸预处理的50 mL离心管,用封口胶密封,低温4℃保存. 24 h内于转速为3000 r ·min-1约30 min,4℃恒温条件下高速离心沉积物固相和液相,用针式过滤器以0.45 μm(Millipore)滤膜获得沉积物间隙水,用于分析DHg、 DMeHg.
1.2.3 水样分析与质量控制水样分析参照USEPA Method 1630和Method 1631[9, 10]进行. 分别取未过滤水样和过滤水样经氯化溴氧化,氯化亚锡还原,金管富集-冷原子荧光光谱法(CVAFS)测定,得出水样THg、 DHg浓度,将THg-DHg=PHg. 取未过滤水样直接用氯化亚锡还原,金管富集-CVAFS测定,得出水样RHg浓度. 分别取未过滤水样和过滤水样,采样蒸馏-乙基化-GC-CVAFS法测定,分别得出TMeHg、 DMeHg浓度,将TMeHg-DMeHg=PMeHg. 采用不大于样品最小值20%的方法空白、 实验器皿空白、 野外空白确保样品各形态汞的质量分析准确性[11]. 分析过程中的质量控制采用平行样控制及加标回收率,加标回收率为80%~112%,并对5%的样品进行重复测定,相对标准偏差<9%.
阴阳离子按照Method 300 Revision 2.1(EPA,1993)采用DX-120(Dionex,USA)进行分析. pH用PT-10(Sartorius,Germany)测定. 溶解氧(DO)用YSI 550A(Washington,USA)测定; DOC使用Sievers InnovOx Laboratory TOC Analyzer(GE USA)进行分析.
1.2.4 数据处理数据管理采用Microsoft Excel(2010),正态分布检验采用Origin 8.0软件,统计分析采用SPSS 16.0.
1.2.5 沉积物孔隙水中的汞对上覆水体的贡献率根据Fick's First Law并结合浓度梯度,计算出长寿湖水库沉积物/水界面溶解态甲基汞和溶解态汞的扩散通量F[12].

 是溶质的最大浓度梯度; φ是沉积物孔隙度(表层0~5 cm沉积物的孔隙度为0.93[12]),θ是弯曲度,Dw 为溶液中的分子扩散系数. MMHg 和DHg 的扩散系数分别为1.84×10-5 cm2 ·s-1和8.65×10-6 cm2 ·s-1[12].
是溶质的最大浓度梯度; φ是沉积物孔隙度(表层0~5 cm沉积物的孔隙度为0.93[12]),θ是弯曲度,Dw 为溶液中的分子扩散系数. MMHg 和DHg 的扩散系数分别为1.84×10-5 cm2 ·s-1和8.65×10-6 cm2 ·s-1[12].
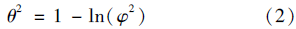
式(2)是孔隙度与弯曲度之间的关系式.
假设沿浓度梯度扩散是沉积物中的汞向上覆水体迁移的主要途径,根据式(3)可以估算出沉积物间隙水中汞对上覆水体汞的贡献程度η:

式中,η为贡献率,F为扩散通量,h为长寿湖水库平均水深15 m,tw为长寿湖水库水力停留时间0.38 a,c为上覆水体中汞的平均浓度(ng ·L-1).
2 结果与讨论 2.1 垂直剖面水体各形态汞浓度季节变化长寿湖水库不同形态汞浓度垂直分布如图 2~5所示. 长寿湖水库水体总汞浓度变化范围为1.86~70.33ng ·L-1,平均值为(14.77± 12.24)ng ·L-1,远低于我国环境质量标准(GB 3838-2002)规定的一类地表水汞浓度标准限值(50 ng ·L-1). 总汞浓度春季>夏季>冬季>秋季. 从水体垂直剖面来看,春季浓度变化波动最为明显,总汞浓度从表层到4~8 m降低,分析原因是大量径流携带汞入库造成表层总汞含量偏高,随着水深增加,颗粒物携汞逐渐沉降,因而总汞含量逐渐降低. 当接近湖底,总汞含量增高明显,这与沉积物的扰动和再悬浮有关. 通过将长寿湖水库水体总汞浓度与世界上其他湖泊水库相比较(表 1),高于北欧北美未受污染天然水体[13, 14, 15],与云南滇池汞浓度相当[16]. 与同属西南地区湖泊的乌江渡,东风水库[17]和阿哈水库[18]对比,汞含量在同一数量级. 究其原因如下: ① 重庆长寿湖水库周边地区土壤重金属Hg[(0.54±0.22)mg ·kg-1]富集较为严重,超过了土壤质量一级标准(0.15 mg ·kg-1)[19]. 水库流域农业活动密集,且土壤蓄水能力弱,坡耕地受径流冲刷严重,会造成大量总汞、 溶解态汞以及颗粒态汞随径流进入长寿湖. ②覃蔡清等[6] 对重庆降雨研究发现总汞含量7.47~120.11 ng ·L-1,大气湿沉降是水库流域的重要汞输入. ③ 长寿湖水库唯一主要来水龙溪河两岸分布长寿化工厂、 村落以及大片果园,工业以及农业生活污水所带入的外源性污染物可能是各形态汞的主要来源.
 | 图 2 长寿湖水库水体总汞剖面季节分布 Fig. 2 Distribution of THg in water columns of Changshou Reservior |
 | 图 3 长寿湖水库水体活性汞剖面季节分布 Fig. 3 Distribution of RHg in water columns of Changshou Reservior |
长寿湖水库水体颗粒态汞浓度平均值为(9.13±11.51)ng ·L-1. 全年中春季水体颗粒态汞浓度最高,且水体垂直剖面上颗粒态汞浓度表现出先降低再升高的趋势,在表层下8 m和20 m处出现浓度跃增,原因可能是春季进入丰水期,入库径流水温较水库本身水温低,即入库径流密度较水库水体大,因而这种密度差异导致径流在表层10 m以下深处潜流进入水库,造成水库中下部水体颗粒态汞浓度增加.
从图 5可以看出,长寿湖水库溶解态汞浓度平均值为(5.62±4.75)ng ·L-1. 溶解态汞浓度大小顺序依次为: 夏季>春季>冬季>秋季. 长寿湖水库秋、 冬、 春、 夏季溶解态汞占总汞比例分别为53.4%±25.6%、 41.4%±23.6%%、 31.2%±23.9%、 63.9%±14.2%. 夏季水体垂直剖面表层和底层溶解态出现升高,一方面是由于夏季丰水期暴雨径流带入大量颗粒态汞同时表层溶解态汞的浓度相应升高,另一方面夏季温跃层的以下的水体逐渐进入缺氧还原状态,湖底沉积物吸附的汞解析再悬浮进入水体底部水体.
 | 图 4 长寿湖水库水体颗粒态汞剖面季节分布
Fig. 4 Distribution of PHg in water columns of Changshou Reservior
|
 | 图 5 长寿湖水库水体溶解态汞剖面季节分布
Fig. 5 Distribution of DHg in water columns of Changshou Reservior
|
| 表 1 长寿湖水库总汞、 甲基汞浓度与世界其他湖泊比较 Table 1 Comparison of THg and TMeHg concentrations in the Changshou Reservior with other aquatic systems |
长寿湖水库活性汞浓度平均值为(2.30±2.43)ng ·L-1. 类似于总汞,春季和夏季由于降水和地表径流等外源性输入增加,表层水体活性汞增高显著,而后随水体深度增加整体变化波动变化明显. 长寿湖水库水体活性汞与总汞之间呈显著性相关关系(r=0.754**,P<0.01),这表明长寿湖水库水体活性汞浓度受总汞影响显著.
从图 6~8可以看出,长寿湖水库水体总甲基汞浓度平均值为(0.41±0.47)ng ·L-1. 秋、 冬、 春、 夏季甲基汞浓度分别为: (0.46±0.17)、 (0.32±0.24)、 (0.41±0.26)、 (0.46±0.31)ng ·L-1,在夏秋季节随着剖面垂直深度增加,表层下10 m左右出现峰值,而后又逐步降低,接近湖底部又明显增加. Watras等[22]研究发现,暖季水体8m处温度的分层和溶解氧的跌落,有利于该处甲基汞的形成. 因此,一方面长寿湖水库夏季上部湖水分层,水体垂直剖面中部的峰值与自身甲基化的生成有关,另一方面底部浓度的跃增与季节性的湖底厌氧环境,结合夏季的高温,更有利于甲基化速率的增加,沉积物间隙水总甲基汞向上的扩散从而使得水体底部总甲基汞浓度增加.
 | 图 6 长寿湖水库水体总甲基汞剖面分布
Fig. 6 Distribution of TMeHg in water columns of Changshou Reservior
|
溶解态甲基汞浓度平均值为(0.17±0.18)ng ·L-1. 秋、 冬、 春、 夏季溶解态甲基汞浓度分别为: (0.27±0.10)、 (0.09±0.05)、 (0.25±0.16)、 (0.07±0.03)ng ·L-1. 从垂直剖面上看,夏秋季采样点溶解态甲基汞浓度在表层下4~8 m出现峰值,随之其值降低近湖底部再次跃增. 主要原因为湖体高温厌氧环境中,沉积物表面有机物腐烂过程中形成的气泡,使已经沉降的悬浮物再浮起,同时还原条件下具有较大比表面积的铁和锰的氧化物及氢氧化物溶解,大量甲基汞得以向水体释放,溶解态甲基汞由沉积物再次进入上覆水体,使其溶解态甲基汞浓度增加.
颗粒态甲基汞浓度在秋、 冬、 春、 夏季分别为: (0.23±0.11)、 (0.21±0.15)、 (0.24±0.12)、 (0.27±0.17)ng ·L-1. 颗粒态甲基汞浓度大小顺序依次为: 夏季>春季>秋季>冬季. 从图 8可以看出,全年中大多数时候颗粒态甲基汞的峰值并没有出现在沉积物-水体界面处,而是在湖水体中下部8~20 m处. He等[21]研究指出上层颗粒物的沉降会导致缺氧层颗粒态甲基汞的升高. 因而,长寿湖水库水体剖面中颗粒态甲基汞增高并不来源于沉积物的再悬浮,而是上层水体颗粒态甲基汞的沉降.
2.2 沉积物间隙水中溶解态汞与溶解态甲基汞分布沉积物间隙水水化学是沉积物形成和与水体进行物质交换的敏感指示器[24, 25]. 长寿湖水库沉积物间隙水溶解态汞浓度分布如图 9所示,其变化范围为1.85~85.39ng ·L-1,平均值为14.39ng ·L-1. 间隙水中无机汞浓度季节趋势: 秋季>夏季>春季>冬季. Barkay等[26]研究发现汞在沉积物固相与液相的分配会受到pH、 Eh因素影响. 因此,长寿湖水库沉积物间隙水溶解态汞在垂直剖面波动范围较大,不固定峰值的出现与间隙水中氧化还原条件,配位反应等环境因素的影响有关. 总体而言,间隙水中溶解态汞的浓度高于上覆水体中溶解态汞的浓度.
从<图 10可以看出间隙水溶解态甲基汞浓度变化范围为0.01~17.35ng ·L-1,平均值为2.62ng ·L-1. 间隙水中溶解态甲基汞浓度季节趋势:秋季>夏季>春季>冬季,且间隙水中溶解态甲基汞的浓度远高于上覆水体中溶解态甲基汞的浓度. Hines等[13]研究发现在Spring 湖孔隙水甲基汞浓度峰值出现在表层下20 cm和31 cm 处. 长寿湖水库垂直剖面间隙水甲基汞峰值出现在表层下16 cm和28 cm,可能硫酸盐还原细菌活动扩展到更深的区域,从而导致了沉积物深处甲基化率的提高.
研究表明,水生系统中甲基汞占总汞比例(DMeHg/THg)是判断甲基汞产率的重要指标[27, 28]. 分析发现,长寿湖水库间隙水四季DMeHg/DHg(%)分别为: 2013年9月10.9%±8.5%; 2013年12月26.1%±7.8%; 2014年3月24.5%±6.3%; 2014年7月32.3%±15.6%,总体高于乌江流域乌江渡水库15%和引子渡水库13%,但远低于北美北欧所报道的新建水库水体比例(50%~80%)[29],长寿湖水库属于中等甲基汞产率湖泊.
2.3 沉积物/水界面溶解态汞和溶解态甲基汞的扩散通量对于深水水库而言,沉积物间隙水与上覆水体浓度梯度所引起的分子扩散作用是沉积物与上覆水体之间进行物质交换的主要形式[30]. 长寿湖水库沉积物间隙水溶解态汞和溶解态甲基汞向水体扩散通量见表 2. 可以看出,长寿湖水库间隙水溶解态汞和溶解态甲基汞扩散通量明显季节变化. 间隙水溶解态汞秋季>夏季>春季>冬季. 间隙水溶解态甲基汞在夏季和秋季向上覆水体扩散通量分别为30.0和28.2 ng ·(m2 ·d)-1,远高于冬季3.8 ng ·(m2 ·d)-1. 夏秋季节长寿湖水库沉积物的厌氧层中大量难溶的HgS解析,同时具有较大比表面积的铁锰氧化物及氢氧化物逐渐溶解,使得大量吸附的甲基汞向水体释放[31],造成液相溶解态甲基汞浓度的增加. 因此,长寿湖水库沉积物与水体界面间季节性厌氧环境对促使间隙水汞扩散通量增加起到重要作用.
 | 图 7 长寿湖水库水体溶解态甲基汞剖面分布Fig. 7 Distribution of DMeHg in water columns of Changshou Reservior
|
 | 图 8 长寿湖水库水体颗粒态甲基汞剖面分布
Fig. 8 Distribution of PMeHg in water columns of Changshou Reservior
|
 | 图 9 长寿湖水库沉积物间隙水溶解态汞剖面分布
Fig. 9 Distribution of DMeHg in sediment porewater profiles
|
| 表 2 长寿湖水库DHg、 DMeHg扩散通量及贡献率 Table 2 Diffusion flux and contribution rate of DHg and DMeHg in Changshou Reservoir |
甲基汞是水环境中最常见的有机汞形式,一般通过Hg2+甲基化而来[31]. PMeHg在水库中的沉降解析为DMeHg,沉积态汞向间隙水溶出DMeHg并向上覆水体扩散重新入水体的过程均与水环境条件(如水温、 溶解氧、 氧化还原电位等)有着重要关系. 因此,水体水质参数条件对水体甲基汞的影响非常重要.
3.1 水温水温作为重要的水环境影响因子之一,通过影响微生物活动的活性影响着水体甲基汞的形成[32].
长寿湖水库全年水体垂直剖面温度9.0~33.2℃,平均值20.1℃(如图 11). 从长寿湖水库水体甲基汞所占比例MeHg/THg(%)来看,夏季最高57%,其次为春季52%、 秋季32%、 冬季26%. 这表明夏季的到来,水体温度升高明显,硫酸盐还原菌、 铁还原菌等微生物的活跃繁殖,有利于汞向甲基汞转化; 在冬季微生物代谢和生长活动的低速率使得MeHg的产生量显著降低. 有研究者在San Francisco Bay注意到沉积物微生物Hg的甲基化进程在35℃具有最高值[29]. 因此,长寿湖水库适宜的水温有利于提高水中微生物的活性而促进汞的甲基化作用,较低温度抑制汞的甲基化或者有利于汞脱甲基化进程.
3.2 溶解氧汞的甲基化进程大多发生在厌氧环境,好氧环境有利于去甲基化进行[29]. 长寿湖水库水体垂直剖面中DO变化范围1.1~13mg ·L-1,均值5.8 mg ·L-1(图 12).
长寿湖水库DO与夏季水体DMeHg浓度呈极显著负相关关系(r=-0.482**,P<0.05),春季显著负相关关系(r=-0.339*,P<0.01),秋季和冬季不具有相关性. 夏季长寿湖水库水体DO随水深深度增加而逐渐减小,同时水体温度的分层有效抑制了上、 下水团的交换,逐渐形成水库底部厌氧环境. 湖底水体厌氧条件下,由于溶解态硫化物复合体的形成以及铁锰氧化物及氢氧化物的溶解,大量甲基汞得以向水体释放,造成水体溶解态甲基汞浓度的增加[32]. 因此,长寿湖水库水环境中季节性低DO有助于DMeHg的解析和释放.
3.3 溶解有机碳长寿湖水库水体溶解有机碳DOC变化范围9.67~14.4 mg ·L-1,均值10.8 mg ·L-1,远高于乌江流域的红枫湖水库(2.5 mg ·L-1)和乌江渡水库(1.3 mg ·L-1). 通过长寿湖水库水体DMeHg与水体DOC浓度之间的相关分析发现两者均没有相关性. DOC对Hg的内在影响因素尚有争议. Barkay 等[26]证实高DOC通过降低Hg2+对甲基化进程细菌的适宜性从而抑制MMHg的合成速率. 而Watras 等[22]注意到Wisconsin湖水中随着DOC的增加而MMHg部分增加,特别是DOC浓度大于5 mg ·L-1. 长寿湖水库中有机质降解同时水中溶解氧消耗量随之增加,导致沉积物/水体界面更多以厌氧环境为主,增加了无机汞的移动性以及加速了潜在甲基化进程. 同时湖中高DOC值意味着汞与有机配体结合型的增加,从而降低了汞对于细菌的微生物适宜性. 因此,长寿湖水库水体DOC对DMeHg影响是多方面的,有待以后进一步深入研究.
4 结论(1)长寿湖水库水体总汞浓度平均值为(14.77± 12.24)ng ·L-1,长寿湖水库水体总甲基汞浓度平均值为(0.41±0.47)ng ·L-1. 夏秋季采样点溶解态甲基汞浓度在表层下4~8 m出现峰值,随之其值降低近湖底部再次跃增. 颗粒态甲基汞浓度峰值出现在表层下8~20 m而非在沉积物-水体界面处,主要与上层水体颗粒物吸附甲基汞的沉降有关.
(2)长寿湖水库垂直剖面间隙水甲基汞峰值出现在表层下16 cm和28 cm,可能硫酸盐还原细菌活动扩展到更深的区域,从而导致了沉积物深处甲基化率的提高. 间隙水溶解态甲基汞在秋季和夏季向上覆水体扩散通量分别为28.2 ng ·(m2 ·d)-1和30.0 ng ·(m2 ·d)-1,远高于冬季3.8 ng ·(m2 ·d)-1.
(3)长寿湖水库适宜的水温有利于提高水中微生物的活性从而促进汞的甲基化作用,较低温度抑制汞的甲基化或者有利于汞脱甲基化进程. 夏季、 春季水体DMeHg浓度与DO相关关系(r=-0.482**,P<0.05; r=-0.339*,P<0.01),秋季和冬季不具有相关性.
 | 图 11 长寿湖水库水体水温参数
Fig. 11 Water temperature in Changshou Reservior
|
 | 图 10 长寿湖水库沉积物间隙甲基汞剖面分布
Fig. 10 Distribution of DMeHg in sediment porewater profiles
|
 | 图 12 长寿湖水库水体溶解氧参数
Fig. 12 Dissovled oxygen in Changshou Reservior
|
| [1] | Muresan B, Cossa D, Jézéquel D, et al.The biogeochemistry of mercury at the sediment-water interface in the Thau lagoon.1.Partition and speciation[J].Estuarine, Coastal and Shelf Science, 2007, 72 (3): 472-484. |
| [2] | Yan H Y, Feng X B, Shang L H, et al.The variations of mercury in sediment profiles from a historically mercury-contaminated reservoir, Guizhou province, China [J].Science of the Total Environment, 2008, 407 (1): 497-506. |
| [3] | Zhu L L, Yan B X, Wang L X, et al.Mercury concentration in the muscle of seven fish species from Chagan Lake, Northeast China[J].Environmental Monitoring and Assessment, 2012, 184 (3): 1299-1310. |
| [4] | He T R, Feng X B, Guo Y N, et al.Geochemical Cycling of Mercury in the Sediment of Hongfeng Reservior[J].Environmental Science, 2008, 29 (7): 1768-1774. |
| [5] | 闫金龙, 江韬, 高洁, 等.两江交汇处水体溶解性有机质的吸收和荧光光谱特征: 以渠江-嘉陵江、涪江-嘉陵江为例 [J].环境科学, 2015, 36 (3): 869-878. |
| [6] | 覃蔡清, 王永敏, 彭玉龙, 等.重庆缙云山降水中不同形态汞的含量及其沉降量[J].环境科学, 2015, 36 (3): 809-816. |
| [7] | Gao N, Armatas N G, Shanley J B, et al.Mass balance assessment for mercury in Lake Champlain [J].Environmental Science & Technology, 2006, 40 (1): 82-89. |
| [8] | 王雨春, 黄荣贵, 万国江.SWB-1型便携式湖泊沉积物-界面水取样器的研制[J].地质地球化学, 1998, (1): 94-96. |
| [9] | US EPA.Method 1630: Methyl mercury in water by distillation, aqueous ethylation, purge and trap, and CVAFS[S].Washington, D.C.: US EPA, 2001. |
| [10] | USEPA.Method 1631, Revision E: Mercury in water by oxidation, purge and trap, and cold vapor atomic fluorescence spectrometry[S].Washington, D.C.: U.S.EPA, 2002. |
| [11] | 闫海鱼, 冯新斌, 商立海, 等.天然水体中痕量汞的形态分析方法研究[J].分析测试学报, 2003, 22 (5): 10-13. |
| [12] | 何天容.贵州红枫湖汞的生物地球化学循环[D].贵阳: 中国科学院地球化学研究所, 2007. |
| [13] | Hines N A, Brezonik P L, Engstrom D R.Sediment and porewater profiles and fluxes of mercury and methylmercury in a small seepage lake in northern Minnesota[J].Environmental Science & Technology, 2004, 38 (24): 6610-6617. |
| [14] | Gray J E, Hines M E.Biogeochemical mercury methylation influenced by reservoir eutrophication, Salmon Falls Creek Reservoir, Idaho, USA[J].Chemical Geology, 2009, 258 (3-4): 157-167. |
| [15] | Hall B D, Louis V L S, Rolfhus K R, et al.Impacts of reservoir creation on the biogeochemical cycling of methyl mercury and total mercury in boreal upland forests[J].Ecosystems, 2005, 8 (3): 248-266. |
| [16] | Wang S F, Zhang M M, Li B, et al.Comparison of mercury speciation and distribution in the water column and sediments between the algal type zone and the macrophytic type zone in a hypereutrophic lake (Dianchi Lake) in Southwestern China[J].Science of the Total Environment, 2012, 417-418: 204-213. |
| [17] | Fengv X B, Jiang H M, Qiu G L, et al.Geochemical processes of mercury in Wujiangdu and Dongfeng reservoirs, Guizhou, China[J].Environmental Pollution, 2009, 157 (11): 2970-2984. |
| [18] | Feng X, Bai W, Shang L, et al.Mercury speciation and distribution in Aha Reservoir which was contaminated by coal mining activities in Guiyang, Guizhou, China[J].Applied Geochemistry,2011, 26 (2): 213-221. |
| [19] | 罗真富, 谭德军, 谢洪斌, 等.重庆长寿湖周边地区土壤重金属污染评价[J].湖北农业科学, 2012, 51 (1): 30-34. |
| [20] | Feng X B, Bai W Y, Shang L H, et al.Mercury speciation and distribution in Aha Reservoir which was contaminated by coal mining activities in Guiyang, Guizhou, China[J].Applied Geochemistry, 2011, 26 (2): 213-221. |
| [21] | He T R, Feng X B, Guo Y N, et al.The impact of eutrophication on the biogeochemical cycling of mercury species in a reservoir: A case study from Hongfeng Reservoir, Guizhou, China[J].Environment Pollution, 2008, 154 (1): 56-67. |
| [22] | Watras C J, Morrison K A, Host J S, et al.Concentration of mercury species in relationship to other site-specific factors in the surface waters of northern Wisconsin lakes[J].Limnology and Oceanography, 1995, 40 (3): 556-572. |
| [23] | Meli M.Mercury in lakes and rivers[A].In: Sigel A, Sigel H (Eds.).Mercury and its Effect on Environment and Biology[M].New York: Marcel Dekker Inc, 1997. |
| [24] | Todorova S G, Driscoll C T, Steven W E, et al.Changes in the long-term supply of mercury species to the upper mixed waters of a recovering lake [J].Environmental Pollution, 2014, 185: 314-321. |
| [25] | 吉芳英, 王图锦, 胡学斌, 等.三峡库区消落区水体-沉积物重金属迁移转化特征[J].环境科学, 2009, 30 (12): 3481-3487. |
| [26] | Barkay T, Gillman M, Turner R R.Effects of dissolved organic carbon and salinity on bioavailability of mercury[J].Applied and Environmental Microbialogy, 1997, 63 (11): 1267-1271. |
| [27] | 王娅, 赵铮, 木志坚, 等.三峡库区典型农田小流域水体汞的时空分布特征[J].环境科学, 2014, 35 (11): 4095-4102. |
| [28] | Moingt M, Lucotte M, Paquet S, et al.Deciphering the impact of land-uses on terrestrial organic matter and mercury inputs to large boreal lakes of central Québec using lignin biomarkers [J].Applied Geochemistry, 2014, 41: 34-48. |
| [29] | Marvin-DiPasquale M, Agee J L, Microbial mercury cycling in sediments of the San Francisco Bay-Delta[J].Estuaries, 2003, 26 (6): 1517-1528. |
| [30] | 李昆, 王玲, 李兆华, 等.丰水期洪湖水质空间变异特征及驱动力分析 [J].环境科学, 2015, 36 (4): 1285-1292. |
| [31] | 张成, 陈宏, 王定勇, 等.三峡库区消落带土壤汞形态分布与风险评价[J].环境科学, 2014, 35 (3): 1060-1067. |
| [32] | Cain A, Morgan J T, Brooks N.Mercury policy in the Great Lakes states: past successes and future opportunities [J].Ecotoxicology, 2011, 20 (7): 1500-1511. |
 2015, Vol. 36
2015, Vol. 36


