2. 中国海洋大学海洋环境与生态教育部重点实验室, 青岛 266100
2. Key Laboratory of Marine Environmental Science and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China
HNO3、 HNO2、 HCl和SO2是大气中重要的酸性气体,HNO3和HNO2主要来源于气态污染物NOx在大气中的光化学反应[1]. HCl主要来源于煤炭、 垃圾和生物质燃烧等的一次排放[2,3],还可来源于HNO3气体与海盐气溶胶中NaCl的二次反应[4]. SO2主要来源于化石燃料的燃烧,并通过水相或气相氧化反应生成S(Ⅵ),因大气中H2SO4气体的蒸气压较低,故大部分S(Ⅵ)以颗粒态SO2-4的形式存在[5,6]. NH3是大气中含量最多的碱性气体,主要来源于农业施肥、 畜牧业以及生物质燃烧的排放[7].
大气中NH3与酸性气体发生中和反应生成颗粒态NH4HSO4、 (NH4)2SO4、 NH4NO3、 NH4NO2和NH4Cl[8],这种气-粒转化过程形成的二次气溶胶是大气中PM2.5的重要来源. 大气气溶胶中的化学组分与其气态前体物之间的气-粒平衡关系对区域大气的收支平衡及气体和气溶胶的传输距离有着重要影响[9]. 但目前有关气溶胶的研究多关注其化学组成的分布特征和来源,对气溶胶中化学组分和气态前体物之间平衡关系的观测研究相对较少. 本研究通过对2012年11~12月在青岛采集的大气样品的分析,探讨了大气中酸碱气体和PM2.5中相应化学组分的浓度特征和气-粒平衡关系,并应用ISORROPIA Ⅱ模型评估了PM2.5对前体物排放强度变化的响应程度,这一工作对深入认识PM2.5的来源以及控制因素具有重要意义.
1 样品采集与分析 1.1 样品采集
采样时间为2012年11月1~14日和12月6~20日,每天分别在日间(07:00~19:00)和夜间(19:00~次日07:00)采集2套气态和PM2.5样品,共采集58套样品. 采集地点设在中国海洋大学崂山校区内(36°6′N,120°19′E),采样点周围多树木、 农田,仅邻一条交通干道,人为干扰少. 采样仪器为Thermo Fisher Scientific ChemCombTM Model 3500 PM2.5采样器(含denuder),流量为16.7 L ·min-1. 样品采用聚四氟乙烯滤膜收集,滤膜下衬尼龙膜和石英膜用以捕获采集到膜上的气溶胶在持续采样过程中挥发出来的组分,其中尼龙膜用于捕获HNO3等酸性组分,柠檬酸处理过的石英膜用于捕获NH3等碱性组分. 酸性和碱性气态样品分别采用预先涂布过Na2CO3溶液和柠檬酸溶液的denuder采集. 采样结束后,小心取出两个denuder,分别准确加入20.0 mL Milli-Q水提取吸附在denuder上的气体,提取液转移到洁净的样品瓶中,3种采样膜取出后分别放入洁净的膜盒中,于-20℃保存待分析. 采样前后的denuder和膜的处理均在VD-650超净台(洁净度:≥0.5 μm)中完成[10]. 采样同期记录气温、 相对湿度、 风速和风向等气象参数和天气状况(Micaps天气图资料).
1.2 样品处理及分析取样品于一定体积的Milli-Q水中,在0℃下超声波萃取,萃取液经0.45 μm 滤膜过滤后保存在洁净的样品瓶中. 解冻后的denuder气体样品提取液和PM2.5采样膜萃取液中的阴阳离子采用ICS-3000离子色谱仪(美国戴安公司)分析. 阳离子分析采用CS12A色谱柱,淋洗液为18 mmol ·L-1的甲烷磺酸溶液; 阴离子分析采用AS11-HC色谱柱,淋洗液为NaOH溶液. 详细的分析方法和质量控制见文献[10].
本研究的采样方法可以捕获挥发损失的NH4NO3等组分,文中PM2.5中NH4+和NO3-的浓度分别为聚四氟乙烯滤膜的分析结果与石英膜和尼龙膜分析结果的加和.
1.3 ISORROPIA Ⅱ模型ISORROPIA Ⅱ模型可模拟K+-Ca2+-Mg2+-NH4+-Na+-SO2-4-NO3--Cl--H2O气溶胶系统在稳态(stable)和亚稳态(metastable)下的热力学平衡[11]. 这里稳态是指气溶胶中的盐在水相中达到饱和时即析出,而亚稳态是指盐始终处于水相,而不考虑其饱和析出. 该模型采用“forward problem”和“reverse problem”两种模式推算平衡状态下气溶胶中各种离子和气相中酸碱性气体的浓度. “forward problem”计算模式以NH3、 HNO3、 HCl、 H2SO4、 K、 Ca、 Na、 Mg各组分在气相和气溶胶相中的总浓度,以及气温和相对湿度为输入参数进行模拟计算,“reverse problem”计算模式则以各组分在气溶胶相中的浓度为输入参数进行模拟计算. 本文采用“forward problem”模式模拟稳态下气溶胶系统的热力学平衡.
2 结果与讨论 2.1 青岛大气中酸碱气体的浓度特征
采样期间,青岛大气中酸性气体HNO3、 HNO2、 HCl和SO2浓度平均分别为1.36、 1.64、 1.46和27.58 μg ·m-3; 碱性气体NH3浓度平均为2.95 μg ·m-3(图 1). 与以往青岛的研究结果相比,HNO3平均浓度低于5月但高于6~7月的结果,HNO2浓度高于5~7月的结果,NH3浓度则低于5~7月的结果[10,12]. 与世界其他地区相比(表 1),青岛大气中HNO3、 HNO2和NH3浓度处于较低水平,HCl和SO2浓度则处于较高水平. 采样期间HNO3、 HCl和SO2平均浓度均为日间高于夜间,HNO2浓度则为日间低于夜间,NH3浓度日间略低于夜间(图 1). 独立样本检验结果显示,仅HNO3和HNO2浓度的昼夜差异显著(P<0.05),HCl、 SO2和NH3浓度的昼夜差异均不显著(P>0.05). 这些结果与以往的研究基本一致[1, 13, 14, 15, 16, 17, 18].
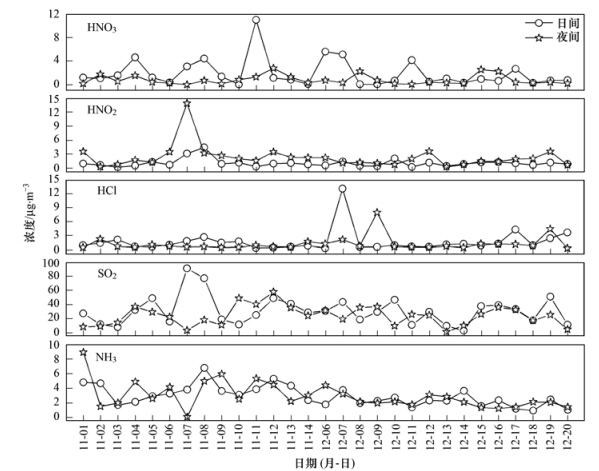 | 图 1 青岛大气中HNO3、 HNO2、 HCl、 SO2和NH3的浓度 Fig. 1 Concentrations of gaseous HNO3,HNO2,HCl,SO2 and NH3 in Qingdao atmosphere |
| 表 1 世界各地大气中HNO3、 HNO2、 HCl、 SO2和NH3浓度的比较 Table 1 Comparison of gaseous HNO3,HNO2,HCl,SO2 and NH3 in different regions atmosphere |
大气中气体和气溶胶的化学组分浓度除与污染物的排放水平有关外,还受到天气条件的影响[12,19],因为天气条件的变化能够影响污染物在大气中的累积、 扩散、 沉降和化学转化等. 根据Micaps天气图资料,采样期间青岛经历了晴天、 阴雨天、 雾天和霾天等4类天气,其中晴天时采集的样品为23个,阴雨天时为11个,雾天时为15个,霾天时为9个. 统计结果显示(图 2),青岛大气中HNO3、 HCl、 SO2和NH3浓度均在霾天时最高,
 | 图 2 不同天气条件下青岛大气中HNO3、HNO2、 HCl、 SO2和NH3的浓度 Fig. 2 Comparison of gaseous HNO3,HNO2,HCl,SO2 and NH3 in atmosphere of Qingdao during different weather conditions |
与晴天时相比分别增加了28%、 84%、 46%和6%. HNO2浓度则在雾天最高,其次是霾天,相比于晴天分别增加了57%和35%. 霾天时,大气中酸碱气体浓度不同程度地增加是由于稳定的大气层有助于污染气体在 大气中累积. HNO3、 HNO2和SO2浓度在阴雨天最低,表明降雨对大气中这3种酸性气体有一定的清除作用. 但NH3在阴雨天的浓度并非最低,这可能是因为非连续型的降雨使土壤湿度增加,土壤微生物的活性增强,从而促进了土壤对NH3的释放能力[12]. HCl的最低浓度出现在雾天,有研究表明,日本神户地区雾天时气溶胶中Cl-浓度往往会升高,原因可能是雾天导致较多的HCl转化为颗粒态Cl-,这也使得雾天时大气中HCl的浓度降低[20].
2.2 PM2.5中水溶性离子的浓度特征观测期间,青岛PM2.5中阴离子NO3-、 NO2-、 Cl-和SO2-4浓度平均分别为6.49、 0.12、 1.95和9.36 μg ·m-3,对PM2.5质量浓度的贡献分别为10.5%、 0.3%、 3.9%和17.1%; 阳离子NH4+浓度平均为6.04 μg ·m-3,对PM2.5质量浓度的贡献为11.0%(图 3). 与以往青岛的研究结果相比,NO3-和NH4+浓度低于6~7月的结果,NO2-浓度略高于6~7月的结果[10]. 与世界其他地区相比(表 2),青岛大气中NO3-、 Cl-、 SO2-4和NH4+浓度处于中等水平,NO2-浓度处于较低水平. 采样期间NO3-、 NO2-、 Cl-、 SO2-4和NH4+平均浓度均为日间略高于夜间(图 3). 但独立样本检验结果显示各离子浓度的昼夜差异均不显著(P>0.05). 这些结果与Lin等[1]、 Chiwa[14]和Shon等[17]在台湾台中、 日本福冈和韩国首尔的研究结果基本一致.
 | 图 3 青岛大气PM2.5及其中NO3-、 NO2-、 Cl-、 SO2-4和NH4+的浓度 Fig. 3 Concentrations of PM2.5 and particulate NO3-,NO2-, Cl-,SO2-4,NH4+ in atmosphere of Qingdao |
| 表 2 世界各地大气PM2.5中NO3-、 NO2-、 Cl-、 SO2-4和NH4+浓度的比较 Table 2 Comparison of particulate NO3-,NO2-,Cl-,SO2-4 and NH4+ in different regions atmosphere |
不同天气条件下青岛PM2.5中水溶性离子浓度的统计结果显示(图 4),NO3-、 SO2-4和NH4+浓度均在霾天、 雾天时较高,晴天、 阴雨天时较低. 相比于晴天,霾天时NO3-、 SO2-4和NH4+浓度分别增加了250%、 143%和115%,雾天时分别增加了145%、 157%、 104%. Cl-浓度与NO3-、 SO2-4和NH4+
的变化趋势一致,但其增幅较低,在霾天和雾天时分别比晴天增加了68%和14%. NO2-浓度在不同天气下相差不大,原因可能是其在大气中不稳定,能以较快速率转化为NO3-的缘故[27]. 雾、 霾天时这些水溶性离子与其气态前体物相比有更高的浓度增幅,说明了雾霾天更有利于气体向颗粒态的转
化而生成PM2.5. 李丽珍等[28]在研究西安大气气溶胶中水溶性离子时也发现,霾天气条件下大气中SO2和NOx向颗粒态SO2-4和NO3-的转化速率比正常天气条件下更快; 王英等[29]在研究北京雾天气溶胶中的无机离子时发现,雾的形成有利于SO2转化为颗粒态SO2-4.
 | 图 4 不同天气条件下青岛大气PM2.5中NO3-、 NO2-、 Cl-、 SO2-4和NH4+的浓度 Fig. 4 Comparison of particulate NO3-,NO2-,Cl-,SO2-4 and NH4+ in atmosphere of Qingdao during different weather conditions |
分析青岛大气PM2.5中NO3-、 NO2-、 Cl-、 SO2-4和NH4+与其气态前体物的相关关系,发现NO3-与HNO3、 NO2-与HNO2及NH4+与NH3无显著相关关系,Cl-与HCl、 SO2-4与SO2的相关关系显著(r=0.40,P<0.01; r=0.32,P<0.05). 这表明Cl-可能主要来自HCl的气粒转化,SO2-4主要与SO2气相氧化生成的H2SO4有关,NO3-、 NO2-和NH4+则除来自HNO3、 HNO2及NH3的非均相反应外,还受到其他源的影响,其形成可能由多种机制共同控制[26, 32]. PM2.5中NO3-、 SO2-4和NH4+彼此之间有显著的相关关系(r>0.84,P<0.01),表明这三者可能经历了相似的二次生成、 转化过程,也可能是经历了相似的累积过程. 大气中NH3与H2SO4和HNO3等酸性气体发生酸碱反应转化为颗粒态的(NH4)2SO4和NH4NO3等,由于H2SO4的蒸气压较低,NH3将优先与其反应,剩余的NH3再与HNO3反应[33]. 比较NH4+和SO2-4的浓度[图 5(a)],发现其比值为3.19(>2),表明气溶胶中的NH4+可以完全中和SO2-4,剩余的NH4+可能与NO3-和Cl-结合. 进一步比较NH4+与NO3-和SO2-4的浓度[图 5(b)],发现其比值为1.01,表明青岛PM2.5中的NH4+除可以完全中和SO2-4外,还可以基本中和所有的NO3-. NH4+-SO2-4-NO3-的三元图显示(图 6),青岛PM2.5中大部分的NH4+与SO2-4结合,即60%左右的NH4+以(NH4)2SO4的形式存在,30%左右的NH4+以NH4NO3的形式存在.
 | 图 5 NH4+与SO2-4和NO3-+2SO2-4浓度的相关关系 Fig. 5 Concentrations of NH4+ versus SO2-4 and sum of NO3-and SO2-4 |
过剩NH3指数(=NH3+NH4+-2SO2-4-NO3--HNO3,μmol ·m-3)可以用来指示NO3-气溶胶的形成是受HNO3或NH3的限制[34]. 当过剩NH3指数<0时,表示NO3-气溶胶的形成受NH3的限制; 相反,当其值>0时,则NO3-气溶胶的形成受HNO3的限制. 计算青岛大气中的过剩NH3指数为0.19 μmol ·m-3,这表明观测期间青岛大气为富NH3环境,且PM2.5中NO3-的生成主要受HNO3气体的限制.
 | 图中的比例以各组分的当量浓度计算图 6 观测期间青岛大气中气溶胶态NH4+、 SO2-4和 NO3-的三元图 Fig. 6 Ternary plots of NH4+,SO2-4 and NO3- in PM2.5 in Qingdao during the study period |
利用ISORROPIA Ⅱ模型,以“forward problem”为主模式模拟稳态下气溶胶系统的热力学平衡. 输入参数中NH3、 HNO3、 HCl为其在气相和气溶胶相中的浓度之和,H2SO4因气相中H2SO4的浓度很低,这里假设为零,故H2SO4为其在气溶胶相中的浓度,K+、 Ca2+、 Na+、 Mg2+等参数为颗粒相中的浓度,气温和相对湿度为每个样品采集期间的平均值. 模拟结果显示(表 3),PM2.5中主要的二次离子NH4+、 NO3-和 SO2-4的模拟值与实测值有很好的相关关系. SO2-4的模拟值与实测值基本相等,平均偏差(MB)和均方根误差(RMSE)均较低,但NH4+和NO3-的模拟值与实测值相差较大,总体上NH4+被低估了26.9%,NO3-被高估了17.8%.
| 表 3 PM2.5中NH4+、 NO3-和 SO2-4的模拟结果 1) Table 3 Model-predicted concentrations of NH4+,NO3- and SO2-4 in PM2.5 |
PM2.5中化学组分与其气态前体物的气粒平衡关系控制着PM2.5的生成,这种平衡关系与前体物的浓度密切相关,其对前体物浓度变化的敏感性可用于评估PM2.5对前体物排放强度变化的响应程度. 尽管ISORROPIA Ⅱ模型模拟青岛PM2.5中NH4+和NO3-浓度有18%~27%的不确定性,但其能很好地模拟出气溶胶中二次离子的变化趋势,因此可以利用该模型进行敏感性实验评价前体物排放强度变化时PM2.5中二次离子的相对变化程度. 本研究中将总H2SO4(TSO4)、 总NH3(TNH3)、 总HNO3(TNO3)的浓度分别改变±20%,模拟青岛大气PM2.5中NH4+、 NO3-和SO2-4的浓度,计算其相对于未加扰动时的模拟浓度的变化率(Δx). 结果显示(表 4),NH4+对TNH3变化±20%的响应不敏感,Δx在±5%以内,但对TSO4和TNO3的变化响应较为敏感,Δx分别为-19.8%和19.4%、 -10.8%和10.2%. NO3-对TSO4和TNH3的变化响应均不敏感,Δx分别在±1.5%和±3.5%以内. NO3-主要受到TNO3浓度变化的影响,TNO3变化±20%时,Δx为20.1%和-20.3%,这可能是因为观测期间青岛 大气为富氨的环境,而NO3-的生成主要受HNO3的 限制,这一结果与Takahama等[35]和Fountoukis等[36]的研究一致. SO2-4仅对TSO4的变化响应敏感,TSO4增加或减少20%时,Δx为±20.0%,这可能是因为大气中的NH3首先与H2SO4反应,且观测期间青岛大气中总NH3的浓度较高,其与SO2-4的
摩尔浓度比值平均为7.1,明显高于2. 这些结果表明,在青岛秋冬季,为降低PM2.5中NO3-的浓度需控制TNO3的排放,降低NH4+的浓度需减少TSO4和TNO3的排放,降低SO2-4的浓度需减少TSO4的排放.
| 表 4 PM2.5中NH4+、 NO3-和SO2-4对前体物浓度变化的敏感性分析 Table 4 Sensitivity of NH4+,NO3- and SO2-4 in PM2.5 to aerosol precursor concentrations |
(1)秋冬季青岛大气中HNO3、 HNO2、 HCl、 SO2和NH3浓度平均分别为1.36、 1.64、 1.46、 27.58和2.95 μg ·m-3. PM2.5中NO3-、 NO2-、 Cl-、 SO2-4和NH4+浓度分别为6.49、 0.12、 1.95、 9.36和6.04 μg ·m-3. 与世界其他地区相比,青岛大气中HNO3、 HNO2和NH3浓度处于较低水平,HCl和SO2浓度处于较高水平; PM2.5中NO2-浓度处于较低水平,其他离子浓度处于中等水平.
(2)霾天时,大气中酸性气体浓度较之晴天时增加28%~84%,NH3浓度仅增加6%,PM2.5中NO3-、 SO2-4和NH4+浓度则增加115%~250%,Cl-浓度增加68%; 雾天时,仅HNO2浓度较之晴天时增加57%,其他气体浓度均低于晴天,PM2.5中NO3-、 SO2-4、 NH4+浓度则增加104%~145%,Cl-浓度增加14%.
(3)PM2.5中SO2-4和Cl-与其气态前体物有显著相关关系,但NO3-、 NO2-和NH4+与其气态前体物相关关系较弱. NO3-、 SO2-4和NH4+彼此之间有显著相关关系,NH4+主要以(NH4)2SO4的形式存在. 青岛为富NH3的大气环境,NO3-的生成受HNO3限制.
(4)应用ISORROPIA Ⅱ模型评估PM2.5中NH4+、 NO3-和SO2-4对前体物排放强度变化的响应. NH4+对TNH3变化响应不敏感,但对TSO4和TNO3变化响应敏感; NO3-和SO2-4则分别仅对TNO3和TSO4变化响应敏感,这暗示了减少TNO3和TSO4而不是TNH3的排放对降低青岛大气中PM2.5浓度更有效.
| [1] | Lin Y C, Cheng M T, Ting W Y, et al. Characteristics of gaseous HNO2, HNO3, NH3 and particulate ammonium nitrate in an urban city of Central Taiwan[J]. Atmospheric Environment, 2006, 40 (25): 4725-4733. |
| [2] | Andreae M O, Atlas E, Harris G W, et al. Methyl halide emissions from savanna fires in southern Africa[J]. Journal of Geophysical Research-Atmospheres, 1996, 101 (D19): 23603-23613. |
| [3] | Kaneyasu N, Yoshikado H, Mizuno T, et al. Chemical forms and sources of extremely high nitrate and chloride in winter aerosol pollution in the Kanto Plain of Japan[J]. Atmospheric Environment, 1999, 33 (11): 1745-1756. |
| [4] | Eldering A, Solomon P A, Salmon L G, et al. Hydrochloric acid: A regional perspective on concentrations and formation in the atmosphere of Southern California[J]. Atmospheric Environment. Part A. General Topics, 1991, 25 (10): 2091-2102. |
| [5] | Luria M, Peleg M, Sharf G, et al. Atmospheric sulfur over the east Mediterranean region[J]. Journal of Geophysical Research, 1996, 101 (D20): 25917-25930. |
| [6] | Stelson A W, Seinfeld J H. Thermodynamic prediction of the water activity, NH4NO3 dissociation-constant, density and refractive index for the NH4NO3-(NH4)2SO4-H2O system at 25℃[J]. Atmospheric Environment, 1982, 16 (10): 2507-2514. |
| [7] | Krupa S V. Effects of atmospheric ammonia (NH3) on terrestrial vegetation: a review[J]. Environmental Pollution, 2003, 124 (2): 179-221. |
| [8] | Baek B H, Aneja V P. Measurement and analysis of the relationship between ammonia, acid gases, and fine particles in Eastern North Carolina[J]. Journal of the Air & Waste Management Association, 2004, 54 (5): 623-633. |
| [9] | Han Y J, Kim S R, Jung J H. Long-term measurements of atmospheric PM2.5 and its chemical composition in rural Korea[J]. Journal of Atmospheric Chemistry, 2012, 68 (4): 281-298. |
| [10] | 李丽平, 石金辉, 李非非, 等. 青岛大气中HNO3、HNO2和NH3以及PM2.5中氮组分的浓度特征和气-粒平衡关系[J]. 环境科学学报, 2014, 34 (11): 2869-2877. |
| [11] | Fountoukis C, Nenes A. ISORROPIA Ⅱ: a computationally efficient thermodynamic equilibrium model for K+-Ca2+-Mg2+-NH4+-Na+-SO42--NO3--Cl--H2O aerosols[J]. Atmospheric Chemistry and Physics, 2007, 7 (17): 4639-4659. |
| [12] | 李非非, 石金辉, 李丽平, 等. 青岛大气中HNO3, HNO2和NH3的浓度及其影响因素[J]. 环境科学学报, 2013, 33 (10): 2671-2678. |
| [13] | Hassan S K, El-Abssawy A A, Khoder M I. Characteristics of gas-phase nitric acid and ammonium-nitrate-sulfate aerosol, and their gas-phase precursors in a suburban area in Cairo, Egypt[J]. Atmospheric Pollution Research, 2013, 4 (1): 117-129. |
| [14] | Chiwa M. Characteristics of atmospheric nitrogen and sulfur containing compounds in an inland suburban-forested site in northern Kyushu, western Japan[J]. Atmospheric Research, 2010, 96 (4): 531-543. |
| [15] | Wu Z J, Hu M, Shao K S, et al. Acidic gases, NH3 and secondary inorganic ions in PM10 during summertime in Beijing, China and their relation to air mass history[J]. Chemosphere, 2009, 76 (8): 1028-1035. |
| [16] | Hu M, Wu Z J, Slanina J, et al. Acidic gases, ammonia and water-soluble ions in PM2.5 at a coastal site in the Pearl River Delta, China[J]. Atmospheric Environment, 2008, 42 (25): 6310-6320. |
| [17] | Shon Z H, Ghosh S, Kim K H, et al. Analysis of water-soluble ions and their precursor gases over diurnal cycle[J]. Atmospheric Research, 2013, 132-133: 309-321. |
| [18] | Biswas K F, Ghauri B M, Husain L. Gaseous and aerosol pollutants during fog and clear episodes in South Asian urban atmosphere[J]. Atmospheric Environment, 2008, 42 (33): 7775-7785. |
| [19] | 乔佳佳, 祁建华, 刘苗苗, 等. 青岛采暖期不同天气状况下大气颗粒态无机氮分布研究 [J]. 环境科学, 2010, 31 (1): 29-35. |
| [20] | Aikawa M, Hiraki T, Suzuki M, et al. Separate chemical characterizations of fog water, aerosol, and gas before, during, and after fog events near an industrialized area in Japan[J]. Atmospheric Environment, 2007, 41 (9): 1950-1959. |
| [21] | Plessow K, Spindler G, Zimmermann F, et al. Seasonal variations and interactions of N-containing gases and particles over a coniferous forest, Saxony, Germany[J]. Atmospheric Environment, 2005, 39 (37): 6995-7007. |
| [22] | Behera S N, Sharma M. Investigating the potential role of ammonia in ion chemistry of fine particulate matter formation for an urban environment[J]. Science of the total Environment, 2010, 408 (17): 3569-3575. |
| [23] | Behera S N, Betha R, Balasubramanian R. Insights into chemical coupling among acidic gases, ammonia and secondary inorganic aerosols[J]. Aerosol and Air Quality Research, 2013, 13 (4): 1282-1296. |
| [24] | Chang L T C, Tsai J H, Lin J M, et al. Particulate matter and gaseous pollutants during a tropical storm and air pollution episode in Southern Taiwan[J]. Atmospheric Research, 2011, 99 (1): 67-79. |
| [25] | Tsai J H, Chang L P, Chiang H L, et al. Size mass distribution of water-soluble ionic species and gas conversion to sulfate and nitrate in particulate matter in southern Taiwan[J]. Environmental Science and Pollution Research, 2012, 20 (7): 4587-4602. |
| [26] | Wei L F, Duan J C, Tan J H, et al. Gas-to-particle conversion of atmospheric ammonia and sampling artifacts of ammonium in spring of Beijing[J]. Science China: Earth Sciences, 2015, 58 (3): 345-355. |
| [27] | Sinha S N, Desai N M, Patel G M, et al. Concentration of nitrite in respirable particulate matter of ambient air in Vadodara, Gujarat, India[J]. Journal of Environmental Biology, 2010, 31 (3): 375-378. |
| [28] | 李丽珍, 沈振兴, 杜娜, 等. 霾和正常天气下西安大气颗粒物中水溶性离子特征[J]. 中国科学院研究生院学报, 2007, 24 (5): 674-679. |
| [29] | 王英, 李令军, 李金香, 等. 北京冬季雾日大气污染结构特征[J]. 环境科学研究, 2009, 22 (9): 1032-1038. |
| [30] | Manigrasso M, Abballe F, Jack R F, et al. Time-resolved measurement of the ionic fraction of atmospheric fine particulate matter[J]. Journal of Chromatographic Science, 2010, 48 (7): 549-552. |
| [31] | Wang Y, Zhuang G S, Zhang X Y, et al. The ion chemistry, seasonal cycle, and sources of PM2.5 and TSP aerosol in Shanghai[J]. Atmospheric Environment, 2006, 40 (16): 2935-2952. |
| [32] | 张婷, 曹军骥, 吴枫, 等. 西安春夏季气体及 PM2.5中水溶性组分的污染特征[J]. 中国科学院研究生院学报, 2007, 24 (5): 641-647. |
| [33] | Shon Z H, Kim K H, Song S K, et al. Relationship between water-soluble ions in PM2.5and their precursor gases in Seoul megacity[J]. Atmospheric Environment, 2012, 59: 540-550. |
| [34] | Blanchard C L, Roth P M, Tanenbaum S J, et al. The use of ambient measurements to identify which precursor species limit aerosol nitrate formation[J]. Journal of the Air & Waste Management Association, 2000, 50 (12): 2073-2084. |
| [35] | Takahama S, Wittig A E, Vayenas D V, et al. Modeling the diurnal variation of nitrate during the Pittsburgh Air Quality Study[J]. Journal of Geophyasical Research, 2004, 109 (D16): D16S06. |
| [36] | Fountoukis C, Nenes A, Sullivan A, et al. Thermodynamic characterization of Mexico City aerosol during MILAGRO 2006[J]. Atmospheric Chemistry and Physics, 2009, 9 (6): 2141-2156." |
 2015, Vol. 36
2015, Vol. 36


