近年来,随着我国城市建设的扩张以及产业布局的调整,大量的工业场地的搬迁、 关停等,例如电镀、 采矿、 冶炼、 燃料和化工等产生的镉(Cd),进入土壤甚至是地下水,影响场地的再次开发使用. Cd是《重金属污染综合防治“十二五”规划》重点监控与污染物排放量控制的5种重金属之一[1]. Cd污染场地的修复已经成为国内研究的热点领域. 化学稳定化是重金属污染土壤的重要修复技术之一,通过添加稳定化药剂降低土壤中活性态重金属的含量. Cd稳定化药剂主要包括碱性材料[2,3]、 含磷材料[4]、 活性炭[5]、 有机物[6]、 铁化合物[7]和黏土矿物[8]. 黏土矿物以其低价环保而受到广泛青睐.
凹凸棒土(凹土,ATP)是一种链层状结构的含水富镁硅酸盐黏土矿物,由于其具有多孔结构、 高比表面积、 特征结构负电荷以及表面富含活性硅醇基等特点,在吸附重金属方面具有独特的优势,被广泛用于水体中重金属的去除以及农田中重金属的钝化[9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20],其吸附机制主要包括阳离子交换和表面的—OH配位反应. 研究发现,改性后的凹土对重金属的吸附能力显著提高. 例如,丙烯酸-丙烯酰胺改性后的凹土能显著提高对水中Pb2+、 Cd2+等的去除[13]; 氨基改性后的凹土显著提高了对水中Cd2+的吸附[14]. 铁离子(Fe2+、 Fe3+)改性凹土多应用在水体和气体中有机物等的催化反应中[15,16],用于重金属的吸附去除的报道较少[17,18],且对吸附机制研究的较少. 目前,尚未见以浸出毒性来评价凹土对土壤中重金属的吸附稳定化的报道.
本研究将Fe3+改性凹土(Fe/ATP),通过Cd与Fe—O、 Fe—OH、 ATP—OH基团形成配位体来显著降低Cd浸出浓度,从而达到稳定化的目的. 本文研究Fe/ATP对土壤中Cd的稳定化效果,通过傅里叶变换显微红外光谱仪(FTIR)、 配备X射线能谱探测器的扫描电子显微镜(SEM-EDAX)、 比表面积分析仪(BET)、 X射线荧光光谱仪(XRD)、 X射线光电子能谱仪(XPS)等手段表征吸附前后凹土和Fe/ATP的形貌和结构特征,探讨稳定化机制. 该制备方法简单、 价格低廉、 处理工艺简单且环境友好,土壤重金属稳定化修复有较好的应用前景. 1 材料与方法 1.1 材料与仪器
Fe(NO3)3 ·9H2O(A.R)、 CdCl2 ·2.5H2O(A.R)、 凹土(A.R)、 盐酸(G.R)、 氢氟酸(G.R)、 硫酸(G.R)和硝酸(G.R)均购自国药集团化学试剂有限公司. 高岭土来自安徽省三二七地质队原料化工厂. 实验使用的仪器包括Barnstead EASY pourⅡ型纯水仪(上海百基生物科技有限公司)、 ACCULAB型电子分析天平(郑州朋来仪器有限公司)、 101型电鼓风干燥箱(北京中兴伟业仪器有限公司)、 SX2-1-10型马弗炉(湖北英山县建力电炉制造有限公司)、 DB-2A 电热板(江苏晨阳电子仪器厂)、 novAA400P火焰原子吸收光谱仪(美国 Perkin Elmer公司). 1.2 Fe/ATP制备与表征
称取80.8 g Fe(NO3)3 ·9H2O溶解于1 L去离子水中,加入100 g 凹土,搅拌浸渍24 h,过滤,去离子水清洗3遍,105℃烘干4 h,400℃焙烧3 h,研磨过200目筛,待用. 称取0.2 g制备好的Fe/ATP于50 mL聚四氟乙烯坩埚中消解,加去离子水润湿,加入10 mL浓盐酸,在120℃电热板加热至残渣变白,逐次加入1 mL HF继续消解至白色溶解,冷却定容至50 mL容量瓶,0.45 μm水相滤头过滤后用原子吸收分光光度计(AAS)测定消解液中Fe的质量分数为9%.
FTIR(ERTE7系列,德国bruker)分析化合物基团及其在分子中的相对位置. SEM-EDAX(Nova 450 Nano,荷兰FEI)获取形貌特征和晶体结构等信息以及元素的组成和相对含量. BET(JW-BK122W型,北京精微高博公司)分析材料的孔道结构参数,采用BJH模型获取孔体积和孔径分布,由BET方程得到样品的比表面积. XRD(RINT 2500,XRD-RigakuU 公司,日本)获取化合物结构特征. XPS(GENESIS型,美国EDAX)获取化学元素成分和分布信息. 1.3 稳定化实验
称取600 g高岭土和0.12 g CdCl2 ·2.5H2O加入750 mL去离子水,搅拌混匀,室温放置3 d. 105℃烘12 h,研磨,室温放置一个月,密封备用. 模拟土样中Cd含量为0.1 mg ·kg-1,浸出浓度为9.8 mg ·L-1. 称取10 g Cd污染土样品,置于500 mL带盖玻璃磨口三角瓶中,分别加入2 g ATP和Fe/ATP,加入20 mL去离子水使得土壤完全浸润,机械搅拌20 min,室温静置24 h后分析Cd的浸出浓度. 浸出浓度的提取方法参考硫酸硝酸法[《固体废物浸出毒性浸出方法硫酸硝酸法》(HJ/T 299-2007)],取1 g土壤,固液比为1 ∶10,在150 r ·min-1下水平振荡浸提18 h,AAS测定浸提液中Cd浓度. 2 凹土和Fe/ATP形貌表征
取1 mg样品与100 mg KBr混合,研磨10 min后,压片10 min制得约1 mm厚的混合压片样品,FTIR光谱扫描范围 400~4000 cm-1. 凹土的吸收峰主要分布在两大区域:4000~1300 cm-1和1200~400 cm-1(图 1). 前者主要是由凹土中的水以及Si—OH、 Al—OH、 Mg—O振动引起,后者则来自凹土骨架振动[19,20]. 凹土中的水包括结构水、 结晶水、 沸石水和吸附水. 制备Fe/ATP过程中经过400℃高温焙烧后脱去吸附水、 沸石水和部分结晶水,但仍保留有结构水和部分结晶水. 因此Fe/ATP上—OH振动峰均有不同程度的减弱. 另一方面,与Al—O和Mg—O键相比,Fe—O键结合更为紧密[21,22],也会导致—OH振动峰的减弱. 凹土骨架振动峰略有偏移,主要是由Fe—O—Fe振动引起[23].
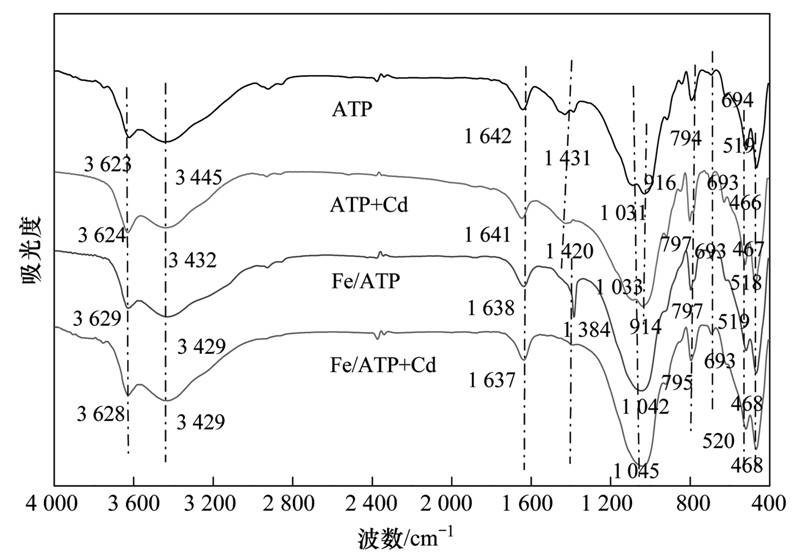 | 图 1 凹土和Fe/ATP吸附Cd前后FTIR图 Fig. 1 FTIR spectra of ATP and Fe/ATP before and after Cd adsorption |
SEM显示凹土呈现坍塌的片层结构夹杂棒束[图 2(a)]. 载铁经高温煅烧后,凹土失水部分结构坍塌. 由于Fe—O的作用力较强,凹土结构收缩,形成多孔状层片结构,片层中夹杂棒束[图 2(b)]. 可观察到Fe3+较均匀地分散在凹土表面. EDAX分析显示Fe与凹土质量比为9%,这与AAS分析结果一致.
BET分析表明(图 3),凹土和Fe/ATP的比表面积分别为142 m2 ·g-1和154 m2 ·g-1,平均孔径分别为12.61 nm和7.56 nm,说明Fe3+改性后,凹土的孔径有所收缩,而比表面积增大,这与SEM图一致.
 | 图 2 凹土和Fe/ATP SEM图 Fig. 2 SEM images of ATP and Fe/ATP |
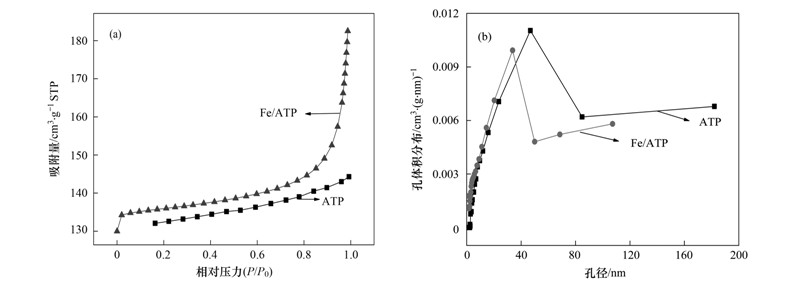 | 图 3 凹土和Fe/ATP的N2吸附等温曲线和孔径分布曲线图 Fig. 3 N2 adsorption isotherms and corresponding pore-size distribution curves of ATP and Fe/ATP |
加入2 g凹土,土壤中Cd的浸出浓度从9.8 mg ·L-1降到了5.1 mg ·L-1(图 4),降低了45%; 而加入2 g Fe/ATP,Cd的浸出浓度下降了91%,表明Fe/ATP对土壤中Cd具有显著的稳定化作用. 研究表明[16, 17, 18],凹土结构中存在大量活性硅醇基(—OH),有利于与重金属形成配位体从而提高对重金属的吸附. 凹土带有负电荷而存在大量晶格缺陷,因此可通过阳离子交换或静电作用吸附重金属. 一般来说,阳离子交换和静电吸附力较弱,经过硫酸硝酸18 h的浸提,吸附的Cd会从凹土中脱附出来再次进入到浸提液中. 因此,凹土对土壤中Cd的稳定化主要来自活性硅醇基和晶格缺陷的贡献. 吸附实验结束后的浸提液中未检测到Fe3+离子,说明Fe/ATP中Fe3+未与土壤中Cd2+发生离子交换. 从图 1可看出,尽管高温焙烧失去了部分结晶水,Fe/ATP但依然保留有—OH基团,这些残留的活性硅醇基可与Cd形成配位体. 吸附结束后,用磁铁吸出部分Fe/ATP进行EDAX分析,结果表明Cd进入凹土晶格(图略). 研究表明[24,25],Cd可通过桥氧形成Fe—O—Cd而稳定在黏土矿物中. 因此,Fe/ATP对土壤中Cd稳定化作用可能主要是硅醇基以及Fe—O中桥氧的贡献.
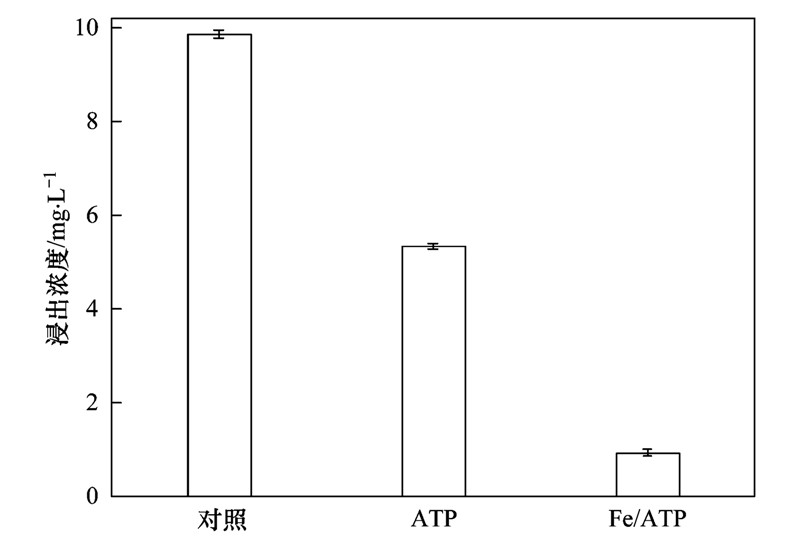 | 图 4 凹土和Fe/ATP对土壤中Cd的浸出浓度影响 Fig. 4 Influence of ATP and Fe/ATP on the leaching concentration of Cd in soil |
为了进一步探讨凹土和Fe/ATP对Cd的吸附机制,将100 mL浓度为100 mg ·L-1 CdCl2溶液分别加入1 g 凹土和Fe/ATP,水浴恒温(25℃),150 r ·min-1水平振荡48 h,离心过滤. FTIR分析吸附后凹土和Fe/ATP中的形貌变化(图 1). 吸附Cd后,凹土中来自—OH和水振动的吸收峰(3445、 1642和916 cm-1)均有不同程度的减弱,而凹土骨架振动引起的吸收峰(794、 519和466 cm-1)则明显增强(图 1). 3445 cm-1是由凹土中Si—OH、 Al—OH、 Mg—OH和H—OH振动引起[19,20]; 1642 cm-1则是δ(H2O)变形所致; 916 cm-1为凹土骨架中与Al3+和Si4+连接的—OH基团的特征吸收峰[19,20]. 吸附Cd后,Cd通过共价键或氢键与—OH或—O结合[10,12][公式(1)],由于结合力增强,削弱了这些特征吸收峰的强度.
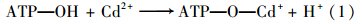
凹土中存在大量晶格缺陷,Cd可进入凹土骨架[公式(2)],使得骨架振动特征峰明显增强.
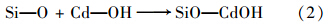
凹土表面带有大量的负电荷,也有利于吸附Cd2+[14],但这种依赖静电吸附的作用力较弱,一般来说,强酸浸出过程中会通过离子交换再次从凹土中脱附出来. 因此,凹土主要是通过结构中存在的水、 —OH基团以及晶格缺陷来稳定土壤中的Cd.
Fe/ATP中Fe3+与凹土晶格中桥氧紧密结合,形成Si—O—Fe、 Fe—O—H聚合物,还有部分成无定型的铁氧化物分散在凹土表面[26]. 研究表明桥氧键具有更高的活性[27],Cd可能进入凹土晶格中和聚合物中的桥氧键结合而被稳定[24][公式(3)~(6)],从FTIR分析可看出(图 1),Fe/ATP吸附Cd后,来自骨架振动的吸收峰发生了显著变化,可能是Cd进入凹土骨架引起. 另外,Cd可与铁氧化物中游离的羟基结合[10,24][公式(7)]:
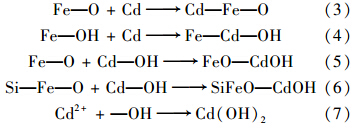
但在强酸浸提的过程中,Cd(OH)2易溶解,因此沉淀反应不能引起浸出浓度的变化. XRD分析表明Fe/ATP吸附Cd后,在30.4°、 37.1°、 48.9°出现明显的Cd(OH)2特征峰(JCPDF 84-1767)(图 5),说明Cd可能是通过配位体的方式稳定在Fe/ATP中30.4°、 50.1°、 58.4°和75.6°出现CdCO3特征峰(JCPDF 85-0989),这是由于Cd与Fe/ATP晶格中的晶格氧结合,易吸收空气中的CO2而形成CdCO3沉淀[12].
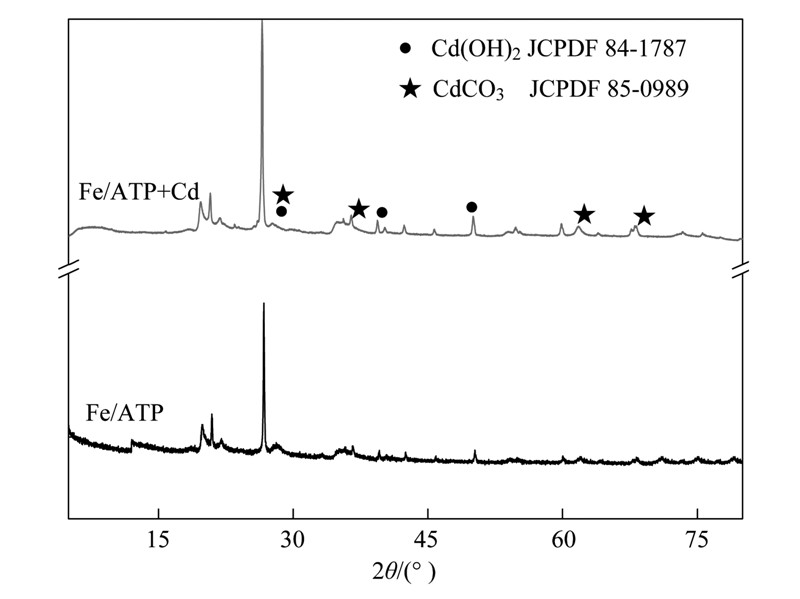 | 图 5 吸附Cd前后Fe/ATP的XRD图 Fig. 5 XRD patterns of Fe/ATP before and after Cd adsorption |
XPS分析也表明,吸附Cd后,Fe/ATP出现Cd3d谱峰(407 eV)[图 6(a)],蒙脱石类黏土吸附Cd2+也出现了类似特征峰[28],该特征峰源于Cd—O键合[29],推测可能由于Fe/ATP中部分Si—O、 Fe—O官能团中桥氧键与Cd键合所致. 吸附Cd后,Fe/ATP中一些铁原子的特征吸收峰也发生了变化[图 6(b)]. 例如,712.3 eV是Fe/ATP晶格中Fe原子的吸收峰[30],该处峰强明显降低,说明Cd进入晶格可能与Fe—O、 Si—Fe—O成键; 711.6 eV源于Fe2O3中的Fe原子[31]吸收峰,位移至711.2 eV,说明吸附Cd可能进入Fe2O3晶格影响其结合能. 从以上XPS谱图分析进一步验证了Cd与凹土中桥氧结合以及铁氧化物吸附稳定机制.
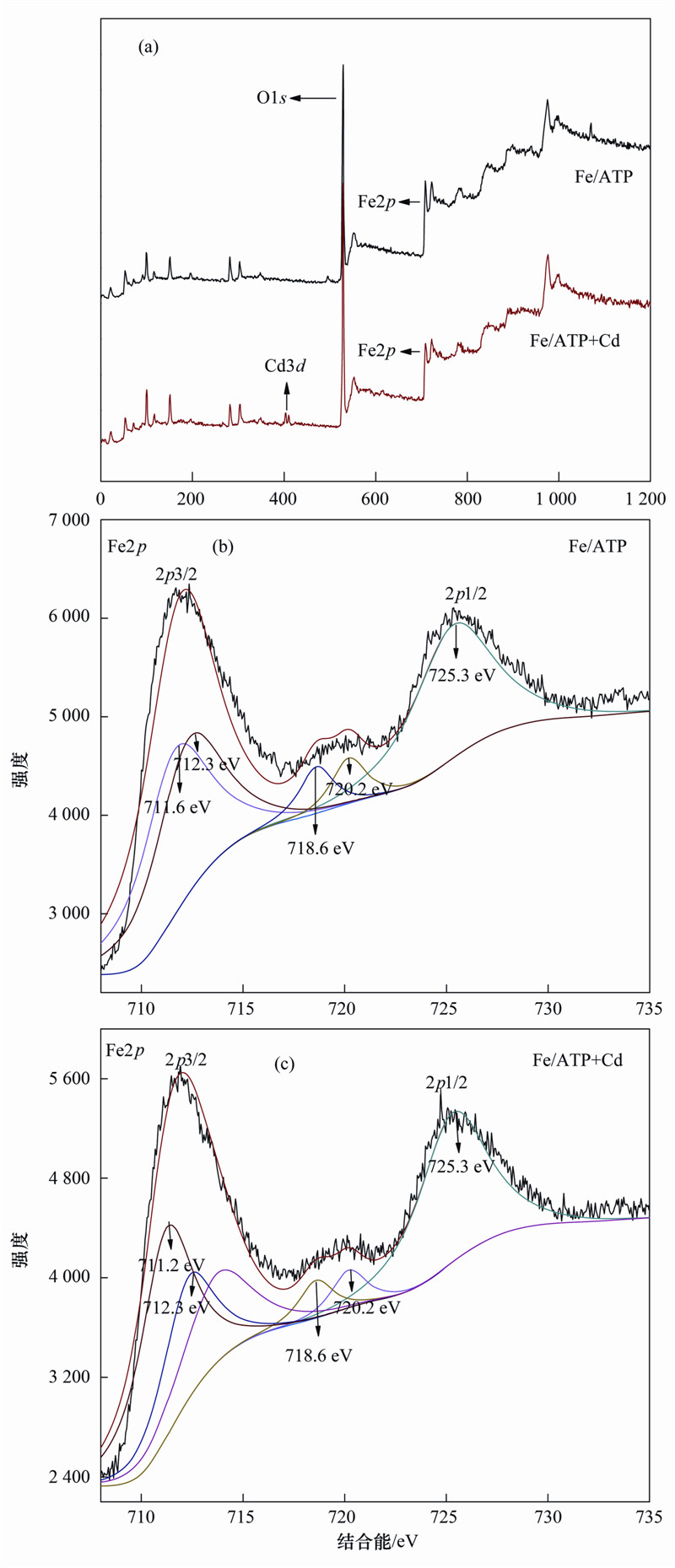 | 图 6 Fe/ATP吸附Cd前后XPS图 Fig. 6 XPS of Fe/ATP before and after Cd adsorption |
(1) 应用浸渍法成功制备了Fe/ATP,载Fe3+后凹土依然保持原有的形貌特征. 部分Fe3+进入凹土晶格,部分则以无定型氧化物形式分散在凹土表面. 与凹土相比,Fe/ATP粒径减小,比表面积增大,吸附性能提高.
(2) 加入20%凹土,土壤中Cd浸出浓度降低45%,主要是由于凹土中水、 —OH基团以及晶格缺陷的贡献; 而加入Fe/ATP,土壤中Cd的浸出浓度降低了91%以上,显著提高了Cd的稳定化. Fe3+与凹土中—OH基团中氧原子以及骨架中氧原子的结合,增加了这些桥氧的活性,有利于结合Cd,形成了—Fe—O—Cd—; 另外Cd与Fe2O3中—O形成配位体也促进了Cd的稳定化.
(3) Fe/ATP制备方法简单,价格低廉,处理工艺简单,对土壤中Cd有较好的稳定效果,在场地重金属稳定化修复中具有较好的应用前景.
| [1] | 中华人民共和国环境保护部和国土资源部. 全国土壤污染状况调查公报[R]. 2014. |
| [2] | Yun S W, Yu C. The leaching characteristics of Cd, Zn, and As from submerged paddy soil and the effect of limestone treatment [J]. Paddy and Water Environment, 2015, 13 (1): 61-69. |
| [3] | 李翔, 宋云, 刘永兵. 石灰干化污泥稳定后土壤中Pb、Cd和Zn浸出行为的研究[J]. 环境科学, 2014, 35 (5): 1946-1954. |
| [4] | Osborne L R, Baker L L, Strawn D G. Lead immobilization and phosphorus availability in phosphate-amended, mine-contaminated soils[J]. Journal of Environmental Quality, 2015, 44 (1): 183-190. |
| [5] | Jha V K, Matsuda M, Miyake M. Sorption properties of the activated carbon-zeolite composite prepared from coal fly ash for Ni2+, Cu2+, Cd2+ and Pb2+[J]. Journal of Hazardous Materials, 2008, 160 (1): 148-153. |
| [6] | Xu Y, Fang S R. Stabilization of heavy metals in contaminated sediments using organic chelating agents[J]. Water Environment Research, 2015, 87 (1): 52-60. |
| [7] | Shaheen S M, Tsadilas C D, Rinklebe J. Immobilization of soil copper using organic and inorganic amendments[J]. Journal of Plant Nutrition and Soil Science, 2015, 178 (1): 112-117. |
| [8] | Sun Y B, Sun G H, Xu Y M, et al. Assessment of natural sepiolite on cadmium stabilization, microbial communities, and enzyme activities in acidic soil[J]. Environmental Science and Pollution Research, 2013, 20 (5): 3290-3299. |
| [9] | Chae H S, Piao S H, Maity A, et al. Additive role of attapulgite nanoclay on carbonyl iron-based magnetorheological suspension[J]. Colloid and Polymer Science, 2015, 293 (1): 89-95. |
| [10] | Han J, Xu Y M, Liang X F, et al. Sorption stability and mechanism exploration of palygorskite as immobilization agent for Cd in polluted soil[J]. Water, Air, & Soil Pollution, 2014, 225 (10): 2160. |
| [11] | Zhang G Y, Lin Y Q, Wang M K. Remediation of copper polluted red soils with clay materials[J]. Journal of Environmental Sciences, 2011, 23 (3): 461-467. |
| [12] | Liang X F, Han J, Xu Y M, et al. In situ field-scale remediation of Cd polluted paddy soil using sepiolite and palygorskite[J]. Geoderma, 2014, 235-236 (4): 9-18. |
| [13] | Liu P, Jiang L P, Zhu L G, et al. Synthesis of covalently crosslinked attapulgite/poly(acrylic acid-co-acrylamide) nanocomposite hydrogels and their evaluation as adsorbent for heavy metal ions[J]. Journal of Industrial and Engineering Chemistry, 2015, 23 : 188-193. |
| [14] | Liang X F, Han J, Xu Y M, et al. Sorption of Cd2+ on mercapto and amino functionalized palygorskite[J]. Applied Surface Science, 2014, 322 : 194-201. |
| [15] | Zhang Z H, Liang H J, Du X G, et al. H2S removal: correlation between performance and loading species of Zn-Fe/attapulgite[J]. Environmental Progress & Sustainable Energy, 2014, 33 (2): 378-384. |
| [16] | Mu B, Wang A Q. One-pot fabrication of multifunctional superparamagnetic attapulgite/Fe3O4/polyaniline nanocomposites served as an adsorbent and catalyst support[J]. Journal of Materials Chemistry A, 2015, 3 (1): 281-289. |
| [17] | Fan Q H, Li P, Chen Y F, et al. Preparation and application of attapulgite/iron oxide magnetic composites for the removal of U(VI) from aqueous solution[J]. Journal of Hazardous Materials, 2011, 192 (3): 1851-1859. |
| [18] | Zhang W P, Xu H B, Wang J, et al. Removal of As (V) from drinking water by attapulgite loaded with Fe (III) adsorbent[J]. Advanced Materials Research, 2013, 750-752 : 1452-1456. |
| [19] | Chen W C, Ding C C, Sun Y B, et al. Fabrication of fungus/attapulgite composites and their removal of U(VI) from aqueous solution[J]. Chemical Engineering Journal, 2015, 269 : 1-8. |
| [20] | Jiang L P, Liu P, Zhao S B. Magnetic ATP/FA/Poly(AA-co-AM) ternary nanocomposite microgel as selective adsorbent for removal of heavy metals from wastewater[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2015, 470 : 31-38. |
| [21] | Panov G I, Starokon E V, Pirutko L V, et al. New reaction of anion radicals O-with water on the surface of FeZSM-5[J]. Journal of Catalysis, 2008, 254 (1): 110-120. |
| [22] | Wichtelová B, Sobaltk Z, Dědeěek J. Redox catalysis over metallo-zeolites: contribution to environmental catalysis[J]. Applied Catalysis B: Environmental, 2003, 41 (1-2): 97-114. |
| [23] | Yu B Y, Kwak S Y. Assembly of magnetite nanocrystals into spherical mesoporous aggregates with a 3-D wormhole-like pore structure[J]. Journal of Materials Chemistry, 2010, 20 (38): 8320-8328. |
| [24] | Soto K T S, Guzmán-Blas R G, Ortiz-Quiles E O, et al. Highly organized nanofiber formation from zero valent iron nanoparticles after cadmium water remediation[J]. RSC Advances, 2014, 5 (4): 2777-2784. |
| [25] | Turapan S, Kongkachuichay P, Worathanakul P. Synthesis and characterization of Fe/SUZ-4 zeolite worathanakul[J]. Procedia Engineering, 2012, 32 : 191-197. |
| [26] | Stockenhuber M, Joyner R W, Dixon J M, et al. Transition metal containing mesoporous silicas-redox properties, structure and catalytic activity[J]. Microporous and Mesoporous Materials, 2001, 44-45 : 367-375. |
| [27] | Hu E, Cheng H F. Catalytic effect of transition metals on microwave-induced degration of atrazine in mineral micropores[J]. Water Research, 2014, 57 : 8-19. |
| [28] | Kim S H, Heo N H, Kim G H, et al. Preparation, crystal structure, and thermal stability of the cadmium sulfide nanoclusters Cd6S4+ and Cd2Na2S4+ in the sodalite cavities of zeolite A(LTA)[J]. The Journal of Physical Chemistry B, 2006, 110 (51): 25964-25974. |
| [29] | Setty M S, Shinha A P B. Characterization of highly conducting PbO-doped Cd2SnO4 thick films[J]. Thin Solid Films, 1986, 144 (1): 7-19. |
| [30] | Seyama H, Soma M. Fe2p spectra of silicate minerals[J]. Journal of Electron Spectroscopy and Related Phenomena, 1987, 42 (1): 97-101. |
| [31] | Zhao Y M, Li Y H, Ma R Z, et al. Growth and characterization of iron oxide nanorods/nanobelts prepared by a simple iron-water reaction[J]. Small, 2006, 2 (3): 422-427. |
 2015, Vol. 36
2015, Vol. 36


