近年来,碳纳米管因其优良的理化特性在众多领域广泛使用,不可避免地进入天然水体,关于碳纳米管的毒性[1]、其在光催化处理有机污染物领域的应用[2, 3]以及作为吸附剂的应用[4, 5]等方面已有大量研究工作,但是它们对天然水体中有机污染物环境行为的影响的研究却十分匮乏[6]. 光化学过程是有机污染物在自然界中发生的重要过程之一,对于其转化和归趋有着极为重要的影响. 而国内外近年来对碳纳米管光化学行为的研究更为关注碳纳米管自身的光化学活性[7, 8, 9, 10, 11, 12, 13, 14],对于碳纳米管与天然水体中的活性物质之间的相互作用的研究较为匮乏. 因此,研究碳纳米管及其与天然水体活性物质共同对有机物光解过程的影响具有较高的理论和实践意义.
天然水体中存在很多光活性物质,如三价铁离子. 偏酸性条件下,三价铁离子主要以Fe(OH)2+形态存在,Fe(OH)2+光照能够产生 ·OH,如式(1)所示[15]. 碳纳米管具有巨大的表面积和表面疏水性,表面带有负电荷,对有机污染物以及金属离子具有很强的吸附能力[16],因此,研究碳纳米管对三价铁离子光化学活性的影响具有很大的意义.

本研究选取了沙丁胺醇(SAL)作为目标污染物. 沙丁胺醇作为广泛使用的临床药物,在环境中广泛检出,一些水体环境中浓度高达471 ng ·L-1[17]. 研究指出SAL对人体的心脏和肝肾具有一定的毒性[18].
本文研究了3种碳纳米管(SCNT、MWNT-OH和MWNT-COOH)对SAL光解的影响,探究CNTs对SAL光解速率的影响;以呋喃甲醇(furfuryl alcohol,FFA)作为单线态氧的分子探针,探讨了CNTs光致产生单线态氧的能力以及单线态氧对SAL光解速率的影响. 通过CNTs与Fe3+的吸附实验探究了碳纳米管与Fe3+之间的相互作用及其对Fe3+光化学活性的影响. 1 材料与方法 1.1 试剂
沙丁胺醇 (Salbutamol,纯度≥98%);色谱级甲醇、异丙醇,购自 Tedia公司;色谱级甲酸,购自美国ROE公司;SCNT(纯度 ≥97%)、 MWNT-OH(纯度≥97%)和 MWNT-COOH(纯度≥97%)购自深圳纳米港有限公司,直径 20~40 nm、长度 5 μm、比表面积 30~50 m2 ·g-1;呋喃甲醇(FFA,纯度≥99%),购自 Sigma-Aldrich公司; Milli-Q超纯水 (Milli-pore,18 MΩ ·cm);其余试剂均为分析纯,购自南京化学试剂有限公司. 1.2 仪器
光化学反应器(XPA-Ⅱ型,配 1000W氙灯,南京胥江机电厂);高效液相色谱仪(Agilent 1200,带紫外检测器,美国);精密 pH计(Sartorius PB-10,德国);TOC分析仪(Shimadzu 2200,日本);紫外可见分光光度仪(Shimadzu UV-2450,日本);火焰原子吸收分光光度计(Thermo M6,美国). 1.3 实验方法
光降解实验在 XPA-Ⅱ型光化学反应器内进行. 采用 1 000 W氙灯(北京电光源研究所)作为模拟太阳光源,并使用光量子测量仪(北京师范大学)测得其在 365 nm处的辐照强度为 350 μW ·cm-2. 氙灯灯管置于一双层玻璃冷阱内部(壁厚 4 mm,可滤除 290 nm以下的紫外光),玻璃冷阱由外接的自来水进行冷却. 溶液装于 50 mL带盖的石英试管(外径 2.8 cm,内径 2.6 cm,长度 18.2 cm),试管垂直并等距置于冷阱外侧. 装置开启后,使氙灯预热 10 min,开始光照反应,定时取样 1 mL,用 0.22 μm孔径水相针式滤器(安谱,中国上海)滤掉碳纳米管后用高效液相色谱分析.
吸附实验在旋转培养仪上进行. 样品溶液置于 40 mL带盖的玻璃吸附瓶,使用橡皮筋固定,以固定速率匀速转动,定时取样 2 mL,用 0.22 μm孔径水相针式滤器(安谱,中国上海)滤掉碳纳米管,滤液使用火焰原子吸收分光光度计或高效液相色谱分析.
SAL的浓度由高效液相色谱分析. 分析条件: Agilent TC-C18色谱柱(250 mm×4.6 mm,i.d.5 μm),柱温 30℃,流动相为甲醇/甲酸(体积比 0.5%)=15/85,流速为 1 mL ·min-1,检测波长为 224 nm,进样量 20 μL.
Fe3+的浓度由火焰原子吸收分光光度计分析. 分析条件:Thermo 空心阴极铁灯,2 mL样品溶液用1%(体积比)硝酸(优级纯)酸化,吸取时间2~3 s,吸收波长248.3 nm. 2 结果与讨论 2.1 CNTs对 SAL降解速率的影响
如图 1所示,SAL的直接光解遵循准一级动力学. 在中性条件(pH=6.5)下,20 μmol ·L-1 SAL直接光解速率为5×10-4 min-1. 在避光条件下,进行碳纳米管对沙丁胺醇的吸附实验,6 h内,SAL在3种碳纳米管分散液中的浓度变化不超过2.4%,实验结果表明3种碳纳米管对SAL无吸附作用. 由表 1中数据可知,3种碳纳米管的存在能够抑制SAL的光解. 为深入探讨3种CNTs对SAL光解的影响机制,本研究着重分析了光屏蔽效应以及自由基作用.
 | 图 1 SAL直接光解 Fig. 1 Direct photolysis of salbutamol cSAL=20 μmol ·L-1,pH=6.5 |
3种碳纳米管在280~330 nm范围具有较强的吸收,与SAL的吸收峰有一定的重叠,可能存在光屏蔽的机制. 因此,在深入探讨CNTs对SAL光解的影响机制时,需要将光屏蔽的影响因素首先扣除. 使用紫外可见分光光度计扫描溶液在280~330 nm的吸光度,代入公式(2),可以计算在某一特定波长下3种碳纳米管对SAL的屏蔽因子Sλ[19, 20]. 然后,利用公式(3)进行计算,可以求得3种碳纳米管在280~330 nm范围内的平均光屏蔽因子.

式中,αλ是特定波长衰减系数(cm-1),l(1.885 cm)是反应中的光程差. 结果如表 1所示. 碳纳米管浓度越高,光屏蔽因子数值越小. 碳纳米管浓度越高,实验测得其吸光度越高,透光率越低,吸收的光子越多,其屏蔽作用越强. 将光屏蔽因子代入公式(4)[21]进行计算,得出不同浓度的3种碳纳米管对SAL光解影响的动力学参数(kCNTs)(表 1).

| 表 1 3种碳纳米管对SAL光降解影响的动力学参数 Table 1 Kinetics parameters of the influence of 3 types of CNTs on the photolysis of salbutamol |
扣除对SAL的光屏蔽作用后,碳纳米管对SAL光降解起促进作用,推测可能是由于碳纳米管光照产生活性氧自由基(ROS). 有研究表明,羧基衍生化单壁碳纳米管(SWCNT-COOH)水溶液在光照条件下可以产生活性氧[7, 8]. 本文选取呋喃甲醇作为检测单线态氧的分子探针,研究MWNT-COOH、MWNT-OH与SCNT产生1 O2的能力,并通过曝气实验验证1 O2对SAL降解的影响.
由公式(5)~(8)可以算出1 O2的稳态浓度(c[1 O2]ss),结果见表 2.

| 表 2 3种碳纳米管光致产生1 O2的稳态浓度 Table 2 Steady state concentrations of 1 O2 generated by three CNTs under irradiation |
为了验证1 O2对SAL降解的影响,本研究采取了曝气实验. 有文献报道多数含苯环的有机污染物激发三重态的能量大于250 kJ ·mol-1,而从3O2激发到1 O2只需要94 kJ ·mol-1,因此在光照条件下,有机物的激发三重态与溶解氧之间可能发生能量转移导致1 O2的产生[23]. 曝氮气可以减少溶液中溶解氧的含量,从而抑制1 O2的产生. 将样品溶液通入氮气30 min,将样品管液封后进行光照实验,曝氮气后SAL的降解速率为3.9×10-4 min-1,比起对照组直接光解速率的6.0×10-4 min-1明显降低,实验证明1 O2对SAL的光解具有促进作用,CNTs可以通过自身光照产生1 O2促进SAL光解. 2.2 CNTs在 Fe3+-SAL体系中对 SAL光解的影响
天然水体中Fe3+具有一定的光化学活性[24]. 在酸性条件下,Fe3+(20 μmol ·L-1)存在时SAL的降解速率(66.2×10-4 min-1)明显高于其直接光解速率(4.3×10-4 min-1);加入足量的 ·OH淬灭剂异丙醇(100 mmol ·L-1)后,SAL的降解速率明显降低,如图 2所示,证明三价铁离子在酸性条件下主要是通过光致产生 ·OH,加速SAL的降解.
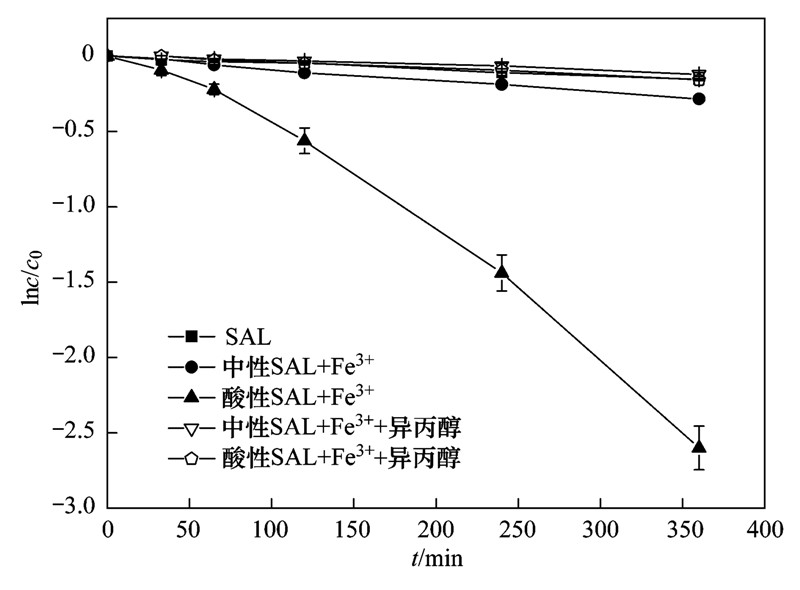 | 图 2 Fe3+对SAL光解的影响 Fig. 2 Influence of Fe3+ on the photodegradation of salbutamol cFe3+=20 μmol ·L-1,cSAL=20 μmol ·L-1, c异丙醇=100 mmol ·L-1,酸性pH=3.5,中性pH=6.5 |
加入MWNT-OH和MWNT-COOH后,与对照组相比,SAL的降解明显受到了抑制,如图 3所示. 碳纳米管是由石墨层构成,具有大量π—π共轭电子,表面带负电荷,Fe3+带正电,易与碳纳米管表面发生 静电吸附,从而影响其光化学活性. 基于碳纳米管 对金属离子的吸附效应,在环境领域中,将碳纳米管应用于吸附去除水体中的重金属离子(Fe3+、Pb2+、Cu2+、Cr3+等)的技术也日趋成熟[25, 26, 27, 28].
 | 图 3 MWNT-COOH与MWNT-OH对Fe-SAL体系中SAL光降解的影响 Fig. 3 Influence of MWNT-COOH and MWNT-OH on the photodegradation of salbutamol in the presence of Fe3+ cFe3+=20 μmol ·L-1,cSAL=20 μmol ·L-1,pH=3.5 |
以MWCNT-COOH为例,图 4是吸附实验中测得Fe3+在CNTs分散液中的浓度变化,在100 min内,Fe3+的浓度由20 μmol ·L-1降到10 μmol ·L-1,然后达到吸附平衡,浓度趋于稳定,从而推出在CNTs与Fe3+混合后发生静电吸附,被吸附到碳纳米管表面的Fe3+失去光化学活性.
 | 图 4 MWNT-COOH分散液中Fe3+的浓度变化 Fig. 4 Change of the Fe3+ concentration in MWNT-COOH dispersion cFe3+=20 μmol ·L-1,pH=3.5 |
(1)SAL的直接光解符合准一级反应动力学;SCNT、MWNT-COOH、MWNT-OH能通过光屏蔽效应抑制SAL光解,且CNTs浓度越大,SAL降解速率越慢.
(2)SCNT、MWNT-COOH、MWNT-OH在光照下能产生稳态浓度10-14 mol ·L-1的1 O2,并通过1 O2促进SAL的光降解.
(3)CNTs对SAL光解的影响有两种机制:光屏蔽效应及自由基作用. 在较高(10 mg ·L-1)及较低浓度(0.1 mg ·L-1)的CNTs环境中,光屏蔽效应占主导地位;在1mg ·L-1的浓度下,两者比较接近.
(4)酸性条件下Fe3+能产生 ·OH从而促进SAL光解. MWNT-COOH、MWNT-OH通过静电吸附抑制Fe3+的光化学活性,从而影响SAL的光解速率.
| [1] | 禹露, 唐志强, 梁跃, 等. 碳纳米管材料的释放途径、生态毒性及环境归趋[J]. 化工新型材料, 2014, 42 (8): 1-3, 25. |
| [2] | 续丽丽, 李巧玲, 万郁楠, 等. Ag-TiO2/CNTs的复合及光催化性能[J]. 化工新型材料, 2014, 42 (3): 114-117. |
| [3] | Mahmoodi N M. Synthesis of magnetic carbon nanotube and photocatalytic dye degradation ability[J]. Environmental Monitoring and Assessment, 2014, 186 (9): 5595-5604. |
| [4] | 赵兴兴, 于水利, 王哲. 氧氟沙星在碳纳米管上的吸附机制研究[J]. 环境科学, 2014, 35 (2): 663-668. |
| [5] | 徐立恒, 张明, 陈锋. 碳纳米管基复合吸附剂的制备及其吸附性能[J]. 环境科学学报, 2014, 34 (6): 1443-1448. |
| [6] | Wiesner M R, Lowry G V, Jones K L, et al. Decreasing uncertainties in assessing environmental exposure, risk, and ecological implications of nanomaterials[J]. Environmental Science & Technology, 2009, 43 (17): 6458-6462. |
| [7] | Chen C Y, Jafvert C T. Photoreactivity of carboxylated single-walled carbon nanotubes in sunlight: reactive oxygen species production in water[J]. Environmental Science & Technology, 2010, 44 (17): 6674-6679. |
| [8] | Chen C Y, Jafvert C T. The role of surface functionalization in the solar light-induced production of reactive oxygen species by single-walled carbon nanotubes in water[J]. Carbon, 2011, 49 (15): 5099-5106. |
| [9] | Bitter J L, Yang J, Milani S B, et al. Transformations of oxidized multiwalled carbon nanotubes exposed to UVC (254 nm) irradiation[J]. Environmental Science: Nano, 2014, 1 (4): 324-337. |
| [10] | Humeres E, de Souza E P, Debacher N A, et al. Photolysis of Phenylalanine in the Presence of Oxidized Carbon Nanotubes[J]. Langmuir, 2015, 31 (1): 164-170. |
| [11] | Hou W C, BeigzadehMilani S, Jafvert C T, et al. Photoreactivity of Unfunctionalized Single-Wall Carbon Nanotubes Involving Hydroxyl Radical: Chiral Dependency and Surface Coating Effect[J]. Environmental Science & Technology, 2014, 48 (7): 3875-3882. |
| [12] | Maeda Y, Hasuike Y, Ohkubo K, et al. Photochemical Behavior of Single-Walled Carbon Nanotubes in the Presence of Propylamine[J]. Chemphyschem, 2014, 15 (9): 1821-1826. |
| [13] | Qu X L, Alvarez P J J, Li Q L. Photochemical Transformation of Carboxylated Multiwalled Carbon Nanotubes: Role of Reactive Oxygen Species[J]. Environmental Science & Technology, 2013, 47 (24): 14080-14088. |
| [14] | Hwang Y S, Qu X L, Li Q L. The role of photochemical transformations in the aggregation and deposition of carboxylated multiwall carbon nanotubes suspended in water[J]. Carbon, 2013, 55 : 81-89. |
| [15] | Sedlak D L, Hoigne J. The role of copper and oxalate in the redox cycling of iron in atmospheric waters[J]. Atmospheric Environment. Part A. General Topics, 1993, 27 (14): 2173-2185. |
| [16] | Gao J, Xu D D, Ma L L, et al. Research progress in the adsorption of pollutants on carbon nanotubes in water[J]. New Chemical Materials, 2011, 39 (11): 6-8. |
| [17] | Bound J P, Voulvoulis N. Predicted and measured concentrations for selected pharmaceuticals in UK rivers: Implications for risk assessment[J]. Water Research, 2006, 40 (15): 2885-2892. |
| [18] | Libretto S E. A review of the toxicology of salbutamol(albuterol)[J]. Archives of Toxicology, 1994, 68 (4): 213-216. |
| [19] | Guerard J J, Miller P L, Trouts T D, et al. The role of fulvic acid composition in the photosensitized degradation of aquatic contaminants[J]. Aquatic Sciences, 2009, 71 (2): 160-169. |
| [20] | Miller P L, Chin Y P. Photoinduced degradation of carbaryl in a wetland surface water[J]. Journal of Agricultural and Food Chemistry, 2002, 50 (23): 6758-6765. |
| [21] | Zeng C, Ji Y F, Zhou L, et al. The role of dissolved organic matters in the aquatic photodegradation of atenolol [J]. Journal of Hazardous Materials, 2012, 239-240 (18): 340-347. |
| [22] | Haag W R, HoignéJ, Gassman E, et al. Singlet Oxygen in Surface Waters—Part 1: Furfuryl alcohol as a trapping agent[J]. Chemosphere, 1984, 13 (5-6): 631-640. |
| [23] | Zepp R G, Hoigne J, Bader H. Nitrate-induced photooxidation of trace organic-chemicals in water[J]. Environmental Science & Technology, 1987, 21 (5): 443-450. |
| [24] | 邓南圣, 吴峰. 环境光化学[M]. 北京: 化学工业出版社, 2003. |
| [25] | 许乾慰, 陈丽丽. 表面活性剂对多壁碳纳米管吸附Pb2+的影响[J]. 环境污染与防治, 2009, 31 (3): 44-47, 51. |
| [26] | 王红娟, 周爱林, 梁家华. 改性多壁碳纳米管对Pb2+, Cu2+ 和Co2+的竞争吸附研究[J]. 化工环保, 2009, 28 (6): 482-486. |
| [27] | 杨迎春, 张丽, 冉静, 等. 改性碳纳米管对Fe3+的吸附研究[J]. 环境科学与技术, 2006, 29 (Z1): 1-2, 39. |
| [28] | Sun W L, Xia J, Shan Y C. Comparison kinetics studies of Cu(Ⅱ) adsorption by multi-walled carbon nanotubes in homo and heterogeneous systems: Effect of nano-SiO2[J]. Chemical Engineering Journal, 2014, 250 : 119-127. |
 2015, Vol. 36
2015, Vol. 36



