2. 中国科学院大学化学与化学工程学院, 北京 100049
2. College of Chemistry and Chemical Engineering, University of Chinese Academy of Sciences, Beijing 100049, China
硫化物是表示水体质量的重要参数之一,其存在能够消耗水体中的氧气,导致水生生物的死亡[1,2]. 在有机物丰富、 pH值较低的水域,硫化物极易生成具有恶臭气味的有毒气体H2S. 一方面,H2S是生成具有强腐蚀性物质硫酸的前驱体,对环境有很大的危害; 而且还是一种强烈的神经毒素,人体吸入不同浓度的H2S会产生头痛、 头晕、 呕吐、 顷刻死亡等症状,严重威胁着人类的生存与发展[3, 4, 5]. 但是另一方面,有研究表明,H2S是除了一氧化氮(NO)和一氧化碳(CO)之外的第3种气体信号分子,具有调剂免疫系统和器官功能、 保护神经细胞和维持机体氧化还原平衡等重要作用,与许多生理病理学过程密切相关[6, 7, 8]. 因此,对H2S进行快速、 灵敏、 准确的检测十分重要.
常规的检测H2S的方法主要有电化学法[9]、 比色法[10]、 分光光度法[11,12]、 色谱法[13,14]等. 这些方法常常要对样品进行复杂的预处理和昂贵的仪器,步骤繁琐,耗时长. 而荧光分析法具有灵敏度高、 选择性好、 检测限低、 操作简单和可原位实时检测等优点,近年来在环境领域中的应用越来越得到科研工作者的关注[15, 16, 17, 18]. 利用荧光探针检测各种环境污染物如Cu2+、 Hg2+、 CN-、 F-、 I-等[19,20]的研究都已多次被报道. 本研究利用H2S具有较强的亲核性,可促使含有吸电子基团的醚键断裂的特性,设计合成了一种新型的可视化H2S荧光探针1(图 1). 探针1可通过2-(2′-羟基苯基)苯并咪唑(HBI)与4-氯-7-硝基苯并呋喃(NBD-Cl)反应所得. HBI及其衍生物可以发生激发态分子内质子转移(ESIPT)过程而形成互变异构体,从而产生发射波长长、 stokes 位移大、 荧光量子产率高的特征荧光. 此类化合物已被广泛地应用于荧光探针的设计. 但是有关H2S荧光探针的报道还较少[21, 22, 23].
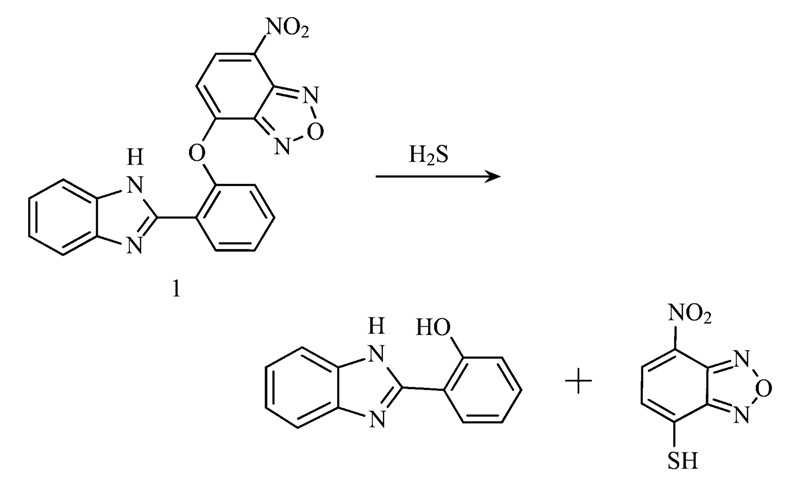 | 图 1 探针1与H2S反应机制
Fig. 1 Detection mechanism of probe 1 for H2S
|
化合物的1H NMR和13 C NMR谱图从Bruker 400 MHz 核磁共振仪(DMSO-d6为溶剂,TMS为内标)得到; 分子的质谱从Brooker maXis 4G质谱仪得到; 使用日本Hitachi F-7000荧光分光光度计测试荧光发射光谱(狭缝宽度为2.5 cm); 用Mettler toledo pH计测试pH值.
邻苯二胺、 水杨醛、 亚硫酸氢钠、 4-氯-7-硝基-苯并呋喃、 碳酸钾,以上试剂均为分析纯,使用之前未经预处理纯化. 实验用水为MilliQ系统制备的超纯水. 1.2 实验过程
目标化合物1的合成路线见图 2.
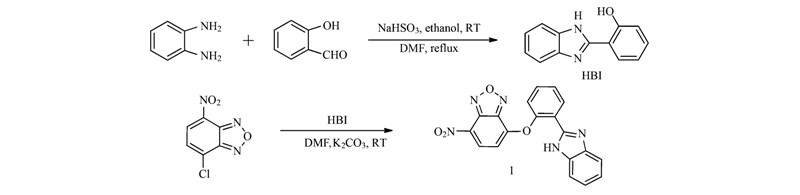 | 图 2 探针1的合成
Fig. 2 Synthesis of probe 1
|
将水杨醛(0.61 g,5 mmol)和亚硫酸氢钠(0.52 g,5 mmol)置于100 mL三口烧瓶中,加入20 mL无水乙醇溶解,室温下搅拌4 h. 然后将邻苯二胺(0.54 g,5 mmol)溶解在20 mL DMF中,滴加到上述溶液,加热回流并用TLC监测. 反应完成后,将反应物倒入冰水中,析出沉淀,抽滤,干燥,无水乙醇重结晶得到白色中间体HBI 0.788 g,产率75%. 1H NMR(DMSO,400 MHz),δ: 13.20(s,1H),13.16(s,1H),8.06(d,J=6.8 Hz,1H),7.72(d,J=6.4 Hz,1H),7.61(d,J=6.4 Hz,1H),7.73~7.29(m,3H),7.05~7.00(m,2H); 13 C NMR(DMSO,100 MHz),δ: 158.0,151.7,140.8,133.1,131.7,126.2,123.3,122.4,119.1,117.9,117.2,112.6,111.5; ESI-HRMS(C13H10N2 O计算值),m/z: 211.0876(211.0866) [M+H]+. 1.2.2 目标化化合物1的合成
将上述得到的中间体HBI 0.21 g(1 mmol)、 NBD-Cl 0.22 mg(1.1 mmol)和碳酸钾0.28 g(2 mmol)置于50 mL单口烧瓶中,加入DMF(5 mL),室温下搅拌2.5 h. 反应完毕后水洗、 干燥、 浓缩,经硅胶柱层析提纯(乙酸乙酯/石油醚=4/1),得到黄色固体0.26 g,产率71%. 1H NMR(DMSO-d6,400 MHz),δ: 9.91(s,1 H),8.74(d,J=8.0 Hz,1H),7.85(d,J=8.0 Hz,1H),7.64(dd,J1=1.2 Hz,J2=7.6 Hz,1H),7.61(d,J=7.6 Hz,1H),7.43~7.37(m,2H),7.34~7.27(m,2H),6.95(t,J=7.6 Hz,1H),6.68(d,J=8.0 Hz,1H); 13 C NMR(DMSO-d6,100 MHz),δ: 155.0,151.4,147.8,144.0,142.4,135.5,135.2,132.7,132.2,131.9,131.6,127.1,123.8,123.4,119.6,119.3,116.1,115.7,111.5; ESI-HRMS(C19H11N5O4计算值),m/z: 372.0698(372.0727) [M-H]-. 1.3 实验方法 1.3.1 标准液的配制
用去离子水新鲜配制 1.0 mmol ·L-1的硫化钠(Na2S)标准溶液(实验中常用的H2S供体); 用DMSO配备1.0 mmol ·L-1的探针储备液; 干扰离子检测液(0.1 mol ·L-1)采用该阴离子的钠盐或钾盐溶于去离子水得到; 配制磷酸盐缓冲溶液(PBS,pH=7.4)/DMSO(体积比1 ∶1)的测试溶液. 1.3.2 光谱测试
用移液枪准确移取适量体积Na2S标准溶液于比色管中,用PBS/DMSO测试溶液调节体积到3.96 mL. 将0.04 mL探针储备液加入检测体系中,使探针的浓度为10 μmol ·L-1,充分混匀,室温下放置5 min. 移取3 mL加入1 cm石英比色皿测其光谱数据. 2 结果与讨论
化合物1本身在检测体系中荧光很弱,加入Na2S后,荧光信号大幅度增加,溶液颜色也瞬间由淡黄色变成了肉眼可见的紫色,通过肉眼即可判断溶液中是否存在H2S. 通过三维激发-荧光发射光谱矩阵(3D-EEM),确定探针的最佳激发/发射波长为320/460 nm. 从图 3中可以看出,在10 μmol ·L-1的探针溶液中加入20 μmol ·L-1Na2S后,在360 nm和460 nm处分别出现了新的荧光发射峰. 360 nm、 460 nm是HBI的荧光发射峰. 由于HBI是一类具有激发态质子转移效应的化合物,存在烯醇式和酮式两种构型. 360 nm处是烯醇式构型分子的发射峰,460 nm是酮式构型的发射峰[24,25]. 因为检测体系(DMSO/PBS=1/1)具有极性,HBI大部分以酮式构型存在,烯醇式构型很少,因此360 nm处的荧光发射峰很弱.
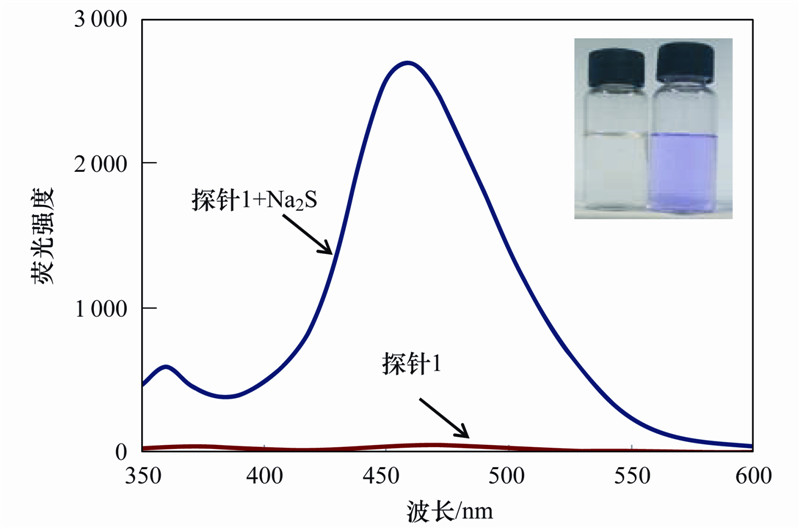 | 图 3 室温下加入Na2S前后探针1荧光强度与颜色的变化
Fig. 3 Fluorescence and colour changes of probe 1 before and after adding Na2S at room temperature
|
室温下,取80 μL的Na2S标准溶液加入比色管中,用DMSO/PBS测试溶液调节体积到3.96 mL,加入40 μL探针标准液,得到探针浓度为10 μmol ·L-1和Na2S浓度为20 μmol ·L-1的溶液,测定体系荧光强度变化和时间的关系曲线. 由图 4可以看出,探针1在460 nm处的荧光强度在加入Na2S 后增加很快,5 min之后变化很小,几乎形成了一个平台,表明反应基本完成. 探针1本身在测试的20 min之内没有明显的变化. 因此,本研究选择探针1与H2S反应5 min之后进行测试. 与文献报道的大部分H2S荧光探针(响应时间一般为20 min~2 h)相比,探针1能够更快速地检测H2S. 鉴于H2S不稳定和在生物体系中代谢迅速的特点,探针1在实时检测上具有较大的优势[26,27].
 | 图 4 室温下加入Na2S后探针1在460 nm处荧光强度随时间的变化
Fig. 4 Time-dependent fluorescence spectra of probe 1 on reaction with Na2S at room temperature
|
实验中用盐酸和氢氧化钾调节溶液的pH,待pH稳定后,向该溶液中加入Na2S,充分混匀放置5 min 后进行荧光测试. 同时以探针1的空白溶液作为对照. 图 5为加入Na2S之前和加入Na2S之后探针1在其最大发射波长460 nm处的荧光强度与pH在3~11之间的关系曲线. 从中可以看出,在6~9之间,探针1的荧光强度比较稳定. 加入Na2S后,荧光强度的增加远远大于探针所引起的荧光的变化. 因此可将pH 6~9作为探针的可靠检测范围. 在此范围内,探针自身带来的荧光变化可不予考虑.
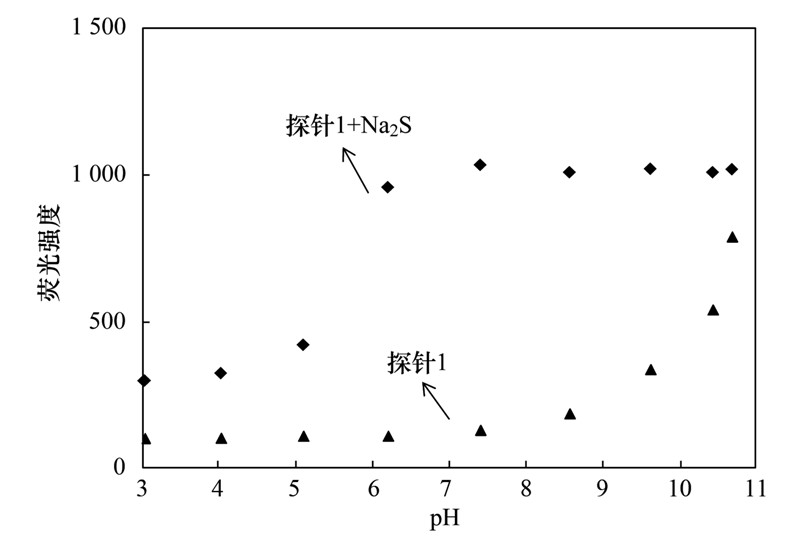 | 图 5 探针1+Na2S/探针1在不同pH值条件下在460 nm处的荧光强度
Fig. 5 Fluorescence intensity of probe 1+Na2S/probe 1 at 460 nm under different pH
|
图 6为测试体系中,探针1对不同浓度Na2S响应的荧光发射光谱. 从中可以看出,当Na2S的浓度从0增加到50 μmol ·L-1,探针1在460 nm处的荧光强度逐渐增强,增强倍数大于100倍. 在0~10 μmol ·L-1浓度范围内,Na2S浓度和荧光强度呈现良好的相关性,相关系数R2=0.99. 探针1对H2S的检测限为6 μmol ·L-1(S/N=3).
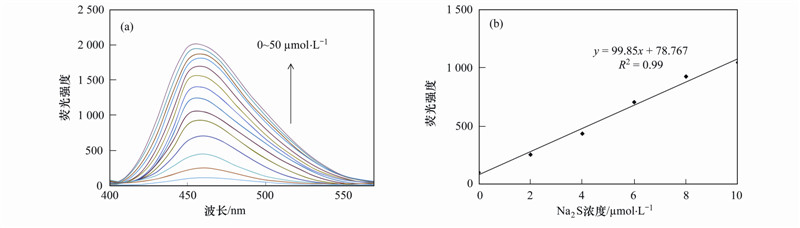 | 从下到上,Na2S 的浓度分别为0、 2、 4、 6、 8、 10、 15、 20、 25、 30、 35、 40、 45、 50 μmol ·L-1图 6 探针1与Na2S的荧光滴定曲线
Fig. 6 Fluorescence titration curves of probe 1 with Na2S
|
为了测试探针对H2S的选择性,笔者考察了一些常见的阴离子 F-、 Cl-、 Br-、 I-、 CO2-3、 HCO-3、 HPO2-4、 NO-2、 NO-3、 SO2-4、 CH3COO-、 SO2-3、 S2O2-3、 CN-、 citrate和N-3对荧光强度的影 响(图 7),探针浓度为10 μmol ·L-1,各阴离子浓度均为1mmol ·L-1. 加入上述离子后,体系在460 nm处的荧光强度没有明显的变化. 而加入20 μmol ·L-1的Na2S后,荧光强度迅速增加. 同时,即使存在高浓度的其他阴离子,探针对Na2S的荧光响应也不受明显的影响. 这些结果表明,探针1能够很好地区分H2S和其他阴离子,对H2S的检测具有很高的选择性.
 | 从1~16离子分别是: F-、 Cl-、 Br-、 I-、 CO2-3、 HCO-3、 HPO2-4、 NO-2、 NO-3、 SO2-4、 CH3COO-、 SO2-3、
S2O2-3、 CN-、 citrate和N-3; 白色柱: 探针1+阴离子,黑色柱: 探针1+阴离子+Na2S图 7 探针1的离子选择性研究
Fig. 7 Study on ion selectivity of probe 1
|
在探针浓度一定时,体系的颜色和Na2S的浓度有关. 由图 8可以看出,随着Na2S浓度的增加,体系颜色逐渐加深,当Na2S的浓度增加到3 μmol ·L-1时,体系的颜色变化是肉眼可见的,说明探针1可以作为一个可视化荧光探针用于检测H2S. 基于探针颜色的变化与Na2S浓度之间的相关性,可以制作一张比色图表(图 9),通过肉眼对比检测体系和比色表的颜色,可以简便、 快速地实现H2S的半定量检测.
 | 从左到右Na2S浓度为0、 2、 3、 5、 10、 30、 50 μmol ·L-1图 8 随Na2S浓度的增加探针1颜色的变化
Fig. 8 “Naked-eye” color changes of probe 1 upon
addition of different concentrations of Na2S
|
 | 从左到右Na2S浓度为0、 3、 10、 30、 50 μmol ·L-1图 9 根据不同浓度Na2S溶液的颜色制备的比色图表
Fig. 9 Prepared color chart according to the solution
color with different concentrations of Na2S
|
以2-(2′-羟基苯基)苯并咪唑为荧光团,基于H2S较强的亲核性,可使NBD醚键发生断裂的特性,设计并合成了一种新型的可视化检测H2S的荧光探针. 该探针的可视化检测限为3 μmol ·L-1,荧光检测限为6 μmol ·L-1. 由于HBI是激发态分子内质子转移化合物,因此探针具有较大的Stokes位移(约100 nm),有利于降低检测中激发的干扰. 该探针对H2S的选择性好,不易受其他阴离子的干扰; 响应时间短,5 min可完成检测; 在pH 6~9范围内,探针仍然表现出较好的荧光响应. 该探针为H2S的检测提供了一种新的有效方法.
| [1] | Orem W, Gilmour C, Axelrad D, et al. Sulfur in the south florida ecosystem: distribution, sources, biogeochemistry, impacts, and management for restoration[J]. Critical Reviews in Environmental Science and Technology, 2011, 41 (S1): 249-288. |
| [2] | Riesch R, Plath M, Schlupp I, et al. Colonisation of toxic environments drives predictable life-history evolution in livebearing fishes(Poeciliidae)[J]. Ecology Letters, 2014, 17 (1): 65-71. |
| [3] | 钱东升, 房俊逸, 陈东之, 等. 板式生物滴滤塔高效净化硫化氢废气的研究[J]. 环境科学, 2011, 32 (9): 2786-2793. |
| [4] | 李华琴, 何觉聪, 陈洲洋, 等. 低温等离子体-生物法处理硫化氢气体研究[J]. 环境科学, 2014, 35 (4): 1256-1262. |
| [5] | Yeatts K B, El-Sadig M, Leith D, et al. Indoor air pollutants and health in the United Arab Emirates[J]. Environmental Health Perspectives, 2012, 120 (5): 687-694. |
| [6] | Dongo K, Tiembré I, Koné B A, et al. Exposure to toxic waste containing high concentrations of hydrogen sulphide illegally dumped in Abidjan, Cte dIvoire[J]. Environmental Science and Pollution Research, 2012, 19 (8): 3192-3199. |
| [7] | di Villa Bianca R E, Sorrentino R, Mirone V, et al. Hydrogen sulfide and erectile function: a novel therapeutic target[J]. Nature Reviews Urology, 2011, 8 (5): 286-289. |
| [8] | 黄德乾, 李东伟, 唐杰, 等. 内源H2S生理学作用的研究进展[J]. 环境化学, 2011, 30 (1): 194-199. |
| [9] | Schiavon G, Zotti G, Toniolo R, et al. Electrochemical detection of trace hydrogen sulfide in gaseous samples by porous silver electrodes supported on ion-exchange membranes(solid polymer electrolytes)[J]. Analytical Chemistry, 1995, 67 (2): 318-323. |
| [10] | Choi M G, Cha S, Lee H, et al. Sulfide-selective chemosignaling by a Cu2+ complex of dipicolylamine appended fluorescein[J]. Chemical Communications, 2009, 45 (47): 7390-7392. |
| [11] | Guenther E A, Johnson K S, Coale K H, et al. Direct ultraviolet spectrophotometric determination of total sulfide and iodide in natural waters[J]. Analytical Chemistry, 2001, 73 (14): 3481-3487. |
| [12] | Kass M, Ivaska A. Spectrophotometric determination of sulphur dioxide and hydrogen sulphide in gas phase by sequential injection analysis technique[J]. Analytica Chimica Acta, 2001, 449 (1-2): 189-197. |
| [13] | Bramanti E, D'Ulivo L, Lomonte C, et al. Determination of hydrogen sulfide and volatile thiols in air samples by mercury probe derivatization coupled with liquid chromatography-atomic fluorescence spectrometry[J]. Analytica Chimica Acta, 2006, 579 (1): 38-46. |
| [14] | Ubuka T, Abe T, Kajikawa R, et al. Determination of hydrogen sulfide and acid-labile sulfur in animal tissues by gas chromatography and ion chromatography[J]. Journal of Chromatography B: Biomedical Sciences and Applications, 2001, 757 (1): 31-37. |
| [15] | Ren X M, Guo L H. Assessment of the binding of hydroxylated polybrominated diphenyl ethers to thyroid hormone transport proteins using a site-specific fluorescence probe[J]. Environmental Science & Technology, 2012, 46 (8): 4633-4640. |
| [16] | 梁文艳, 张元春, 曹敬灿, 等. 采用尼罗红荧光探针对微藻中油脂的定量测定[J]. 环境化学, 2013, 32 (8): 1491-1495. |
| [17] | Ishida T, Alexandrov M, Nishimura T, et al. Selective detection of airborne asbestos fibers using protein-based fluorescent probes[J]. Environmental Science & Technology, 2010, 44 (2): 755-759. |
| [18] | 朱国营, 陈萍萍. 柱孢藻毒素对草鱼淋巴细胞毒效应及氧化损伤机理研究[J]. 环境科学学报, 2012, 32 (5): 1199-1205. |
| [19] | Wang M L, Meng G W, Huang Q, et al. Electrospun 1, 4-DHAQ-doped cellulose nanofiber films for reusable fluorescence detection of trace Cu2+and further for Cr3+[J]. Environmental Science & Technology, 2012, 46 (1): 367-373. |
| [20] | Zhang H M, Li Y B, Liu X L, et al. Determination of iodide via direct fluorescence quenching at nitrogen-doped carbon quantum dot fluorophores[J]. Environmental Science & Technology, 2014, 1 (1): 87-91. |
| [21] | Liu Y, Feng G Q. A visible light excitable colorimetric and fluorescent ESIPT probe for rapid and selective detection of hydrogen sulfide[J]. Organic & Biomolecular Chemistry, 2014, 12 (3): 438-445. |
| [22] | Xu Z, Xu L, Zhou J, et al. A highly selective fluorescent probe for fast detection of hydrogen sulfide in aqueous solution and living cells[J]. Chemical Communications, 2012, 48 (88): 10871-10873. |
| [23] | Wang J L, Lin W Y, Li W L. Three-channel fluorescent sensing via organic white light-emitting dyes for detection of hydrogen sulfide in living cells[J]. Biomaterials, 2013, 34 (30): 7429-7436. |
| [24] | Luber S, Adamczyk K, Nibbering E T J, et al. Photoinduced proton coupled electron transfer in 2-(2'-hydroxyphenyl)-benzothiazole[J]. The Journal of Physical Chemistry A, 2013, 117 (25): 5269-5279. |
| [25] | Kungwan N, Plasser F, Aquino A J A, et al. The effect of hydrogen bonding on the excited-state proton transfer in 2-(2'-hydroxyphenyl)benzothiazole: A TDDFT molecular dynamics study[J]. Physical Chemistry Chemical Physics, 2012, 14 (25): 9016-9025. |
| [26] | Wu Z S, Li Z, Yang L, et al. Fluorogenic detection of hydrogen sulfide via reductive unmasking of o-azidomethylbenzoyl-coumarin conjugate[J]. Chemical Communications, 2012, 48 (81): 10120-10122. |
| [27] | Chen Y C, Zhu C C, Yang Z H, et al. A ratiometric fluorescent probe for rapid detection of hydrogen sulfide in mitochondria[J]. Angewandte Chemie, 2013, 125 (6): 1732-1735. |
 2015, Vol. 36
2015, Vol. 36


