多氯联苯(polychlorinated biphenyls,PCBs)是环境中最广泛分布的持久性有机污染物(persistent organic pollutants,POPs)之一,从一氯联苯到十氯联苯共有209种同系物,具有极低的水溶解度(Sw)、 高辛醇-水分配系数(Kow)和高沉积物吸附系数(Koc)[1],一旦进入环境后会被强烈地吸附到土壤颗粒表面或沉积到底泥中,向环境中缓慢释放,生物有效性低[2,3].
疏水性有机物(hydrophobic organic compounds,HOCs)可以通过溶解在表面活性剂胶束(≥临界胶束浓度,CMC)中而增加其在水相中的溶解度[4]. Fan等[5]在运用电动学方法修复受PCBs污染的土壤时,发现添加表面活性剂lgepal CA-720能使土壤吸附的PCBs部分溶于水相,促使其迁移到负极而被氧化,且lgepal CA-720的最适量为2%. 施周等[6]对表面活性剂溶液中PCBs的溶解特性进行了研究,发现表面活性剂是通过形成胶束显著的增加疏水性污染物PCBs的表观溶解度,而POL(10)和TX-100等非离子型表面活性剂对PCBs的增溶效果优于阴离子型表面活性剂.
在针对PCBs污染的修复技术中需要解决的首要问题是高效降解体系的构建. Ponce等[7]发现添加维生素E或浆果提取物等抗氧化物质能通过保护Burkholderia xenovorans LB400的细胞膜,从而提高水溶液中PCBs的降解速率. Rehmann等[8]发现B. xenovorans LB400在降解Aroclor 1242的过程中菌种活性不断下降,但通过添加联苯等共代谢基质能实现Aroclor 1242的持续降解. Liu等[9]在利用Pseudomonas sp. strain LB400降解土壤中PCBs的实验中,添加了鼠李糖脂(RL)作为PCBs的增溶剂和代谢碳源,显著提高了菌种生物量和PCBs降解速率. B. xenovorans LB400作为PCBs高效降解菌种与对PCBs有增溶作用的表面活性剂联合构成降解体系可能会对PCBs的降解带来理想的促进效果,而国内外学者对这方面少有开展系统的基础性研究.
本研究选取具有PCBs广谱降解能力的优势菌Burkholderia xenovorans LB400以及3种典型的表面活性剂(TX-100、 Tween 80、 RL crude)和HPCD来构建PCBs降解体系,从PCBs的增溶性和菌种的生长状况等方面,探讨表面活性剂环境和菌种活性条件对PCBs降解的影响,以期为基于不同表面活性剂因子的低氯代PCBs降解提供依据.
1 材料与方法 1.1 试剂和耗材3种典型的低氯代PCBs(nCl≤4):PCB3(4-CB)、 PCB5(2,3-CB)和PCB31(2,4′,5-CB)均购自北京百灵威试剂有限公司,纯度分别为100%、 99.9%和100%,用色谱纯丙酮分别配成50、 10和10 g ·L-1的PCBs标准溶液. 联苯(GC纯)购自上海阿拉丁试剂有限公司,用色谱纯丙酮配成20 g ·L-1的标准溶液. 在降解体系中作为PCBs增溶剂的TX-100(非离子型)、 Tween 80(非离子型)和RL crude(阴离子型)3种表面活性剂,以及HPCD均为国产分析纯,其基本性质如表 1所示[10,11]. 3种表面活性剂和HPCD均配成系列浓度的溶液. 作为菌种培养的碳源与能源物质的丁二酸钠亦为分析纯.
| 表 1 3种表面活性剂和β-环糊精的基本性质1)Table 1 Basic properties of three surfactants and HPCD |
实验菌种选择B. xenovorans LB400(LB400),该菌种为Goris等在莫罗(美国纽约)填埋场一处受PCBs污染的土壤中分离出来的具有降解广谱PCBs能力的优势菌[12],购于瑞典University of Gteborg菌种保藏中心,菌种编号为CCUG 46959.
LB400经CASO培养基活化后,以700 mg ·L-1联苯作为唯一碳源,利用M9复合盐培养液在28℃,150 r ·min-1的条件下进行培养驯化[13],待菌种生长进入对数期后进行转接操作. M9复合盐培养液的成分为[7]:Na2HPO4 ·12H2O 17.1 g ·L-1; KH2PO4 3.0 g ·L-1; NaCl 0.5 g ·L-1; NH4Cl 1.0 g ·L-1; MgSO4 0.24 g ·L-1; CaCl2 0.01 g ·L-1; 微量元素和维生素. M9无机盐复合培养基、 TX-100、 Tween 80、 RL crude和HPCD溶液在实验前均经过102.9 kPa(1.05 kg ·cm-2),125℃,高温高压灭菌30 min.
1.3 Burkholderia xenovorans LB400降解能力实验采用吸光度法测定菌种的生物量,将LB400的菌液在600 nm的吸光度值(D600)作为测定生物量的标准. 菌种培养2 d即达到对数生长期中后期(D600约为0.65),经2 000 r ·min-1离心20 min去除残留的联苯固体后,取D600=0.65的生长细胞菌液作为PCBs降解体系的接种菌液. 在15 mL棕色圆底培养管中,用5 μL或10 μL微量进样针分别加入单一碳源物质PCB3、 PCB5、 PCB31标准溶液5、 10和5 μL,待丙酮挥发完全后,加入5 mL M9复合盐培养液,使其浓度分别达到50、 20和10 mg ·L-1,同时接种LB400菌液500 μL,接种量为9%,用透气封口膜封好管口,放入160 r ·min-1的恒温摇床28℃下培养3 d. 为加快微生物好氧代谢PCBs,分别加入10、 20、 40 mg ·L-1联苯作为PCBs降解的共代谢物质.
1.4 表面活性剂对Burkholderia xenovorans LB400降解PCBs的影响用5 μL微量进样针在15 mL棕色圆底培养管中分别加入PCB5、 PCB31和联苯标准溶液5、 2.5和2.5 μL,待丙酮完全挥发后,加入5 mL M9复合盐培养液,使以上3种物质浓度分别为10、 5和10 mg ·L-1,LB400菌液的接种量为9%; 同时向培养管中定量加入不同浓度的表面活性剂和HPCD溶液,使TX-100、 Tween 80、 RL crude的系列浓度均为0、 0.1、 0.25、 0.5、 1、 3、 5、 7 CMC,HPCD的系列浓度为0、 10、 25、 50、 100、 500、 1 000、 1 500 mg ·L-1; 最后用透气封口膜封管口,放入160 r ·min-1的恒温摇床28℃下培养3 d.
1.5 表面活性剂对PCBs的增溶作用在15 mL棕色圆底培养管中用5 μL或10 μL微量进样针加入PCB5和PCB31标准溶液10 μL和5 μL,待丙酮完全挥发后,加入5 mL M9复合盐培养液,使其浓度分别达到20 mg ·L-1和10 mg ·L-1,同时按1.4节中的设计向培养管中定量加入表面活性剂和HPCD溶液,并加入少量Na3N作为抑菌剂,之后用带有聚四氟乙烯衬层的盖子拧紧管口,放入160 r ·min-1的恒温摇床28℃下振荡2 d.
1.6 表面活性剂对Burkholderia xenovorans LB400生长的影响在50 mL锥形瓶中加入810 mg ·L-1丁二酸钠作为碳源和能源培养LB400[14],同时向锥形瓶中按1.4节中的设计定量加入表面活性剂和HPCD溶液,放入160 r ·min-1的恒温摇床28℃下培养20 h后,以测量菌液D600来表征菌体的生长状况.
1.7 分析方法降解体系中PCBs的测定:实验均设置3个平行(下同),并设置不加菌液的空白对照(加入少量Na3N作为抑菌剂),以扣除在培养过程中PCBs的挥发损失. 用整管萃取的方法测定PCBs剩余量:向5 mL培养液中加入5 mL色谱纯乙酸乙酯作为萃取剂[7],用带有聚四氟乙烯衬层的盖子拧紧管口,涡旋振荡1 min,静置分层,抽取上层含PCBs的乙酸乙酯,重复操作3次,合并3次萃取液,旋转蒸发、 定容至5 mL,样品进HPLC. 3种PCBs的萃取率≥98%. 测定用的HPLC型号为岛津LC-20AT,色谱柱为Syncronis C18柱,流动相为乙腈 ∶水=9 ∶1,样品中PCBs含量用标准曲线定量.
增溶体系中PCBs的测定:在2 d取出培养管,培养管经10 000 r ·min-1离心20 min,抽取上清液3 mL,加入3 mL色谱纯乙酸乙酯进行上述的萃取操作和测定,以上清液中PCBs的含量多少作为增溶效果的评价标准.
表面活性剂对菌种生长的影响测定:每个锥形瓶抽取10 mL培养液经2 000 r ·min-1离心20 min后,用UV-2800分光光度计(Unico,上海)测定菌液的D600来确定LB400的生物量[11].
2 结果与讨论 2.1 Burkholderia xenovorans LB400对3种PCBs的降解以PCBs为唯一碳源及以联苯为共基质条件的情况下LB400对3种PCBs的降解见图 1. 在以PCBs为唯一碳源时,3 d内LB400降解的速率顺序是:PCB3>PCB5>PCB31; 随着时间的延长,3种PCBs降解速率的增量也是同样趋势. 这是由于PCBs的氯代程度越高,其在水相中的溶解度越低,LB400越难以利用其作为生长底物而进行自身的代谢增殖. 微生物降解PCBs遵循的是联苯代谢途径,主要通过2,3双加氧酶攻击2,3位C—C键,实现PCBs的间位开环降解; 氯原子数目过多会阻止PCBs与酶活性位点结合,故PCBs的氯代程度越高,微生物好氧降解越困难,且速率越慢[15,16].
 | 图 1 LB400对PCB3(50 mg ·L-1)、 PCB5(20 mg ·L-1)和PCB31(10 mg ·L-1)的单一碳源降解以及联苯共代谢降解Fig. 1 Degradation ratios of PCB3 (50 mg ·L-1),PCB5 (20 mg ·L-1) and PCB31 (10 mg ·L-1) as sole carbon sources and biphenyl co-metabolism |
在添加联苯处理中,低联苯浓度(<20 mg ·L-1)的条件下对PCB31的降解几乎没有影响. 添加20 mg ·L-1、 40 mg ·L-1联苯后,0~2 d内PCB31的降解效率没有明显提高反而有所下降,这可能是由于LB400在前期优先利用含量较大且更易降解的联苯; 在2~3 d PCB31的降解效率明显高于没有添加联苯的处理,且随着联苯添加量的增加,PCB31的共基质降解效率有显著提高. 同时,在3 d后各处理的菌液D600的大小顺序为:0.357(40 mg ·L-1)>0.195(20 mg ·L-1)﹥0.178(10 mg ·L-1)﹥0.092(0 mg ·L-1),这说明添加联苯除了有助于诱导PCBs降解酶外[14],还有利于维持或提高降解菌的数量,促使LB400以共代谢的方式降解PCBs,加速难溶性的PCBs向水相的迁移和溶解.
2.2 表面活性剂对2种PCBs的增溶效果强化PCBs好氧降解的措施主要有两方面:一是促使PCBs的降解以共代谢方式进行,如添加适量联苯; 二是增强PCBs的水溶性以提高其生物有效性,如添加表面活性剂. 为增加PCBs的溶解度,笔者考察了表面活性剂对PCB5和PCB31的增溶效果. 由图 2可知,当TX-100、 Tween 80和RL crude在浓度低于各自的CMC(见表 1)以及HPCD在浓度低于100 mg ·L-1时,均对2种PCBs没有明显的增溶作用. 而当TX-100、 Tween 80和RL crude在浓度高于(或等于)各自的CMC以及HPCD在浓度高于500 mg ·L-1时,均对2种PCBs有明显的增溶作用,且不同表面活性剂的增溶效果有明显差别. 实验2 d后,培养管中2种PCBs的实际量为PCB5 19.0 mg ·L-1、 PCB31 9.8 mg ·L-1,扣除空白对照,TX-100、 Tween 80、 RL crude浓度在1~7 CMC时和HPCD浓度在500~1 500 mg ·L-1时对PCB5和PCB31溶出率分别达到:54.7%~100%(100%为PCBs几乎完全溶解)、 59.8%~100%; 10.5%~40.8%、 6.8%~31.6%; 10.3%~19.9%、 3.3%~11.6%; 19.5%~34.2%、 4.2%~10.7%,从以上数据可见,3种表面活性剂和HPCD中对PCB5和PCB31增溶效果最为显著的是TX-100,其次是Tween 80,最差的是RL crude,其中因为HPCD的结构为具有一定内径的外缘亲水,空腔疏水的桶状大分子,故可能对分子直径较小的PCB5具有更好的增溶效果[17],因此表面活性剂的添加有利于增加PCBs的溶解度,提高其生物有效性.
 | (b)为(a)的局部放大,(d)为(c)的局部放大图 2 TX-100、 Tween 80、 RL crude和HPCD对PCB5(20 mg ·L-1)和PCB31(10 mg ·L-1)的增溶效果Fig. 2 Solubility of PCB5 (20 mg ·L-1) and PCB31 (10 mg ·L-1) in TX-100,Tween 80,RL crude and HPCD solutions |
由图 2可知,PCBs的增溶效果随表面活性剂浓度的增加而增大,但同时表面活性剂可能对微生物的生长也有抑制或毒害,因此考察了不同的表面活性剂存在对LB400的生长影响,结果见图 3. 从中可以看出,TX-100和Tween 80对LB400的生长起明显的抑制作用,其中最为显著的是TX-100,这可能与TX-100的生物降解性能不好以及毒性作用有关; 当TX-100浓度<50 mg ·L-1时,对LB400的生长几乎没有抑制作用,而浓度在1~7 CMC时则有明显的抑制作用,且浓度越大,抑制作用越强烈,抑制率达到30.3%~45.8%. Tween 80浓度在0.1~1 CMC时对LB400的生长有较明显的抑制作用,抑制率为10.0%~15.4%,而当浓度>CMC时,抑制作用则逐步减轻. 不同的表面活性剂会对不同菌种的生长产生促进/抑制效应,这可能与表面活性剂-细胞膜酶蛋白的相互作用有关[11,18]. HPCD对LB400的生长没有明显的影响,而RL crude在浓度≤CMC时对LB400的生长有较小的抑制作用,而在高浓度(>150 mg ·L-1)的情况下,却能显著的促进LB400的生长,且经进一步实验验证,LB400能以RL crude为唯一碳源和能源进行细胞增殖,这也与前人的研究结果相一致[9].
 | 图 3 TX-100、 Tween 80、 RL crude和HPCD对LB400生长的影响Fig. 3 Impacts of TX-100,Tween 80,RL crude and HPCD on growth of Burkholderia xenovorans LB400 |
由2.2节和2.3节的分析可知,表面活性剂一方面能通过增加PCBs的溶解度来提高其生物可利用性,另一方面又会在一定浓度范围内抑制(如TX-100和Tween 80)或促进(如RL crude)LB400的生长,因此有必要构建基于表面活性剂环境因子的微生物降解体系来确定表面活性剂发挥强化PCBs降解作用的合适条件.
2.4 表面活性剂-Burkholderia xenovorans LB400体系对2种PCBs的降解在表面活性剂存在的条件下,微生物对PCBs的降解效率是PCBs的增溶性和菌种的生长抑制两方面因素竞争的结果,因此笔者探讨了基于表面活性剂因子的Burkholderia xenovorans LB400对PCBs好氧降解的影响,结果见图 4. 由图 4(a)可知,在Tween 80浓度≤13.1 mg ·L-1(CMC)时,PCB31的降解效率均明显低于空白对照,这可能是因为未形成胶束状态(﹤CMC时)的自由的表面活性剂基团吸附在细胞表面和PCB31疏水性表面,降低了整个PCB31疏水性表面与细胞的接触几率,从而阻碍了LB400在PCBs-细胞作用界面上分泌胞外酶对其进行降解[18, 19, 20]; 且低浓度的Tween 80对LB400的生长有更加明显的抑制作用(图 3). 在Tween 80浓度在1~7 CMC时,PCB31的降解效率随Tween 80浓度的提高而呈显著增大的趋势,与空白对照相比,PCB31的降解效率显著提高了14.6%~44.3%. 研究表明,表面活性剂浓度﹥CMC时,会通过形成PCBs-表面活性剂的胶束来提高PCBs的表观溶解度,从而加强PCBs与细胞间的亲水性接触,提高降解效率[21, 22, 23, 24],这与Tween 80浓度﹥CMC时对PCB31有显著的增溶作用的结果相吻合(图 2),且Tween 80在这浓度范围内对LB400的抑制作用已大大减轻.
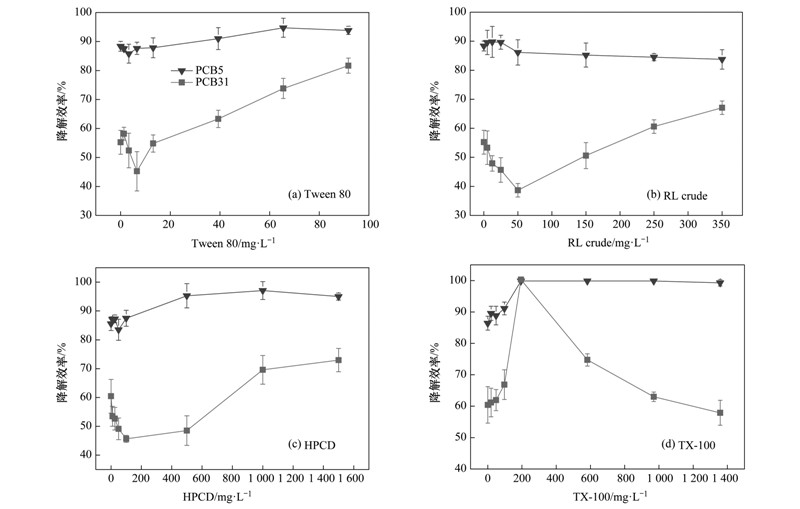 | 图 4 Tween 80、 RL crude、 HPCD和TX-100对LB400降解PCB5(10 mg ·L-1) 和PCB31(5 mg ·L-1)效率的影响Fig. 4 Impacts of Tween 80,RL crude,HPCD and TX-100 on degradation ratios of PCB5 (10 mg ·L-1) and PCB31 (5 mg ·L-1) by Burkholderia xenovorans LB400 |
在RL crude浓度≤50 mg ·L-1(CMC)和HPCD浓度≤500 mg ·L-1时,LB400对PCB31降解效率的变化与Tween 80浓度≤CMC时的情况基本相同. 由图 4(b)和4(c)可知,当RL crude浓度﹥CMC时,PCB31的降解效率比空白对照低,这可能是因为RL crude能作为LB400的碳源和能源与此时溶解度仍然很低的PCB31进行竞争,故导致PCB31降解效率的下降; 直到RL crude浓度在5~7 CMC时,PCB31在水相中的表观溶解度开始有明显的增加,PCB31的降解效率与空白对照相比也相应提高了9.6%~27.2%,而此时虽然RL crude对LB400的生长有促进作用,但它本身对PCB31的增溶作用较小且已趋于饱和(图 2),故对PCB31降解效率提高较小. 在HPCD浓度≥1 000 mg ·L-1时,PCB31的降解效率比空白对照增大15.3%~20.7%,虽然HPCD对LB400的生长没有明显的抑制作用(图 3),但它对PCB31的溶解效果是最差的(图 2),故当HPCD的浓度增大到一定程度后,它对PCB31的降解效果已经没有明显的促进作用.
由图 4(d)可知,在TX-100的浓度﹤194 mg ·L-1(CMC)时,水相中PCB31的溶解度没有明显的增加,而PCB31的降解效率随TX-100浓度的增大有较小幅度的提高,这与Tween 80、 RL crude和HPCD的结果相反,这一方面可能是由于TX-100在浓度﹤CMC时对LB400的生长几乎没有抑制作用,另一方面可能是由于TX-100本身的结构或官能团能改善细胞和PCB31疏水性表面之间的接触[25,26]. 在TX-100浓度=CMC时,LB400对PCB31的降解效率达到100%,与空白对照相比极为显著地提高了65.5%,同时TX-100对PCB31的溶解效果也有极为显著的提高(图 2),表观溶解度远高于其它处理; 尽管此时TX-100对LB400的生长已有30.3%的抑制率,远高于其它处理,但LB400对PCB31的降解仍然有显著增强的效果,目前为止未见相关研究报道; 然而在TX-100浓度﹥CMC时,LB400对PCB31的降解效率随TX-100浓度的增大而急剧下降,尽管此时PCB31的溶出效率接近100%,但高浓度的TX-100环境已使LB400的生长受到严重的抑制. 另外由图 4可知,在3种表面活性剂和HPCD环境中,PCB5降解效率的变化不明显,这可能是相对于PCB31而言,PCB5本身具有较高的溶解度和较好的降解性能.
在表面活性剂环境下微生物降解PCBs的效率主要受两方面因素的影响:①水相中PCBs-表面活性剂的胶束浓度; ②表面活性剂自身对细胞生长代谢的影响. 总体来说,水相中PCBs-表面活性剂的胶束浓度越高,即PCBs在溶液中的表观溶解度越大,LB400对PCBs的降解效率越高,但必须同时定性定量地考虑表面活性剂本身对菌体生长的影响. 在本实验中当设置TX-100和Tween 80浓度分别为1和7 CMC时,LB400对PCB31的降解效率有显著提高.
3 结论(1)在表面活性剂环境下,Burkholderia xenovorans LB400降解低氯代PCBs的效率主要受两方面因素的影响:①水相中PCBs-表面活性剂的胶束浓度; ②表面活性剂对LB400的生长抑制. 在浓度≥CMC时,3种表面活性剂和HPCD(≥500 mg ·L-1)对低氯代PCBs增溶效果最为显著的是TX-100、 其次是Tween 80,RL crude和HPCD效果较差; 相应地TX-100和Tween 80对于LB400降解低氯代PCBs也有极为显著的促进作用; 然而TX-100和Tween 80浓度分别在1~7 CMC和0.1~1 CMC时会不同程度地抑制LB400的生长.
(2)总体来说,水相中PCBs-表面活性剂的胶束浓度越高,即PCBs在溶液中的表观溶解度越大,LB400对PCBs的降解效率越高,但必须同时定性定量地考虑表面活性剂本身对菌体生长的抑制作用.
(3)在水溶液培养体系中当设置TX-100和Tween 80浓度分别在1和7 CMC时,PCB31(5 mg ·L-1)的降解效率达到100%和81.7%,而此时B. xenovorans LB400生长的抑制率为30.3%和5.4%,但对于受工业PCBs(如Aroclor)污染的实际土壤而言,仍需进一步探讨表面活性剂对PCBs微生物修复带来的影响.
| [1] | Xu W G, Wang X, Cai Z W. Analytical chemistry of the persistent organic pollutants identified in the Stockholm Convention: a review[J]. Analytica Chimica Acta, 2013, 790: 1-13. |
| [2] | Cao M H, Hu Y, Sun Q, et al. Enhanced desorption of PCB and trace metal elements (Pb and Cu) from contaminated soils by saponin and EDDS mixed solution[J]. Environmental Pollution, 2013, 174: 93-99. |
| [3] | Gomes H I, Dias-Ferreira C, Ribeiro A B. Overview of in situ and ex situ remediation technologies for PCB-contaminated soils and sediments and obstacles for full-scale application[J]. Science of the Total Environment, 2013, 445-446: 237-260. |
| [4] | Doong R, Lei W G. Solubilization and mineralization of polycyclic aromatic hydrocarbons by Pseudomonas putida in the presence of surfactant[J]. Journal of Hazardous Materials, 2003, 96 (1): 15-27. |
| [5] | Fan G P, Cang L, Fang G D, et al. Surfactant and oxidant enhanced electrokinetic remediation of a PCBs polluted soil[J]. Separation and Purification Technology, 2014, 123:106-113. |
| [6] | 施周, Ghosh M M. 表面活性剂溶液中多氯联苯溶解的特性[J]. 中国环境科学, 2001, 21 (5): 456-459. |
| [7] | Ponce B L, Latorre V K, González M, et al. Antioxidant compounds improved PCB-degradation by Burkholderia xenovorans strain LB400[J]. Enzyme and Microbial Technology, 2011, 49 (6-7): 509-516. |
| [8] | Rehmann L, Daugulis A J. Enhancement of PCB degradation by Burkholderia xenovorans LB400 in biphasic systems by manipulating culture conditions[J]. Biotechnology and Bioengineering, 2008, 99 (3): 521-528. |
| [9] | Liu Y S, Ma M Y, Shi Z. Application of rhamnolipid biosurfactant for removing polychlorinated biphenyls from contaminated soil[J]. Advanced Materials Research, 2011, 233-235: 608-613. |
| [10] | 田齐东, 王国庆, 赵欣, 等. 3种表面活性剂对有机氯农药污染场地土壤的增效洗脱修复效应[J]. 生态与农村环境学报, 2012, 28 (2): 196-202. |
| [11] | Fernando Bautista L, Sanz R, Carmen Molina M, et al. Effect of different non-ionic surfactants on the biodegradation of PAHs by diverse aerobic bacteria[J]. International Biodeterioration & Biodegradation, 2009, 63 (7): 913-922. |
| [12] | Goris J, De Vos P, Caballero-Mellado J, et al. Classification of the biphenyl-and polychlorinated biphenyl-degrading strain LB400T and relatives as Burkholderia xenovorans sp. nov[J]. International Journal of Systematic and Evolutionary Microbiology, 2004, 54 (5): 1677-1681. |
| [13] | Denef V J, Patrauchan M A, Florizone C, et al. Growth substrate-and phase-specific expression of biphenyl, benzoate, and C1 metabolic pathways in Burkholderia xenovorans LB400[J]. Journal of Bacteriology, 2005, 187 (23): 7996-8005. |
| [14] | Parnell J J, Denef V J, Park J, et al. Environmentally relevant parameters affecting PCB degradation: carbon source-and growth phase-mitigated effects of the expression of the biphenyl pathway and associated genes in Burkholderia xenovorans LB400[J]. Biodegradation, 2010, 21 (1): 147-156. |
| [15] | Arnett C M, Parales J V, Haddock J D. Influence of chlorine substituents on rates of oxidation of chlorinated biphenyls by the biphenyl dioxygenase of Burkholderia sp. Strain LB400[J]. Applied and Environmental Microbiology, 2000, 66 (7): 2928-2933. |
| [16] | Zorádová-Murínová S, Dudáová H, Lukáová L, et al. Adaptation mechanisms of bacteria during the degradation of polychlorinated biphenyls in the presence of natural and synthetic terpenes as potential degradation inducers[J]. Applied Microbiology and Biotechnology, 2012, 94 (5): 1375-1385. |
| [17] | 丁娟, 罗坤, 周娟, 等. 表面活性剂Tween 80和β-环糊精对白腐菌降解多环芳烃的影响[J]. 南京大学学报(自然科学版), 2007, 43 (5): 561-566. |
| [18] | Song M, Bielefeldt A R. Toxicity and inhibition of bacterial growth by series of alkylphenol polyethoxylate nonionic surfactants[J]. Journal of Hazardous Materials, 2012, 219-220: 127-132. |
| [19] | Feng W, Swift S, Singhal N. Effects of surfactants on cell surface tension parameters and hydrophobicity of Pseudomonas putida 852 and Rhodococcus erythropolis 3586[J]. Colloids and Surfaces B: Biointerfaces, 2013, 105: 43-50. |
| [20] | Zhang D, Zhu L Z. Effects of Tween 80 on the removal, sorption and biodegradation of pyrene by Klebsiella oxytoca PYR-1[J]. Environmental Pollution, 2012, 164: 169-174. |
| [21] | González N, Simarro R, Molina M C, et al. Effect of surfactants on PAH biodegradation by a bacterial consortium and on the dynamics of the bacterial community during the process[J]. Bioresource Technology, 2011, 102 (20): 9438-9446. |
| [22] | Sarma S J, Pakshirajan K. Surfactant aided biodegradation of pyrene using immobilized cells of Mycobacterium frederiksbergense[J]. International Biodeterioration & Biodegradation, 2011, 65 (1): 73-77. |
| [23] | Zhang D, Zhu L H, Li F. Influences and mechanisms of surfactants on pyrene biodegradation based on interactions of surfactant with a Klebsiella oxytoca strain[J]. Bioresource Technology, 2013, 142: 454-461. |
| [24] | Lanzon J B, Brown D G. Partitioning of phenanthrene into surfactant hemi-micelles on the bacterial cell surface and implications for surfactant-enhanced biodegradation[J]. Water Research, 2013, 47 (13): 4612-4620. |
| [25] | Neu T R. Significance of bacterial surface-active compounds in interaction of bacteria with interfaces[J]. Microbiological Reviews, 1996, 60 (1): 151-166. |
| [26] | Zhang D, Zhu L Z. Controlling microbiological interfacial behaviors of hydrophobic organic compounds by surfactants in biodegradation process[J]. Frontiers of Environmental Science & Engineering, 2014, 8 (3): 305-315. |
 2014, Vol. 35
2014, Vol. 35


