2. 嘉应学院化学与环境学院, 梅州 514015
2. College of Chemistry and Environment, Jiaying University, Meizhou 514015, China
β受体阻滞剂是一类用来治疗心血管疾病的处方药物,世界各国的用量都非常大,临床上使用较多的是阿替洛尔、 美托洛尔和普萘洛尔(propranolol,PRO)[1,2]. 这些药物及其代谢产物排出体外后通过城市污水管网而进入污水处理厂或环境水体. 据报道,β受体阻滞剂在美国一些污水处理厂外排的污水中达到 2 μg·L-1[3],在意大利一些河流中达到240 ng ·L-1[4]. 尽管还没有研究表明,β受体阻滞剂对人体有直接的毒性,但多项研究表明其具有生态毒性,对水藻、 浮游生物以及鱼类的生长均存在抑制作用[5,6].
光化学降解是去除污水处理厂出水及水环境中药物自然降解的有效途径[7, 8, 9, 10]. 药物的光化学降解机制包括直接光降解、 自敏化光降解以及间接光降解[11, 12, 13, 14]. 目前国内外对一些β受体阻滞剂的光降解行为及机制进行过一些研究[9, 15, 16, 17],但主要集中在间接光解如腐殖酸敏化光解的研究方面. 部分β受体阻滞剂如PRO和吲哚洛尔在纯水中能较快光解,对于这些药物,相比间接光解,直接光解和自敏化光解对于其在环境中的消除,具有更加重要的意义. 但目前对于这些药物在纯水中的光解机制却不甚清楚,对于其光解产物的毒性研究也很少.
因此,本研究以PRO作为模型化合物,考察了其在高压汞灯照射下纯水中的光降解行为,并分析了PRO初始浓度和初始pH对光解速率常数的影响; 通过活性氧物种(ROS)猝灭实验和单线态氧(1 O2)稳态浓度的测定探讨了PRO的紫外光降解机制; 通过发光菌毒性实验评价其在光解过程中产物的毒性大小. 这对于自来水厂水源水或污水处理厂出水中PRO的深度处理,保证供水安全以及保护环境水体具有重要的现实意义.
1 材料与方法
1.1 实验仪器和试剂
SGY-Ⅱ型多功能光化学反应仪(南京斯东柯电气设备有限公司); pHS-3C型酸度计(上海精密科学仪器有限公司); LC-20AT高效液相色谱仪(日本岛津公司); DXY-2型生物毒性测试仪(中国科学院南京土壤研究所).
盐酸普萘洛尔(纯度>99%,美国Sigma公司); 山梨酸(纯度>99%,美国Sigma公司); 糠醇(FFA,纯度>99%,美国Sigma公司); 异甲醇、 乙腈(HPLC级,上海安谱科学仪器有限公司); 明亮发光杆菌T3小种冻干粉(中国科学院南京土壤研究所); 磷酸二氢钾、 磷酸氢二钠、 磷酸、 氢氧化钠、 异丙醇和叠氮化钠等(分析纯,成都科龙化工试剂厂); 实验用水均为超纯水.
1.2 实验方法
1.2.1 光解实验
(1)初始浓度(c0)和初始pH的影响
将PRO用超纯水溶解配制成1.0 g ·L-1的储备液,用pH=7.0的磷酸缓冲盐溶液将储备液稀释成1、 5、 10、 15、 20 mg ·L-1的系列溶液. 移取20 mL PRO稀释液于25 mL 石英试管中,将石英试管放入光化学反应仪中进行光解. 光源为120 W高压汞灯,主波长为254 nm,光强为16.60~17.57 mW ·cm-2. 光解过程在0~25 min取样9次,所取的样品立即用HPLC法测定PRO浓度. 在进行pH的影响实验时,将PRO储备液分别用pH为5、 6、 7、 8、 9的磷酸缓冲盐溶液稀释至10 mg ·L-1,获得不同pH的系列PRO溶液. 随后的光解及测定方法同初始浓度实验.
(2)ROS 猝灭实验[18]
在PRO溶液中,添加65 mmol ·L-1 的异丙醇溶液以猝灭羟基自由基( ·OH),添加20 mg ·L-1的叠氮化钠(NaN3)以猝灭羟基自由基( ·OH )和单线态氧(1 O2),添加0.18 mmol ·L-1的山梨酸以猝灭单线态氧(1 O2)和激发三重态PRO(3PRO*).
(3)1 O2稳态浓度测定
在PRO溶液中加入1.5 mmol ·L-1的FFA一同光解,隔一定时间取样用HPLC测定FFA 的浓度以计算FFA的光解速率常数. 1 O2稳态浓度采用以下公式计算得到:
光解实验中每组实验均设置暗对照实验,每个处理均做3次平行,实验结果取平均值.
1.2.2 发光菌毒性实验
采用明亮发光杆菌T3小种冻干粉作为指示生物,测试PRO水溶液在光解过程中的毒性变化[11]. 每个样品均进行3次平行,同时设置空白对照.
1.2.3 分析方法
PRO采用高效液相色谱仪(HPLC)测定,色谱条件:色谱柱为Hypersil ODS柱(4.6 mm×250 mm,5 μm); 流动相是乙腈,pH 3.0的磷酸缓冲溶液(30 ∶70,体积比); 检测器为光电二极管阵列检测器,检测波长为213 nm; 流速为1.0 mL ·min-1; 进样量为10 μL; 柱温为40℃.
FFA 采用HPLC法测定,色谱条件:流动相为甲醇 ∶水(用稀磷酸调至pH 4.0)=(20 ∶80,体积比),检测波长220 nm. 其它色谱条件同PRO测定.
2 结果与讨论
2.1 初始浓度对PRO光降解的影响
PRO初始浓度(c0)对其光解动力学的影响如图 1所示,PRO的光解符合准一级动力学. 在c0为1~20 mg ·L-1范围内,PRO的光解速率常数随着c0增加而减小,光解半衰期随之延长,1、 5、 10、 15、 20 mg ·L-1 PRO溶液的光解半衰期分别为2.38、 2.99、 4.04、 4.61、 5.36 min. 相关分析表明,光解速率常数与c0呈显著负相关,相关系数r2
 | 图 1 初始浓度对PRO光解动力学的影响
Fig. 1 Effects of initial concentrations on PRO photodegradation kinetics
|
关于c0与光解速率常数的负相关关系机制,一些研究认为这是由于在光解过程中[11,20],光源强度不变,光子量不变,随着光解物质初始浓度的增加,单位光解物质分得的光子量减少,从而导致光解速率常数下降,而这些研究也认为除此之外,还有一个原因是由于自敏化光解的参与导致. 2.2 初始pH对PRO光降解的影响
PRO溶液初始pH对光解动力学的影响如图 2所示. 从中可以看出,光解随着溶液pH的升高而加快,pH 9时的光解速率常数为pH 5时的2.81倍. 在不同pH条件下以不同形式存在的药物,其光解动力学显著受pH影响,如磺胺类、 四环素类、 喹诺酮类抗生素[19, 22, 23]. PRO的pKa为9.53[24],当溶液pH从5.0升高至9.0时,质子化形态PRO的比率从100%下降致75%,而去质子化PRO则升高至25%. Chen等[25,26]在研究腐殖酸光敏化降解胺类化合物时,认为随着pH的升高,去质子化氨基上未配对N电子的可利用性提高,这个N电子可快速转移至激发三重态腐殖酸,失去电子的胺类化合物从而迅速降解. 本研究中尽管不存在光敏剂,但PRO如果在UV光照射下产生激发三重态(3PRO*),则在较高pH条件下部分PRO可将N电子转移给3PRO*从而快速降解.
 | 图 2 初始pH对PRO光解动力学的影响
Fig. 2 Effects of initial solution pH on PRO photodegradation kinetics
|

 | 图 3 异丙醇、 叠氮化钠、 山梨酸对PRO光解动力学的影响
Fig. 3 Effects of isopropanol,NaN3 and sorbic acid on the photodegradation kinetics of PRO
|
这说明PRO的光解过程中存在着 ·OH和1 O2参与的自敏化光解和3PRO*参与的直接光解,光解路径如式(6)~(11)所示.
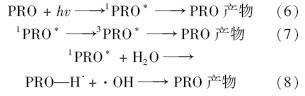

简单描述PRO在纯水中的光降解路径为:PRO吸收紫外光子后,生成激发单重态(1PRO*),1PRO*可继续反应生成PRO产物[式(6)],或将能量传递给水分子生成 ·OH促进PRO的光解[式(8)、式(9)],或经系间窜跃生成3PRO*. 3PRO*可直接光解生成产物[式(7)],或将能量传递给溶解氧,生成1 O2促进PRO的光解[式(10)、式(11)].
为探讨不同溶液条件PRO的光解速率常数差异原因,比较了pH为5、 7、 9 的10 mg ·L-1 PRO溶液以及pH为7 的1 mg ·L-1 PRO溶液中 ·OH、 1 O2和3PRO*直接光解对光解的贡献率,结果如表 1所示.
| 表 1 不同溶液条件 ·OH、 1 O2自敏化光解和3PRO*直接光解对PRO光解的贡献率 Table 1 Contribution of ·OH,1 O2 and 3PRO* for PRO photolysis |
可以看出,不同溶液条件光解过程中,直接光解和自敏化光解的贡献率存在明显差异. 直接光解占比越高,PRO的光解速率常数越大,说明PRO的直接光解速率常数大于自敏化光解速率常数,自敏化光解的发生不利于PRO的光解. 这与Ge等[20]认为自敏化光解的存在降低了光解速率常数的结论一致. 在自敏化光解中,·OH的贡献率基本保持不变,为21.3%~25.8%,而1 O2的贡献率随处理变化较大,可以看出PRO浓度越高,pH越低,1 O2贡献率越大.
为进一步验证1 O2对PRO光解的作用,利用FFA作为1 O2探针,测定了以上4个处理中的1 O2稳态浓度,结果如图 4所示. 其中表明,pH 5的10 mg ·L-1 PRO溶液中FFA的光解速率常数最大,经计算,其1 O2的稳态浓度为4.05×10-12 mol ·L-1,pH 7的1 mg ·L-1 PRO溶液中FFA光解速率常数最小,其1 O2的稳态浓度为3.15×10-12 mol ·L-1. 由此可以得出,1 O2产生量越大,PRO的光解速率常数越小. 因此,进一步证明了1 O2参与的自敏化光解的发生对PRO光解的抑制作用.
 | 图 4 FFA在不同溶液条件PRO溶液中的光解动力学
Fig. 4 FFA photodegradation kinetics in PRO solution under different treatments
|
运用发光菌毒性测定方法监测母体化合物及其产物的联合毒性的变化,毒性大小用发光抑制率表示,结果如图 5所示. 可以看出,母体化合物对发光菌的发光抑制率约为16.8%. 光解后,发光抑制率发生变化,随着光解的进行,抑制率先降低,在光解10 min时达到最高值,对发光菌的发光抑制率达到22.9%,随后下降,在25 min时又升高,对发光菌的发光抑制率约为20.6%.
 | 图 5 PRO光解对发光菌的抑制率
Fig. 5 Bioluminesscence inhibition of Vibrio fischeri by the photodegradation of PRO
|
图 6是PRO的光解产物的液相色谱图,可以看出,在UV照射下,PRO主要产生7个中间产物,出峰时间都早于PRO,即极性要强于PRO,这与PRO在太阳光下光解产物的表现基本一致[15]. 图 7是PRO母体化合物及其产物的峰面积变化,可以看出PRO的峰面积随着光解时间的延长而迅速下降.
 | 图 6 PRO及其光解产物的液相色谱图
Fig. 6 HPLC spectrum of PRO and its photoproducts
P0:PRO,P1~P7:PRO的7个主要光解产物 |
 | 图 7 PRO及其产物峰面积变化趋势
Fig. 7 Appearance/disappearance kinetics of PRO and its photoproducts
|
对照图 5和图 7可以看出,光解10 min时,PRO已降解了80%左右,而反应体系对发光菌的毒性则达到了最大; 光解进行到25 min时,PRO的残余浓度大约只有其起始浓度的1.6%,但体系仍然保持有较高的毒性,且毒性大于PRO降解前的毒性.
从图 7可以看出,在PRO发生光解的25 min时段内,产物浓度也在发生变化,P1、 P3、 P4、 P6浓度随时间增长而增大; P2、 P5浓度在10 min时达到最大,其后又逐渐变小; 而P7浓度则是在5 min时达到最大,5~20 min区间内浓度基本稳定,20 min后又迅速下降.
由此可见,PRO光解过程中产生了多种光解产物,且产物浓度又在不断发生变化,因此PRO光解过程中的反应体系是一个成分复杂体系,各种产物对体系毒性的贡献还不清楚. 但从整体来看,可以推测PRO母体化合物在降解过程中,生成了毒性比PRO自身更强的中间产物. 因此在采用UV光解PRO时,应考虑这一问题.
3 结论
(1) 在UV光照下,PRO可以迅速被光降解,光解速度随初始浓度的减小和溶液pH的升高而加快.
(2) 光解过程包括3PRO*参与的直接光解和 ·OH、 1 O2参与的自敏化光解. 直接光解贡献率越高,1 O2参与的自敏化光解贡献率越低,1 O2稳态浓度越低,光解速度越快.
(3) PRO光解过程中产生了7个主要光解产物,其中有些产物对发光菌的毒性比PRO的毒性更强.
| [1] | Black J W, Stephenson J S. Pharmacology of a new adrenergic beta-receptor-blocking compound (Nethalide)[J]. The Lancet, 1962, 2 (7251): 311-314. |
| [2] | Toda N. Vasodilating β-adrenoceptor blockers as cardiovascular therapeutics[J]. Pharmaco & Therapeut, 2003, 100 (3): 215-234. |
| [3] | Huggett D B, Brooks B W, Peterson B, et al. Toxicity of select beta adrenergic receptor-blocking pharmaceuticals (b-blockers) on aquatic organisms[J]. Archives of Environmental Contamination and Toxicology, 2002, 43 (2): 229-235. |
| [4] | Zuccato E, Castiglioni S, Fanelli R. Identification of the pharmaceuticals for human use contaminating the Italian aquatic environment[J]. Journal of Hazard Materials, 2005, 122 (3): 205-209. |
| [5] | Huguet A, Vacher L, Relexans S, et al. Properties of fluorescent dissolved organic matter in the Gironde Estuary[J]. Organic Geochemistry, 2009, 40 (6): 706-719. |
| [6] | Owen S F, Giltrow E, Huggett D B, et al. Comparative physiology, pharmacology and toxicology of β-blockers: Mammals versus fish[J]. Aquatic Toxicology, 2007, 82 (3): 145-162. |
| [7] | Yong C, Feng W. Environmental photochemistry: Theory and application[J]. Research Journal of Chemistry and Environment, 2011, 15 (2): 1-2. |
| [8] | Yuan F, Hu C, Hu X X, et al. Degradation of selected pharmaceuticals in aqueous solution with UV and UV/H2O2[J]. Water Research, 2009, 43 (6): 1766-1774. |
| [9] | 邵萌, 杨佳朋, 张洪海, 等. 水体系中氧氟沙星的光化学降解研究[J]. 环境科学, 2012, 33 (2): 476-480. |
| [10] | Chen Y, Liu Z Z, Wang Z P, et al. Photodegradation of propranolol by Fe(Ⅲ)-citrate complexes: Kinetics, mechanism and effect of environmental media[J]. Journal of Hazardous Materials, 2011, 194: 202-208. |
| [11] | 马杜鹃, 刘国光, 吕文英, 等. 水中萘普生的紫外光降解机制及其产物毒性研究[J]. 环境科学, 2013, 34 (5): 1782-1789. |
| [12] | Ge L K, Chen J W, Wei X X, et al. Aquatic photochemistry of fluoroquinolone antibiotics: Kinetics, pathways, and multivariate effects of main water constituents[J]. Environmental Science & Technology, 2010, 44 (7): 2400-2405. |
| [13] | Wenk J, von Gunten U, Canonica S. Effect of dissolved organic matter on the transformation of contaminants induced by excited triplet states and the hydroxyl radical[J]. Environmental Science & Technology, 2011, 45 (4): 1334-1340. |
| [14] | 葛林科, 李凯, 杨凯, 等. UV-vis光照下唑类抗菌药氟康唑的光化学反应类型[J]. 环境科学, 2013, 34 (8): 3132-3136. |
| [15] | Piram A, Salvador A, Verne C, et al. Photolysis of β-blockers in environmental waters[J]. Chemosphere, 2008, 73 (8): 1265-1271. |
| [16] | Dantas R F, Rossiter O, Teixeira A K R, et al. Direct UV photolysis of propranolol and metronidazole in aqueous solution[J]. Chemical Engineering Journal, 2010, 158 (2): 143-147. |
| [17] | Liu Q T, Willimas H E. Kinetics and degradation products for direct photolysis of-blockers in water[J]. Environmental Science & Technology, 2007, 41 (3): 803-811. |
| [18] | Xu H M, Cooper W J, Jung J, et al. Photosensitized degradation of amoxicillin in natural organic matter isolate solutions[J]. Water Research, 2011, 45 (2): 632-638. |
| [19] | Boreen A L, Arnold W A, McNeill K. Triplet-sensitized photodegradation of sulfa drugs containing six-membered heterocyclic groups: Identification of an SO2 extrusion photoproduct[J]. Environmental Science & Technology, 2005, 39 (10): 3630-3638. |
| [20] | Ge L K, Chen J W, Qiao X L, et al. Light-source-dependent effects of main water constituents on photodegradation of phenicol antibiotics: mechanism and kinetics[J]. Environmental Science & Technology, 2009, 43 (9): 3101-3107. |
| [21] | Doll T E, Frimmel F H. Fate of pharmaceuticals-photodegradation by simulated solar UV-light[J]. Chemosphere, 2003, 52 (10): 1757-1769. |
| [22] | Boreen A L, Arnold W A, McNeill K. Photochemical fate of sulfa drugs in the aquatic environment: Sulfa drugs containing five-membered heterocyclic groups[J]. Environmental Science & Technology, 2004, 38 (14): 3933-3940. |
| [23] | Werner J J, Arnold W A, McNeill K. Water hardness as a photochemical parameter: Tetracycline photolysis as a function of calcium concentration, magnesium concentration, and pH[J]. Environmental Science & Technology, 2006, 40 (23): 7236-7241. |
| [24] | Kibbey T C G, Paruchuri R, Sabatini D A, et al. Adsorption of beta blockers to environmental surfaces[J]. Environmental Science & Technology, 2007, 41 (15): 5349-5356. |
| [25] | Chen Y, Li H, Wang Z P, et al. Photodegradation of selected β-blockers in aqueous fulvic acid solutions: Kinetics, mechanism, and product analysis[J]. Water Research, 2012, 46 (9): 2965-2972. |
| [26] | Chen Y, Hu C, Hu X X, et al. Indirect photodegradation of amine drugs in aqueous solution under simulated sunlight[J]. Environmental Science & Technology, 2009, 43 (8): 2760-2765. |
 2014, Vol. 35
2014, Vol. 35


