2. 西南民族大学旅游与历史文化学院, 成都 610041
2. School of Tourism and History, Southwest University for Nantionlities, Chengdu 610041, China
由燃煤产生的SO2和NO带来严峻的大气环境污染问题,活性炭材料因其良好吸附性能而被应用于烟气中SO2和NO的脱除. 活性炭脱硫脱硝性能与其本身的物理化学性质具有十分密切的关系[1]. 根据微孔吸附容积填充理论[2],在吸附过程中吸附质分子按吸附势大小依次填充,尺寸越小的微孔势能越高,研究表明[3],吸附剂的孔径达到吸附质分子直径的1.7~3.0倍时,其孔径利用率最高. 刘义等[4]的研究发现,1.1~1.5 nm孔隙是活性炭的主要吸附场所,而Raymundo-Pinero等[5]提出,活性炭的微孔径为0.7 nm时,最有利于SO2吸附. 活性炭表面的化学性质是影响材料对SO2、 NO等酸性气体脱除的另一重要因素,Muniz等[6,7]研究发现,活性炭纤维表面的碱性能够通过化学吸附提高SO2滞留量,Mangun等[8]通过DR方程计算吸附能量,发现活性炭纤维对SO2的吸附量与其氮含量呈线性相关的关系,表明含氮官能团对于SO2的吸附起重要作用. 杨辉等[9]通过NO氧化路径分析发现,活性炭表面的含氧官能团对于NO的吸附起到氧化作用,进而促进NO的脱除作用.
尽管活性炭来源广泛,大部分含碳物质均可以制备成活性炭,但是原料的选择对于活性炭性能起着关键性作用. 植物生物类原料是目前研究较多的活性炭原料之一,包括木材、 锯木屑、 果壳、 果核、 竹子、 秸秆及其他农业废弃物等[10, 11, 12],考虑到原料的成本及生态环境的可持续性,生物废弃物受到研究者的喜好[13, 14, 15],废茶是碳含量较高的植物生物类废弃物,中国作为世界上最大的产茶国之一,每年都会产生大量的废茶,而这些废茶正是一种良好的活性炭前体材料,研究表明废茶活性炭具有较发达的孔径结构以及良好的吸附性能[16, 17, 18, 19, 20].
由于废茶本身携带一定的茶碱类成分,若废茶活性炭能继续保留其碱性官能团,则可在避免后期改性二次污染的前提下,直接提高其对SO2、 NO等酸性气体的脱除作用,然而目前还未见将此类活性炭用于脱硫脱硝性能的研究. 本研究以福建铁观音废茶为原料,通过K2CO3和ZnCl2活化制备携带一定碱性基团的废茶活性炭,并探讨其孔径及表面结构等因素对于SO2、 NO去除效果的影响,以期为制备用于脱硫脱硝的活性炭提供参考.
1 材料与方法 1.1 主要材料
由K2CO3活化制备的废茶活性炭(WTAC-K):WTAC-K-1、 WTAC-K-2、 WTAC-K-3及由ZnCl2活化制备的废茶活性炭(WTAC-Zn):WTAC-Zn-1、 WTAC-Zn-2、 WTAC-Zn-3、 WTAC-Zn-4,详细制备过程如文献[21]所述; 商品活性炭(沪试),国药集团化学试剂有限公司. 各材料的结构参数如表 1所示.
| 表 1 废茶活性炭的结构参数 Table 1 Structural parameters of waste tea activated carbon |
1.2 材料的表征
材料的石墨化程度由拉曼光谱(英国雷尼绍全自动共聚焦显微拉曼系统inVia Reflex)测定,其中激光器波长为534 nm,扫描范围为800~2000 cm-1.
材料的C、 H、 N、 O含量通过有机元素分析仪(北京利曼科技的有机元素分析仪EURO EA3000)测定.
材料的红外光谱通过以KBr为载体压片,再进行红外光谱(美国Thermo Nicolet的红外光谱仪Shimadzu 8400S)扫描.
材料的氮气吸附等温线通过比表面及孔径分析仪(贝士德仪器科技比表面及孔径分析仪3Ⅱ-2000PS1型)于77K下测定.
材料的表面酸碱性官能团由Boehm法测定:称取50 mg活性炭样品放入4只具塞的锥形瓶中,再分别加入50 mL,0.05mol ·L-1的NaOH、 Na2CO3、 NaHCO3、 HCl溶液. 将锥形瓶放在恒温器上25℃、 120 r ·min-1振荡6 h后取出,取上清液10 mL,向上清液中加入过量0.05 mol ·L-1的盐酸溶液. 酚酞作指示剂,用0.05 mol ·L-1的NaOH标准溶液反滴定过量酸至溶液微红. 羧基的数量为NaHCO3的变化量,酚羟基的数量为NaOH变化量减去Na2CO3变化量的差值,内酯基的数量为Na2CO3和NaHCO3变化量的差值,总酸基的数量为NaOH的变化量,总碱基的数量为HCl的变化量. 1.3 活性炭脱硫脱硝装置流程
实验装置如图 1所示,通过控制质量流量计配制SO2流量为0.6 mL ·min-1,NO流量为0.5 mL ·min-1,O2体积分数为3%的实验气体,其中N2为平衡气体,气流量为1 L ·min-1,由水蒸气注射泵控制气体相对湿度为10%,由加热及保温带控制气体温度为30℃±1℃. 称取1.5g活性炭材料于反应器中进行吸附实验,其中烟气浓度由Totes350型烟气分析仪检测,废气经高锰酸钾溶液氧化后由氢氧化钠溶液吸收,SO2或NO的去除率由式(1)计算.
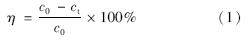
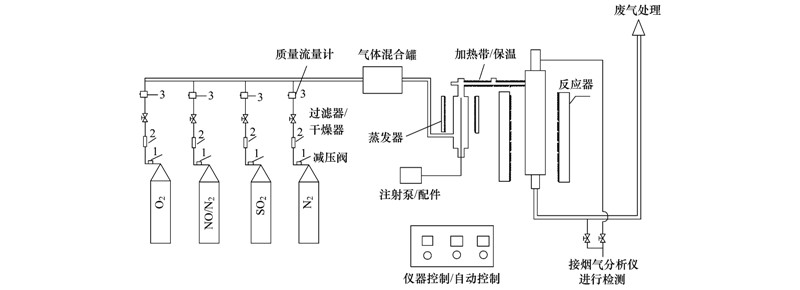 | 图 1 脱硫脱硝实验装置示意
Fig. 1 Experimental device for desulfurization and denitrification
|
活性炭材料的元素含量分析如表 2所示,WTAC-K-1的N元素含量最高为4.37%,而O元素含量最低为24.86%,WTAC-K-2 的N元素含量最低为1.72%,WTAC-K-3的O元素含量最高为33.51%. N、 O元素的含量与材料表面官能团的形成有一定关系,因此吸附材料的表面结构可能存在一定的差异.
| 表 2 废茶活性炭的有机元素含量 /% Table 2 Elemental analysis of waste tea activated carbon/% |
2.1.2 表面结构分析
由Boehm滴定法测定表面酸碱性官能团结果如表 3所示,WTAC-K-1的表面碱性最高,而表面酸性基团含量最低,其余材料的酸性基团含量相对接近,其中WTAC-Zn-4表面的酸性主要为羧基的贡献,WTAC-K-3和WTAC-Zn-2 表面的酸性官能团主要为内酯基,WTAC-K-2表面的酸性官能团主要为酚羟基.
| 表 3 废茶活性炭的Boehm滴定结果 ×10-4/mol ·g-1 Table 3 Boehm titration results of waste tea activated carbon×10-4/mol ·g-1 |
2.1.3 拉曼光谱分析
废茶活性炭吸附材料的拉曼光谱图如图 2所示,吸附材料的拉曼光谱均存在两个峰,一个位于1580 cm-1附近,即G峰,属于单晶石墨固有的特征散射峰; 另一个位于1360 cm-1附近,即D峰,是由石墨晶格缺陷、 边缘无序排列和低对称碳结构等引起的[22]. 因此可由式(2)来表征石墨化程度,其中R值越大,石墨化程度越低,表明石墨微晶尺寸越小[23]. 通过比较R值可得,K2CO3活化制备的活性炭材料石墨化程度相对较低,而ZnCl2活化制备的材料石墨化程度较高,石墨微晶尺寸较大,其结构的有序程度高.

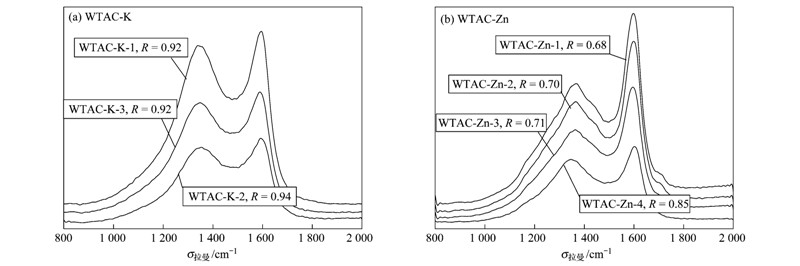 | 图 2 材料的拉曼光谱谱图
Fig. 2 Raman spectra of the material
|
材料在无氧条件下单独脱除SO2的性能曲线如图 3(a)所示,自制废茶活性炭在无氧环境下对于SO2的脱除效果均高于商品活性炭. 7组废茶活性炭对于SO2的吸附穿透时间顺序为:WTAC-K-1>WTAC-K-3>WTAC-K-2>WTAC-Zn-4>WTAC-Zn-3>WTAC-Zn-1>WTAC-Zn-2,其中K2CO3活化制备的材料对于SO2的去除效果明显要优于ZnCl2活化的材料. 由图 2的结果可知,WTAC-Zn的石墨化程度均高于WTAC-K,由此可知活性炭材料的石墨化程度过高反而不利于SO2在活性炭表面的滞留,脱硫效果也因此有所降低.
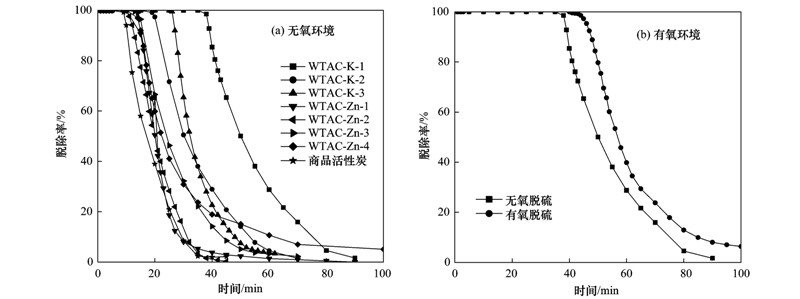 | 图 3 材料单独脱硫性能曲线
Fig. 3 Desulfurization performance curve using different adsorption materials
|
尽管WTAC-Zn-1、 WTAC-Zn-2、 WTAC-Zn-3的石墨化程度接近,但3组材料的脱硫性能曲线仍有一定的差别,这主要是受到材料孔径结构的影响. 结合表 1各材料的孔径结构可发现,虽然WTAC-Zn-2拥有最大的比表面积,但是其吸附性能反而最差,主要由于其平均微孔孔径最大,为0.85 nm,吸附势较低. 文献[5]提出,孔径在0.7 nm左右的微孔利用率最高,最适于SO2的吸附作用,由此可见,微孔径对于SO2吸附效果的影响相对比表面积更重要. 对于其他的吸附剂,其平均微孔孔径均较小,且在0.7 nm左右,因此其吸附效果还和其他的因素有关.
结合表 1可得,尽管WTAC-K-2与WTAC-K-1的孔径结构相近,但WTAC-K-2对于SO2的吸附性能远远低于WTAC-K-1,在20 min左右就已经开始穿透,通过表 2发现,由于两者的N含量存在一定的差异,其中WTAC-K-2的N含量明显较低为1.72%,而WTAC-K-1的N含量较高为4.37%,说明活性炭表面较高的氮含量可促进SO2吸附,这与文献[24, 25]得出的结论相似. WTAC-Zn-1、 WTAC-Zn-3及WTAC-Zn-4的孔径结构相近,且均具有较高的N含量(3.5%以上),然而其脱硫效果也存在一定的差异,这主要是受碱性基团的影响,WTAC-Zn-4的碱性基团含量较高达5.2×10-4mol ·g-1,其吸附时间也相对较长,在40 min时仍保持20%左右的脱硫效率,而WTAC-Zn-1碱性基团含量较低为2.7×10-4mol ·g-1,脱硫效果相对较差,25 min左右脱硫效率就已低于20%. 由此可知,碱性的含氮官能团才有利于SO2的吸附. Bagreev等[26]提出季胺型和吡啶型的含氮官能团能够提高活性炭对SO2的吸附作用,当这些含氮官能团分布在孔内的催化中心时,能够吸引硫酸根离子进行孔径填充作用.
废茶活性炭WTAC-K-1在3%O2环境下单独脱除SO2的性能曲线如图 3(b)所示,在氧气的作用下WTAC-K-1对于SO2的吸附效果有所提高,穿透时间由无氧条件下的39 min延长至44 min. 这是因为在有氧环境下,SO2吸附在活性炭有效吸附位上,通过与O2催化氧化生成SO3从而提高其在活性炭表面的吸附作用[27].
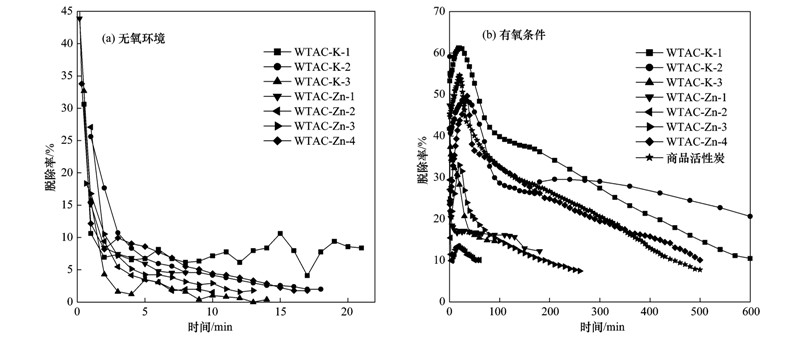 | 图 4 材料单独脱除NO性能曲线
Fig. 4 Denitrification performance curve using different adsorption materials
|
材料单独脱除NO的性能曲线如图 4所示. 由图 4(a)可看出,在无氧条件下,废茶活性炭对于NO的吸附效果很低,在1 min左右就已基本穿透,在5 min时脱除效率均低于10%,与文献[28]报道的结果相似,NO在常温下与吸附剂之间的相互作用力很弱,因此常温下NO很难通过活性炭材料的物理吸附去除[29]. 在实验气体中加入O2,将难以吸附的NO氧化为与吸附剂亲和力较高的NO2可有效提高NO的脱除效果,且随着氧气含量的提高,NO的吸附量随之增大. 本实验在实验气体中加入3%O2后,NO的脱除效率曲线如图 4(b)所示,在有氧条件下NO的脱除效率显著提高,其脱除效率在100 min后均能保持10%以上,其中WTAC-K-1在同等条件下对NO的脱除效率显著高于商品活性炭.
通过有氧脱硝性能曲线可发现,WTAC-K-1、 WTAC-K-2和WTAC-Zn-4这3种材料的吸附效果明显高于其他材料,结合表 1可发现这3个材料的中孔容量均低于0.1cm3 ·g-1,说明中孔结构不利于NO的吸附,由于活性炭表面对于NO的捕获能力较弱,中孔的存在增大了NO的移动空间,使其难以固定在微孔中. 通过分析3个材料的NO脱除效率曲线还可发现,NO的吸附过程大致可分为3个阶段:第一阶段,NO在活性炭表面活性位点的吸附和氧化,首先NO以非常弱的作用力吸附在活性炭表面,然后通过O2的氧化作用迅速将其固定在活性位点上,由于初始阶段活性炭表面的活性位点足够多,NO的氧化速率高于NO的脱附速率,因而随氧化作用的进行,NO的脱除效果逐渐增高,脱除效率曲线逐渐上升; 第二阶段,NO源源不断地固定在活性炭表面,使其表面的活性位点逐渐减少,此时NO的吸附作用开始减小,于是NO在活性炭表面的氧化固定作用相对其脱附作用随之降低,NO的脱除效率也因此开始下降,因而脱除效率曲线出现一个峰值; 第三阶段,NO在活性炭表面位点的吸附和脱附作用达平衡后,NO的脱除效率主要依靠O2的氧化作用,由于可利用的活性位点减少,NO的脱除效率曲线呈现平缓下降的趋势.
结合表 3并分析WTAC-K-1和WTAC-K-2这2种材料的脱硝性能曲线可得WTAC-K-1的脱除效果在300 min以前要高于WTAC-K-2,二者的孔径结构非常相似,因而可能与材料的表面化学性质有关. 通过分析表 2可发现,WTAC-K-1表面的碱性较强,N含量较高,NO的脱除效果较好. 由此可知,碱性含氮官能团对NO的脱除有一定的促进作用. 2.2.3 废茶活性炭同时脱除SO2和NO的性能研究
经以上实验发现WTAC-K-1对于SO2和NO的吸附效果最好,因此选用其进行同时脱除SO2和NO的实验研究. 实验中分别考查了无氧环境(实验气体组成为0.6mL ·min-1 SO2+0.5 mL ·min-1 NO,其中N2作为平衡气体),有氧环境(实验气体组成为0.6mL ·min-1 SO2+0.5 mL ·min-1NO+3% O2,其中N2作为平衡气体),以及湿式有氧环境(实验气体组成为0.6mL ·min-1 SO2+0.5 mL ·min-1NO+3% O2+10%H2O,其中N2作为平衡气体)WTAC-K-1对于SO2和NO的脱除作用,其脱硫脱硝性能曲线如图 5所示.
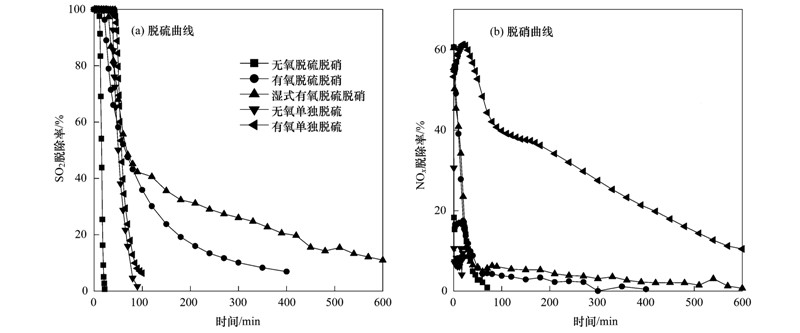 | 图 5 材料同时脱硫脱硝性能曲线
Fig. 5 Simultaneous desulfurization and denitrification performance curve of the material
|
由图 5(a)中无氧环境下活性炭同时脱硫脱硝与单独脱硫相对比可以看出,SO2和NO共同存在时脱硫效果有所降低,穿透时间由单独吸附的39 min降低为23 min. 由图 5(b)可得,无氧环境下的脱硝效果均较差,在1 min内脱硝效率就已低于20%. 由此可见,活性炭在无氧环境下,烟气中的NO能够抑制SO2的脱除,而SO2的存在对于NO脱除效果的影响不大.
在有氧环境下,废茶活性炭在烟气中SO2和NO共存时,SO2的吸附穿透时间由单独脱硫的44 min提前至22 min,但是在吸附实验进行到55 min后SO2的脱除率反而高于单独脱硫时的脱除率且吸附时间延长了4倍左右. 由图 5(b)可发现,活性炭在同时脱硫脱硝的情况下,O2的存在对于NO的脱除效果有所提高,但与有氧环境下的单独脱硝效果相比明显降低了,在20 min左右NO的脱除率便低于20%. SO2、 NO、 O2这3种气体分子对于活性炭的微孔存在竞争吸附的关系,然而3种气体共存时反而延长了对SO2的吸附时间,降低了NO的脱除效果. 文献[30, 31]提出,当烟气中SO2和NOx共存时,较高的NO浓度,尤其在浓度大于200×10-6时,有利于SO2吸附量的提高,而SO2的存在反而抑制了NO的吸附,当其浓度超过700×10-6时NO几乎没有吸附,本实验所采用的SO2浓度为600×10-6,NO浓度为500×10-6,所得结论与文献报导一致.
烟气中存在的水蒸气能够与吸附态的SO2发生化学反应,提高SO2吸附的作用力,从而促进SO2的化学吸附. 由图 5中3条同步吸附的SO2脱除性能曲线也可以看出,水蒸气的加入延长了穿透时间,吸附作用明显得到提高,在400 min时,其脱硫效率仍在20%以上. 由脱硝性能曲线的对比可发现,氧气和水蒸气的加入能够改善活性炭对于NO的吸附作用,然而提高得并不明显,脱除率在20 min左右均已降低至20%以下. 2.3 吸附机制研究 废茶活性炭样品脱硫脱硝后的红外光谱图如图 6所示,无氧环境下同时脱硫脱硝的红外光谱与无氧环境下单独脱硫的谱线相近,它们相对原始活性炭材料在1380 cm-1附近明显增加SO2的反对称伸缩振动峰; 通过观察有氧环境及湿式有氧环境下脱硫脱硝后活性炭材料在1210~1025 cm-1处均增加了一个SO2-4的反对称伸缩振动峰,且湿式有氧环境下进行吸附作用的活性炭在620 cm-1处还有一个SO2-4的不对称变角振动弱峰,由此可判断SO2经活性炭吸附后,在其表面以SO2-4的形式存在. 另外湿式有氧环境同时脱硫脱硝以及有氧环境下单独脱硝的两个材料在1180 cm-1附近均有一个相似的强吸收峰,该峰为亚硝基N O的伸缩振动,说明NO通过亚硝基的形式结合在活性炭表面.
 | 1.吸附前; 2.无氧脱硫脱硝; 3.有氧脱硫脱硝; 4.湿式有氧脱硫脱硝; 5.无氧脱硫; 6.有氧脱硝 图 6 材料吸附SO2、 NO的红外光谱谱图 Fig. 6 IR spectra of the material adsorbing SO2 and/or NO |
对无氧环境、 有氧环境及湿式有氧环境下同时脱硫脱硝的活性炭进行水洗再生处理,以研究废茶活性炭材料再生后结构的变化,进而判断材料对于SO2、 NO的吸附作用. 活性炭的再生实验是将吸附饱和的活性炭用蒸馏水洗至滤液呈中性,然后在105℃下烘干后即得到脱附再生样.
水洗再生得到的废茶活性炭红外光谱谱图如图 7所示,再生后活性炭在无氧脱硫脱硫产生的在1380 cm-1附近处的SO2反对称伸缩振动峰已消失,有氧脱硫脱硝增加1210~1025 cm-1处的硫酸根吸收峰也基本消失. 湿式有氧环境脱硫脱硝增加620 cm-1处硫酸根的不对称变角振动弱峰并未消失,可见活性炭表面吸附的硫酸根并未完全洗去,而1250~1000 cm-1处的吸收峰有所削弱,可能是1180 cm-1附近出现的硝酸根被洗去的缘故. 由此可知,湿式有氧环境下吸附的SO2在活性炭表面以较强的化学键连接,难以通过水洗条件进行脱除.
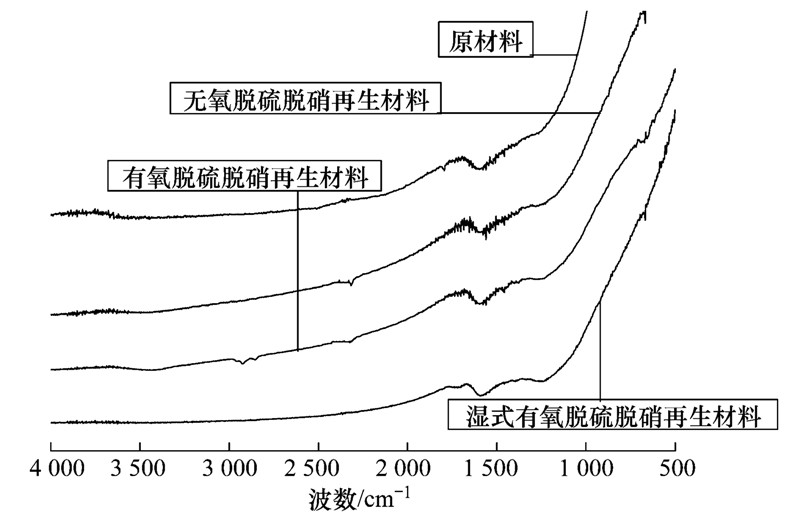 | 图 7 再生活性炭的红外光谱谱图
Fig. 7 IR spectra of regenerated activated carbon
|
再生活性炭的氮气吸附等温线如图 8所示,废茶活性炭经脱硫脱硝并脱附处理后,氮气吸附等温线类型与吸附前的废茶活性炭相似,均为I-B型等温线,表明活性炭经吸附后孔径结构无明显变化,仍以微孔分布为主. 其中在无氧环境和有氧环境下同时吸脱硫脱硝后的再生活性炭对于N2的饱和吸附量与原始活性炭相近,说明经水洗再生后的废茶活性炭能够将吸附态的SO2和NO彻底脱附,由此可判断废茶活性炭在无氧环境和有氧环境下对于SO2和NO吸附的作用力很弱,属于物理吸附作用. 在湿式有氧的环境下,废茶活性炭水洗再生后的N2饱和吸附量明显降低,可见吸附态的SO2和NO与活性炭表面的作用力较强,水蒸气的存在可能促进了活性炭对于SO2、 NO的化学吸附.
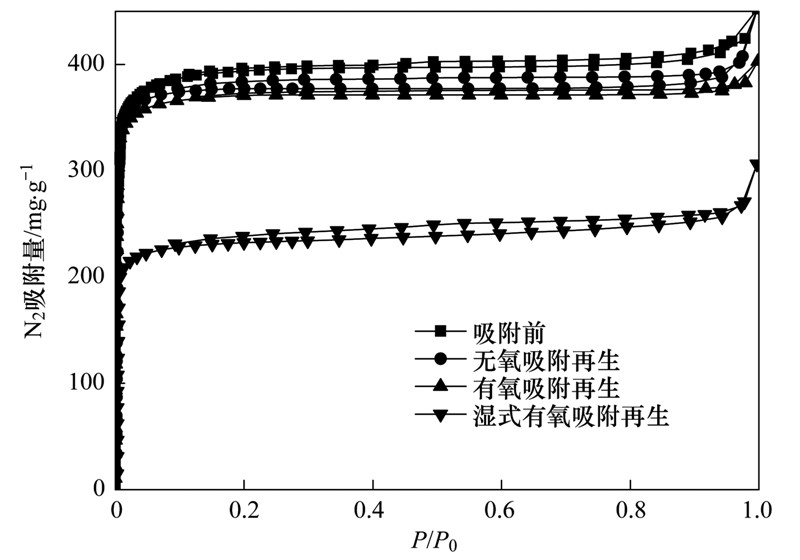 | 图 8 再生活性炭的氮气吸附等温线
Fig. 8 Nitrogen adsorption isotherms of regenerated activated carbon
|
吸附质分子在活性炭表面的吸附过程包括3个阶段:第一阶段为颗粒外部扩散阶段,吸附质分子从外部扩散至活性炭表面; 第二阶段为孔隙扩散阶段,吸附质分子在孔道中的扩散至吸附位点; 第三阶段即为吸附质分子与活性炭孔壁的相互作用,其中速率最慢的过程是主要的速率控制步骤[32]. 吸附过程的动力学研究主要是用来描述吸附剂吸附溶质的速率快慢,通过动力学模型对数据进行拟合,从而探讨活性炭对SO2、 NO吸附过程的控制机制. 常用的模型包括Lagergren准一级速率模型、 准二级速率模型以及Bangham模型,其中Lagergren准一级模型,可用于描述表面反应控制和外扩散控制的过程,Bangham模型对Lagergren模型进行时间补偿,能够很好地描述活性炭的吸附过程. 由前期实验研究发现Bangham模型对于的SO2吸附数据拟合效果最好[33],由此选用Bangham吸附模型对废茶活性炭WTAC-K-1 在不同条件下吸附SO2和NO的数据进行拟合,以期更好地描述废茶活性炭对于SO2和NO吸附过程.
Bangham吸附速率方程[34]可写成如下形式:
dQ/dt=k(Qe-Q)/tz
积分并整理后得:
Q=Qe-Qe/ektz
式中,t为时间,h; z为常数; k为常数(min-z).
废茶活性炭WTAC-K-1在不同环境下吸附SO2
和NO的Bangham模型拟合参数见表 4,由于活性炭在无氧环境下对NO单独吸附量偏低,无法得到模型拟合结果. 从中的数据可以看出,Bangham模型对于SO2和NO的吸附数据拟合效果较好,R2均大于0.989,且由方程得到的Qe与实验数据得到的结果也较接近,可见废茶活性炭对于SO2和NO的吸附受到表面反应控制或外扩散控制. 通过速率常数k的比较可发现,材料在无氧环境下单独吸附SO2的速率低于同时吸附时的速率,氧气和水蒸气的加入均降低了SO2和NO的吸附速率. 主要由于SO2和NO同时存在促进了活性炭表面活性位点的利用率,二者在一定程度上促进彼此的吸附速率,而氧气和水蒸气与吸附态的SO2和NO发生化学反应,使其固定在活性炭表面,这一步骤的进行减缓了活性炭对于SO2和NO的吸附速率.
| 表 4 废茶活性炭对于SO2、 NOx的吸附动力学方程拟合参数 Table 4 Parameters of kinetic models for adsorption of SO2,NOx onto waste tea activated carbon |
(1)废茶活性炭单独脱除SO2的作用主要受材料的石墨化程度、 微孔结构以及表面含氮碱性官能团等因素的制约,其中石墨化程度过高不利于脱硫作用的进行,而平均微孔径较小、 含氮碱性官能团较高的材料脱硫效果较好,材料在有氧条件下的脱硫效率有所提高.
(2)废茶活性炭在无氧环境下对于NO的脱除效率很低,在有氧环境下中孔结构的存在抑制了材料的脱硝作用、 含氮碱性官能团能够促进材料脱硝的作用的进行.
(3)烟气中SO2和NO共存时,材料在无氧环境、 有氧环境及湿式有氧环境下的脱硫脱硝性能均有所降低,结合红外光谱及再生材料的吸附等温线可得,在无氧环境、 有氧环境下材料对SO2和NO的脱除作用以物理吸附为主,而在湿式有氧环境下,水蒸气促进了SO2的化学吸附.
(4)Bangham吸附动力学模型适于描述废茶活性炭对SO2和NO的吸附动力学过程,其R2均高于0.989,氧气和水蒸气的加入均降低了SO2和NO的吸附速率.
| [1] | 谢新苹, 蒋剑春, 孙康, 等. 脱硫脱硝用活性炭研究进展[J]. 生物质化学工程, 2012, 46 (1): 45-50. |
| [2] | 高德霖, 孙小玉. 活性炭纤维和微孔吸附的容积充填理论[J]. 精细化工原料及中间体, 2003, (9): 2-5. |
| [3] | 方平, 岑超平, 唐志雄, 等. 污泥含炭吸附剂对甲苯的吸附性能研究[J]. 高校化学工程学报, 2010, 24 (5): 887-892. |
| [4] | 刘义, 刘光远. 水涤脱附条件下活性炭脱除SO2和NO中吸附反应空间的研究[J]. 西安建筑科技大学学报 (自然科学版), 2012, 44 (2): 253-258. |
| [5] | Raymundo-Pinero E, Cazorla-Amoros D, Salinas-Martinez de Lecea C, et al. Factors controling the SO2 removal by porous carbons relevance of the SO2 oxidation step[J]. Carbon, 2000, 38 (3): 335-344. |
| [6] | Muniz J, Marbán G, Fuertes A B. SO2 retention over polyarylamide-based activated carbon fibers[J]. Environmental Progress, 2000, 19 (4): 246-254. |
| [7] | Muniz J, Herrero J E, Fuertes A B. Treatments to enhance the SO2 capture by activated carbon fibres[J]. Applied Catalysis B: Environmental, 1998, 18 (1-2): 171-179. |
| [8] | Mangun C L, DeBarr J A, Economy J. Adsorption of sulfur dioxide on ammonia-treated activated carbon fibers[J]. Carbon, 2001, 39 (11): 1689-1696. |
| [9] | 杨辉, 刘豪, 周康, 等. 活性炭纤维吸附脱除NO过程中NO氧化路径分析[J]. 燃料化学学报, 2012, 40 (8): 1002-1008. |
| [10] | 姚天保. 不同木材活性炭的比较研究初报[J]. 中南林学院学报, 1989, 9 (1): 66-68. |
| [11] | 潘静霞, 郁万文, 曹福亮. 银杏活性炭的孔隙结构与孔径分布[J]. 经济林研究, 2011, 29 (1): 110-114. |
| [12] | 陈丛瑾, 黎跃, 赵兰线. 微波氯化锌法马占相思木材剩余物制备活性炭[J]. 林产化学与工业, 2007, 27 (1): 101-103. |
| [13] | 董宇, 申哲民, 王茜, 等. 生物质活性炭制备的比较研究[J]. 安徽农业科学, 2011, 39 (6): 3444-3448. |
| [14] | Dias J M, Alvim-Ferraz M C M, Almeida M F, et al. Waste materials for activated carbon preparation and its use in aqueous-phase treatment: a review[J]. Journal of Environmental Management, 2007, 85 (4): 833-846. |
| [15] | Ioannidou O, Zabaniotou A. Agricultural residues as precursors for activated carbon production-a review[J]. Renewable and Sustainable Energy Reviews, 2007, 11 (9): 1966-2005. |
| [16] | Yagmur E, Ozmak M, Aktas Z. A novel method for production of activated carbon from waste tea by chemical activation with microwave energy[J]. Fuel, 2008, 87 (15-16): 3278-3285. |
| [17] | Yagmur E. Preparation of low cost activated carbons from various biomasses with microwave energy[J]. Journal of Porous Materials, 2012, 19 (6): 995-1002. |
| [18] | Gurten I I, Ozmak M, Yagmur E, et al. Preparation and characterisation of activated carbon from waste tea using K2CO3[J]. Biomass and Bioenergy, 2012, 37: 73-81. |
| [19] | Borah L, Senapati K K, Borgohain C, et al. Preparation of ordered porous carbon from tea by chemical activation and its use in Cr(Ⅵ) adsorption[J]. Journal of Porous Materials, 2012, 19 (5): 767-774. |
| [20] | Auta M, Hameed B H. Preparation of waste tea activated carbon using potassium acetate as an activating agent for adsorption of Acid Blue 25 dye[J]. Chemical Engineering Journal, 2011, 171 (2): 502-509. |
| [21] | 宋磊, 张彬, 陈家元, 等. 废茶活性炭的制备及其孔径结构的控制[J]. 化工进展, 2014, 33 (6): 1498-1505. |
| [22] | Reyhani A, Nozad Golikand A, Mortazavi S Z, et al. The effects of multi-walled carbon nanotubes graphitization treated with different atmospheres and electrolyte temperatures on electrochemical hydrogen storage[J]. Electrochimica Acta, 2010, 55 (16): 4700-4705. |
| [23] | Tuinstra F, Koenig J L. Characterization of graphite fiber surfaces with Raman spectroscopy[J]. Journal of Composite Materials, 1970, 4 (4): 492-499. |
| [24] | Davini P. Flue gas desulphurization by activated carbon fibers obtained from polyacrylonitrile by-product[J]. Carbon, 2003, 41 (2): 277-284. |
| [25] | 李开喜, 凌立成, 刘朗, 等. 氨水活化的活性炭纤维的脱硫作用[J]. 环境科学学报, 2001, 21 (1): 74-78. |
| [26] | Bagreev A, Bashkova S, Bandosz T J. Adsorption of SO2 on activated carbons: the effect of nitrogen functionality and pore sizes[J]. Langmuir, 2002, 18 (4): 1257-1264. |
| [27] | Punyawudho K, Ma S, Van Zee J W, et al. Effect of O2 on the adsorption of SO2 on carbon-supported Pt electrocatalysts[J]. Langmuir, 2011, 27 (12): 7524-7530. |
| [28] | Adapa S, Gaur V, Verma N. Catalytic oxidation of NO by activated carbon fiber[J]. Chemical Engineering Journal, 2006, 116 (1): 25-37. |
| [29] | 刘鹤年, 黄正宏, 王明玺, 等. 常温下沥青基活性炭纤维对 NO 的催化氧化性能[J]. 化工学报, 2011, 62 (2): 369-373. |
| [30] | Guo Y, Liu S, Zhang Y, et al. Effects of concentration and adsorption product on the adsorption of SO2 and NO on activated carbon[J]. Energy and Fuels, 2013, 27 (1): 360-366. |
| [31] | 许绿丝, 岑泽文, 曾汉才, 等. 活性炭纤维吸附 NO 和 SO2 的试验研究[J]. 华中科技大学学报 (自然科学版), 2006, 34 (2): 105-107. |
| [32] | 高继贤, 王铁峰, 王光润, 等. 不同烟气水蒸汽体积分数时ZL50活性炭吸附SO2的动力学[J]. 清华大学学报 (自然科学版), 2010, 50 (3): 434-437. |
| [33] | 张彬, 宋磊. 活性炭材料的孔径结构对SO2吸附性能的影响[J], 华侨大学学报 (自然科学版), 2014, 35 (3): 293-298. |
| [34] | Aksu Z. Biosorption of reactive dyes by dried activated sludge: equilibrium and kinetic modeling[J]. Biochemical Engineering Journal, 2001, 7 (1): 79-84. |
 2014, Vol. 35
2014, Vol. 35

