2. 浙江省工业环保设计研究院有限公司,杭州 310005
2. Institute of Zhejiang Environmental Protection Design & Research Co., Ltd., Hangzhou 310005, China
嗜酸性氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans, A.f)是化能自养菌,能生长在亚铁、 单质硫及硫化物矿物上[1],且能通过直接作用或其代谢产物的间接作用,产生氧化、 还原、 络合、 吸附或溶解作用[2],达到浸出固相中重金属的效果.目前已在市政污泥[3, 4]、 制革污泥[5]重金属脱除、 矿山冶金[6, 7]等领域成熟应用.同时,在A.f浸出废弃电子材料[8, 9]、 废旧电池[10, 11]、 熔炼粉尘[12, 13]中重金属方面取得较好试验效果.
为较好地利用A.f浸出固相中重金属,需要对处理对象或浸出液中主要成分对功能菌株活性的影响进行研究,为之后的浸出试验研究提供理论支持,以较好地指导后续的工程推广应用.目前,研究人员进行了Ni2+、 Co2+[14],Cu2+[15],Mg2+[16],Cr3+、 Cr6+、 Mn2+[17]单一重金属离子; Cu2+、 Zn2+、 Fe3+复合重金属离子[18]; 甲酸、 乙酸、 丙酸、 苹果酸等低分子有机物[2, 19]; NO-3、 SO2-4、 Cl-和PO3-4等阴离子[20]; 闪锌矿、 黄铜矿、 黄铁矿、 方铅矿等硫化矿[1, 21]对A.f活性影响的研究.
为了研究、 开发电镀污泥生物浸出技术,需考察电镀污泥浸出液对A.f活性的影响,本课题组之前研究了以Ni2+、 Cr3+、 Cu2+、 Zn2+为主要组分的模拟电镀污泥重金属浸出液对自主分离纯化的氧化亚铁硫杆菌菌株WZ-1(GenBank序列登录号:JQ968461)活性的影响[24],获得了不同浓度、 不同种类重金属离子分别在单一和复合条件下对氧化亚铁硫杆菌WZ-1活性的不同影响结果.本研究在上述试验基础上,以电镀污泥浸出液中常见的无机阴离子作为影响因素,考察分析单一无机阴离子和模拟电镀污泥阴离子浸出液对WZ-1活性的影响,以获得电镀污泥浸出液中无机阴离子对A.f活性的影响规律,以期为后续理论试验研究及技术开发应用奠定基础. 1 材料与方法 1.1 菌株的培养及试验装置
(1)菌株的培养
氧化亚铁硫杆菌WZ-1分离自浙江省温州市龙湾区某制革污水处理站二沉池污泥,经细菌形态观察、 革兰氏染色观察以及16S rDNA的PCR扩增、 序列测定和系统发育树分析,确定该菌为1株氧化亚铁硫杆菌,取名WZ-1,GenBank中的序列登录号为JQ968461.氧化亚铁硫杆菌WZ-1的培养以及相关试验均于9K液体培养基中进行,培养基成分组成如下(g ·L-1):(NH4)2SO4 3.00,MgSO4 ·7H2 O 0.50,K2HPO4 0.50,KCl 0.10,Ca(NO3)2 0.01,FeSO4 ·7H2 O 44.20,pH 2.0.于30℃摇床中培养或试验(150 r ·min-1)[22].
(2)试验装置
试验采用200mL已灭菌的锥形瓶作为培养容器,并选用恒温摇床为试验培养提供恒温及规律摇晃环境.图1为试验期间,某一时刻各试验组溶液的不同颜色区别.
 | 图1试验期间某一时刻各试验组溶液的颜色区别Fig.1 Color difference between different liquids of experimental group at one point |
试验选用Cl-、 NO-3、 F-作为试验用无机阴离子,向140 mL 9K液体培养基中投加不同量的金属盐配制不同浓度试验组.接种对数期WZ-1到试验组,用1.0 mol ·L-1稀硫酸调节体系初始pH至2.0,然后置于恒温摇床中在30℃、 150 r ·min-1条件下培养.培养过程中,每12 h测定培养液pH值、 ORP以及Fe2+浓度.试验开始后第0h、 第48 h、 第96 h测定WZ-1的累计耗氧量.试验用金属盐分别为:ZnCl2、 Zn(NO3)2、NaF.试验组设置见表1 .
| 表1 单一无机阴离子对WZ-1活性影响试验试验组设置1) Table 1 Group settings of the experiment for investigating the influence of single inorganic anion on WZ-1s bioactivity |
该试验以1.2节试验结果为设计依据,分别选取对WZ-1活性影响最小的无机阴离子浓度作为模拟电镀污泥阴离子浸出液中各无机阴离子浓度,其中,试验组初始条件、 试验过程和方法同1.3节,试验组设置见表2.
| 表2 模拟电镀污泥无机阴离子浸出液对WZ-1活性影响试验试验组设置1) Table 2 Group settings of the experiment for investigating the influence of simulated anion leaching solution of electroplating sludge on WZ-1s bioactivity |
(1)pH、 ORP和Fe2+监测方法[22] pH、 ORP采用FE20K精密pH计测定,pH电极型号为LE438,ORP电极型号为LE510(梅特勒- 托利多仪器(上海)有限公司); Fe2+浓度测定采用 邻菲啰啉分光光度法[23].
(2)WZ-1累计耗氧量和表观呼吸速率测定方法[22]
WZ-1累计耗氧量通过BI-2000电解呼吸仪测定,表观呼吸速率为累计耗氧量曲线斜率.WZ-1在液体培养基中进行好氧呼吸,同时进行Fe2+氧化作用,两者的共同作用会导致水封瓶内O2被消耗,导致瓶内压力降低,外腔与大气相通,由于内外气压差,电解单元内腔液面上升、 外腔液面下降,当外腔探针离开液面时,系统自动接通电解单元电源,开始电解稀硫酸生成O2,补充瓶内被消耗的O2,外腔产生的H2逸出至大气中,压力恢复后,外腔液面上升,当探针重新接触液面后,电解单元停止工作.测试数据直接通过计算机记录,每3 min记录1次.BI-2000电解呼吸仪具有自动磁力搅拌功能,转速为100 r ·min-1,水浴温度为30℃.试验时,准确量取100 mL混合培养液于150 mL水封瓶内,组装完毕后进行系统检漏,检漏成功后运行1 h,待系统温度完全稳定后,正式启动呼吸仪开始监测.
2 结果与讨论 2.1 单一无机阴离子对WZ-1活性的影响 2.1.1 单一无机阴离子对WZ-1 Fe2+氧化活性的影响
Acidithiobacillus ferrooxidans在生物浸出过程中,依靠将Fe2+氧化成Fe3+这一过程来获得自身生长繁殖所需能量,Fe2+的氧化程度能表征其代谢活性[23],Fe2+氧化率依照式(1)计算.
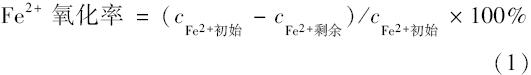
图2为Cl-、 NO-3、 F-对WZ-1氧化Fe2+的影响作用. 从图2可知,空白组CK-2中WZ-1经12 h后即进入对数增长期,培养液中的Fe2+在60 h内被完全氧化,Fe2+氧化平均速率为114.44 mg ·h-1,表明WZ-1具有较好的Fe2+氧化活性.
 | 图2 不同浓度Cl-、 NO-3、 F-对WZ-1氧化Fe2+的影响 Fig.22 Effects of different concentrations of Cl-, NO-3, F- on Fe2+ oxidation of WZ-1 |
由图2(a)、 2(b)分别可知,低浓度Cl-(5.0 g ·L-1)、 NO-3(1.0 g ·L-1)对WZ-1的Fe2+氧化活性几乎没有影响.培养60 h时,Cl-1、 NO3-1已氧化99%以上的Fe2+,Fe2+平均氧化速率分别为115.41 mg ·h-1、 120.69 mg ·h-1,较空白组CK-2几乎没有差别.这一结果与张成桂等[20]的研究结果有所不同,其研究表明:0.05 mol ·L-1(1.775 g ·L-1)的Cl-完全抑制氧化亚铁硫杆菌活性,整个试验过程中,氧化亚铁硫杆菌数量没有增长趋势,pH亦无下降变化; 3.1 g ·L-1的NO-3亦对氧化亚铁硫杆菌产生完全抑制作用,而WZ-1在3.0g ·L-1甚至5.0 g ·L-1的NO-3浓度条件下仍具有较好的Fe2+氧化活性.当Cl-、 NO-3浓度上升,WZ-1的Fe2+氧化活性则开始受到抑制,至浓度分别达到20.0 g ·L-1、 10.0 g ·L-1时,WZ-1完全丧失Fe2+氧化活性.这或许由于WZ-1分离于制革污泥,制革污水中各种阴离子较为复杂,包括Cl-和NO-3,WZ-1长期生活于该环境中,对其已产生一定的耐性,但当浓度上升至一定阶段后,WZ-1还是无法适应高浓度Cl-和NO-3.
由图2(c)可知,WZ-1在25.0 mg ·L-1F-存在的条件下,活性受到一定的抑制,但经过近50 h的停滞期后,WZ-1逐渐适应该环境,并开始快速氧化培养液中的Fe2+,至第96 h时,Fe2+氧化率达到85.87%,亚铁平均氧化率为66.72 mg ·L-1.随着F-浓度的不断上升,WZ-1的Fe2+氧化活性受到完全抑制.研究表明:WZ-1较一般的氧化亚铁硫杆菌对Cl-和NO-3有更好的耐受能力,5.0 g ·L-1的Cl-和1.0g ·L-1的NO-3对WZ-1的活性几乎没有影响,25.0mg ·L-1F-对WZ-1的活性有一定的抑制作用,随着浓度的上升,WZ-1活性开始受到明显抑制,当Cl-、 NO-3和F-浓度分别达到20.0g ·L-1、 10.0g ·L-1和50.0mg ·L-1时,WZ-1完全失活.
根据上述试验结果可知,试验所用3种无机阴离子对WZ-1 Fe2+氧化活性的影响顺序为:F->NO-3>Cl-. 2.1.2 单一无机阴离子对WZ-1累计耗氧量和表观呼吸速率的影响
针对2.1.1节的试验结果,本研究利用BI-2000电解呼吸仪测定WZ-1在不同试验阶段的累计耗氧量并计算其表观呼吸速率,以验证无机阴离子对WZ-1活性的影响规律.
 | 图3 不同浓度Cl-、 NO-3、 F-对WZ-1表观呼吸速率的影响 Fig.3 Effects of different concentrations of Cl-, NO-3, F- on the apparent respiratory rate of WZ-1 |
通过测定分析WZ-1的累计耗氧量和表观呼吸速率,从细菌利用O2进行生命活动的能力方面验证了单一无机阴离子对WZ-1活性的影响.WZ-1呼吸试验的结果与2.1.1节的试验结果一致. 2.2 模拟电镀污泥阴离子浸出液对WZ-1活性的影响
为了考察电镀污泥阴离子浸出液对WZ-1活性的影响,根据2.1节试验结果,选取对WZ-1活性抑制作用较小的各无机阴离子浓度配制模拟电镀污泥阴离子浸出液,而预试验结果显示:Cl-、 NO-3、 F-浓度分别为5.0 g ·L-1、 1.0 g ·L-1、 25 mg ·L-1时,WZ-1完全失活,所有试验组无试验差异,因此,Cl-、 NO-3、 F-的配制浓度改为:2.5 g ·L-1、 0.5 g ·L-1、 25 mg ·L-1.
氧化亚铁硫杆菌被接种到新鲜的9K液体培养基后,能快速氧化其中的Fe2+,这一过程需要消耗培养液中的H+[式(2)],当培养液中大部分Fe2+被氧化为Fe3+后,Fe3+开始水解,并产生H+[式(3)],这就是培养过程中pH先升后降的主要原因[24],因此,pH值是氧化亚铁硫杆菌培养过程中的一个重要指标.

图4反映了不同模拟电镀污泥阴离子浸出液对培养液pH、 ORP、 Fe2+氧化率以及WZ-1表观呼吸速率变化的影响.所有试验组的pH值在12 h内均有所上升,对比CK-1的pH变化趋势,可知这不是由WZ-1氧化Fe2+所引起的pH值上升,而是由于培养基具有一定的pH滞后性所造成的.接种12 h后,CK-2的pH值快速上升,至第48 h时,pH达到最大值2.45,之后由于Fe3+水解作用不断释放H+,培养液的pH值持续下降.相应的,CK-2的ORP在前36 h缓慢上升,由最初的356 mV上升至448 mV,之后快速上升,至第96 h达到614 mV.比较不同试验组的pH值、 ORP变化曲线,可以明显看出不同模拟电镀污泥阴离子浸出液对培养液pH值和ORP变化的影响差异.结合图4(c)中各试验组Fe2+氧化曲线,可见试验组进入Fe2+快速氧化期的拐点与pH快速上升的拐点处于相同时刻,而当培养液中Fe2+氧化率达到50%以上时,溶液的ORP快速上升.
 | 图4 模拟电镀污泥阴离子浸出液对培养液pH值、 ORP、 Fe2+氧化及WZ-1表观呼吸速率变化的影响 Fig.4 Effects of simulated inorganic anion leaching solution of electroplating sludge on changes of pH,ORP,Fe2+ oxidation and apparent respiratory of WZ-1 |
图4(c)中不同模拟电镀污泥阴离子浸出液对WZ-1 Fe2+氧化活性影响的差异明显. Cl-/NO-3/F-和NO-3/F-这2种模拟电镀污泥阴离子浸出液对WZ-1的Fe2+氧化活性抑制最显著,Fe2+氧化率在试验结束时分别仅为17.32%、 19.82%,比较CK-1可知WZ-1几乎完全丧失Fe2+氧化活性.而分别由Cl-、 NO-3和Cl-、 F-组成的模拟电镀污泥阴离子浸出液对WZ-1 Fe2+氧化活性影响较小,试验中,WZ-1虽然分别有近12 h和24 h的停滞期,但随后即进入对数生长期,其Fe2+氧化速率较快,分别于第72 h和第96 h达到99%以上的Fe2+氧化率,与此同时,CK-2达到99%Fe2+氧化率的耗时为60 h.图4(d)中各试验组WZ-1的表观呼吸速率大小顺序及变化趋势与图4(c)的Fe2+氧化曲线在对应时刻的斜率大小及其变化趋势一致.
根据上述试验结果可知,不同模拟电镀污泥阴离子浸出液对WZ-1活性影响的差异明显,Cl-、 NO-3、 F-配制浓度分别为2.5 g ·L-1、 0.5 g ·L-1、 25 mg ·L-1时,Cl-/NO-3/F-和NO-3/F-这2种模拟电镀污泥阴离子浸出液对WZ-1活性产生完全抑制,Cl-/NO-3和Cl-/F-这2种模拟电镀污泥阴离子浸出液对WZ-1活性的影响较小,5种模拟电镀污泥阴离子浸出液对WZ-1活性影响的大小为:Cl-/NO-3/F-≥NO-3/F->Cl-/F->Cl-/NO-3. 3 结论
(1)WZ-1较一般的氧化亚铁硫杆菌对Cl-和NO-3有更好的耐受能力,5.0 g ·L-1的Cl-和1.0 g ·L-1的NO-3对WZ-1的活性几乎没有影响.WZ-1对单一Cl-、 NO-3、 F-的最大耐受浓度分别为10.0 g ·L-1、 5.0 g ·L-1、 25.0 mg ·L-1.
(2)根据模拟电镀污泥阴离子浸出液对WZ-1活性影响大小的顺序,从阴离子这一影响因素角度考虑,WZ-1较适合处理含一定量Cl-/F-或Cl-/NO-3为主要阴离子组分的电镀污泥,对同时含有Cl-/NO-3/F-或者NO-3/F-的电镀污泥则完全失效.
| [1] | 周吉奎, 钮因健, 覃文庆. 硫化矿对浸矿细菌(Fe2+)氧化活性的影响[J]. 中国有色金属学报, 2003, 13 (5): 1278-1282. |
| [2] | 任婉侠, 李培军, 范淑秀, 等. 低分子量有机酸对氧化亚铁硫杆菌影响[J]. 环境工程学报, 2008, 2 (9): 1269-1273. |
| [3] | Tyagi R D, Blais J F, Meunier N, et al. Simultaneous sewage sludge digestion and metal leaching-Effect of sludge solids concentration [J]. Water Research, 1997, 31 (1): 105-118. |
| [4] | 周顺桂, 王世梅, 余素萍, 等. 污泥中氧化亚铁硫杆菌的分离及其应用效果[J]. 环境科学, 2003, 24 (3): 56-60. |
| [5] | 周立祥, 周顺桂, 王世梅, 等. 制革污泥中铬的生物脱除及其对污泥的调理作用[J]. 环境科学学报, 2004, 24 (6): 1014-1020. |
| [6] | Watling H R, Elliot A D, Maley M, et al. Leaching of low-grade, copper-nickel sulfide ore. 1. Key parameters impacting on Cu recovery during column bioleaching [J]. Hydrometallurgy, 2009, 97 (3-4): 204-212. |
| [7] | Cameron R A, Lastra R, Gould W D, et al. Bioleaching of six nickel sulphide ores with different mineralogies in stirred-tank reactors at 30℃ [EB/OL]. http://dx.doi.org/10.1016/j.mineng.2011.03.016, 2011-04-09. |
| [8] | Wang J W, Bai J F, Xu J Q, et al. Bioleaching of metals from printed wire boards by Acidithiobacillus ferrooxidans and Acidithiobacillus thiooxidans and their mixture [J]. Journal of Hazardous Materials, 2009, 172 (2-3): 1100-1105. |
| [9] | Kasper A C, Berselli G B T, Freitas B D, et al. Printed wiring boards for mobile phones: Characterization and recycling of copper [J]. Waste Management, 2011, 31 (12): 2536-2545. |
| [10] | Zeng G S, Deng X R, Luo S L, et al. A copper-catalyzed bioleaching process for enhancement of cobalt dissolution from spent lithium-ion batteries [J]. Journal of Hazardous Materials, 2012, 199-200 : 164-169. |
| [11] | Xin B P, Zhang D, Zhang X, et al. Bioleaching mechanism of Co and Li from spent lithium-ion battery by the mixed culture of acidophilic sulfur-oxidizing and iron-oxidizing bacteria [J]. Bioresource Technology, 2009, 100 (24): 6163-6169. |
| [12] | Vakylabad A B, Ranjbar M, Manafi Z, et al. Tank bioleaching of copper from combined flotation concentrate and smelter dust [J]. International Biodeterioration & Biodegradation, 2011, 65 (8): 1208-1214. |
| [13] | Bakhtiari F, Atashi H, Zivdar M, et al. Bioleaching kinetics of copper from copper smelters dust [J]. Journal of Industrial and Engineering Chemistry, 2011, 17 (1): 29-35. |
| [14] | 李洪枚, 柯家骏. Ni2+和Co2+对氧化亚铁硫杆菌活性的影响[J]. 有色金属, 2000, 52 (1): 49-54. |
| [15] | 李洪枚, 柯家骏. Cu2+对氧化亚铁硫杆菌(T. f)生长活性的影响[J]. 黄金, 2000, 21 (6): 27-29. |
| [16] | 李洪枚, 柯家骏. Mg2+对氧化亚铁硫杆菌生长活性的影响[J]. 中国有色金属学报, 2000, 10 (4): 576-578. |
| [17] | Wong C, Silver M, Kushner D J. Effects of chromium and manganese on Thiobacillus ferrooxidans [J]. Canadian Journal of Microbiology, 1982, 28 (5): 536-544. |
| [18] | Das A, Modak J M, Natarajan K A. Studies on multi-metal ion tolerance of Thiobacillus ferrooxidans [J]. Minerals Engineering, 1997, 10 (7): 743-749. |
| [19] | 张再利, 沈镭, 贾晓珊. 有机碳源对氧化亚铁硫杆菌生长的影响[J]. 中山大学学报(自然科学版), 2006, 45 (6): 121-124. |
| [20] | 张成桂, 张倩, 王晶, 等. 阴离子对嗜酸氧化亚铁硫杆菌生长和硫氧化活性的影响[J]. 中国有色金属学报, 2009, 19 (12): 2237-2242. |
| [21] | 周吉奎, 钮因健, 邱冠周, 等. 闪锌矿对氧化亚铁硫杆菌Fe2+氧化活性的影响[J]. 有色金属, 2003, 55 (4): 51-53. |
| [22] | 谢鑫源, 孙培德, 楼菊青, 等. 模拟电镀污泥重金属浸出液对氧化亚铁硫杆菌活性的影响[J]. 环境科学, 2013, 34 (1): 209-216. |
| [23] | 谢海云, 刘中华, 周峨. 高铁离子浓度下氧化亚铁硫杆菌的生长行为[J]. 过程工程学报, 2004, 4 (1): 43-46. |
| [24] | Xiong H X, Guo R. Effects of chloride acclimation on iron oxyhydroxides and cell morphology during cultivation of Acidithiobacillus ferrooxidans [J]. Environmental Science & Technology, 2010, 45 (1): 235-240. |
 2014, Vol. 35
2014, Vol. 35


