2. 同济大学环境科学与工程学院, 上海 200092
2. College of Environmental Science and Engineering, Tongji University, Shanghai 200092, China
近年来,全球许多地区都检测出抗生素,种类也呈现越来越多的趋势.抗生素的生态风险引起了人们的广泛关注[1, 2, 3, 4, 5, 6].光催化降解是目前抗生素降解研究应用的热点,最常用的催化剂为光敏半导体TiO2.关于吸附和催化降解关系的研究屡见报道,所研究的污染物主要为农药,酚类,染料等[7, 8, 9, 10, 11, 12],但对于抗生素的相关研究较少.因此本研究分析了pH、 TiO2投加量和四环素初始浓度单因素对光催化降解的影响之外,着重探讨了吸附过程与催化降解过程的关联.
另外,在环境水体中发现的抗生素污染呈现出复杂性和多样性的特点[13, 14, 15, 16],因此在应对抗生素污染时,往往需要面对多种抗生素的混合溶液.而目前的大部分研究均着眼于单一抗生素的降解,对于多种抗生素混合溶液的降解特性仍缺乏关注.本研究对四环素与磺胺甲 唑和阿莫西林这2种抗生素混合后在不同pH和TiO2投加量条件下的光催化降解特性进行了初步分析,对于揭示混合抗生素的降解机制与光催化降解技术的实际应用具有积极作用.
本实验中采用的实验材料包括盐酸四环素、 阿莫西林、 TiO2以及缓冲试剂、 分析试剂.盐酸四环素、 磺胺甲 唑、 阿莫西林(纯度>99%)购自Fluka(USA),TiO2 P25购自德国德固赛(Degussa)公司,NaH2PO4购自国药集团药业股份有限公司,色谱纯乙腈(纯度>99.5%)购自德国莫克(Merk)公司,色谱纯甲酸(纯度>96%)购自TEDIA公司.实验中的所有溶液及分析过程中的水相均采用美国Millipore超纯水配制.
待测样品采用HPLC-VWD(Agilent 1200,USA)进行分析,采用紫外检测器,检测波长为:四环素360 nm,磺胺甲 唑265 nm,阿莫西林254 nm.色谱柱均采用C18反向柱(2590 mm×4.5 mm, 5 μm, Agilent,USA).色谱分析具体条件分别为:四环素,磺胺甲 唑,流动相20%乙腈和80%甲酸溶液,pH=6; 阿莫西林,流动相40%乙腈和60% 50 mmol KH2PO4溶液,pH=5.其余条件均相同,流速为1 mL ·min-1; 柱温25℃; 进样量10 μL.
使用不同pH的NaH2PO4缓冲溶液配制一定浓度四环素溶液,投入一定量的纳米TiO2粉末.实验在光催化反应器内进行,光照前置于黑箱内磁力搅拌器上搅拌30 min,待四环素在TiO2上吸附稳定后,打开紫外灯光照.不同实验条件下光照均为10 min,紫外灯功率均为75 W. 365 nm波长处测得的光强为5.3×10-4 W ·cm-2.定时取样, 14000 r ·min-1离心10 min,再用0.45 μm滤膜过滤后测定.
吸附实验中,四环素溶液在暗处配制,称取一定量的四环素与TiO2(保证催化剂投加量为1.0 g ·L-1),用NaH2PO4缓冲液溶解至所需浓度,并用H3PO4和NaOH调节pH(pH为3、 6、 9).溶液在黑箱内的磁力搅拌器上搅拌30 min,以达到吸附平衡.采取2 mL溶液样品迅速离心过滤测定(离心及过滤条件同单因素实验).所有吸附实验都进行3次平行实验.
光照实验在一个圆柱形反应器内进行,反应器分为内外两部分,外部为反应容器,容积为0.8 L,是反应器的主要区域,并用小型气泵进行曝气供氧; 内部为石英双层冷却套管,内层放置紫外灯,夹层为冷水浴.光源为一支75 W的紫外光汞灯(波长=365 nm), 365 nm波长处测得的光强为5.3×10-4 W ·cm-2.圆柱形光反应器置于磁力搅拌器上保证TiO2分散均匀,并用不锈钢黑箱遮光.将缓冲溶液配制的初始浓度为50 mg ·L-1的四环素溶液(混合溶液的实验中,四环素、磺胺甲 唑、 阿莫西林浓度均为50mg ·L-1)的pH用H3PO4和NaOH调节为3、 6和9进行光催化降解实验,吸附平衡后光照10 min.取样离心过滤(操作条件同吸附实验)测定,每组进行3次平行实验.
在不同pH条件下四环素降解率的实验结果如图 1.该结果表明,随着pH值从酸性(pH值3.0)变化到弱碱性(pH值9.0)四环素降解率略有上升[17].此外,弱酸pH值(pH=3.0)对四环素降解率的影响不明显,但在最低(1.0)和最高pH值(11.0)对四环素降解率有较明显的抑制作用.pH值作为光催化反应中重要参数,对四环素的水解形态,TiO2表面电荷性质和吸附行为有很大影响[18, 19].可见,pH值对光催化过程中的影响机制极为复杂,需从pH对半导体表面,溶剂分子与基层属性的影响作用[20, 21]等角度进一步研究.
 |
图 1pH值对四环素降解率的影响Fig.1Effect of pH on the degradation of TTC |
TiO2投加量对于四环素光催化降解的影响如图 2所示.当TiO2投加浓度在0.50~1.50 g ·L-1逐渐升高时,四环素降解率也随之升高.然而,当TiO2投加浓度达到2.00 g ·L-1后,四环素的降解率反而低于投加浓度为1.50 g ·L-1时的降解率.由此可知,过低或过高的TiO2投加浓度均会对四环素的降解率和降解速率造成不利影响.这是由于反应器的几何形状,工作条件和一定的TiO2暴露表面积所致.增加催化剂浓度可使更多的TiO2表面受到照射产生更多的羟基自由基.然而,较高TiO2颗粒的浓度会阻碍紫外线在溶液中的穿透,不利于降解率的进一步提高.因此,在实际应用中,必须确定一个最佳TiO2投加浓度以避免过量,并确保吸收足够光子辐射达到高效降解.
 |
图 2投加量对四环素降解率的影响Fig.2Effect of TiO2 dosage on the degradation of TTC |
另一个重要参数是降解过程中四环素的初始浓度,因为它影响着四环素的初始降解速率.为此设计了一组实验观察四环素初始浓度与降解率的关系,相应结果如图 3所示.可以明显看出,当四环素浓度由15mg ·L-1升高到60mg ·L-1的过程中其降解率逐渐升高,经过10 min光照后,四环初始浓度为45mg ·L-1时,大约有90%被分解; 而在四环素初始浓度升高到90mg ·L-1时,其降解率表现出下降趋势,光照10 min后降解率仅有75%左右.因此可推论,尽管四环素初始浓度越高,吸附在TiO2表面的四环素分子越多,有利于初始降解速率的提高.而在TiO2表面形成的羟基自由基( ·OH)和阴离子自由基( ·O2)的初步浓度是恒定的[22],因此,初始浓度过高会使自由基与四环素分子有效结合对数降低.图 3中四环素降解率趋势的变化与上述现象相符.
 |
图 3四环素初始浓度对四环素降解率的影响Fig.3Effect of TTC initial concentration on the degradation of TTC |
不同pH条件下四环素在TiO2上的吸附等温线如图 4所示.从中可看出,在3个pH条件下TiO2对于四环素的吸附量均随着平衡浓度的增大而增大; 在酸性(pH=3)或中性条件(pH=6)下,吸附量上升趋势较为平缓,而在碱性条件下(pH=9)其吸附量上升趋势明显较高.
 |
图 4不同pH下TiO2对四环素的吸附等温线及Langmuir拟合Fig.4Adsorption isotherm of TTC under different pH and fitting to Langmuir model |
由图 4的Langmuir拟合曲线和表1拟合的等温方程参数可知,方程拟合相关系数R2均高于0.999,说明采用Langmuir方程均能很好地描述不同pH值条件下四环素在TiO2表面的吸附行为.这表明四环素在TiO2上的吸附属于单分子层吸附.
| 表1 四环素在TiO2上的Langmuir等温线拟合参数 1) Table 1 Fitting parameters of Langmuir model for TTC adsorption on TiO2 |
虽然TiO2对于四环素的吸附容量较小(范围在1~3.5 mg ·g-1),吸附效果较差,但是受pH值影响很大,在pH=9的条件下TiO2的吸附容量比pH=6或3时高出1倍以上,表明pH对四环素光催化降解的影响可能是多种因素交互影响的结果.因此又进一步研究了四环素在TiO2上的吸附与光催化降解的关系.
光催化降解动力学实验结果见图 5.
 |
图 5不同pH条件下中四环素浓度的变化Fig.5TTC concentration variation at different pH |
图 5中曲线表明四环素的光催化降解动力学可用一级反应动力学方程式表示:

按照一级反应动力学方程对图 5中的数据进行拟合,得到的线性方程的斜率即为表观光降解及光催化反应速率常数,实验得出的在3种不同pH条件下四环素光催化降解反应速率常数值参见表2.
| 表2 不同pH下四环素光催化降解的反应速率常数 Table 2 Constant of TTC photocatalytic degradation reaction at different pH |
从拟合结果来看, 3个不同pH下四环素的光催化降解均很好地符合一级反应动力学方程.而pH对于反应速率的影响较大, pH为3和6时,反应速率常数相近,而pH=9时,反应速率常数提高近40%,表明合适的pH能够促进四环素的光催化降解反应.
为了研究吸附及降解的相关性,分开测定了四环素在不同pH条件下吸附率与降解率.图 6为四环素在不同pH值条件下吸附率和降解率的变化情况(为紫外灯照射10 min后的降解率).可见,在pH值3~9的范围内,四环素的降解率与吸附率均随着pH值的升高而升高,且在pH=9时达到最大值,两者的变化趋势相同.说明四环素的光催化降解对于吸附的有一定的依赖性,推断其降解过程主要发生在TiO2表面.整个过程可分为吸附,催化降解两个部分,四环素由溶液至TiO2表面的吸附过程,这个过程可能很快,所以有研究表明吸附性较好的抗生素TiO2的光催化作用较好[23].
 |
图 6四环素在不同pH下吸附率与降解率的变化Fig.6Adsorption and degradation of TTC at different pH |
为了进一步确定吸附对于光催化降解反应速率的影响,通过初始浓度的变化对反应速率的影响探究四环素在TiO2表面的吸附对整个光催化降解反应的控制性作用.TiO2对四环素pH=9下的吸附等温线及改变反应初始浓度后考察初反应速率变化的曲线分别如图 7和图 8所示,大多数有机物在光催化降解中反应物初始浓度对反应初速率的影响可由Langmuire-Hinshelwood模型描述[24, 25],公式如下:


利用吸附实验及光催化降解实验所得出的碱性条件下(pH=9)的吸附平衡常数(K=0.0313)与光催化降解反应速率常数(kr=0.375)进行动力学计算,可得出整个反应过程的初始速率,结果如图 8所示.
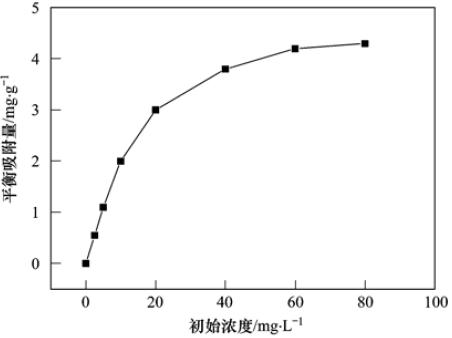 |
图 7pH=9时四环素在TiO2表面的吸附等温线Fig.7Adsorption isotherm of TTC on TiO2 surface (pH=9) |
 |
图 8pH=9时初始浓度对反应初速率的影响曲线Fig.8Effect of TTC initial concentration on the initial reaction rate (pH=9) |
图 8中初始四环素浓度对反应初始速率影响曲线与pH=9的条件下TiO2对四环素的吸附等温线类似(图 7), 反应速率开始时随初始浓度的增大而升高,但当初始浓度增大到60mg ·L-1以后,平衡吸附量与反应速率的增幅均开始变缓.这意味着当TiO2接近最大吸附量后反应速率的变化也就不大了,进而可以推断整个光催化降解反应实际是由吸附在催化剂表面的四环素量所控制.
从图 9可以看出,pH对四环素和磺胺甲 唑两种抗生素的光降解及光催化降解效果都有较大的影响,在不同的pH值条件下,两种抗生素的降解产生了选择性.在酸性条件(pH=3)未投加TiO2的条件下,优先降解磺胺甲 唑,紫外灯照射7~8 min,其选择性最好,四环素降解率仅为35%左右,而磺胺甲 唑的降解率已接近100%.随着pH值的升高, 磺胺甲 唑的光降解效果变差,而四环素的光降解效果提高,当溶液pH达到9时,优先降解四环素,但选择性不佳.投加TiO2后,酸性和中性条件下催化降解没有选择性,可能是由于加入催化剂后,一方面四环素降解路径产生变化,开始通过吸附于催化剂表面发生光催化降解,降解率提高.
 |
图 9不同pH条件下四环素(TTC)和磺胺甲 唑(SMX)在水溶液中的光降解随时间变化曲线Fig.9TTC and SMX photocatalytic-degradation curve with time at different pH |
而另一方面磺胺甲 唑在溶液相中发生少量光催化降解的同时,由于催化剂降低了溶液的透光性导致其光降解减弱,从而降低了两者降解的选择性,在中性条件下(pH=6)选择性最差.在碱性条件(pH=9)并投加1 g ·L-1 TiO2的条件下,优先降解四环素,紫外灯照射5 min左右,其选择性最好,四环素降解率达到90%以上,磺胺甲 唑降解率仅为40%左右.
在相同条件下光照四环素与磺胺甲 唑的混合溶液,pH对两者的降解产生了一定的选择性,在碱性条件优先降解四环素,选择性明显; 而在酸性和中性条件下优先降解磺胺甲 唑,选择性较弱.
在pH=9的条件下,改变催化剂TiO2投加量,对四环素与阿莫西林混合溶液的降解特性进行了研究,结果如图 10所示.
 |
图 10四环素(TTC)和阿莫西林(AMX)在不同TiO2浓度悬浮液中光降解率随时间变化曲线 (pH=9)Fig.10TTC and AMX photocatalytic-degradation curve with time at different TiO2 dosage (pH=9) |
未投加TiO2时,两种抗生素的光降解效果较好,光照10 min后降解率均达到80%以上,光照30 min后降解率近100%,没有表现出选择性.但从图10(b)~10(d)中对比可知,TiO2的投加对两种抗生素的降解产生了明显的选择性.
随着投加量的增加四环素的光催化降解反应得以促进而阿莫西林的光降解受到了很严重的抑制.推测原因可能是由于四环素的降解主要发生在催化剂表面,随着TiO2浓度的增加,有效的反应点位增多,促进了四环素的降解,这也印证了前文中得到的结论; 而阿莫西林主要发生直接光降解反应,只有少量游离在溶液中的 ·OH与阿莫西林分子结合,而TiO2浓度不断地增加,悬浮溶液的透光率就来越小,光散射越来越强,严重影响了阿莫西林对紫外光的吸收,降解率反而有很大程度上的降低.投加1 g ·L-1 TiO2时,优先降解四环素,光照5 min选择性最好,阿莫西林仅降解30%左右,而四环素的降解率已达到90%以上; 投加1.5 g ·L-1 TiO2时,同样优先降解四环素,选择性更高,光照2~5 min都保持了很好的选择性,阿莫西林降解率在27%以下,而四环素在光照2 min后降解率已达到83%.
(1) pH、 TiO2投加量和四环素初始浓度3个单因素对于四环素光催化降解的影响均不是完全线性的,存在一个较有利的范围.单因素最佳范围分别为,pH在9.0左右,TiO2投加量1.25~1.75 g ·L-1,四环素初始浓度45~75 mg ·L-1.
(2) 不同pH下,四环素在TiO2上的吸附率与其降解率有一定的关联.动力学实验表明,当TiO2接近吸附饱和时光催化降解反应速率基本不再提高,推断吸附步骤是整个光催化降解过程的控制步骤.
(3) 改变pH及TiO2投加量会使多种抗生素的共同降解产生选择性.具体规律为:四环素与磺胺甲 唑共同降解时,碱性条件下优先降解四环素,酸性条件下优先降解磺胺甲 唑; 四环素与阿莫西林共同降解时,随着TiO2的投加,促进四环素的降解,而阿莫西林的降解受到抑制,其机制有待进一步研究.
| [1] | 闾幸, 余卫娟, 兰亚琼, 等. 嘉兴市地表水中兽用抗生素的污染现状调查[J]. 环境科学, 2013, 34 (9): 3368-3373. |
| [2] | 邰义萍, 莫测辉, 李彦文, 等. 长期施用粪肥菜地土壤中四环素类抗生素的含量与分布特征[J]. 环境科学, 2011, 32 (4): 1182-1187. |
| [3] | 刘苗苗, 张昱, 李栋, 等. 制药废水受纳河流中四环素抗药基因及微生物群落结构变化研究[J]. 环境科学学报, 2010, 30 (8): 1551-1557. |
| [4] | 李彦文, 张艳, 莫测辉, 等. 广州市蔬菜中喹诺酮类抗生素污染特征及健康风险初步研究[J]. 环境科学, 2010, 31 (10): 2445-2449. |
| [5] | Ge L K, Chen J W, Wei X X, et al. Aquatic photochemistry of fluoroquinolone antibiotics: kinetics, pathways, and multivariate effects of main water constituents[J]. Environment Science and Technology, 2010, 44 (7): 2400-2405. |
| [6] | Andreozzi R, Canterino M, Giudice R L, et al. Lincomycin solar photodegradation, algal toxicity and removal from wastewaters by means of ozonation[J]. Water Research, 2006, 40 (3): 630-638. |
| [7] | 阳海, 曾健, 黎源, 等. 氙灯/TiO2体系下敌草隆光催化降解动力学的研究[J]. 环境科学, 2013, 34( 8): 3137-3142. |
| [8] | 阳海, 周硕林, 尹明亮, 等. 克百威光催化降解动力学的研究[J]. 中国环境科学, 2013, 33 (1): 82-87. |
| [9] | Chusaksri S, Lomda J, Saleepochn T, et al. Photocatalytic degradation of 3,4-dichlorophenylurea in aqueous gold nanoparticles-modified titanium dioxide suspension under simulated solar light[J]. Journal of Hazardous Materials, 2011, 190 (1-3): 930-937. |
| [10] | 刘姝, 陈冰. pH值对TiO2光催化降解苯酚、邻氯苯酚的影响[J]. 硅谷, 2010, (19): 188. |
| [11] | 冷文华, 张莉, 成少安, 等. 附载二氧化钛光催化降解水中对氯苯胺(PCA)[J]. 环境科学, 2000, 21 (11): 46-50. |
| [12] | 董永春, 王秋芳, 顿咪娜, 等. 不同结构偶氮染料在TiO2纳米颗粒表面的吸附和光催化降解[J]. 过程工程学报, 2007, 7 (4): 668-673. |
| [13] | Hughes S R, Kay P, Brown L E. Global synthesis and critical evaluation of pharmaceutical data sets collected from river systems[J]. Environment Science and Technology, 2013, 47 (2): 661-677. |
| [14] | Kolpin D W, Furlong E T, Meyer M T, et al. Pharmaceuticals, hormones, and other organic wastewater contaminants in U.S. streams, 1999-2000: a national reconnaissance[J]. Environment Science and Technology, 2002, 36 (6): 1202-1211. |
| [15] | Sarmah A K, Meyer M T, Boxall A B A. A global perspective on the use, sales, exposure pathways, occurrence, fate and effects of veterinary antibiotics (VAs) in the environment[J]. Chemosphere, 2006, 65 (5): 725-759. |
| [16] | Batt A L, Bruce I B, Aga D S. Evaluating the vulnerability of surface waters to antibiotic contamination from varying wastewater treatment plant discharges[J]. Environmental Pollution, 2006, 142 (2): 295-302. |
| [17] | 朱向东, 王玉军, 孙瑞娟, 等. 溶液酸度对四环素类物质光降解和光催化降解速率的影响[J]. 生态与农村环境学报, 2012, 28 (6): 742-745. |
| [18] | Wei X X, Chen J W, Xie Q, et al. Distinct photolytic mechanisms and products for different dissociation species of ciprofloxacin[J]. Environment Science and Technology, 2013, 47 (9): 4284-4290. |
| [19] | 宋晨怡, 胡霞林, 尹大强. 四环素在光催化TiO2上的吸附研究[J]. 环境化学, 2011, 30 (7): 1292-1296. |
| [20] | Velegraki T, Mantzavinos D. Conversion of benzoic acid during TiO2-mediated photocatalytic degradation in water[J]. Chemical Engineering Journal, 2008, 140 (1-3): 15-21. |
| [21] | Klavarioti M, Mantzavinos D, Kassinos D. Removal of residual pharmaceuticals from aqueous systems by advanced oxidation processes[J]. Environment International, 2009, 35 (2): 402-417. |
| [22] | Betianu C, Caliman F A, Gavrilescu M, et al. Response surface methodology applied for Orange Ⅱ photocatalytic degradation in TiO2 aqueous suspensions[J]. Journal of Chemical Technology and Biotechnology, 2008, 83 (11): 1454-1465. |
| [23] | Kaniou S, Pitarakis K, Barlagianni I, et al. Photocatalytic oxidation of sulfamethazine[J]. Chemosphere, 2005, 60 (3): 372-380. |
| [24] | 慕容心, 李丽媛, 邵芸, 等. TiO2纳米棒对四环素的光催化降解[J]. 环境化学, 2010, 29 (3): 476-480. |
| [25] | 潘纲, 刘媛媛. 吸附模式对有机物光催化降解的影响3. MEA-Langmuir-Hinshelwood光催化降解动力学方程[J]. 环境科学, 2006, 25 (1): 11-15. |
 2014, Vol.35
2014, Vol.35 


